酶法制取低热量大豆功能性油脂的研究
2013-05-15高向阳孙树坤李博群富校轶
高向阳,孙树坤,李博群,富校轶,3,*
(1.东北农业大学,黑龙江哈尔滨150030;2.国家大豆工程技术研究中心东北农业大学,黑龙江哈尔滨150030;3.吉林医药学院,吉林吉林 132013)
油脂不仅能赋予食品独特的口感和风味,同时也能提供人体所需的能量。但油脂的过量摄入严重损害了人类的健康[1]。因此开发一种具有同天然油脂功能性相似,热量低,稳定性好的新型油脂产品已经成为油脂行业研究的热点[2]。
现阶段对低热量油脂的研究主要是利用脂肪酶催化油脂改性,以中链脂肪酸与各种菜籽油、葵花油作为反应基质制取所需的功能性油脂产品[3],如陈翔等[4]以菜籽油和辛酸为原料,在无溶剂体系中酶解合成结构脂质,结果辛酸合成率达40%。张凤秀等[5]以猪胰腺脂肪酶为催化剂合成辛酸辛酯,使辛酸的转化率达到98.12%。李新舟等[6]研究了不同条件下脂肪酶催化大豆油与辛酸甲酯的酯交换反应工艺条件。丁双等[7]研究了固定化脂肪酶催化大豆油与辛酸酶解制备结构脂质的工艺,结果辛酸的插入率为43%。
大豆油在全球的生产和消费量都很高,大豆油中含有维生素E、亚麻酸、亚油酸等不饱和脂肪酸,其脂肪酸构成比较适合人体消化吸收,在人体内起着重要的生理作用[8]。因此以大豆油为反应的基质在我国有很大的应用空间和发展潜力。短链脂肪酸(C2~C6)易挥发、分子量小、水中溶解度高、脂肪酸链短,在胃中吸收速度比中链脂肪酸快,并且短链脂肪酸合成的结构脂质热量值低且具有降低胆固醇的功效[9]。因此本研究主要应用酶解法[10-12],以脂肪酶为催化剂,在非水介质中通过短链脂肪酸丙酸酶解反应对大豆油进行改性,制备高附加值的低热量功能性油脂,探讨了在非溶剂体系中,酶添加量、底物摩尔比、反应温度、反应时间等因素对丙酸插入率的影响,从而确定最佳的反应工艺。
1 材料与方法
1.1 材料与仪器
金龙鱼大豆油(一级大豆油) 沃尔玛超市;固定化1,3定向脂肪酶Lipozyme RM IM(507.2U/g)、Lipozyme TL IM(358.7U/g) 丹麦Novozyme公司;正丙酸(99%) 天津市光复精细化工研究所;脂肪酸标样 Sigma公司;正己烷等其他有机溶剂和试剂 均为国产分析纯或色谱纯。
HZS-Hx型水浴振荡器 哈尔滨市东联电子技术开发有限公司;电子天平 赛多利斯科学仪器(北京)有限公司;Z36HK型低温高速离心机 Germany;HH-4型田瑞数显恒温水浴锅 金坛市双捷实验仪器厂;气相色谱仪 美国安捷伦。
1.2 实验方法
1.2.1 结构脂质的制备及纯化 采用无溶剂体系,称取10.00g的大豆油与丙酸置于一具塞100mL三角瓶中,加入6%(以底物的质量计)脂肪酶,将其放入恒温水浴振荡器中,保持80r/min振荡速率和60℃温度,反应6h后终止,过滤除去脂肪酶,将反应混合物置于锥形瓶中,加入2~3滴1%酚酞溶液,结合计算所得的理论加碱量,使用KOH溶液滴定,滴至微红色。再加入25mL热水(水化)洗涤。取上层油脂层,经烘箱干燥后离心,最后取上清液放入-4℃冰箱以备分析。
1.2.2 脂肪酶的选择方法 选用Li-pozyme TL IM、Li-pozyme RM IM两种固定化1-3定向脂肪酶,筛选方法为:称取10.00g大豆油,按照2∶1(丙酸/大豆油,摩尔比)的底物比加入丙酸,再加入6%的脂肪酶(以底物质量计),在振荡速率80r/min和一定的温度条件下,将样品放入水浴振荡器中,反应2h后,按照1.2.1的实验方法,得到的产物放入-4℃冰箱以备分析。
1.2.3 酶法制取低热量油脂的单因素实验方法
1.2.3.1 酶解温度的确定 称取10.00g的油脂,在底物比2∶1(丙酸/大豆油,摩尔比),酶用量6%,反应时间6h的条件下,按照1.2.1的实验方法。观察40、50、60、70和80℃五个温度梯度对丙酸插入率的影响。以确定最佳的反应温度范围。
1.2.3.2 酶解时间的确定 称取10.00g的油脂,在底物比2∶1(丙酸/大豆油,摩尔比),酶用量6%,反应温度60℃的条件下,按照1.2.1的实验方法。观察2、4、6、8和10h五个时间梯度对丙酸插入率的影响。以确定最佳的反应时间范围。
1.2.3.3 酶添加量的确定 称取10.00g的油脂,在底物比2∶1(丙酸/大豆油,摩尔比),反应温度60℃,反应时间8h的条件下,按照1.2.1的实验方法。观察2%、4%、6%、8%和10%五个酶添加量梯度对丙酸插入率影响。以确定最佳的酶添加量范围。
1.2.3.4 底物摩尔比的确定 称取10.00g的油脂,在反应温度60℃,酶用量6%,反应时间8h的条件下,按照1.2.1的实验方法。观察2∶1、3∶1、4∶1、5∶1和6∶1五个底物摩尔比梯度对丙酸插入率的影响。以确定最佳的底物摩尔比范围。
1.2.4 响应面优化实验 采用二次回归正交旋转组合设计方法设计四因素三水平实验。以温度、时间、底物比、加酶量四个因素为自变量,丙酸插入率为响应值。实验因素水平编码值见表1。实验结果采用Design Expert 7.1软件进行分析。
1.3 分析方法
1.3.1 甲酯化方法 称取约50mg已制备好的低热量功能性油脂于10mL具塞试管中,用移液管取1mL KOH-甲醇水溶液(13.1g/100mL)利用快速混匀器混匀,再取5mL正己烷振荡30s,静置放置澄清后,即可取上层清液进行GC分析。
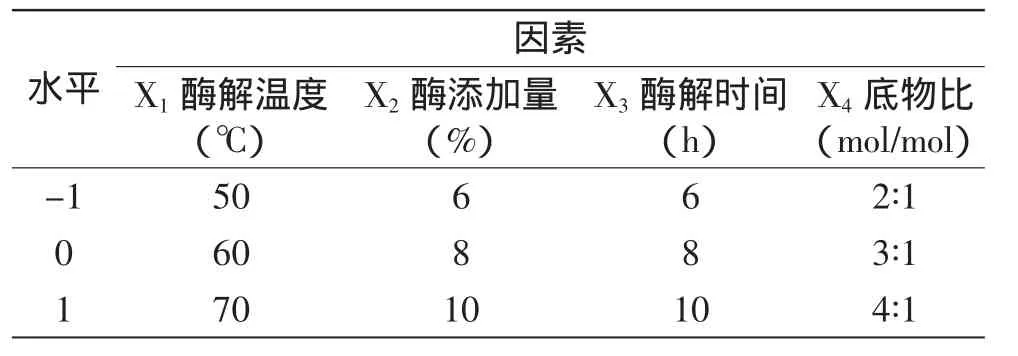
表1 四因素三水平实验编码表Table 1 Four factors three levels test code table
1.3.2 气相色谱分析条件 a.CP-Sil 88毛细管柱(100m×0.25mm×0.2μm,美国安捷伦)。b.进样量1μL,进样温度260℃,分流比20∶1,柱压力20cm/sec。c.程序升温:柱箱平衡1min,140℃保留5min,然后以4℃/min的升温速率将温度升至220℃并保持25min,再以10℃/min的速率将温度升至230℃并保持5min。d.检测器:氢焰离子化检测器(FID),260℃,氢气流量40mL/min、空气流量400mL/min、氮气流量30mL/min。
然后调整柱箱的初始温度和载气的线速度直到能较好的检测出结果以确定最终的色谱条件。
1.3.3 丙酸插入率的计算 丙酸插入率(丙酸含量)=结构脂质甲酯化后丙酸甲酯的面积百分含量/结构脂质甲酯化后所有脂肪酸甲酯的面积百分含量总和。
1.3.4 油脂的热分析——氧弹法 先称取约1.000g已制备好的低热量功能性油脂,放入热量计氧弹内,然后向其冲入约3MPa的氧气,再将氧弹放在一个盛有约2L足够浸没氧弹的水桶中,并使氧弹内的物质点火燃烧,放出的热量被桶中的水吸收并使水温升高,根据升温程度计算油样的热值。
2 结果与分析
2.1 脂肪酶的选择
在酶解反应体系中为了筛选出催化活性较高的脂肪酶,分别选用两种不同的脂肪酶Li-pozyme TL IM和Li-pozyme RM IM在不同的温度梯度下进行酶解比较。
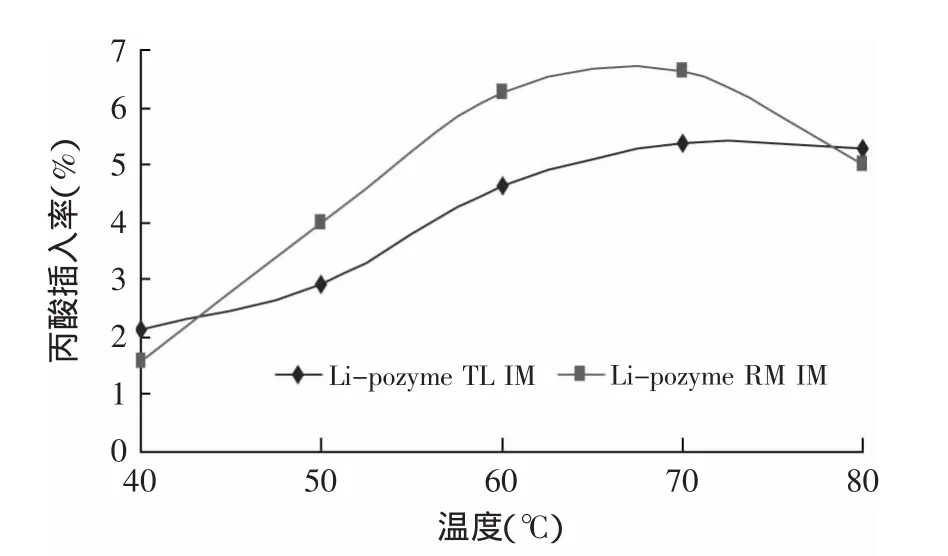
图1 两种脂肪酶催化活力比较Fig.1 Different lipases catalyses ability comparison
由图1可知,两种脂肪酶都有较好的催化效率,但在不同的反应温度下却呈现出了明显的变化趋势,Lipozyme RM IM脂肪酶催化酶解所制备的低热量功能性油脂中丙酸的插入率较高,因此在后续的实验中选用Lipozyme RM IM做催化剂。
2.2 影响酶法制取低热量功能性油脂的单因素实验研究
2.2.1 温度对酶解反应的影响 由图2可知,在非溶剂体系中,随着反应温度的升高,可加速酶解反应使结合到甘油骨架上的丙酸含量增加,而其他脂肪酸含量也相应的有所变化,当温度从40℃上升到60℃时,大豆油中丙酸含量明显增大,温度超过70℃以后,丙酸含量逐渐减小。其原因主要为随温度升高,反应体系的粘度、传质阻力变小增加反应速率。但继续升温,酶易失活而发生变性,致使酶活力降低。因此在本研究的优化设计中,将酶解温度选为50~70℃。

图2 温度对酶解反应的影响Fig.2 Effects of temperature on enzymolysis reaction
2.2.2 时间对酶解反应的影响 由图3可知,在反应初期,改性油脂中丙酸含量呈增加趋势,但反应到一定阶段后,产物中丙酸含量变化趋于缓和,反应体系最终达到平衡。如果继续延长反应时间不但增加了丙酸位移,也没有实际意义。因此在优化设计中,选取时间为6~8h。
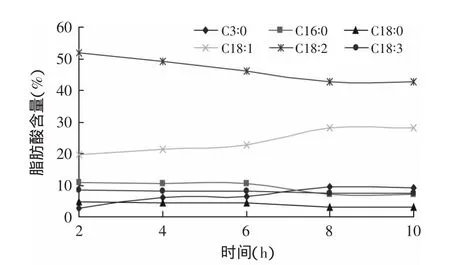
图3 时间对酶解反应的影响Fig.3 Effects of time on enzymolysis reaction
2.2.3 脂肪酶用量对酶解反应的影响 由图4可知,在酶添加量由2%增至8%的过程中,改性油脂中丙酸含量增加速率较快。当酶用量继续增加时,反应体系中丙酸含量增加幅度减小,最后接近平衡。其原因可能为反应初期,底物与酶分子接触机会增多,酯交换频率增大,产物中丙酸含量增加。反应一段时间后,由于底物含量减少,并且底物与产物对酶的传质阻率增大,使得产物中丙酸含量减小。此外考虑到酶价较高。所以选取酶添加量的较佳区域为6%~10%。
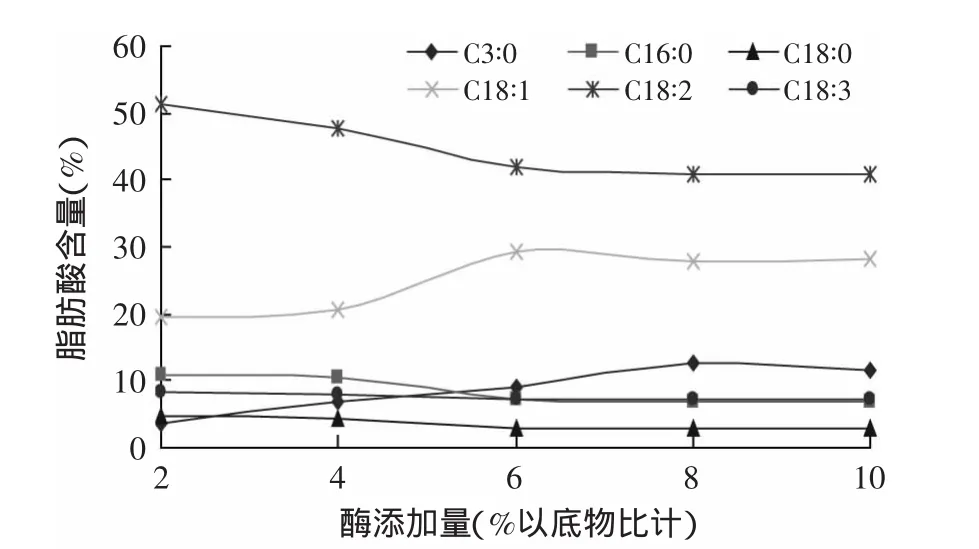
图4 脂肪酶用量对酶解反应的影响Fig.4 Effects of enzyme load on enzymolysis reaction
2.2.4 底物摩尔比对酶解反应的影响 由图5可知,当丙酸/大豆油的摩尔比从2∶1上升到3∶1时,丙酸含量增加的较快,当底物比例超过3∶1,丙酸含量增加缓慢并呈现下降趋势。其原因可能为丙酸的初始浓度大有利于大豆油中丙酸含量的增加。因此在后面的优化实验中,底物比选用2∶1~4∶1。

图5 底物摩尔比对酶解反应的影响Fig.5 Effects of substrate molar ratio on enzymolysis reaction
2.3 响应面实验结果
根据表1实验因素和水平的设计,进行29个实验点,其中24个为析因实验点,5个中心实验点,优选最佳提取工艺。
对表2在不同条件下所测得的丙酸插入率,利用Design expert 7.1软件进行回归拟合,得到丙酸插入率的回归方程:
Y=14.64+1.69X1+1.12X2+1.08X3+0.26X4+1.16X1X2-0.29X1X3+0.67X1X4-0.0075X2X3+1.62X2X4+0.21X3X4-2.10X12-4.90X22-2.03X32-2.05X42
2.3.1 模型方差分析 利用Design expert 7.1统计软件进行二次多元回归拟合,得到回归方程模型的方差分析和回归方程系数估计值,见表3。
回归方程中各变量对指标(响应值)影响的显著性,由F检验来判定,概率p的值越小,则响应变量的显著性越高。由表3可知,四个因素对丙酸插入率的影响顺序为:酶解温度>酶添加量>酶解时间>底物摩尔比。从方差分析可以看出模型Prob>F小于0.01,表明该模型方程高度显著,不同处理间的差异高度显著。模型失拟项的Prob>F值0.6898>0.05,模型失拟项不显著,模型选择合适。由此可见,各具体实验因素对响应值的影响不是简单的线性关系。相关系数R2=257.74/262.82=0.981,R2adj=0.9613说明丙酸插入率实际值与预测值之间具有较好的拟合度,因此该模型可用于预测响应值丙酸插入率Y的实际情况。
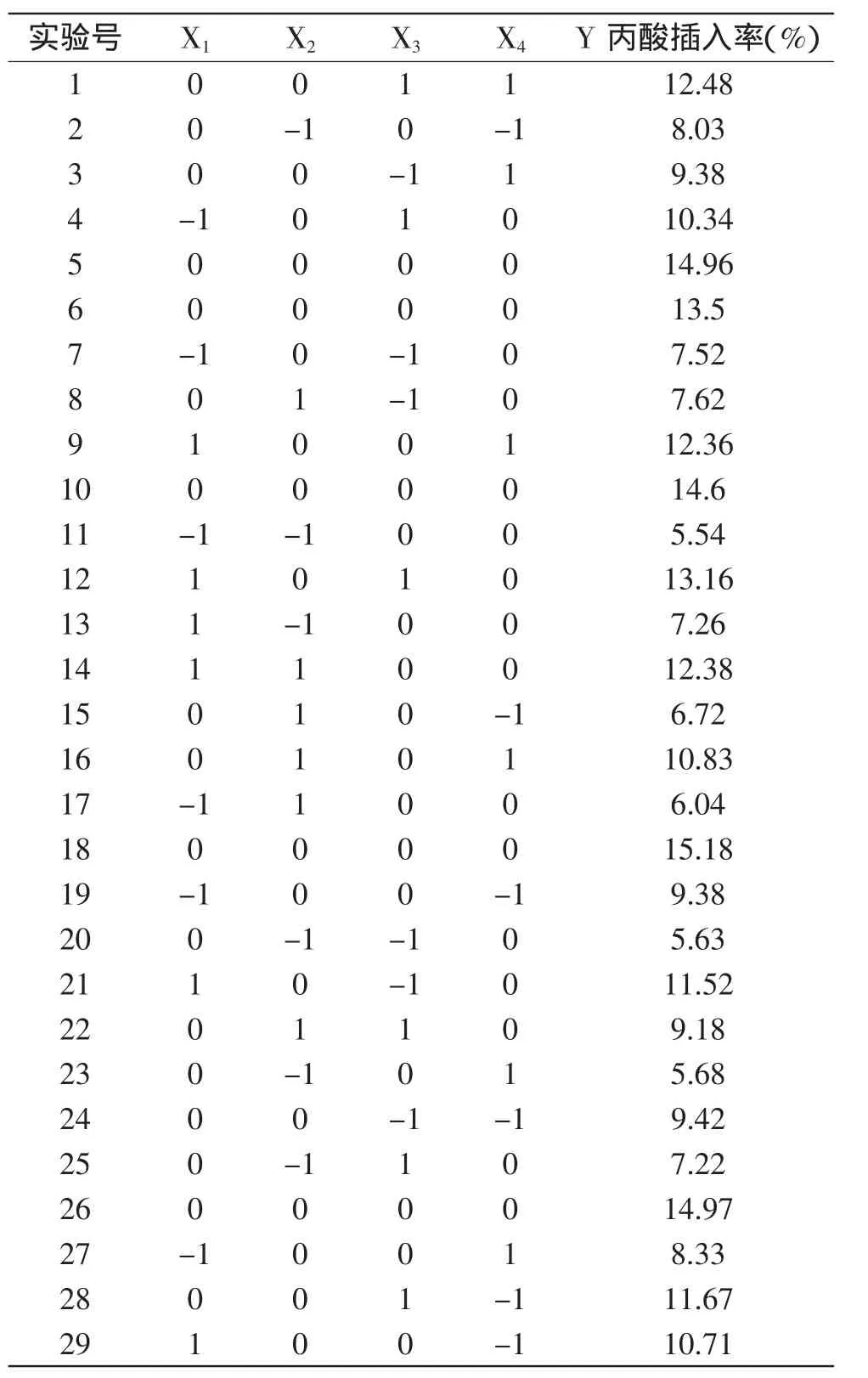
表2 Box-behnken设计方案及实验结果Table 2 Box-behnken design plan and experimental results
2.3.2 响应曲面分析与最优工艺条件的确定 根据回归分析结果,做出响应曲面图,如图6~图11。从响应曲面分析图中可以找到最佳参数及各参数之间的交互作用。
如图6~图11直观地反映了各因素对响应值的影响。比较6组图可知,酶解温度、酶添加量、酶解时间和底物比对丙酸插入率的影响较为显著,表现为曲线较陡。丙酸插入率的响应面趋势呈抛物线形,因此回归方程有极大值,结合方程与响应曲面可得到酶法制取低热量大豆功能性油脂的最优参数为:酶解温度64.4℃,酶添加量8.4%,酶解时间8.8h,底物比
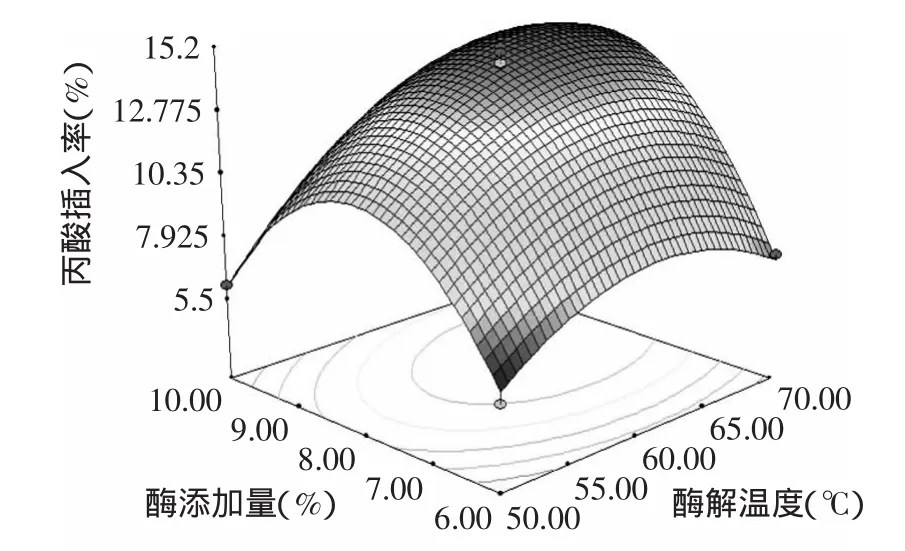
图6 酶添加量与酶解温度的交互作用Fig.6 The interaction of enzyme additives and enzymolysis temperature

表3 回归方程的方差分析Table 3 Variance analysis of regression equation

图7 底物比与酶添加量的交互作用Fig.7 The interaction of substrate ration and enzyme additives
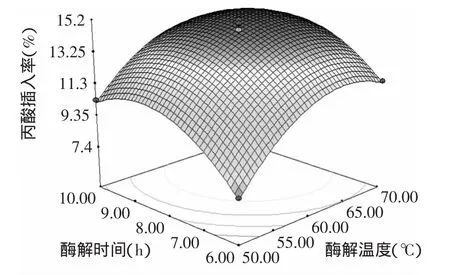
图8 酶解时间与酶解温度的交互作用Fig.8 The interaction of enzymolysis time and enzymolysis temperature
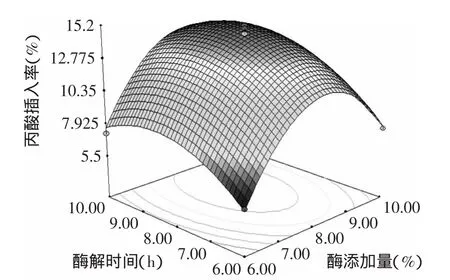
图9 酶解时间与酶添加量的交互作用Fig.9 The interaction of enzymolysis time and enzyme additives
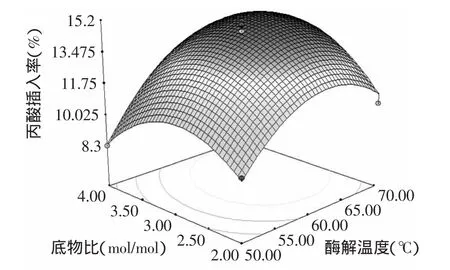
图10 底物比与酶解温度的交互作用Fig.10 The interaction of substrate ration and enzymolysis temperature
3.3 ∶1,丙酸插入率为15.26%。
根据最佳工艺条件,做三组验证性实验,结果如表4所示。
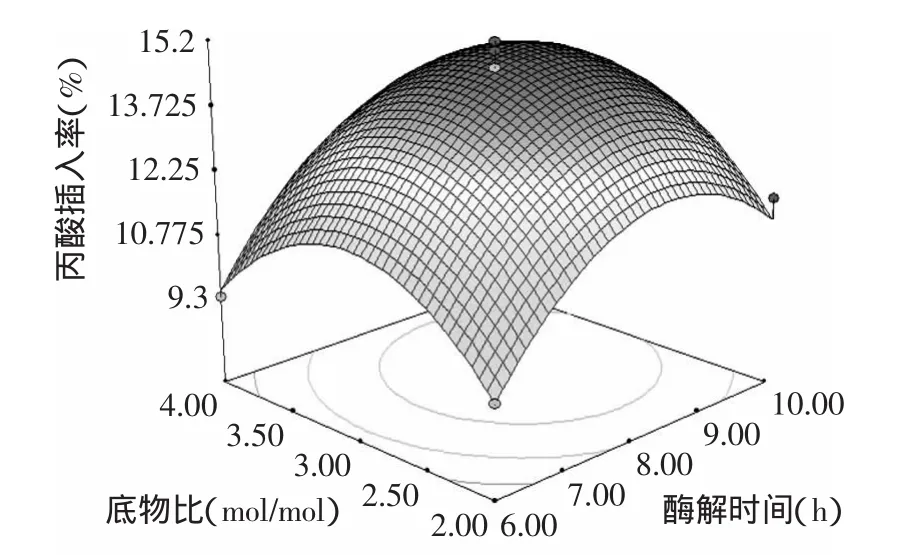
图11 底物比与酶解时间的交互作用Fig.11 The interaction of substrate ration and enzymolysis time

表4 最佳工艺条件验证结果Table 4 Verify results of the best process conditions
由表4可以看出,在所得的最佳工艺条件下丙酸插入率与预测值接近,因此进一步验证了实验结果。
2.4 低热量功能性油脂的热分析
采用1.3.4所述方法测定油脂产生的热值,得到原大豆油的热值为39.96MJ/kg。
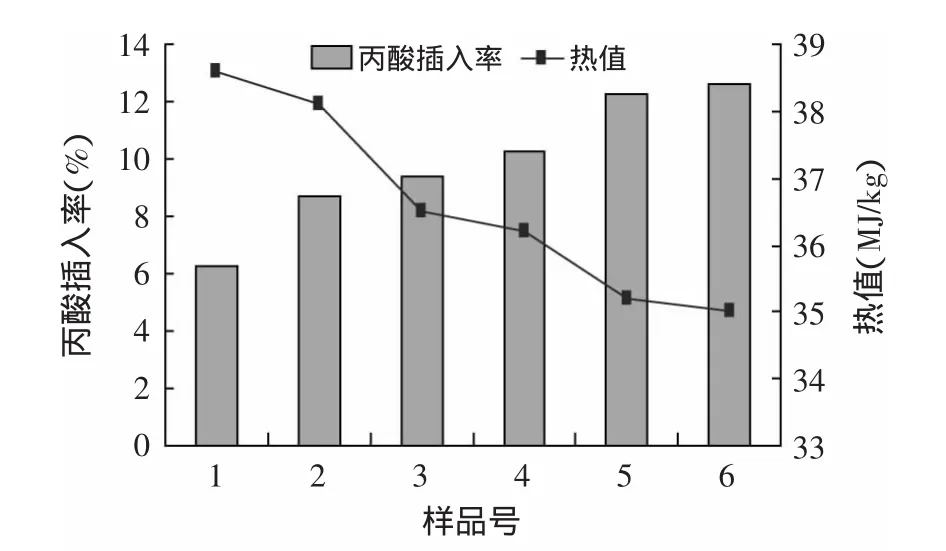
图12 低热量功能性油脂热值与丙酸插入率的关系Fig.12 Relationship betwee low calorie functional oil and propionic acid insertion rate
由图12可知,在所有被测的低热量功能性油脂中,热值最低的为32.57MJ/kg,与原大豆油相比热值降低了约18.5%。
3 结论
本研究以大豆油与丙酸为反应基质,通过筛选在非溶剂体系中以Lipozyme RM IM固定化1-3定向脂肪酶做催化剂制备低热量功能性油脂,利用安捷伦气相色谱仪测定低热量功能性油脂的脂肪酸组成。在单因素以及四因素三水平的响应面法实验基础上,建立了响应值和各因素之间的数据模型。四个因素对丙酸含量的影响顺序为:酶解温度>酶添加量>酶解时间>底物摩尔比。确定了酶法制取低热量大豆功能性油脂的最佳工艺参数:酶解温度64.4℃,酶解时间8.8h,酶添加量8.4%,底物摩尔比3.3∶1。在此条件下低热量功能性油脂的理论丙酸插入率为15.26%。验证值可达14.85%。
通过产品的热分析图可知,大豆油中丙酸的插入起到了降低油脂热量的功效,低热量功能性与原大豆油相比热量值降低了约18.5%。
[1]何川,王海清,赵敏生,等.低热量油脂的制备和精炼工艺研究[J].中国油脂,2005(3):14-16.
[2]宋慧波,张玉军,刘彩丽.低热量油脂的研究进展[J].粮油食品科技,2005(6):19-21.
[3]万银松.酶催化制取结构脂质的研究一菜籽油的改性[D].石河子:石河子大学,2007.
[4]陈翔,王瑛瑶,栾霞,等.无溶剂体系中酶催化合成结构脂质条件初探[J].中国油脂,2010(3):35-38.
[5]张凤秀、张光先.有机溶剂中脂肪酶催化辛酸辛酯的合成[J].食品科学,2010(15):44-49.
[6]李新舟,丁双.酶法合成功能性油脂新工艺研究[J].现代农业科技,2011(7):355-356.
[7]丁双,杨江科,闫云君.酶法改良大豆油制备质构脂质的研究[J].食品科学,2008(1):173-176.
[8]黄雨洋,李杨,肖志刚.浅述大豆制品[J].粮食加工,2008(4):36-38.
[9]孟祥河,段作营,毛忠贵.重构脂质的研究进展[J].中国油脂,2002(2):14-17.
[10]Halldorsson A ,Magnusson CD ,Haraldsson GG .Chemoenzymatic synthesis of structured triacylglycerols by highly regioselective acylation [J]. Tetrahedron,2003,59(46):9101-9109.
[11]Halldorsson A , Magnusson CD , Haraldsson GG .Chemoenzymatic synthesis of structured triacylglycerols [J].Tetrahedron Letters,2001,42(43):7675-7677.
[12]Soumanou MM,Bornscheuer UT,Schmid RD. Two -step enzymatic reaction for the synthesis of pure structured triacylglycerides[J]. J Am Oil Chem Soc,1998,75(6):703-710.
