牛玻璃酸酶酶学特性的研究
2013-05-15杨萌萌李儒仁余群力左秀峰韩广星郭兆斌
杨萌萌,韩 玲,*,李儒仁,余群力,左秀峰,韩广星,郭兆斌
(1.甘肃农业大学食品科学与工程学院,甘肃兰州730070;2.山东绿润食品有限公司,山东临沂276000)
牛玻璃酸酶(Hyaluronidase),是从牛睾丸中提取的一类水解酶,是我国生化制药行业的重要产品之一。牛玻璃酸酶能够水解透明质酸,用于人体能暂时降低细胞间质粘性,可促使皮下输液、局部积贮的渗出液或血液加快扩散而利于吸收,是一种重要的药物扩散剂。临床用作药物渗透剂,促进药物吸收,促进手术及创伤后局部水肿或血肿消散。玻璃酸酶不但在医药领域有着广泛的应用,而且在保健品、食品添加剂领域也有卓越的贡献。人为补充玻璃酸酶保健品可消除皱纹或使局部器官增厚增高,使皮肤保持弹性。
目前,对玻璃酸酶的研究主要针对哺乳动物睾丸、蝎毒、蜂毒、蛇毒等,并且已经从牛睾丸[1]、虾胰腺[2]以及蝎毒[3-4]、蜂毒[5]、蛇毒[6-8]、鱼毒[9]、毛虫毒[10]中分离出了玻璃酸酶。但是,国内对于玻璃酸酶的研究主要是粗酶液的制备和粗酶液性质的研究,并且,针对同一原料,对其粗酶液的性质研究出现了不同的结果,由于粗酶液中存在大量杂蛋白,杂蛋白对酶的稳定性以及酶学性质的研究有很大影响。因此,实验以色谱层析纯化后的牛玻璃酸酶为原料,对牛玻璃酸酶酶学性质进行研究,为玻璃酸酶的应用提供参考。
1 材料与方法
1.1 材料与仪器
新鲜牛睾丸 采自山东绿润食品有限公司,选取检疫合格的牛睾丸,清除表面异物,用聚乙烯塑料包装袋密封包装,液氮冻藏后于-80℃贮藏,备用;透明质酸钠、N-乙酰-D-氨基葡萄糖、乙酸、乙酸钠、NaCl、硫酸铵、丙烯酰胺、N-N-甲叉双丙稀酰胺、甘氨酸、Tris、甘油、考马斯亮蓝、甲醇、冰醋酸 分析纯;SP Sepharose Fast Flow、Sephacryl S-100(GE)。
DS-1型组织捣碎机 金坛市金南仪器厂;PHS-3C型pH计 上海精密科学仪器有限公司;TGL-16M型台式高速冷冻离心机 湘仪离心机仪器有限公司;HH-2型恒温水浴锅 上海博迅实业公司医疗设备厂;AL204型电子天平 梅特勒-托利多仪器公司;SP-756P型紫外可见分光光度计 上海光谱仪器有限公司;DYY-6c型电泳仪电源、25D型电泳槽 北京市六一仪器厂;DPS-2型蛋白纯化系统 上海金达生化仪器有限公司。
1.2 实验方法
1.2.1 牛玻璃酸酶粗酶液的提取 牛睾丸去外膜后,切成块状,加入提前预冷的提取剂(w/v=1∶2),匀浆3min,4℃冰箱中静置提取12h,离心(8000r/min,4℃,20min),弃去沉淀,得到牛玻璃酸酶提取液;在提取液中加入饱和硫酸铵溶液使硫酸铵的浓度达到35%,混匀静置4h,离心(8000r/min,4℃,20min),得上清液;上清液中加入饱和硫酸铵溶液使其浓度达到70%,混匀静置8h,离心(8000r/min,4℃,20min)得沉淀,在4℃蒸馏水中透析,透析后得到牛玻璃酸酶粗酶液[11]。
1.2.2 牛玻璃酸酶的纯化 将粗酶液加载到离子交换预装柱(SP Sepharose Fast Flow),平衡缓冲液为50mmol/L乙酸-乙酸钠(pH5.4),洗脱缓冲液为50mmol/L乙酸-乙酸钠(pH5.4,包含1mol/L NaCl),流速为5mL/min。收集有活性的部分用于凝胶过滤层析(Sephacryl S-100)纯化,平衡缓冲液与洗脱缓冲液为50mmol/L乙酸-乙酸钠(pH5.4,包含0.15mol/L NaCl),流速为0.5mL/min。收集有活性的部分用于SDS-PAGE和酶学性质的研究[12-14]。
1.2.3 牛玻璃酸酶酶活的测定 参照Mayumi[15]的方法并予以改进。0.2mL酶液与0.8mL透明质酸钠储备液,混合后37℃下保温15min,同时做空白实验。孵化结束后立即加入0.22mL四硼酸钾沸水浴4.5min,迅速冷却4min;加6mL稀释至10倍体积的DMAB显色剂,然后37℃保温20min,迅速冷却5min。显色反应结束后,10000r/min,4℃离心10min,585nm下测吸光度值。一个酶活单位(U)被定义为,在最适反应温度(37℃)条件下,玻璃酸酶分解透明质酸钠,每分钟释放1μmol N-乙酰-D-氨基葡萄糖的量。
1.2.4 蛋白质含量的测定 采用考马斯亮蓝法[16]。
1.2.5 SDS-PAGE 经过色谱层析纯化的样品用于SDS-PAGE,聚丙烯酰胺凝胶浓度为12%,Tris-glycine(pH8.8)作为电泳缓冲液,电泳结束后用考马斯亮蓝染色液染色1h。
1.2.6 牛玻璃酸酶酶学性质的研究
1.2.6.1 最适反应温度及热稳定性 在pH4.5的条件下,以透明质酸钠为底物,分别测定玻璃酸酶在4、15、24(室温)、37、45、50、55、60、70℃条件下的酶活力。此外,将玻璃酸酶在上述温度下分别预处理60min,观察其热稳定性[17]。
1.2.6.2 pH对牛玻璃酸酶活性的影响 用0.2mol/L乙酸钠溶液和0.2mol/L乙酸溶液配成pH2.5、3、3.5、4、4.5、5、5.5、6、6.5、7、7.5的乙酸-乙酸钠缓冲溶液(0.1mol/L)。以透明质酸钠为底物,测定牛玻璃酸酶在2.5~7.5不同pH条件下的酶活。
1.2.6.3 NaCl浓度对牛玻璃酸酶活性的影响 用0.2mol/L乙酸钠溶液和0.2mol/L乙酸溶液配成pH4.5的乙酸-乙酸钠缓冲溶液(0.1mol/L),其中NaCl浓度分别为0、0.05、0.1、0.15、0.2、0.25、0.3、0.35、0.4、0.45、0.5mol/L。用上述含不同NaCl浓度的乙酸-乙酸钠缓冲溶液配制底物透明质酸钠,测定酶活,考察NaCl浓度对酶活的影响。
1.2.6.4 BSA浓度对牛玻璃酸酶活性的影响 用0.2mol/L乙酸钠溶液和0.2mol/L乙酸溶液配成pH为4.5的乙酸-乙酸钠缓冲溶液(0.1mol/L),其中BSA浓度 分别为 0、0.15、0.3、0.45、0.6、0.75、0.9、1.05mol/L。用上述含不同BSA浓度的乙酸-乙酸钠缓冲溶液配制底物透明质酸钠,测定酶活,观察BSA浓度对酶活的影响。
1.2.6.5 金属离子对牛玻璃酸酶活性的影响 玻璃酸酶中分别加入Fe3+、Ca2+、Zn2+、Mg2+、Mn2+、Al3+、K+,使各离子溶液在酶液中的终浓度为0.8mmol/L,室温下反应60min后检测酶活变化。空白不加任何离子,考察酶活变化情况[18]。
1.2.6.6 不同物质浓度对牛玻璃酸酶活性的影响 在0.1mol/L的乙酸乙酸钠缓冲液(pH4.5)中,玻璃酸酶分别与不同浓度的肝素、硫酸软骨素(A、B、C)、人类血清蛋白及半胱氨酸混合均匀,4℃下反应30min后测其酶活。反应条件一致的情况下,对照不加抑制剂和激活剂,观察酶活变化情况。
2 结果与讨论
2.1 SDS-PAGE
由图1可知,阳离子交换层析之后(IEX),杂蛋白较多;粗酶液经过阳离子交换层析和凝胶过滤(GF)层析两步纯化后,1号泳道出现两个浓度较高的条带,其分子量在55~72ku之间。这一结果与Malcolm Lyon[1]的研究结果一致,这两条带显示的酶属于同工酶,均属于糖蛋白。

图1 牛玻璃酸酶SDS-PAGEFig.1 SDS-PAGE of hyaluronidase from bovine testicular
2.2 温度对牛玻璃酸酶活性的影响
由图2可知,在4~70℃范围内,牛玻璃酸酶的酶活随着温度的升高呈现先上升后下降的趋势,37℃时达到最大值,这与Yang[19]的结果一致。60、70℃的酶活分别为最高酶活的14.84%和4.31%。不同温度下预处理1h之后,温度从4℃升高至37℃的过程中,酶活稳定;从37℃升高至60℃过程中,牛玻璃酸酶很不稳定,并且酶活损失严重,在60℃下酶活完全丧失。
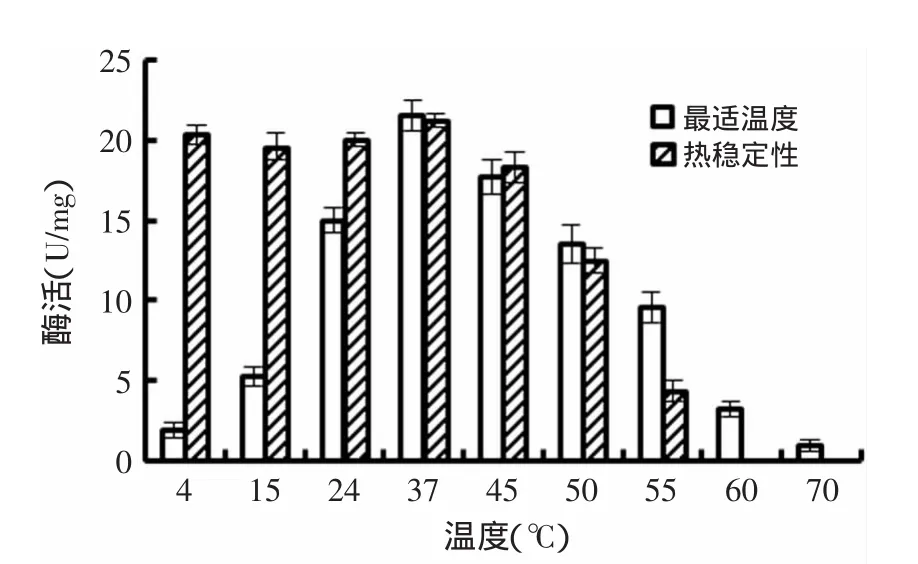
图2 牛玻璃酸酶的最适温度和热稳定性Fig.2 Optimal temperature and thermal stability of hyaluronidase from bovine testicular
2.3 pH对牛玻璃酸酶活性的影响
酸性环境对牛玻璃酸酶维持活性是必不可少的条件,如图3所示,不同pH的0.1mol/L乙酸乙酸钠溶液对玻璃酸酶酶活的影响不同,呈现先上升后下降的趋势。高酸性抑制酶活,pH为2.5时,酶活趋近于零;碱性环境对酶起抑制作用;pH为4.5时,酶活最高。

图3 牛玻璃酸酶的最适pHFig.3 Optimal pH of hyaluronidase from bovine testicular
2.4 NaCl浓度对牛玻璃酸酶活性的影响

图4 NaCl浓度对牛玻璃酸酶活性的影响Fig.4 Effect of NaCl on the activity of hyaluronidase from bovine testicular
由图4可知,不同浓度的NaCl对玻璃酸酶酶活的影响各不相同。以不添加NaCl的为基准,浓度在0.05~0.45mol/L的范围内提高酶活,超过0.45mol/L时抑制酶活,0.2mol/L时酶活最高,比不添加NaCl的高出了20U/mg。
2.5 BSA浓度对牛玻璃酸酶活性的影响
由图5可知,以不加BSA为基准,浓度在0~0.75mol/L的范围内增加酶活,0.45mol/L时酶活最高,增加了34%。当BSA浓度超过0.75mol/L时,BSA开始抑制酶活,1.05mol/L时损失了33%的酶活。

图5 BSA浓度对牛玻璃酸酶活性的影响Fig.5 Effect of BSA on the activity of hyaluronidase from bovine testicular
2.6 金属离子对牛玻璃酸酶活性的影响
由图6可知,以不加金属离子为基准,七种离子对牛睾丸玻璃酸酶均有不同程度的抑制作用,酶活损失较多。其中Fe3+对该酶的抑制作用相对其他离子较强,Mg2+的抑制作用相对较弱。金属离子可以对玻璃酸酶产生抑制作用,可能是因为其阻碍了酶和底物的结合作用,从而抑制了该酶的酶活。
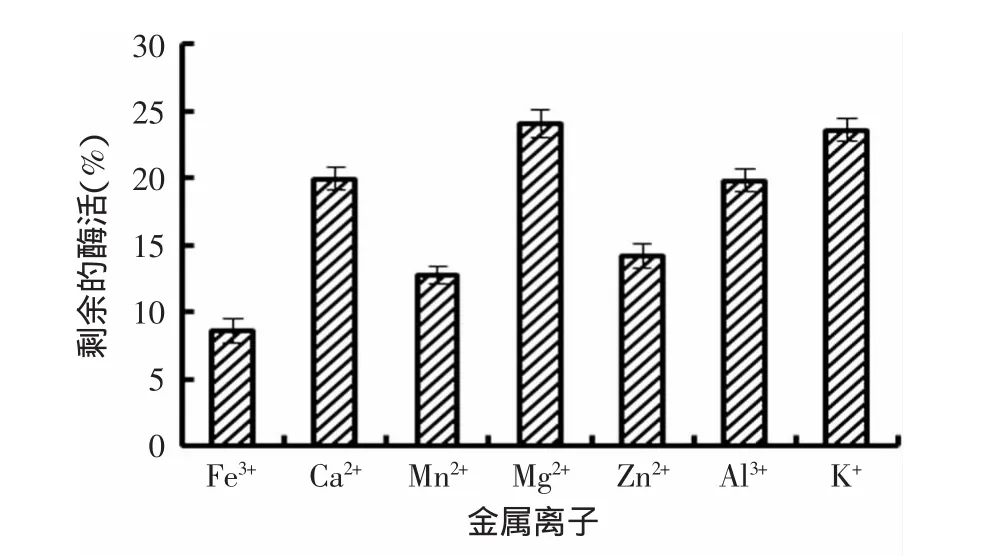
图6 金属离子对牛玻璃酸酶活性的影响Fig.6 Effect of metal ions on the activity of hyaluronidase from bovine testicular
2.7 不同物质浓度对牛玻璃酸酶活性的影响
由图7可知,不同物质的浓度对玻璃酸酶酶活的影响各不相同。硫酸软骨素A的浓度为1.2mg/mL时,损失了31.08%的酶活,随着浓度的下降,酶活损失的就越少,当浓度为0.012mg/mL时,酶活基本上没有损失。不同浓度的硫酸软骨素B对酶活的影响不大,1.2、0.12mg/mL时分别损失了7.23%和5.07%,0.012mg/mL增加了1.36%的酶活。硫酸软骨素C对酶活的影响显著,1.2mg/mL时损失了45.07%的酶活,低浓度时酶活基本没有损失。肝素对酶活起着较小的抑制作用,损失在10%之内。低浓度的人类血清蛋白可增加1.05%的酶活。半胱氨酸使酶完全失活。
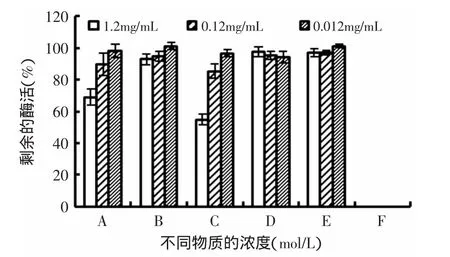
图7 不同物质浓度对牛玻璃酸酶活性的影响Fig.7 Effect of different material on the activity of hyaluronidase from bovine testicular
3 结论
3.1 牛玻璃酸酶水解透明质酸钠的最适pH和温度分别为4.5和37℃,在4~45℃条件下稳定性较好。NaCl和BSA浓度分别为0.2、0.45mol/L时酶活最高。
3.2 金属离子Mg2+对该酶的抑制作用较弱,Fe3+的抑制作用较强。硫酸软骨素A浓度为1.2mg/mL时对酶有抑制作用,低浓度0.012mg/mL时对酶基本没有影响。硫酸软骨素B对酶的抑制作用较小,浓度0.012mgm/L时可增加少许酶活。硫酸软骨素C浓度为1.2mg/mL时,对酶的抑制作用较强。肝素在浓度低时抑制作用较高。人类血清蛋白在低浓度时增加1.05%的酶活。半胱氨酸使酶失活。
[1]Malcolm Lyon,Charles F Phelps.A rapid purification of bovine testicular hyaluronidase by chromatography on dermatan sulphate-substituted 1,6-diaminohexane-Sepharose 4B[J].The Biochemical Society,1981,199:419-426.
[2]Ashok M Krishnapillai,K D Anthony Taylor,Anne E J Morris.Characterisation of Norway lobster(Nephrops norvegicus)hyaluronidase and comparison with sheep and bovine testicular hyaluronidase[J].Food Chemistry,1999,65:515-521.
[3]Andrea C Pessini,Tania T Takao,Elisangela C Cavalheiro,et al.A hyaluronidase from Tityus serrulatus scorpion venom:isolation,characterization and inhibition by flavonoids[J].Toxicon,2001,39:1495-1504.
[4]Luo Feng,Rong Gao,Ponnampalam Gopalakrishnakone.Isolation and characterization of a hyaluronidase from the venom of Chinese red scorpion Buthus martensi[J].Comparative Biochemistry and Physiology,2008,148:250-257.
[5]Gmachl M,Kreil G.Bee venom hyaluronidase is homologous to a membrane protein of mammalian sperm[J].Proceedings of the National Academy of Sciences USA,1993,90:3569-3573.
[6]K S Girish,R Shashidharamurthy,S Nagaraju,et al.Isolation and characterization of hyaluronidase a“spreading factor”from Indian cobra(Naja naja) venom[J].Biochimie,2004,86:193-202.
[7]徐洵,王贤舜,席杏团,等.尖吻蝮(Agkitrodon aeutus)蛇毒的研究[J].生物化学与生物物理学报,1983,15(6):577-582.
[8]Karla C F Bordon,Márcio G Perino,José R Giglio,et al.Isolation,Enzymatic Characterization and Action as Spreading Factor of a Hyaluronidase from Crotalus durissus terrificus Snake Venom[J].Toxicon,2012,60:197.
[9]Marta R Magalhaes,Nelson Jorge da Silva Jr,Cirano J Ulhoa.A hyaluronidase from Potamotrygon motoro(freshwater stingrays)venom:Isolation and characterization[J].Toxicon,2008,51:1060-1067.
[10]Ana Isabel da C B Gouveia,Rafael B da Silveira,Helena B Nader,etal.Identification and partialcharacterisation of hyaluronidases in Lonomia obliqua venom[J].Toxicon,2005,45:403-410.
[11]李丹,郭育涛,杨永利,等.牛睾丸中透明质酸酶提取工艺研究[J].应用化工,2011,40(8):1417-1429.
[12]Batista C V,Roman-Gonzalez S A,Salas-Castillo S P,et al.Proteomic analysis of the venom from the scorpion Tityus stigmurus:Biochemical and physiological comparison with other Tityus species[J].Comparative Biochemistry and Physiology,2007,146:147-157.
[13]Morey S S,Kiran K M,Gadag J R.Purification and properties of hyaluronidase from Palamneus gravimanus(Indian black scorpion)venom[J].Toxicon,2006,47:188-195.
[14]Kudo K,Tu A T.Characterization of hyaluronidase isolated from Agkistrodon contortrix contortrix(Southern Copperhead)venom[J].Archives of Biochemistry and Biophysics,2001,386:154-162.
[15]Mayumi Ikegami-Kawai,Tomoko Takahashi.Microanalysis of hyaluronan oligosaccharides by polyacrylamide gel electrophoresis and its application to assay of hyaluronidase activity[J].Analytical Biochemistry,2002,311:157-165.
[16]王学奎.植物生理生化实验原理和技术[M].北京:高等教育出版社,2006:190-192.
[17]王文婷,韩玲,田甲春,等.牦牛肉组织蛋白酶L酶学特性的研究[J].食品工业科技,2012,33(15):141-144.
[18]Ikuko Kakizaki,Isoshi Nukatsuka,Keiichi Takagaki.Effects of divalent cations on bovine testicular hyaluronidase catalyzed transglycosylation of chondroitin sulfates[J].Biochemical and Biophysical Research Communications,2011,406:239-244.
[19]Yang C-H,Srivastava P N.Purification and properties of hyaluronidase from bull sperm[J].Journal of Biological Chemistry,1975,250(1):79-83.
