不同剂量甲氨蝶呤联合放疗治疗原发性中枢神经系统淋巴瘤疗效分析
2012-12-29代荣钦
代荣钦 时 杰
河南省人民医院 1)中心ICU 2)血液科 郑州 450003
原发性中枢神经系统淋巴瘤(primary central nervous system lymphoma,PCNSL)是原发于脑、脊髓和脑脊膜的高度恶性的非霍奇金淋巴瘤,占颅内原发肿瘤的3%~5%[1]。多数病理表现为B细胞来源的非霍奇金淋巴瘤,颅内病灶多发,影像学形态多样。PCNSL在免疫功能正常的人群中发病率有上升趋势。发病年龄也趋于年轻化。现有的治疗方案总体疗效并不理想。近年来大量的研究证明大剂量甲氨蝶呤为基础的化疗方案可明显改善患者预后[1-2]。但大剂量甲氨蝶呤的最合适剂量尚未统一。本研究收集25例PCNSL患者,探讨不同剂量甲氨蝶呤的治疗效果及不良反应。
1 对象与方法
1.1 一般资料 2000-01—2010-06我科治疗的 PCNSL患者25例,男14例,女11例;平均47.5岁。所有患者均无免疫缺陷、器官移植及免疫功能低下等,HIV抗体均为阴性。
1.2 临床表现 所有患者均存在不同程度的头痛、恶心、呕吐、视盘水肿等颅内压增高症状,局灶性神经系统损害包括:肢体活动障碍14例,失语2例,共济失调4例,记忆力减退3例,意识障碍2例。
1.3 影像学检查 患者均行CT及MRI检查。其中单一病灶15例,≥2个病灶10例;CT平扫示等密度或稍高密度病变,病变周围脑组织水肿较轻,强化后多呈均匀密度增强。MRI显示T1为低信号到等信号,T2为等信号到高信号,多数呈类圆形或圆形,明显均一强化。
1.4 病理检查及脑脊液细胞学检查 术中可见肿瘤呈灰白色或灰红色鱼肉状,血供丰富,出血坏死少见,与周边正常组织边界不清。术后病理:多为B细胞来源的非霍奇金淋巴瘤,其中弥漫大B细胞淋巴瘤22例,前B淋巴母细胞淋巴瘤2例,T淋巴母细胞淋巴瘤1例。25例患者均行腰椎穿刺取脑脊液行脱落细胞检查,8例患者可找到肿瘤细胞。可疑者3例,脑脊液生化检查发现蛋白增高18例。经体检、胸部CT、腹部CT及B型超声检查、浅表淋巴结B型超声等检查未发现中枢神经系统以外的病灶,骨髓穿刺均正常。
1.5 治疗 患者行次全切除或部分切除肿瘤9例,行立体定向活检术16例。明确诊断后转入我科化疗。A组11例接受1g/m2甲氨蝶呤方案化疗,持续24h静滴;B组14例接受3g/m2甲氨蝶呤方案化疗,持续24h静滴。均在甲氨蝶呤输注前给予水化碱化尿液,静脉输液1 500~2 000mL,静滴5%碳酸氢钠200mL。甲氨蝶呤结束后12h起,给予亚叶酸钙解救。每3周重复1次,共进行6~8个周期。化疗后定期检测血常规、肾功能、电解质及甲氨蝶呤血药浓度。外周血中性粒细胞≤0.5×109/L时,每日皮下注射重组人粒细胞集落刺激因子5μg/kg至中性粒细胞恢复至正常值。血小板低于20×109/L或有出血征象时,给予输注血小板及止血药物应用,血红蛋白低于80g/L或有乏力、心悸、耳鸣等症状时,给予红细胞输注。粒细胞缺乏期间并发感染的,给予广谱抗生素抗感染。出现严重的非血液学不良反应或持续较长时间的Ⅳ度骨髓抑制时,推迟下周期化疗,直至白细胞和血小板基本恢复后进行。全程化疗结束后序贯全脑放疗,剂量36Gy,每次2Gy,每周5次。如有病灶残余,局部增加放射10Gy。
1.6 疗效评价 所有患者均随访至2011-12,全部治疗结束后即行评效。按文献[3]行疗效评定:完全缓解(CR):MRI对比增强上的病灶完全缺失,或MRI对比增强上病灶直径<5mm;部分缓解(PR):对比增强上病灶较治疗前缩小50%以上,且达不到完全缓解的标准;稳定(SD):病灶较治疗前缩小25%~49%;进展(PD):病灶较治疗前缩小<25%,或出现新的病灶。
1.7 不良反应评价标准 甲氨蝶呤的主要不良反应包括过敏反应、骨髓抑制、肝肾毒性及皮肤黏膜病变。本研究采用WHO抗肿瘤药毒性分析标准评价血液学、泌尿系统及消化系统毒性。
1.8 统计学处理 计量资料正态性分布用均数±标准差表示,组间比较采用t检验。计数资料采用χ2检验或成组设计两样本比较的秩和检验。2组生存曲线比较采用Log-Rank检验。P<0.05为差异有统计学意义。
2 结果
2.1 临床疗效 治疗结束时A组完全缓解4例,部分缓解4例,稳定2例,进展1例;中位生存期16个月。B组化疗后完全缓解8例,部分缓解3例,稳定2例,进展1例;中位生存期17.22个月。2组治疗后完全缓解率分别为36.36%、57.14%,差异有统计学意义(P<0.05)。B组中位生存期略长于A组,但2组生存曲线无明显差异(P=0.411)。见图1。
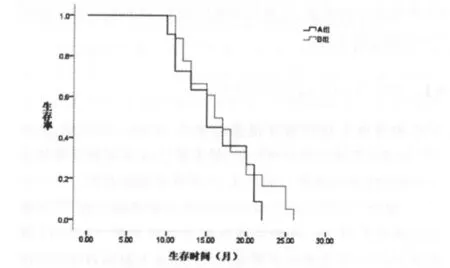
图1 A组(1g/m2甲氨蝶呤)与B组(3g/m2甲氨蝶呤)患者生存曲线
2.2 不良反应 比较骨髓抑制、肌酐、尿素氮变化、谷丙转氨酶升高情况。结果显示B组骨髓抑制作用较强,但在肝肾功能损害方面,2组差异无统计学意义(P>0.05)。2组患者均顺利完成大剂量甲氨蝶呤化疗,无因化疗死亡病例。见表1。
3 讨论
PCNSL起病快,临场表现及辅助检查缺乏特异性,易误诊,与其他结外非霍奇金淋巴瘤相比,治疗总有效率低,生存期短[4]。PCNSL患者使用单纯放疗短期有效率高,但复发率也高,并不能延长生存期,且放疗的远期并发症为白质脑病,可造成患者痴呆、肢体活动障碍。PCNSL对化疗敏感,虽然CHOP方案是治疗非霍奇金淋巴瘤的标准方案,但因环磷酰胺、阿霉素及长春新碱不能透过血脑屏障,因此对PCNSL仅有短期效果,并不能延长生存期。近年来,大量研究证实大剂量甲氨蝶呤为基础的化疗方案,联合WBRT或单独使用可以明显改善患者预后。可能与该药可以较好透过血脑屏障进入肿瘤组织中杀灭肿瘤细胞有关。Gerstner等[5]报道应用大剂量甲氨蝶呤为基础的联合化疗能提高PCNSL的3a存活率至76%,总生存期为71个月。但这种以大剂量甲氨蝶呤为基础的联合化疗有可能产生严重的神经毒性。大剂量甲氨蝶呤的最合适剂量未得到统一。西方国家剂量范围一般在3~8g/m2,2010年美国癌症综合网(National Comprehensive Cancer Network,NCCN)临床实践指南推荐最有效治疗PCNSL的大剂量甲氨蝶呤剂量为≥3.5g/m2,而日本的研究认为甲氨蝶呤剂量≥1g/m2即可发挥有效的治疗作用[6]。
Uhm等[7]回顾性分析了72例新近确诊的PCNSL患者,给予大剂量甲氨蝶呤单药化疗。一组应用1g/m2,一组甲氨蝶呤剂量为3.5g/m2。2组总生存率(OS)及无进展生存率(PFS)差异无统计学意义,但增加甲氨蝶呤剂量可明显提高CR/CRu率。本研究比较1g/m2和3g/m2不同剂量甲氨蝶呤的化疗效果。更大剂量的甲氨蝶呤应用后可达更高的CR率(57.14%vs 36.36%),差异有统计学意义。但2组中位生存期无明显差别。与Uhm等研究结果一致。不良反应方面,加大甲氨蝶呤的剂量,骨髓抑制有所加重,但GCSF应用后均可恢复正常,未观察到严重的感染、出血情况。而肝肾功能损害并无明显加重。
目前,大剂量甲氨蝶呤是治疗PCNSL最有效的单一化疗方法。增加甲氨蝶呤的剂量可进一步提高短期疗效,达到更高质量的缓解。本研究14例PCNSL患者给予大剂量甲氨蝶呤联合放疗均未出现严重不良反应,且无死亡。提示本方案疗效及安全性均较好,大剂量甲氨蝶呤联合放疗是治疗PCNSL的首选方案。
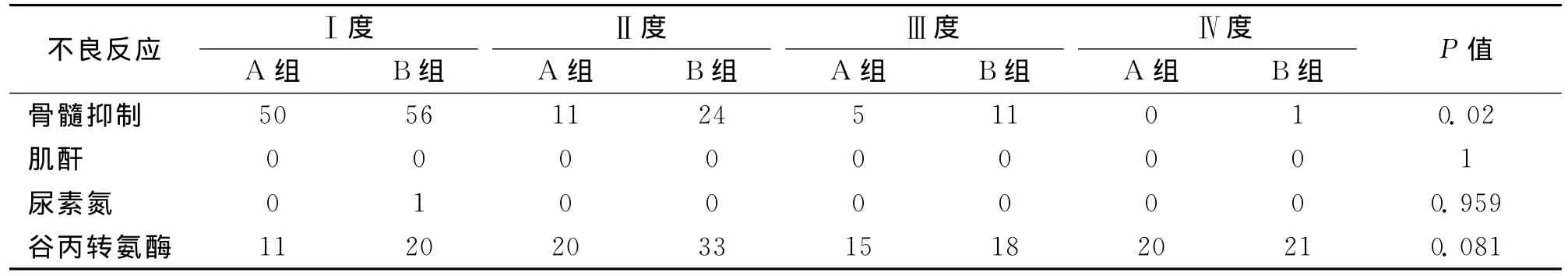
表1 大剂量甲氨蝶呤方案化疗后患者不良反应比较 (A组66例次,B组92例次)
[1]Gerard LM,Imrie KR,Mangel J,et al.High-dose methotrexate based chemotherapy with deferred radiation for treatment of newly diagnosed primary central nervous system lymphoma[J].Leuk Lymphoma,2011,52:1 882-1 890.
[2]Hashemi-Sadraei N,Peereboom DM.Chemotherapy in newly diagnosed primary central nervous system lymphoma[J].Ther Adv Med Oncol,2010,2:273-292.
[3]Schlegel U,Jürgens A,Pels H,et al.Primary central nervous system lymphomas(PCNSL):MRI response criteria revised[J].Neurology,2006,66(8):1 287-1 288.
[4]Muta D,Makino K,Nakamura H,et al.Inhibition of EIF4E phosphorylation reduces cell growth and proliferation in primary central nervous system lymphoma cells[J].J Neurooncol,2011,101:33-39.
[5]Gerstner ER,Carson KA,Grossman SA,et al.Long-term outcome in PCNSL patients treated with high-dose methotrexate and deferred radiation[J].Neurology,2008,70:401-402.
[6]Shibamoto Y ,Ogino H,Suzuki G.Primary central nervous system lymphoma in Japan:changes in clinical features treatment,and prognosis during 1985-2004[J].Neuro Oncol,2008,10:560-568.
[7]Uhm JE,Kim KH,Yi SY,et al.A retrospective study to compare two methotrexate-based regimens for primary central nervous system lymphoma[J].Leuk Lymphoma,2009,50(7):1 110-1 118.
