交联壳聚糖对牛血清蛋白的吸附及释放行为
2012-12-05禹雪晴荆迎军夏文晨杨景涛
刘 麒,禹雪晴,荆迎军,夏文晨,杨景涛
(河北工业大学化工学院,天津300130)
目前,我国对工业废水的处理越来越重视,其中食品工业废水的排放量较大,废水中含有大量的蛋白质等营养物质,直接排放不仅对环境造成污染,也造成了有用物质的浪费[1],所以对废水中蛋白类物质的去除和回收成为研究热点之一。吸附法由于具有工艺简单、投资少和不易产生二次污染等特点[2],比较适合废水中蛋白质的去除和回收,而吸附法的关键问题之一就是筛选高效吸附剂。壳聚糖(CTS)是自然界中最丰富的天然聚合物之一,具有良好的生物降解性、生物相容性、无毒无害[3]。由于其独特的分子结构,在环保、生物和医用等行业具有良好的应用价值,有望成为蛋白类废水的生物吸附剂之一。酸性环境有利于壳聚糖对蛋白质的吸附行为,但在低pH下,壳聚糖易于降解,限制了它的应用。本文以天然高分子壳聚糖为原料,与多聚磷酸钠和环氧氯丙烷通过离子和共价作用改性形成交联壳聚糖(CL-CTS),提高了壳聚糖对低酸体系的耐受度并有利于重复利用[4],在此基础上研究了CL-CTS对蛋白的吸附性能,将为今后壳聚糖在蛋白废水处理方面的应用和研究提供基础理论支持。
1 材料与方法
1.1 材料与仪器
壳聚糖 脱乙酰度为90%,购自天津市久康生物工程开发有限公司;牛血清蛋白(BSA) 购自天津鼎国生物技术有限公司;多聚磷酸钠、环氧氯丙烷、氯化钠等 均为分析纯,购自天津赢达稀贵试剂公司。
722N可见光分光光度计 上海精密科学仪器有限公司;HZS-H水浴振荡器 哈尔滨市东联电子技术开发有限公司;BS 124S电子分析天平 北京赛多利斯仪器系统有限公司。
1.2 实验方法
1.2.1 CL-CTS的制备 将壳聚糖溶于1%的乙酸中配成2.5%的壳聚糖-乙酸溶液,搅拌均匀备用;用注射器依靠自然重力将壳聚糖-乙酸溶液滴落于1%的多聚磷酸钠溶液中,进行初次离子交联反应并成球;4h后用双蒸水将小球洗净并将其放入50mL、1mol/L的NaOH溶液中,加入0.2mL的环氧氯丙烷,在30℃下水浴振荡进行二次共价交联反应,2h后用双蒸水反复洗涤至体系的pH为7.0,即得到CL-CTS。
1.2.2 吸附量和吸附率的测定 在278nm下测定蛋白残余量,然后根据式(1)和式(2)计算吸附量与吸附率。

式中,Q:吸附量,mg/g;η:吸附率,%;C0:BSA的初始浓度,mg/mL;Ce:BSA的平衡浓度,mg/mL;M:CL-CTS 的干重,g;V:溶液的体积,mL。
1.2.3 BSA初始浓度对吸附效果的影响 取1.0g CL-CTS置于pH7.0不同浓度的BSA溶液中,30℃恒温水浴振荡2h后测定CL-CTS对BSA的吸附性能。
1.2.4 CL-CTS用量对吸附效果的影响 取不同用量的CL-CTS置于pH7.0浓度为0.2mg/mL的BSA溶液中,30℃恒温水浴振荡2h后,测定其吸附效果。
1.2.5 pH对吸附效果的影响 称取1.3g CL-CTS置于浓度为0.2mg/mL、不同pH的BSA溶液中,30℃恒温水浴振荡2h后,测定其吸附效果。
1.2.6 吸附条件的优化 在单因素实验基础上,通过正交实验优化BSA初始浓度、CL-CTS用量、pH。正交因素水平见表1。

表1 正交设计因素和水平Table 1 Factors and levels of orthogonal design
1.2.7 吸附等温线的绘制 称取1.3g CL-CTS置于pH5.0、不同浓度的BSA溶液中,一定时间后,测定蛋白的残余量,绘制吸附等温线。
1.2.8 吸附动力学实验 称取1.3g CL-CTS加入到pH5.0、浓度为0.2mg/mL的BSA溶液中,测定不同反应时间后溶液中蛋白的残余量,绘制吸附动力学曲线。
1.2.9 蛋白质的释放及CL-CTS的再利用 在进行解吸处理之前,探讨了离子强度对吸附行为的影响,然后根据此原理,利用一定浓度的中性盐对吸附饱和后的CL-CTS小球进行解吸处理[5]。
2 结果与讨论
2.1 CL-CTS的电镜扫描
壳聚糖的分子链上含有大量的游离氨基和羟基,正因为这些基团的存在,使壳聚糖易于发生交联反应。如图1,壳聚糖与多聚磷酸钠交联内部形成网状结构的笼型分子,加强了壳聚糖的溶胀性以及吸附性能。
2.2 BSA初始浓度对吸附效果的影响

图1 交联壳聚糖的电镜扫描图Fig.1 SEM micrograph of CL-CTS
结果如图2所示,在BSA初始浓度较低的范围内,吸附率呈上升趋势,然后随着浓度的增大,吸附率逐渐降低。在吸附初始阶段,由于壳聚糖的表面积效应和体积效应,并且存在大量的结合位点,导致吸附速率上升较快。然后随着浓度的增大,壳聚糖对蛋白质的吸附达到饱和,吸附率达到最大值后开始下降。

图2 BSA初始浓度对吸附率的影响Fig.2 Effect of BSA concentration on the adsorption rate
2.3 CL-CTS用量对吸附效果的影响
CL-CTS用量对吸附效果的影响见图3。随着壳聚糖用量的增加,吸附率逐渐增大至平衡。这主要是由于CL-CTS用量的增加,分子链中游离的氨基较多,提供了较多的吸附位点,吸附性能大大增加,当吸附达到饱和以后,吸附率趋于平衡。

图3 交联壳聚糖的用量对吸附率的影响Fig.3 Effect of CL-CTS dosage on the adsorption rate
2.4 pH对吸附效果的影响
pH是影响吸附效果的一个重要参数。图4表明,最大平衡吸附率出现在pH5.0附近(BSA等电点),在pH低于或高于BSA的等电点时,由于静电排斥作用,导致吸附率下降。在pH等于BSA的等电点时,蛋白质上没有净电荷,吸附效果最好。
2.5 吸附条件的优化
由以上的结果可知,BSA初始浓度、CL-CTS用量、pH在吸附过程中均起一定的作用。为了确定最佳的工艺操作参数,运用正交实验对吸附体系的影响因素进行分析,结果见表2。

表3 Langmuir,Freundlich方程参数Table 3 Langmuir,Freundlich isotherm constants
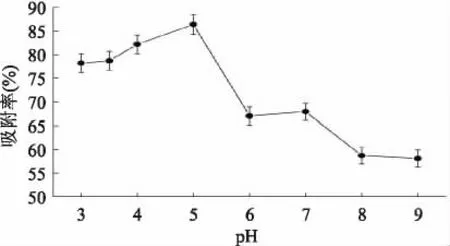
图4 pH对吸附率的影响Fig.4 Effect of pH on the adsorption rate
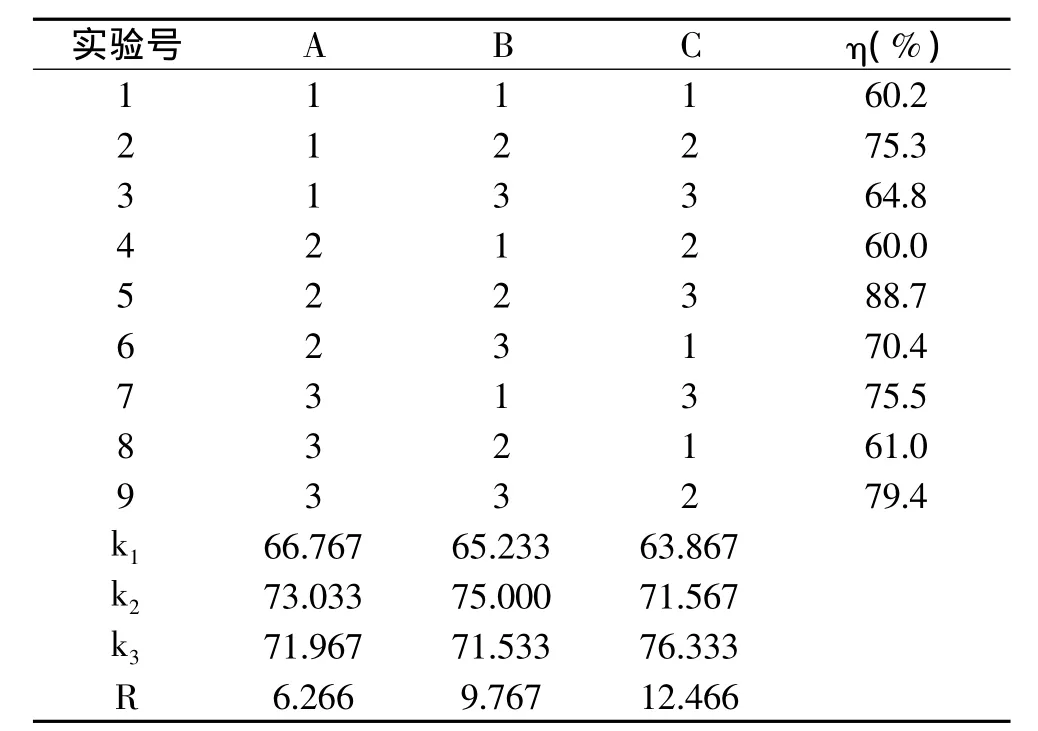
表2 正交实验的结果Table 2 Results of orthogonal experiments
根据统计学原理,极差R可以确定因素对指标影响的大小。极差越大,说明该因素的影响越显著。由表2可知,对BSA吸附效果的影响主次为:pH>CL-CTS用量>BSA初始浓度;正交优化后的最优操作条件为 A2B2C3:BSA的初始浓度为0.2mg/mL,CL-CTS的用量为1.3g,pH5.0,此时吸附率达到88.7%。
2.6 吸附等温线
一定温度下,研究了不同蛋白质浓度对平衡吸附量的影响。随着蛋白质浓度的增大,吸附量在逐渐增大,直至吸附达到平衡。吸附等温线能够进一步描绘吸附剂与被吸附物之间的反应过程,Langmuir和 Freundlich模型常用来表征平衡吸附曲线[6]。
Langmuir等温吸附方程的线性表达式:

式中,C:蛋白质的平衡浓度,mg/mL;Q:平衡吸附量,mg/g;Qe:饱和吸附量,mg/g;b:平衡常数,mL/mg。
Freundlich等温吸附方程的线性表达式:

式中,C和 Q意义同式(3),nF和 kF分别为Freundlich参数。
图5和图6分别为CL-CTS吸附BSA的Langmuir和Freundlich等温吸附曲线,参数见表3。Langmuir模型假设吸附是单分子层的,表面均一且表面吸附能相等。相对 Langmuir模型而言,Freundlich模型更适合描述CL-CTS对BSA的吸附过程,这说明吸附过程接近于多分子层吸附理论,吸附剂的表面是不均一的,交联壳聚糖分子中的每一个吸附位置能够吸附多个蛋白质分子,当所有的吸附位置达到饱和后,吸附达到动态平衡。kF反映体系中可以表征吸附量的大小,nF表示吸附作用的强度,nF>1,说明是优惠吸附,吸附强度较大。

图5 Langmuir等温吸附方程曲线Fig.5 Langmuir adsorption isotherm

图6 Freundlich等温吸附方程曲线Fig.6 Freundlich adsorption isotherm
2.7 吸附动力学
在最优的条件下,进行吸附反应,用得到的相关数据进行动力学方程拟合,可以提供吸附机理的相关信息。明确吸附机理是优化设计和选择正确吸附方法的基础。伪一级动力学模型[7]如下:

式中,Qe、Qt分别为平衡时间和时间t时的吸附量,mg/g;k1:伪一级吸附速率常数,min-1;t:吸附时间,min。
以吸附量随时间变化作曲线,按照伪一级动力学方程进行拟合的R2值比较低(见图7和表4),因而进一步用伪二级动力学方程[8]进行处理,结果见图8和表4。伪二级动力学模型如下:

表4 吸附动力学模型参数Table 4 Adsorption kinetic parameters

式中,k2:伪二级吸附速率常数,g/(mg·min)。
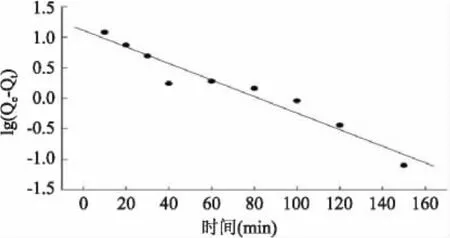
图7 伪一级吸附方程曲线Fig.7 Pseudo-first order plot for adsorption

图8 伪二级吸附方程曲线Fig.8 Pseudo-second order plot for adsorption
由于壳聚糖的分子结构,通常用颗粒扩散速率方程表明吸附速率,能进一步了解吸附作用所涉及到的某些机制和限制因素。颗粒扩散速率方程[9]的表达式为:

式中,ki:颗粒吸附速率常数,mg/(g·min1/2);t:吸附时间,min。
根据颗粒速率方程拟合的图形,如果是一条直线,则表明壳聚糖对蛋白质的吸附过程主要是由内扩散控制的;若是多线性的,则显示有两个或三个阶段影响吸附过程。图9表明了颗粒扩散速率方程的拟合曲线是多线性的,第一阶段代表了大孔隙扩散,速率常数定义为ki,1;第二阶段代表了微孔扩散,速率常数定义为 ki,2。由表 4 可知,ki,1> ki,2,在吸附初期,由于蛋白质的分子量大和空间尺寸分布太宽,蛋白质主要被交联壳聚糖的大孔隙吸附,吸附后期主要在吸附剂微孔内部吸附,扩散阻力逐步增大且浓度推动力越来越小,吸附速率逐渐减缓。在颗粒扩散方程中存在截距,可能的原因之一是由液膜所形成的边界层影响了交联壳聚糖对蛋白质的吸附过程。
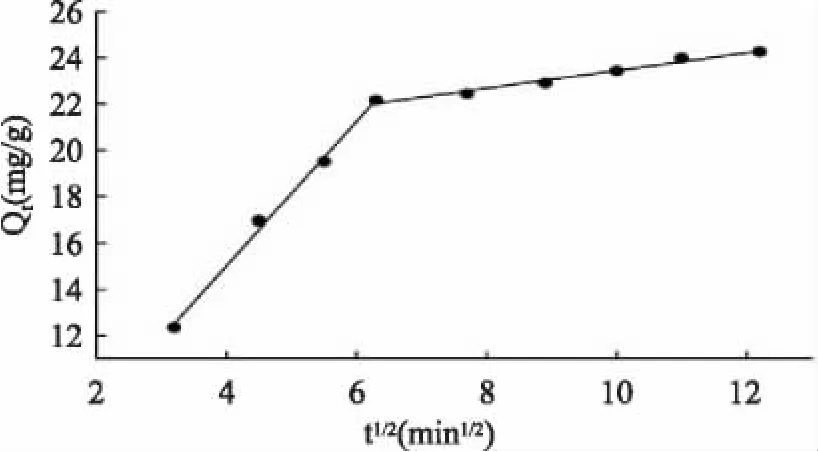
图9 颗粒扩散速率方程曲线Fig.9 Intraparticle diffusion kinetics plot
由表4中的动力学模型参数以及相关系数的数据可以看出伪一级动力学模型的R2相对较低,而伪二级动力学模型的R2较高,达到0.99以上,更能较好地表征交联壳聚糖对蛋白质的吸附行为,且拟合方程计算得出的平衡吸附量Qe与吸附动力学曲线的Qe基本吻合。说明CL-CTS对BSA的吸附主要受化学控制,而不是物质传输步骤控制。
2.8 蛋白质的释放及CL-CTS的再利用
解吸研究对于表明吸附剂与被吸附物之间的稳定性与可再生性至关重要[10]。无机盐离子对CLCTS吸附BSA的过程起抑制作用,随着离子强度的加大,吸附率在逐渐下降,而且在相同的离子强度下,各种离子的抑制吸附效果是不同的(见图10)。这可能是由于离子强度的增加使BSA分子处于较多离子氛围中,增大了静电排斥作用,影响了BSA的分子构象,破坏了壳聚糖分子与BSA分子之间的静电作用力,然后只通过范德华力吸附小部分BSA分子,使得吸附效果呈下降趋势,而且盐离子也可能与壳聚糖分子中的某些基团相结合,使得壳聚糖与BSA分子结合的空间受阻[11]。且由图可知,NaCl对壳聚糖吸附BSA的过程抑制作用较强,更易与壳聚糖分子相结合。因此,选用NaCl作为解吸剂,探讨其对蛋白质的释放行为。

图10 离子强度对吸附率的影响Fig.10 Effect of ionic strength on the adsorption rate
取吸附饱和后的CL-CTS,置于3g/L的NaCl溶液中进行解吸,负载CL-CTS上的蛋白质被释放出来,然后将CL-CTS再次进行吸附BSA的实验,考察重复使用效果,结果见表5。经过4次洗脱周期后,吸附率下降了18.6%,随着重复使用次数的增加,基本维持在这个水平。这表明NaCl对负载牛血清蛋白的壳聚糖洗脱效果较好。

表5 交联壳聚糖的重复使用性Table 5 Reuse of cross-linked chitosan
3 结论
采用多聚磷酸钠和环氧氯丙烷制备的交联壳聚糖,增加了壳聚糖空间网状结构,使电荷更集中,通过静电引力提高了吸附能力。通过对吸附条件的优化,在pH5.0,交联壳聚糖的用量为1.3g,BSA的初始浓度为0.2mg/mL时,吸附率可达到88.7%,吸附过程可用伪二级动力学模型来描述,并符合Freundlich等温吸附模型。NaCl溶液对负载蛋白的CL-CTS洗脱效果较好,可以达到循环利用的效果。因此,壳聚糖作为一种功能材料,探索其在食品工业废水处理中的应用,具有十分广阔的应用前景。
[1]董海丽,任晓燕.磁性壳聚糖微球对大豆乳清废水中蛋白质的吸附作用[J].食品科学,2007,28(7):205-207.
[2]Dalida MLP,Mariano AFV,Futalan CM,et al.Adsorptive removal of Cu(II)from aqueous solutions using non-crosslinked and crosslinked chitosan- coated bentonite beads[J].Desalination,2011,275:154-159.
[3]张宾,张莉,于丽娜,等.固定化胰蛋白酶壳聚糖树脂的制备及其对大豆胰蛋白酶抑制剂的吸附性[J].食品工业科技,2007,28(7):65-68.
[4]Eric G.Interactions of metal ions with chitosan-based sorbents:a review[J].Sep Purif Technol,2004,38:43-74.
[5]辛梅华,李明春,苏丽政,等.修饰壳聚糖微球用于含蛋白废水处理研究[J].环境科学与技术,2010,33(2):161-164.
[6]孟范平,李永富,周游,等.EGDE交联的载镧壳聚糖微球对氟离子的静态和动态吸附[J].化工学报,2011,62(11):3192-3200.
[7]Ho YS,Mckay G.Kinetic models for the sorption of dye from aqueous solution by wood[J].Trans IChemE,1998,76:183-191.
[8]Sarkar M,Majumdar P.Application of response surface methodology for optimization of heavy metal biosorption using surfactant modified chitosan bead[J].Chem Eng J,2011,175:376-387.
[9]Singh SK,Townsend TG,Mazyck D,et al.Equilibrium and intra-particle diffusion of stabilized landfill leachate onto microand meso- porous activated carbon[J].Water Res,2012,46:491-499.
[10]Ozay O,Ekici S,Baran Y,et al.Removal of toxic metal ions with magnetic hydrogels[J].Water Res,2009,43:4403-4411.
[11]Zhang J,Zhang Z,Song Y,et al.Preparation of Cibacron Blue F3GA attached chitosan microspheresand theiradsorption properties for bovine serum album[J].Chemical Journal of Chinese Universities,2005,26:2363-2368.
