玻璃体腔注射替考拉宁对正常兔眼视网膜的影响
2012-11-25毛理纳杜楠楠胡新辉
毛理纳,杜楠楠,罗 予,孙 爽,刘 娜,胡新辉
(1.河南卫生职工学院;2.郑州大学 基础医学院;3.郑州大学 医药科学研究院;4.郑州大学 第一附属医院;5.郑州市第一人民医院,河南 郑州451191)
替考拉宁、万古霉素与去甲万古霉素等属于糖肽类抗生素。替考拉宁在临床主要用于治疗各种严重革兰阳性菌感染性疾病,尤其治疗耐甲氧西林金黄色葡萄球菌(Meticillin-resistant Staphylococcus Aureus,MRSA)等耐药菌引起的感染。替考拉宁的抗菌谱与万古霉素基本一致,体外抗菌试验对大多数革兰阳性菌(如葡萄球菌、链球菌等常见致病菌)均呈现强抗菌活性,受试菌的MIC50在0.06 ~4 mg·L-1[1]。目前替考拉宁的眼内用药情况国内外鲜有报道。本研究通过动物实验,观察玻璃体腔注射替考拉宁对正常兔眼视网膜的毒性作用。
1 材料与方法
1.1 实验动物 24 只健康日本大耳白兔,均无眼疾,体质量2.5 ~3 kg,雌雄各半,由河南康达实验动物有限公司提供,动物许可证号:SCXK(豫)2011-0001。
1.2 实验药品 加立信(注射用替考拉宁:浙江医药股份有限公司新昌制药厂,批号:100720),戊巴比妥钠(国药集团化学试剂有限公司,批号:Lot.No.F20060331),硫酸阿托品眼膏(上海通用药业股份有限公司,批号:100204),倍诺喜(盐酸奥布卡因滴眼液:参天制药株式会社,批号:B0998)。
1.3 实验方法 实验动物随机分为4组,A组:替考拉宁0.5 mg/0.1ml ,B组:替考拉宁1.0 mg/0.1 ml ,C组:替考拉宁2.0 mg/0.1 ml,D组(对照组):灭菌生理盐水0.1 ml。每组6 只,均以右眼为实验眼。硫酸阿托品眼膏充分扩瞳,以50 g·L-1戊巴比妥钠按0.4 ~0.5 ml·kg-1耳缘静脉麻醉,无菌生理盐水冲洗结膜囊,盐酸奥布卡因滴眼液表面麻醉后,裂隙灯和检眼镜检查所有兔眼前、后节均正常,常规眼科消毒,暴露兔眼颞上方巩膜,以带有27 号针头的一次性1 ml 注射器于角巩膜缘后3 mm 经睫状体平坦部入针,注药前先抽取玻璃体液0.1 ml 以保持眼压平衡。
1.4 观察指标 注射后即刻、1、2、3、7、14、28 d 用裂隙灯、直接检眼镜观察各组实验眼眼前节及眼后节变化情况。眼前节检查注意结膜有无充血;角膜表面是否光滑,有无浑浊、水肿等;巩膜有无充血,隆起等;前房有无渗出、浑浊;虹膜有无缺失、渗出、前后粘连等;瞳孔是否对称、边缘是否整齐,对光反射是否正常;晶状体是否透明等。眼后节检查注意观察玻璃体有无混浊、液化、积血及视网膜有无水肿、渗出、出血、脱离等。注射后第14、28 d 从各组中分别随机选取3 只动物用戊巴比妥钠行全身麻醉后摘除眼球再以过量戊巴比妥钠处死动物,取出的眼球标本立即放入眼球混合固定液固定,48 h 后常规脱水,石蜡包埋、切片,HE 染色后在光学显微镜下观察视网膜组织结构的病理变化。
2 结果
2.1 眼前节检查 注射后各观察点A组、B组和D组各实验眼眼前节均未见明显异常改变,C组实验眼(2 眼/6 眼)注药后1 d 可见结膜轻度充血,角膜轻度水肿,之后症状逐渐减轻,注药后7 d 基本恢复正常。
2.2 眼后节检查 注射后1、2 d 各组兔眼均可见药物注射局部的玻璃体轻度混浊,之后玻璃体混浊逐渐吸收。C组玻璃体混浊情况较对照组及替考拉宁其他剂量组严重,注射后7 d 灰白色团块状混浊明显,注射后14、28 d 玻璃体混浊渐减轻,并伴有不同程度的视网膜出血。
2.3 视网膜组织病理学切片检查 A组、D组视网膜标本在注射后14 d 和28 d 均显示正常组织结构。B组注药后第14 d 神经纤维层水肿、增厚,神经节细胞轻度水肿,内外核层轻度紊乱,其余结构大致正常,出现极少量炎性细胞;注药后第28 d 内外核层紊乱及神经节细胞水肿情况基本恢复正常,感光细胞受损较第14 d 重,较C组第28 d 的病变轻。C组注药后第14 d 神经纤维层水肿,神经节细胞肿胀,内网状层肿胀,内外核层细胞数量减少,排列紊乱,细胞间界限不清,有炎细胞浸润;注药后第28 d 视网膜损伤加重,各层组织界限不清,大量细胞坏死、细胞结构破坏,部分已缺失,可见炎细胞浸润。见图1。
3 讨论
药物玻璃体腔注射可以避免血眼屏障的阻碍,使药物直接到达炎症部位,抑制细菌生长繁殖或杀灭细菌,一般小剂量药物就可达到最低抑菌浓度,不仅提高疗效,还可以降低全身毒性反应,所以玻璃体腔注射抗菌药物成为治疗细菌性眼内炎的重要给药途径[2-3],但视网膜是代谢旺盛的神经组织,对各种致病因子及外来理化因素刺激的抵抗力较弱,因此,采用玻璃体腔注射药物时必须考虑到药物的安全剂量,以防止因药物剂量选择不当,导致视网膜毒性产生而影响视功能。
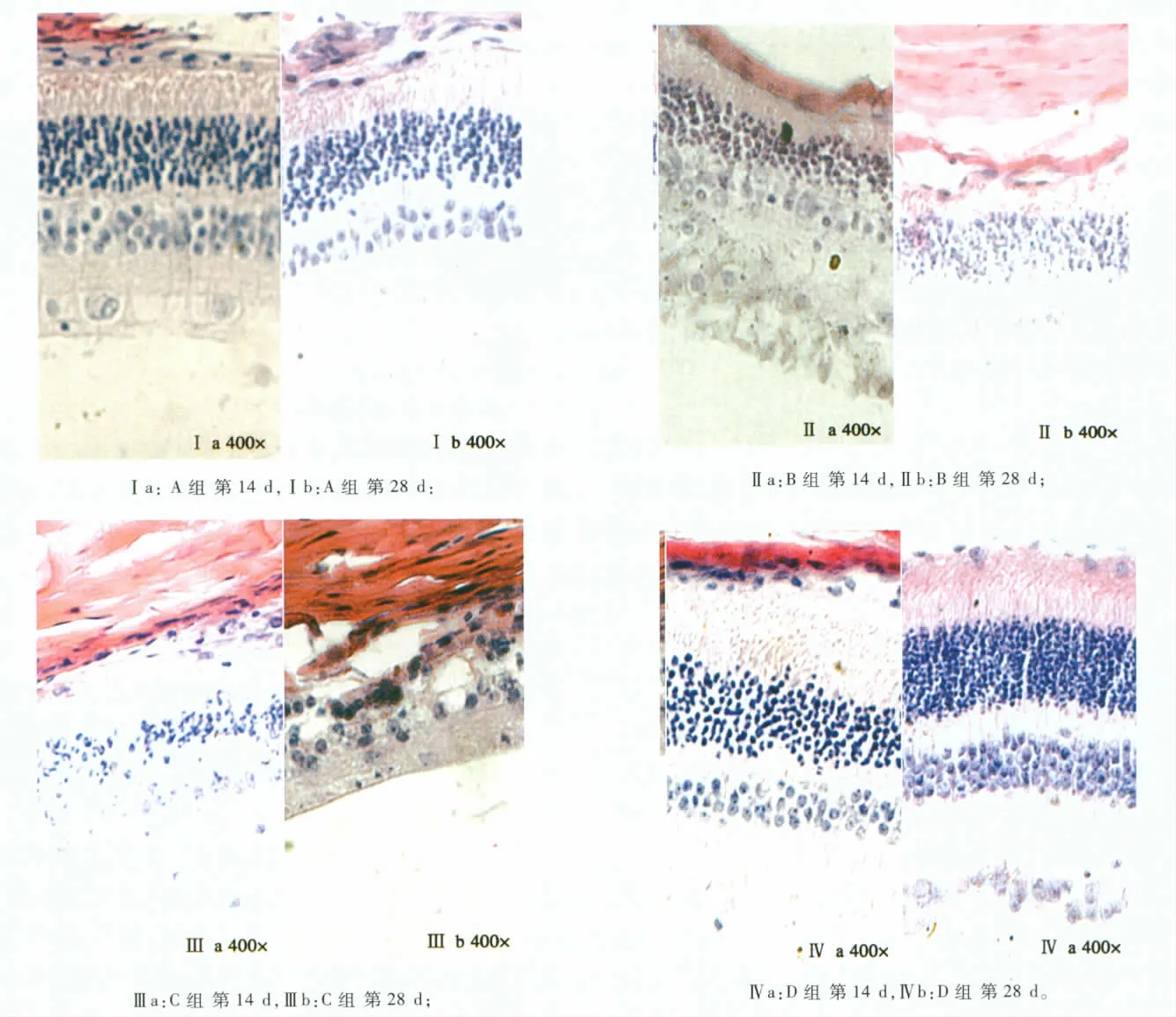
图1 注射后14 d 和28 d 的视网膜光学显微镜检查结果(HE 400 ×)
替考拉宁作为新型糖肽类抗菌药物,分子结构和疗效与万古霉素相似,而不良反应少于万古霉素。目前替考拉宁主要以全身用药为主,其不良反应包括使用替考拉宁的患者可能出现皮疹、红斑、瘙痒等变态反应,局部疼痛、血栓性静脉炎等,部分患者表现为肝肾功能和中枢神经系统损害[4-5],眼局部用药报道很少。Carney 等观察到,兔玻璃体腔注射替考拉宁0.75 mg/0. 1 ml 对视网膜基本无毒性[6]。Homer 等观察了万古霉素对有晶体的白化兔视网膜的毒性,认为小于1 mg 是没有毒性的[7]。Pflugfelder 等用兔眼进行对万古霉素玻璃体内注射的安全剂量实验研究时,发现玻璃体腔内注射2.0 mg 是没有毒性的,小于2.0 mg 是安全剂量,而5.0 mg 则会对视网膜的色素上皮细胞及感光层产生不可逆的损害,应谨慎使用[8]。常青等发现兔眼玻璃体内注射1.6 mg 去甲万古霉素(相当于2 mg 万古霉素)后,在电镜下视网膜有轻微的改变,并且仅局限于内层的神经节细胞,表现为线粒体肿胀、空泡化、峪消失、高尔基体和溶酶体数量增加[9]。该实验发现,玻璃体腔注射替考拉宁14 d 和28 d 后,随药物剂量加大对视网膜的损害作用增加。0.5 mg 未见视网膜毒性,1.0 mg 时可引起较轻的视网膜毒性,2.0 mg 时可引起视网膜组织结构明显改变,28 d 的病理变化大于14 d,各层细胞皆有不可逆性损伤,且有炎细胞浸润。
目前眼内炎的致病菌主要为革兰阳性菌,万古霉素为细菌性眼内炎早期治疗的首选药物[10-12]。随着万古霉素的大量使用,多数监测数据显示:细菌对万古霉素的敏感性随着时间的变化而逐渐降低。万古霉素对耐甲氧西林金黄色葡萄球菌(MRSA)的体外MIC 值则逐渐增加,导致万古霉素对MRSA 感染的临床疗效有所降低[13-15],应用受到限制。
在先前对替考拉宁眼内药动学过程的研究中,发现0.5mg/0.1ml 替考拉宁在玻璃体腔给药后能迅速达到最大药物浓度(358.47 ±21.53)g·L-1,且能在玻璃体腔内获得较长时间的药物治疗浓度,192 h 时仍高于替考拉宁对眼内炎常见革兰阳性球菌的体外MIC(0.06 ~1.00)mg·L-1[16]。玻璃体腔注射替考拉宁0.5 mg/0.1ml 对于治疗细菌性眼内炎应该是既安全又有效的剂量。替考拉宁疗效确切,用药剂量小,不良反应轻,所以在眼内炎治疗中具有良好的临床应用前景。
有关替考拉宁在眼内的其他研究还有待进一步深入,如观察电镜下各剂量替考拉宁对视网膜组织细胞的损伤及其对视网膜功能的影响,不同剂量的替考拉宁在不同给药方式下对正常以及炎症状态下眼内的免疫抑制微环境产生的影响等。
[1]张淑华,欧真容.国产替考拉宁体内外抗菌作用研究[J].中国抗生素杂志,2003,28(1):39 -44.
[2]Callegan MC,Engelbert M,Parke DW,et al. Bacterial endophthalmitis. epidemiology,therapeutics,and bacterium-host interactions[J].Clin Microbiol Rev,2002:15(1):111 -124.
[3]Fintak DR,Shah GK,Blinder KJ,et a1. Incidence of endophthalmitis related to intravitreal injection of bevacizumab and ranibizumab[J].Retina,2008,28(10):1 395 -1 399.
[4]赵 博,陈 取,杜志成,等.万古霉素、替考拉宁、利奈唑胺达托霉素对耐甲氧西林金黄色葡萄球菌抗菌活性及药物优弊的研究[J].中国实用医药,2011,6(18):242 -243.
[5]Wilson AP.Comparative safety of teicoplanin and vancomycin[J].Int J Antimicrob Agents,1998,10(2):143 -152.
[6]Carney M,Kao G,Peyman GA,et al. The intraocular penetration and retinal toxicity of teicoplanin[J]. Ophthalmic Surg,1988,19(2):119 -123.
[7]Homer P,Peyman GA,Koziol J,et al.Intravitreal injection of vancomycin in experimental staphylococcal endophthalmitis[J]. Acta Ophthalmol,1975,53(3):311 -320.
[8]Pflugfelder SC,Hernández E,Fliesler SJ,et al. Intravitreal vancomycin. Retinal toxicity clearance,and interaction with gentamicin[J].Arch Ophthalmol,1987,105(6):831 -837.
[9]常 青,王文吉.国产盐酸去甲万古霉素的视网膜毒性[J].中华眼底病杂志,1997,13(3):138.
[10]Benz MS,Scott IU,Flynn HW Jr,et a1. Endophthalmitis isolates and antibiotic sensit - ivities:a 6-year review of culture-proven cases[J].Am J Ophthalmol,2004,137(1):38 -42.
[11]Donahue SP,Kowalski RP,Eller AW,et al.Empiric treatment of endophthalmitis. Are aminoglycosides necessary[J]. Arch ophthalmol,1994,112(l):45 -47.
[12]贾亚丁,高晓红,刘 芳,等. 玻璃体切除联合球内注入万古霉素+丁胺卡那霉素治疗眼内炎[J]. 中国药物与临床,2002,2(6):372 -373.
[13]Macclayton DO,Suda KJ,Coval KA,et al. Case-control study of the relationship between MRSA bacteremia with a vancomycin MIC of 2 μg/mL and risk factors,costs,and outcomes in inpatients undergoing hemodialysis[J]. Clin Ther,2006,28:1 208-1 216.
[14]Moise-Broder PA,Sakoulas G,Eliopoulos GM,et al. Accessory gene regulator group II polymorphism in methicillin - resistant Staphylococcus aureus is predictive of failure of vancomycin therapy[J].Clin Infect Dis,2004,38(2):1 700 -1 705.
[15]Sakoulas G,Moise-Broder PA,Schentag JJ,et al. Relationship of MIC and bactericidal activity to efficacy of vancomycin for treatment of methicillin - resistant Staphylococcus aureus bacteremia[J].J Clin Microbiol,2004,42:2 398 -2 402.
[16]蔡木禹,林朝仙,黄雯雯. 利奈唑胺、替考拉宁和万古霉素等抗菌药物对常见需氧革兰阳性球菌的体外抗菌活性[J]. 海峡药学,2009,21(10):98 -101.
