盐酸曲马多缓释滴丸兔体内药动学研究*
2012-10-22智成芳姜言丽曲韵智
智成芳,姜言丽,曲韵智,景 舒
(1.内蒙古医学院药学院,呼和浩特 010110;2.北京正大绿洲制药有限公司,北京 101113)
1 仪器与试药
1.1 仪器 Alltech 426型泵(Alltech,美国);UVIS 200型检测器(Alltech,美国);Allchrom Plus色谱工作站(Alltech,美国);液体涡流混合器(江苏海门市麒麟医用仪器厂);微量定量移液器(Brand,德国);奥立龙868型酸度计(Thermo Orion,美国);BP211D型电子分析天平(Sartorius,德国);SHB-Ⅲ型循环水式真空泵(郑州长城科工贸有限公司)。
1.2 试药 盐酸曲马多缓释滴丸(北京正大绿洲制药有限公司);盐酸曲马多片(石药集团欧意药业有限公司);盐酸曲马多对照品(中国药品生物制品鉴定所,批号200503);氧氟沙星对照品(中国药品生物制品鉴定所,批号200403);磷酸(分析纯,北京化工厂);三乙胺(北京化工厂);乙腈(色谱纯,Fisher,美国);甲醇(色谱纯,Fisher,美国);乙酸乙酯(分析纯,北京化工厂);正己烷(分析纯,广东汕头市西陇化工厂)。
1.3 实验动物 新西兰白兔(约1~1.5 kg),雄性,由北京大学医学部实验动物部提供,动物合格证号:SCXK京2005-0002。
2 方法与结果
2.1 溶液的配制
2.1.1 盐酸曲马多(Tr)对照液的制备 精密称取Tr对照品25.15 mg于25 ml量瓶中,加水溶解并稀释至刻度,摇匀。精密量取2.5 ml于50 ml量瓶中,加水稀释至刻度,摇匀,作为盐酸曲马多对照液(0.053 mg/ml)。
2.1.2 内标溶液的配制 精密称取氧氟沙星对照品24.72 mg于25 ml量瓶中,加甲醇溶解并稀释至刻度,摇匀。精密量取5 ml于50 ml量瓶中,加甲醇稀释至刻度,摇匀,得内标溶液(0.098 9 mg/ml)。
2.2 色谱条件 色谱柱:Agela C18柱(250 mm×4.6 mm,5 μm);保护柱:Dikma C18柱;流动相:乙腈-0.5%三乙胺水溶液(加磷酸调 pH值至3.5)(22∶78);检测波长:220 nm;流速:1 ml/min。
2.3 血浆样品处理方法 取血浆1 ml,置10 ml具塞离心管中,加入内标物溶液20 μl,涡漩混合0.5 min,加 0.1 mol/L NaOH 溶液 0.5 m l,涡漩混合 1 min,加入乙酸乙酯1 ml和正己烷4 ml,涡旋混合3 min,4 500 r/min离心 10 min,于 - 18 ℃ 冰箱中冷冻 2 h[1,2]。移取有机层置5 ml离心管中,40℃水浴挥干,加100 μl流动相,涡漩混合1 min,取20 μl注入高效液相色谱仪,记录色谱图。
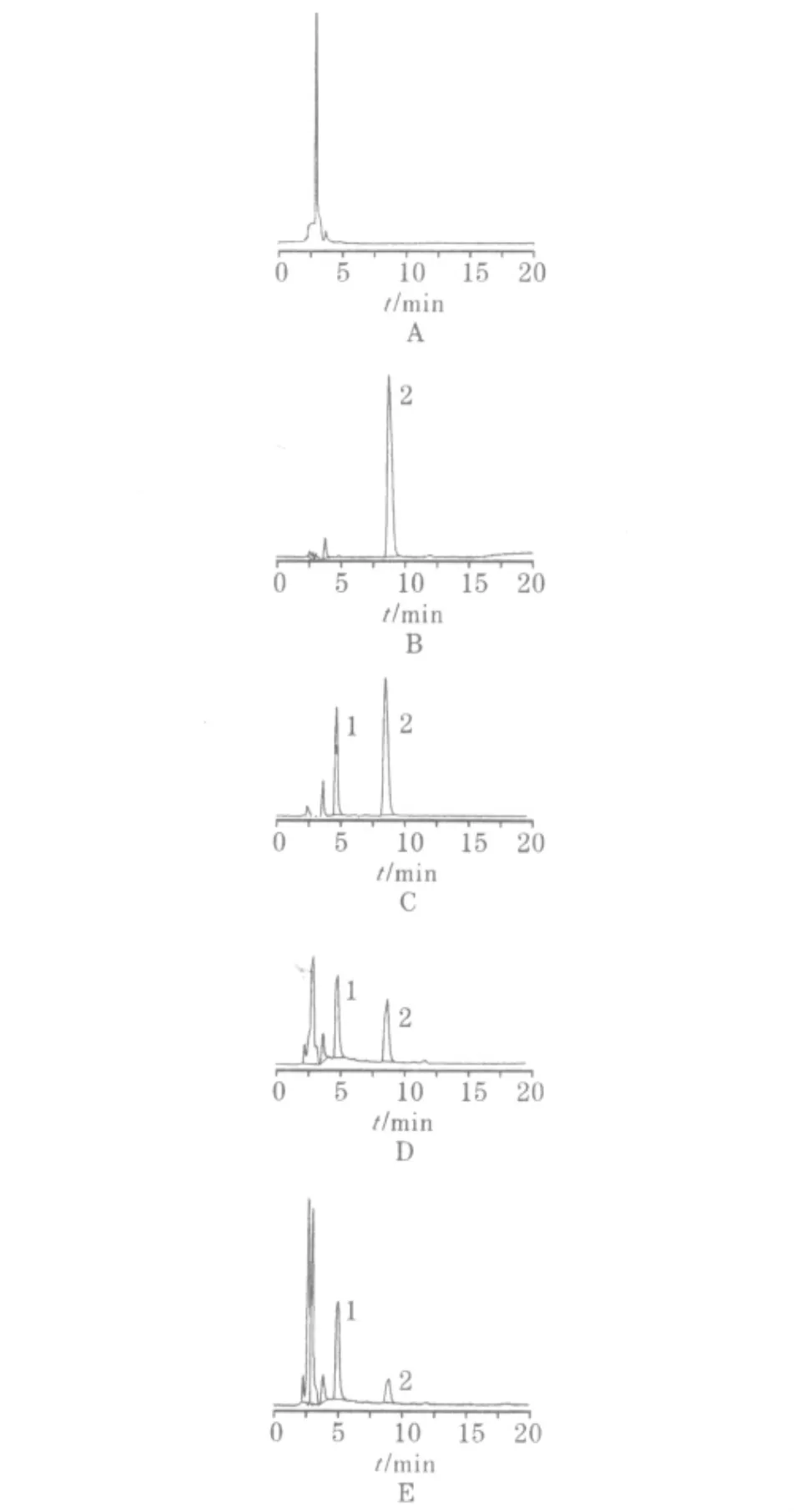
图1 空白血浆(A)Tr(B)Tr+内标(C)空白血浆+Tr+内标(D)血浆样品(E)HPLC图谱
2.4 分离度和专属性 按上述色谱条件进行分析,记录色谱图。Tr、内标及血浆中的内源物分离良好,由图1可知,内标与Tr的保留时间分别为4.983 min和8.833 min。
2.5 标准曲线的制备
2.5.1 溶液标准曲线的制备 分别精密量取Tr对照液 0.1、0.2、0.4、1.0、2.0、4.0 和 8.0 ml于 10 ml量瓶中,各加入内标溶液2 ml,加流动相稀释至刻度,摇匀,进样20 μl,记录色谱图。以Tr浓度为横坐标,以Tr峰面积和内标峰面积之比(A s/A i)为纵坐标,进行线性回归,得标准曲线方程1:
Y=0.027 5 X -0.007 3(r=0.999 8,n=7)
Tr在0.053 ~40.24 μg/ml范围内,浓度与 A s/A i有良好的线性关系。
2.5.2 血浆标准曲线的制备 取空白血浆1 ml于10 ml具塞试管中,加入计算量的Tr对照液,使血浆中药物浓度分别为 20、80、200、400、1 000、2 000 和 4 000 ng/ml,按“血浆样品处理方法”自“加入内标物溶液20 μl”起同法操作,以Tr浓度为横坐标,以Tr峰面积和内标峰面积之比(A s/A i)为纵坐标,进行线性回归,得标准曲线方程2:
Y=0.000 5 X -0.008 6(r=0.998 3,n=7)
结果表明,Tr血药浓度在20~4 000 ng/ml范围内线性关系较好,符合体内测定要求。方法最低检测浓度为20 ng/ml。
2.6 方法学验证
2.6.1 提取回收率 取空白血浆1 ml于10 ml具塞试管中,加入Tr对照液适量,使血浆中药物浓度分别为80、400和2 000 ng/ml,按“血浆样品处理方法”加0.1 mol/L NaOH 溶液 0.5 ml,涡漩混合 1 min,加入乙酸乙酯1 ml和正己烷4 ml,涡旋混合3 min,4 500 r/min离心10 min,于-18℃冰箱中冷冻2 h。移取有机层置5 ml离心管中,40℃水浴挥干,加100 μl流动相,涡漩混合1 min,取20 μl注入高效液相色谱仪,记录色谱图。将(A s/A i)代入溶液标准曲线,计算血浆中Tr的回收率,结果见表1。
2.6.2 方法回收率 取空白血浆1 ml于10 ml具塞试管中,加入Tr对照液适量,使血浆中药物浓度分别为80、400和2 000 ng/ml,按“血浆样品的处理”项下操作,记录色谱图。将(A s/A i)代入血浆标准曲线,计算血浆中Tr的回收率,结果见表1。
2.6.3 精密度试验 取空白血浆1 ml于10 ml具塞试管中,加入Tr对照液适量,使血浆中药物浓度分别为80、400和2 000 ng/ml,每个浓度分别配制5份,按“血浆样品的处理”项下操作,分别在日内和日间取20 μl注入高效液相色谱仪,记录色谱图。将(A s/A i)代入血浆标准曲线,计算日内和日间精密度,结果见表1。
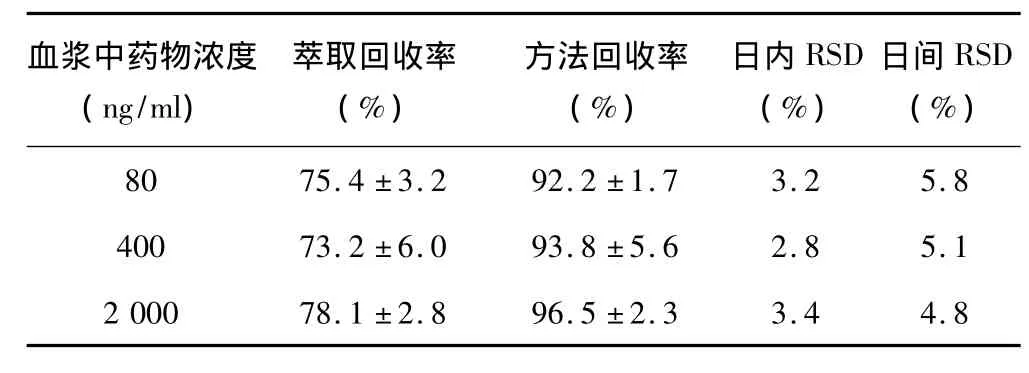
表1 回收率和精密度表
2.7 Tr缓释滴丸兔体内药动学研究
2.7.1 服药方案及样品采集 单剂量交叉口服给药[3-6]:将10只兔子随机分成两组,每组5只。第1组口服盐酸曲马多缓释滴丸片(50 mg),第二组口服盐酸曲马多(50 mg),于给药后不同时间(缓释滴丸0.5、1.0、2.0、3.0、4.0、5.0、6.0、8.0、10.0、12.0 和 24.0 h;片剂 0.25、0.5、1.0、1.5、2.0、2.5、3.0、4.0、5.0、6.0、8.0和12.0 h)由耳缘静脉取血3 ml,并立即将其移入管壁涂有肝素钠的离心管中,4 500 r/min离心10 min,分离得到血浆,置冰箱中保存,备用。间隔1周后交叉服药,同法操作。
2.7.2 样品血药浓度的测定 取血浆样品1 ml,按“血浆样品处理方法”项下操作,记录样品峰面积与内标峰面积之比(A s/A i),将其代入血浆标准曲线,计算求得各时刻的血药浓度。
2.8 实验结果
2.8.1 血药浓度-时间曲线 盐酸曲马多缓释滴丸和普通片剂为实验样品,按照上述操作对实验动物给药、取血,并对血浆样品处理后进行测定,根据血浆标准曲线计算药物浓度。根据实验动物各时间点的血药浓度的平均值与时间的关系,绘制血药浓度-时间曲线,见图2。
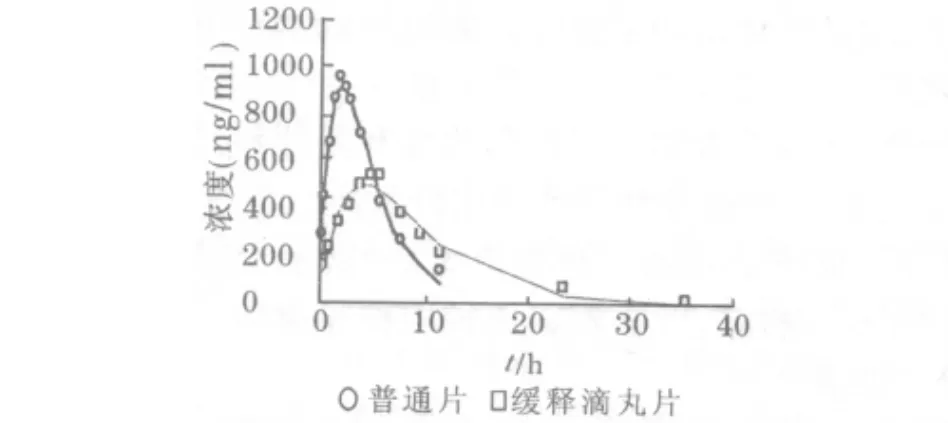
图2 兔体内药时曲线
结果缓释滴丸与普通片的 AUC 分别为;(6 567.71 ±231.69)ng/ml·h 和(5 954.87 ±93.85)ng/ml·h;缓释滴丸在兔体内具有明显的缓释特性。与普通制剂相比,缓释滴丸的药时曲线比较平稳,峰浓度明显降低,达峰时间明显后移。
2.8.2 药动学参数计算 应用孙瑞元等提供的DAS软件计算药动学参数。对Tr缓释滴丸和普通片的药时曲线进行拟合,得出两种样品在兔体内的房室模型均符合一级模型。
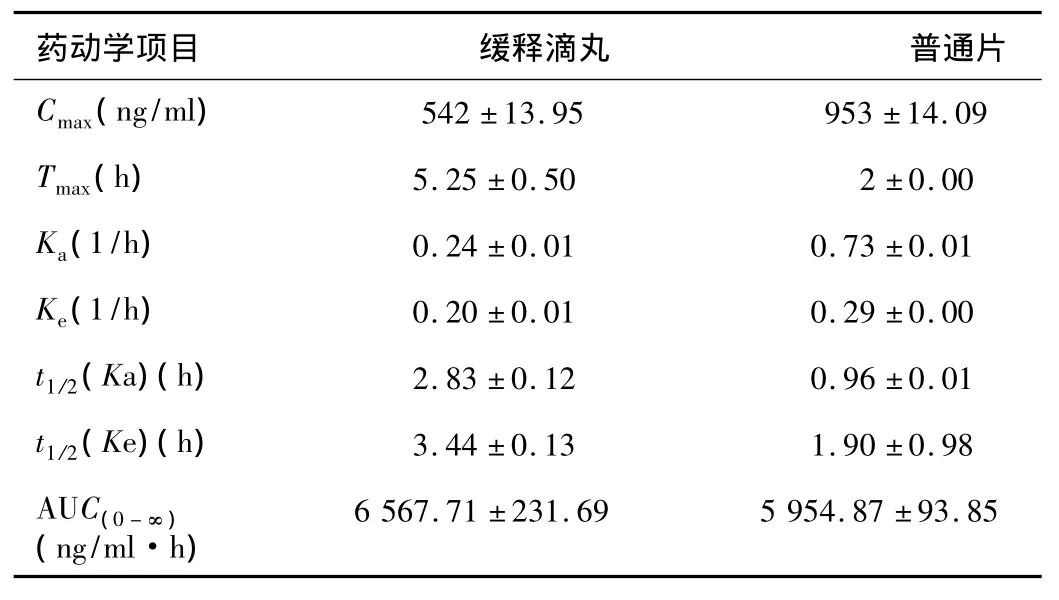
表2 盐酸曲马多缓释滴丸和普通片剂药动学参数
从表中数据可以看出,缓释滴丸的消除速率常数K减少,约为普通片剂的0.69倍,半衰期延长,约为普通片剂的1.81倍。
2.8.3 相对生物利用度[7]根据公式:F r=(AU C0-∞)T/(AU C0-∞)R×100% ,计算 Tr缓释滴丸相对于普通片剂的生物利用度。其中,F r为相对生物利用度,(AU C0-∞)T、(AU C0-∞)R分别为测试制剂与参比制剂的药时曲线下面积,计算结果Tr的相对生物利用度为 F r=6 567.71/5 954.87 ×100%=110.29%。
3 结论
本实验建立了高效液相色谱法测定盐酸曲马多缓释滴丸血药浓度的分析方法,该方法专属性强,灵敏度高,重现性好。与普通片剂相比,缓释滴丸的血药浓度比较平稳,Cmax降低,Tmax后移。缓释滴丸的Cmax、Tmax分别为542 ng/ml和5.25 h;普通片的 Cmax、Tmax分别为953 ng/ml和2 h。缓释滴丸与普通片的相对生物利用度为110.29%。由此可见,缓释滴丸比普通片能持久地维持更平稳的血药浓度,增强了用药的有效性和安全性。
1 张冕,王锦军.高效液相色谱法测定盐酸曲马多的血药浓度.中国医院药学杂志,2007,27(11):1629
2 屈凌波,冯书惠,吴拥军,等.高效液相色谱法测定血浆中盐酸曲马多.四川大学学报(医学版),2003,34(3):574
3 S H Gan,R Ismail,W A Wan Adnan,et al.Method development and validation of a high-performance liquid chromatographic method for tramadol in human plasma using liquid - liquid extraction.Journal of Chromatography B,2002,772:123
4 Milan Nobilis,Jiri Psstera,Pavel Anzenbacher,et al.High - performance liquid chromatographic determination of tramadol in human plasma.Journal of Chromatography B,1996,681:177
5 Mohammad - Reza Rouini,Yalda Hosseinzadeh Ardakani,Faezeh Soltani,et al.Development and validation of a rapid HPLC method for simultaneous determination of tramadol,and its two main metabolites in human plasma.Journal of Chromatography B,2006,830:207
6 赵东祥,王彦慧,夏东亚,等.单剂量口服盐酸曲马多在蒙古族和汉族健康受试者的药代动力学.中国临床药理学杂志,2008,24(2):126
7 赵学玲,龚显峰,威志平,等.盐酸曲马多控释片的制备及犬体内生物利用度研究.中国新药杂志,2008,17(6):494
