一元弱酸溶液中氢离子浓度计算公式的使用条件*
2012-09-25张耀东蔡亚楠刘爱华
张耀东 蔡亚楠 刘爱华
(陕西省生命分析化学重点实验室 陕西师范大学化学化工学院 陕西西安 710062)
1 问题的提出
酸碱溶液中氢离子浓度的计算是分析化学课程教学的重点和难点之一。利用精确式计算酸碱溶液中氢离子浓度比较复杂,通常也没有必要,因此,理解并掌握氢离子浓度的近似计算是很重要的。然而,不同版本的教材给出的使用条件差异较大,没有统一的标准,也没有对近似条件给出明确的解释与过程推导,导致教师在教学中很难把握,学生在学习过程中也常常会感到困惑,不能很好地理解近似计算的使用条件。
2 解决问题的思路
处理酸碱平衡的通用方法是根据有关平衡条件正确写出质子条件式(PBE),即求解[H+]或[OH-]的方程式。PBE反映溶液中质子转移的量的关系,根据溶液中质子得失的量相等的原则,可直接列出PBE。
对于一元弱酸HA溶液,PBE为:
[H+]=[OH-]+[A-]
其意义是一元弱酸溶液中的H+来自两部分:弱酸的解离(A-项)和水的质子自递反应(OH-项)。联立质子平衡、物料平衡和解离平衡这3大平衡所得的方程式,可得出求解氢离子浓度的精确式。然后根据具体情况略去次要项,保留主要项。一般是根据允许的相对误差在±5%以内,即两项相加时,当主要组分浓度大于次要组分浓度的20倍以上时,可忽略次要组分。以此为标准,我们结合在教学实践中的体会,推导了一元弱酸溶液中氢离子浓度的各类计算公式,并对它们的使用条件进行了推导和解释。
3 计算公式及其使用条件
3.1 精确式的推导
对于浓度为c(mol/L)的一元弱酸HA溶液,PBE为:
[H+]=[OH-]+[A-]
定义δ为分布分数,指溶液中某酸碱组分的平衡浓度占其总浓度的分数。对于一元弱酸,由定义知:
即:
(1)

[H+]3+Ka[H+]2-(Kac+Kw)[H+]-KaKw=0
(2)
式(2)是计算一元弱酸溶液氢离子浓度的精确式。
3.2 近似公式及使用条件
根据计算氢离子浓度时的允许误差,可视弱酸Ka和c的大小,采用近似方法进行计算。方法如下:
浓度为c(mol/L)的一元弱酸HA溶液,PBE为:
[H+]=[OH-]+[A-]
为了使计算简化,首先将PBE简化。当弱酸的浓度不是非常稀且酸的强度不是极弱时, H2O的解离可忽略,即[OH-]可忽略。当主要组分浓度大于次要组分浓度的20倍以上时,次要组分可忽略。因此,当[A-]≥20[OH-]时,[OH-]项可忽略,此时计算结果的相对误差不大于5%。
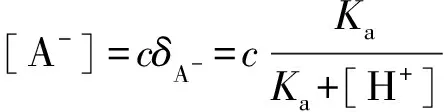
因为
Ka+[H+]>[H+]
所以
Kac≥20Kw
此时,PBE可简化为[H+]≈[A-],精确式(1)可简化为:
(3)
根据物料平衡和解离平衡计量关系,对于浓度为c的弱酸HA溶液,有:
[HA]=c-[A-]=c-[H+]+[OH-]≈c-[H+]
将此式代入式(3),得:
解得:
(4)
式(4)即计算一元弱酸溶液氢离子浓度的近似式。
当满足条件Kac≥20Kw时,可采用近似式计算。
3.3 最简式及使用条件
对于浓度为c(mol/L)的一元弱酸HA溶液,PBE为:
[H+]=[OH-]+[A-]

(5)
式(5)即计算一元弱酸溶液中H+浓度的最简式。
将式(5)代入[H+]≥20Ka,得:
即:

3.4 极稀或极弱酸溶液

(6)

本文根据酸碱质子理论,利用一元弱酸溶液的质子条件式,运用等量代换,推导出一元弱酸氢离子浓度的各类计算公式;并根据在分析化学中计算允许的相对误差一般在±5%以内,对一元弱酸溶液中氢离子浓度的近似计算式的使用条件进行了推导和解释。有助于对氢离子浓度各类计算公式使用条件的统一,从而能使学生更好地理解和掌握酸碱溶液中氢离子浓度的计算。应该指出的是,对多元弱酸溶液中氢离子浓度计算公式的使用条件也可做类似的推理和解释。上述近似处理的条件是根据对计算结果的准确度要求而确定的,因而相应的条件可按照相对误差的要求而相应变化。
[1] 廖力夫.分析化学.武汉:华中科技大学出版社,2008
[2] 薛华.分析化学.北京:清华大学出版社,1986
[3] 陈庆榆,张雪梅.分析化学.合肥:合肥工业大学出版社,2010
[4] 尹权,杨代菱.分析化学例题与习题.吉林:吉林人民出版社,1985
[5] 孙毓庆,胡育筑.分析化学.第2版.北京:科学出版社,2006
[6] 钟国清,赵明宪.大学基础化学.北京:科学出版社,2003
[7] 铁步荣,邵丽心.无机化学.北京:科学出版社,2002
[8] 曾百肇,张华山,潘祖亭.分析化学.第5版.北京:高等教育出版社,2006
[9] 齐美玲,赵郑通.定量分析化学.北京:北京理工大学出版社,2009
[10] 陈久标,邓基芹.分析化学.上海:华东理工大学出版社,2010
[11] 孟凡昌.分析化学教程.武汉:武汉大学出版社,2009
[12] 冯辉霞.无机及分析化学.武汉:华中科技大学出版社,2008
[13] 钟金昌.分析化学.北京:水利电力出版社,1985
