新型电-多相催化工艺去除阳离子红染料废水
2012-08-01陈锦芳张亚平王俊毅
陈锦芳 ,张亚平 ,王俊毅
(1.集美大学 生物工程学院,福建 厦门,361021;2.集美大学 环境工程研究所,福建 厦门,361021)
印染废水是对水环境污染构成严重威胁的工业废水之一,其排放量约占工业废水排放总量的35%[1]。偶氮染料是工业生产中最重要的染料系列,占工业应用染料总量的50%以上[2],已有采用生物法[3]、吸附法、化学沉淀法[4]、膜分离法[5]、电化学氧化法[6]、臭氧氧化法、次氯酸盐氧化法、Fenton法[7-8]、光催化氧化法[9]、超声催化氧化法[10]处理偶氮染料的报道。生物法对化学需氧量(COD)、色度去除效果不佳;化学沉淀法仅是污染物相态的转移,还需额外的后处理;膜分离法造价高、膜易产生污染;臭氧、次氯酸盐和Fenton氧化法运行成本高;超声波氧化、光催化氧化反应速度慢、处理能力有限[11]。电化学氧化法因其在电解下产生的强氧化剂,如羟基自由基(·OH),对染料具有很好的脱色和矿化效果而受到国内外学者的青睐,唯一缺点是耗电量大、工艺成本高[12]。近年来,有通过使用电催化剂等手段来提高电化学氧化法的电流效率、降低能耗,国内已有稀土元素、Fenton试剂电催化降解染料废水的报道[13-14],但采用电-多相催化降解染料废水的研究较少。鉴于此,本文作者将化学修饰电极、多相催化和电催化3种技术结合,在电极基体表面固定具有优良催化性能的物质,装填活性炭于传统二维电解槽的电极间形成三维电极;加入H2O2和不同载体的Al2O3负载型电催化剂,构建新型电-多相催化体系,以阳离子红GTL为模拟废水进行处理,以期为电化学方法处理染料废水寻找新方法、新途径。
1 实验
1.1 电极修饰
采用涂层热解法对电极进行修饰[15]。将粉末状TiO2按摩尔质量M(TiO2):M(无水乙醇)=1:4溶解,分别在预处理后的石墨电极(直径×长度为1.5 cm×16 cm)、钛电极(长×宽×厚为11.5 cm×2.4 cm×0.2 cm)和铁电极(长×宽×厚为11 cm×1.8 cm×0.05 cm)表面均匀涂刷TiO2/乙醇溶液,在100 ℃烘干,反复5次,在550 ℃热处理10 min。待冷却后,分别制得Ti/TiO2,C/TiO2,Fe/TiO2修饰电极。
1.2 催化剂的制备
将Al2O3颗粒加入到0.05 mol/L的偏钒酸铵中等量浸渍,过滤后,100 ℃烘3 h,500 ℃焙烧4 h,冷却2 h后取出,制得V2O5-Al2O3催化剂。以同样的方法制备CuO-Al2O3,Fe2O3-Al2O3,ZnO-Al2O3,NiO-Al2O3和CoO-Al2O3催化剂[16]。
1.3 电-多相催化去除阳离子红
电催化处理前将活性炭颗粒浸泡于阳离子红GTL溶液中至吸附饱和,以消除吸附作用对去除效果的影响。将电极固定于电化学反应器的电解槽中(图1),反应器由直流电源、电解槽、主电极板和床体填料4部分组成,两极板间距约7.0 cm,床体填料为活性炭颗粒和负载型Al2O3催化剂。取500 mL阳离子红GTL溶液(质量浓度为50 mg/L)置于电解槽中,分别用HCl/NaOH调节pH,改变主电极、催化剂及其用量、H2O2投加量,开启曝气泵源和直流电源,进行电催化实验。每隔5 min取定量的水样,于波长530 nm下测定阳离子红去除率。其CODcr采用重铬酸盐法(GB11914—89)测定。

图1 电化学反应器装置图Fig.1 Schematic diagram of experimental apparatus
1.4 分析方法
采用Leo1530场发射扫描电子显微镜(SEM,德国里奥电镜有限公司生产)观察电极和修饰电极的表面形貌。阳离子红降解过程的中间产物采用Carry50紫外-可见分光光度计(东南化学仪器有限公司生产)扫描分析。
2 结果与讨论
2.1 不同电极组合对阳离子红去除率的影响
在3.3 g/L H2O2,0.2 g/L V2O5-Al2O3催化剂、20 V槽电压下,反应40 min,考察不同电极组合对阳离子红GTL去除率的影响,结果如图2所示。由图2可知:修饰电极组合的处理效果明显优于未修饰电极的处理效果。这是因为向石墨、钛和铁电极基体表面涂敷了具有良好稳定性和催化活性的TiO2涂层所致[17]。其中,Fe/TiO2(+)-C/TiO2(-)电极组合处理效果最佳,但是该电极电解过程中产生了大量沉淀,应是铁阳极发生溶出现象而引入的新杂质Fe(OH)3所致[18],因此不宜采用。Ti/TiO2(+)-Ti(-)电极组合在处理初期效果次之,20 min后去除率与Fe/TiO2(+)-C/TiO2(-)电极相当,电解过程无沉淀产生。C/TiO2(+)-C/TiO2(-)电极组合在处理初期效果仅次于上述2种电极,25 min后处理效果与前2种电极组合相当。为了探究修饰电极催化效果优于非修饰电极的原因,对C,C/TiO2,Ti和Ti/TiO2进行SEM表征,结果如图3所示。从图3可见:修饰电极中TiO2颗粒均匀地涂敷在C,Ti电极的表层,粒径约在100 nm左右,这些纳米颗粒的引入大大地增加了C,Ti电极的活性比表面积,有利于催化反应的进行。进一步比较发现:Ti电极表层涂敷的TiO2颗粒相对C电极的更均匀,因此,以下实验均采用Ti/TiO2(+)-Ti(-)的电极组合。

图2 不同电极组合对GTL去除率的影响Fig.2 Effect of electrode on removal of GTL
2.2 催化剂及用量对阳离子红去除率的影响
在3.3 g/L H2O2,20 V槽电压下,以Ti/TiO2为阳极、Ti为阴极,反应40 min,考察了不同催化剂对阳离子红去除率的影响,结果见图4。由图4可知:催化剂的催化活性从大到小顺序为:V2O5,Fe2O3,CoO,CuO,ZnO,NiO,整体而言,n型半导体催化性能优于p型半导体,可能是由于n型半导体在吸附还原性有机物时易于p型半导体所致。V2O5是一种常用于气相催化和光催化反应的催化剂,关于其水相方面的研究较少,国内仅有Niu等[19]将其用于催化乙二醛的报道。本研究首次将V2O5用于液相电催化降解染料废水,结果发现V2O5-Al2O3催化去除阳离子红的效果优于其他负载型催化剂,这主要是因为V2O5表面酸性高,氧化电位大,易于吸附碱性阳离子红发生催化反应[20]。改变V2O5-Al2O3用量,考察其对阳离子红去除率的影响,结果如图5所示。由图5可知:随着催化剂用量的增加,阳离子红去除率明显增加,投加量为0.8 g/L时,阳离子红去除率达97.2%。随后催化剂用量增加,去除率几乎不变,过多的催化剂在催化过程可能产生2种影响作用:一是使自由基·OH产生速度过快,易发生复合反应,降低氧化能力;二是催化剂自身相互重叠概率提高,与有机物质结合的有效面积减少。故催化剂投加量选用0.8 g/L。

图3 不同电极的SEM像Fig.3 SEM images of various electrodes
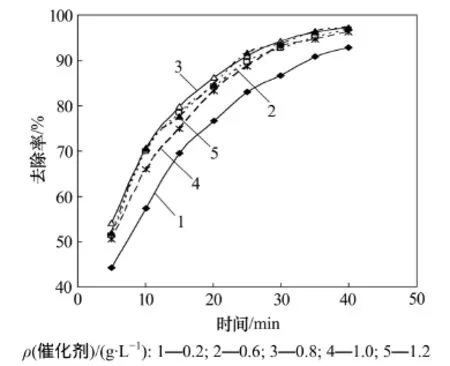
图5 催化剂投加量对阳离子红去除率的影响Fig.5 Effect of amount of catalyst on removal of GTL
2.3 槽电压对阳离子红去除率的影响
以Ti/TiO2为阳极、Ti为阴极,在0.8 g/L V2O5-Al2O3催化剂、3.3 g/L H2O2条件下,改变槽电压,反应40 min,结果见图6。可见:随着槽电压增加,阳离子红去除率明显增加,当槽电压为20 V时,阳离子红去除率达92.7%,随后电压增加,去除率基本不变。当电极面积不变时,槽电压增大会使电极电位及电流密度增大,提高阳极氧化速率,加大溶液中带电粒子的推动力,使溶液中强氧化基团·OH浓度升高,提高去除率[21]。但过高槽电压会使阳极极化、析氧严重,产生大量焦耳热,消耗部分电流,因此,槽电压最优值为20 V。

图6 槽电压对阳离子红去除率的影响Fig.6 Effect of cell voltage on removal of GTL
2.4 pH对阳离子红去除率的影响
以Ti/TiO2为阳极、Ti为阴极,在0.8 g/L V2O5-Al2O3催化剂、3.3 g/L H2O2、槽电压20 V条件下,考察了pH对阳离子红去除率的影响,结果如图7所示。由图7可知:随着pH的升高,阳离子红去除率逐渐减小,说明酸性条件有利于三维电极电催化反应的进行,主要是酸性条件有利于阴极产生H2O2的电化学反应,而当pH>7.0时,阳极易发生析氧反应[22]。考虑到酸性条件下,电极损耗程度大且TiO2涂层易脱落,引入新杂质,故选择溶液初始pH=7.0。

图7 pH对阳离子红去除率的影响Fig.7 Effect of pH on removal of GTL
2.5 H2O2投加量对阳离子红降解的影响
以Ti/TiO2为阳极、Ti为阴极,在0.8 g/L V2O5-Al2O3催化剂、3.3 g/L H2O2、槽电压20 V,pH为7.0的条件下,改变H2O2投加量,反应40 min,结果见图8。由图8可知:随着H2O2投加量增加,去除率增加,当H2O2投加量为1.98 g/L时,去除率达98%,随后H2O2投加量增加,阳离子红去除率变化不大。H2O2是一种很好的电子受体,是·OH的主要来源,其自身也可直接氧化有机物,H2O2的增加可提高电-多相催化的氧化能力,但过多H2O2会成为自由基清除剂[23],故选投加量为1.98 g/L。

图8 H2O2投加量对阳离子红去除率的影响Fig.8 Effect of amount of H2O2 on removal of GTL
2.6 阳离子红初始质量浓度对其去除率的影响
以Ti/TiO2为阳极、Ti为阴极,在0.8 g/L V2O5-Al2O3催化剂、1.98 g/L H2O2、槽电压20 V, pH为7.0的条件下,反应40 min,考察了阳离子红初始质量浓度对其去除率的影响。由图9可知:在反应初期,随着阳离子红初始浓度的增加,去除率降低;20 min后,初始浓度对阳离子红去除率的影响趋缓。说明反应前期,催化体系对阳离子红的催化反应速率较高,后期的速率较低,电-催化氧化脱色反应主要发生在处理前期。
2.7 不同工艺对阳离子红去除的影响

图9 初始质量浓度对阳离子红去除率的影响Fig.9 Effect of initial concentration on removal of GTL

图10 不同工艺对阳离子红去除率的影响Fig.10 Effect of different processes on removal of GTL
取50 mg/L的阳离子红溶液500 mL置于电解槽中,分别采用工艺Ⅰ:Ti/TiO2(+)-Ti(-)与活性炭填充构成的复极性三维电极;工艺Ⅱ:0.8 g/L V2O5-Al2O3、1.98 g/L H2O2;工艺Ⅲ:Ti/TiO2(+)-Ti(-)与活性炭三维电极、0.8 g/L V2O5-Al2O3、1.98 g/L H2O2,在槽电压20 V下,反应40 min,结果如图10所示。由图10可知:电极修饰与活性炭填充构成的三维电极(工艺Ⅰ)对阳离子红的去除效果一般,反应40 min去除率为89%,但该电极对有机物的去除效率仍高于传统二维电极,主要是引入了相当于第三电极的活性炭粒子电极,加大了工作电极的表面积、减少反应物的迁移距离,提高了电流效率[24]。工艺Ⅱ中,阳离子红去除率仅为6.9%,这是因为在没有外电压作用下,V2O5-Al2O3仅与 H2O2发生类Fenton 的反应,因此对阳离子红去除效果不佳。新型电-多相催化法 (工艺Ⅲ)对阳离子红去除效果最好,反应40 min阳离子红去除率达98.0%,优于工艺Ⅱ和工艺Ⅰ的理论耦合线(图10),说明H2O2-V2O5-Al2O3非均相催化体系与Ti/TiO2(+)-Ti(-)-活性炭三维电极的结合产生了良好的协同效应。其原因可能有2方面:一方面V2O5-Al2O3充当了三维电极的粒子电极和电-多相氧化的催化剂,提高了电流效率和有机物氧化的速度[25];另一方面,活性炭为V2O5-Al2O3催化剂提供了活性表面,促进了有机物分子的催化氧化[26]。新型电-多相催体系的初始氧化速率远高于传统三维电极,5 min时阳离子红去除率可达近70%,20 min时达95%。因此在实际运用中,该工艺可在较短时间内去除阳离子红,提高电流效率,降低能耗、节约成本。
2.8 反应动力学分析
以Ti/TiO2为阳极、Ti为阴极,在0.8 g/L V2O5-Al2O3,1.98 g/L H2O2,槽电压20 V及pH为7.0的条件下,采用新型电-多相催化法降解初始浓度为50 mg/L的阳离子红溶液,探讨CODCr的变化规律以及该反应的动力学特征,结果如图11所示。由图11可知:初始CODCr质量浓度为63 mg/L时,反应40 min后,阳离子红降解率为98.0%,CODCr的去除率为89.7%。阳离子红和COD降解的动力学规律如图12所示。由图12可知:二者的初始质量浓度ρ0与剩余质量浓度ρ之比ln(ρ0/ρ)与反应时间t均呈现良好的线性关系,表明在新型电-多相催化处理过程中,阳离子红和COD的去除反应在表观上均遵循一级反应动力学规律,二者的表观速率常数分别为0.111 5和0.059 4 min-1。
2.9 电-多相催化降解阳离子红原理

图11 催化反应过程中CODCr的变化Fig.11 Time course of CODCr

图12 ln(ρ0/ρ)与时间t的关系Fig.12 Curves of ln(ρ0/ρ)vs time t

图13 电催化的紫外光谱分析图Fig.13 UV-Vis adsorption spectra during electrolysis process
阳离子红降解过程中的紫外-可见光谱图如图13所示。由图13可知:未处理的阳离子红具有2个特征吸收峰(280和530 nm)。对于偶氮染料而言,一般认为紫外光区的吸收峰是由苯环共轭体系的π-π*跃迁引起的,而可见光区的吸收峰是由偶氮结构的n-π*跃迁引起的[13],因此280 nm处的强吸收对应为苯环结构,530 nm处对应的是偶氮结构。从图13可知,随着降解时间的增加,阳离子红在280和530 nm处的最大吸收波峰不断降低。530 nm处的吸收峰在处理20 min后,趋于平坦,说明阳离子红的偶氮键基本断裂,进而破坏了整个染料分子的共轭发色体系,与前述的脱色反应主要发生在前期的推论相符合;280 nm处的吸收峰在处理40 min后,也基本趋于平坦,说明苯环结构消失,溶液中绝大部分阳离子红被降解[27]。
电催化氧化降解有机物过程复杂,其机理研究尚在探索中,有研究者认为主要是电解H2O产生的具有强氧化能力的羟基自由基(·OH)使许多难降解的有机物分解为CO2或其他简单化合物[14]。本研究中阳离子红是通过以下3种电催化氧化途径的协同作用降解:
(1)直接氧化,即阳离子红首先传质吸附在粒子电极和主电极表面,在上述电极催化作用下失去电子直接被氧化降解。
(2)间接氧化,由电解水生成·OH等氧化中间体间接氧化降解[26],在酸性条件下,间接氧化的反应式如下:

(3)催化剂表面的多相催化,主要是通过活性组分V吸附有机物(Rad)后的价态转换而实现,反应式如下[28]:

3 结论
(1)H2O2-V2O5-Al2O3非均相催化体系与Ti/TiO2(+)-Ti(-)-活性炭三维电极结合处理阳离子红具有良好的协同效应,二者构成的新型电-多相催化体系相对传统三维电极而言,染料的氧化初始速率高,电流效率高,能耗低,是一种具有应用前景的方法。
(2)新型电-多相催化体系处理阳离子红的较优工艺条件是:pH=7.0,Ti/TiO2(+)-Ti(-)电极组合,0.8 g/L V2O5-Al2O3催化剂,槽电压20 V,1.98 g/L H2O2,电极距离7.0 cm,在此条件下,50 mg/L阳离子红降解40 min,其去除率达98.0%,CODCr去除率达89.7%。
(3)该体系下,阳离子红和COD的去除反应在表观上均遵循一级反应动力学规律。二者的表观速率常数分别为0.111 5和0.059 4 min-1,COD的去除速率低于阳离子红的去除速率。
(4)在电催化氧化过程中,偶氮键的断裂即阳离子红的脱色主要发生在反应初期,该反应在间接氧化、直接氧化和活性组分V多相催化氧化的协同作用下进行。
[1]任松洁, 丛纬, 张国亮, 等.印染工业废水处理与回用技术的研究[J].水处理技术, 2009, 35(8): 14-18.REN Song-jie, CONG Wei, ZHANG Guo-liang, et al.Research and analysis on technology of dyeing wastewater treatment and reutilization[J].Technology of Water Treatment, 2009, 35(8):14-18.
[2]Zhu C M, Wang L Y, Kong L R, et a1.Photocatalytic degradation of AZO dyes by supported TiO2+UV in aqueous solution[J].Chemosphere, 2000, 41(3): 303-309.
[3]Wang X, Gu X, Lin D.Treatment of acid rose dye containing wastewater by ozonizing biological aerated filter[J].Dyes and Pigments, 2006, 67: 1-5.
[4]Goloba V, Vinderb A, Simonic M.Efficiency of the coagulation/flocculation method for the treatment of dyebath effluents[J].Dyes and Pigments, 2005, 67: 93-97.
[5]Koyuncu I.Reactive dye removal in dye/salt mixtures by nanofiltration membranes containing vinyl sulphone dyes effects of feed concentration and cross flow velocity[J].Desalination,2002, 143(3): 243-253.
[6]Grimau V, Gutierrez M.Decolourisation of simulated reactive dyebath effluents by electrochemical oxidation assisted by UV light[J].Chemosphere, 2006, 62: 106-112.
[7]Idil A A, Betul H G, Jens E S.Advanced oxidation of acid and reactive dyes: Effect of Fenton treatment on aerobic, anoxic and anaerobic processes[J].Dyes and Pigments, 2008, 78: 117-130.
[8]Szpyrkowicz L, Juzzolino C, Kaul S.A comparative study on oxidation of disperse dyes by electrochemical process,ozone,hypochlorite and Fenton reagent[J].Water Research, 2001, 35(9):2129-2136.
[9]Mahmoodi N, Arami M.Decolorization and aromatic ring degradation kinetics of Directed 80 by UV oxidation in the presence of hydrogen peroxide utilizing TiO2as a photocatalyst[J].Journal of Chemical Engineering, 2005, 11(12):191-196.
[10]Vajnhandl S, Marechal A M L.Case study of the sonochemical decolouration of textile azo dye Reactive Black 5[J].Journal of Hazardous Materials, 2007, 141(1): 329-335.
[11]Malik P K, Saha S K.Oxidation of direct dyes with hydrogen peroxide using ferrous ion catalyst[J].Separation and Purification Technology, 2003, 3l(3): 241-250.
[12]矫彩山, 孙艳, 门雪燕, 等.电催化氧化技术处理难生化有机废水的研究现状及进展[J].环境科学与管理, 2007, 32(1):107-110.JIAO Cai-shan, SUN Yan, MEN Xue-yan, et al.Research status and progress of electro-catalytic oxidation technology in refractory organic wastewater treatment[J].Environmental Science and Management, 2007, 32(1): 107-110.
[13]刘泳, 邹文慧, 廖洋, 等.Ce3+电催化降解甲基橙模拟废水的研究[J].中国稀土学报, 2011, 29(1): 105-111.LIU Yong, ZOU Wen-hui, LIAO Yang, et al.Treatment on methyl orange-containing simulation wastewater by Ce3+ion homogenous electro-catalytic degradation process[J].Journal of the Chinese Rare Earth Society, 2011, 29(1): 105-111.
[14]王娟, 申婷婷, 李小明, 等.Fe(Ⅱ)EDTA/H2O2电催化降解甲基橙模拟废水的研究[J].环境工程学报, 2010, 4(4): 833-838.WANG Juan, SHEN Ting-ting, LI Xiao-ming, et al.Electro-catalytic degradation of simulated methyl orange wastewater by Fe(Ⅱ)EDTA/H2O2[J].Chinese Journal of Environmental Engineering, 2010, 4(4): 833-838.
[15]侯俭秋, 崔阳.钛基修饰锡锑铅氧化物电极制备及性能研究[J].环境科学与技术, 2008, 31(8): 117-124.HOU Jian-qiu, CUI Yang.Preparation and properties of titanium based Sn-Sb-Pb oxides coating electrode[J].Environmental Science and Technology, 2008, 31(8): 117-124.
[16]张亚平, 韦朝海, 吴超飞.光Fenton反应的Ce-Fe/AlO3催化剂制备及性能表征[J].中国环境科学, 2006, 26(3): 320-323.ZHANG Ya-ping, WEI Chao-hai, WU Chao-fei.Preparation and characterization of CeO2doped with Fe/Al2O3catalyst in photo-Fenton reaction[J].China Environmental Science, 2006,26(3): 320-323.
[17]彭贤玉.电催化氧化处理染料废水的机理及研究进展[J].湖南理工学院学报: 自然科学版, 2008, 21(1): 54-56.PENG Xian-yu.Mechanism and development of electrocatalysis of oxygen in reduction of dyeing wastewater[J].Journal of Hunan Institute of Science and Technology: Natural Sciences,2008, 21(1): 54-56.
[18]岳琳, 王启山, 石岩, 等.电-多相催化反应体系对垃圾渗滤液的降解[J].中国环境科学, 2008, 28(2): 131-135.YUE Lin, WANG Qi-shan, SHI Yan, et al.Degradation of landfill leachate by electro-heterogeneous catalysis[J].China Environmental Science, 2008, 28(2): 131-135.
[19]Niu Y L, Li R F.V2O5/C catalyst for liquid phase oxidation of glyoxal to glyoxylic acid[J].Science in China Series B:Chemistry, 2009, 52(7): 1057-1062.
[20]毛丽秋, 张同来, 冯长根.V2O5-Ag2O/η-Al2O3催化剂上甲苯氧化制苯甲醛的研究[J].分子催化, 2003, 17(2): 146-150.MAO Li-qiu, ZHANG Tong-lai, FENG Chang-gen.Research on V2O5-Ag2O/η-Al2O3catalysts for oxidation of toluene to benzaldehyde[J].Journal of Molecular Catalysis, 2003, 17(2):146-150.
[21]刘伟丽, 张爱丽, 周集体, 等.电-多相催化反应器处理苯胺废水的研究[J].环境科学与技术, 2006, 29(8): 93-95.LIU Wei-li, ZHANG Ai-li, ZHOU Ji-ti, et al.Degradation of aniline easte water by rlectro-heterogeneous catalytic reactor[J].Environmental Science and Technology, 2006, 29(8): 93-95.
[22]崔艳萍, 杨昌柱.复极性三维电极处理含酚废水的研究[J].能源环境保护, 2004, 18(2): 23-26.CUI Yan-ping, YANG Chang-zhu.Study on degradation of phenol waster water by bipolar tree-dimensional electrode[J].Energy Environmental Protection, 2004, 18(2): 23-26.
[23]张亚平, 韦朝海.光助Fenton氧化降解染料阳离子红GTL[J].中南大学学报: 自然科学版, 2008, 39(4): 688-693.ZHANG Ya-ping, WEI Chao-hai.Oxidation degradation of cationic red GTL by photo-Fenton[J].Journal of Central South University: Science and Technology 2008, 39(4): 688-693.
[24]熊林, 李明玉, 尹华.三维电极流化床对印染废水降解脱色处理[J].给水排水, 2005, 31(1): 59-62.XIONG Lin, LI Ming-yu, YIN Hua.Degradation and decolorization for treating dyeing wastewater using Three-Dimensional fluidized bed electrode[J].Water and Wastewater Engineering, 2005, 31(1): 59-62.
[25]张芳, 李光明, 盛怡, 等.三维电解法处理苯酚废水的粒子电极研究[J].环境科学, 2007, 28(8): 1715-1719.ZHANG Fang, LI Guang-ming, SHENG Yi, et al.Preparation of particle-electrodes for treating phenol wastewater using Three-Dimensional electrolysis[J].Environmental Science, 2007,28(8): 1715-1719.
[26]Lin S H, Lai C L.Catalytic oxidation of dye wastewater by metal oxide catalyst and granular activated carbon[J].Environment International, 1999, 25(4): 497-504.
[27]Zhao W R, Shi H X, Wang D H.Ozonation of cationic red X-GRL in aqueous solution degradation and mechanism[J].Chemosphere, 2004, 57(9): 1189-1199.
[28]张步江, 闫征, 刘浏, 等.V2O5基催化剂的应用及催化机理[J].山西化工, 2008, 28(5): 33-36.ZHANG Bu-jiang, YAN Zheng, LIU Liu, et al.Applications and catalytic mechanisms of vanadium pentoxide catalysts[J].Shanxi Chemical Industry, 2008, 28(5): 33-36.
