姜黄素自微乳颗粒的研究
2012-05-01国大亮朱晓薇张艳军
国大亮,朱晓薇,张艳军
(天津中医药大学,天津 300193)
姜黄素是从姜科植物姜黄(Curcuma longa L.)的干燥根茎中提取的一种二苯基庚二酮类化合物[1]。姜黄素是姜黄的主要有效成分之一,有重要的经济价值和广泛的药理作用,动物实验和文献报道表明其具有降血脂、抗肿瘤、抗氧化、抗凝、抗淀粉样蛋白聚合、抑制HIV-1整合酶活性等作用[2]。姜黄素亲脂性强,难溶于水,对酸、碱、光、热、金属离子均不稳定,口服吸收差,生物利用度低,因而限制了姜黄素在临床上的应用和进一步的研究开发[3]。
鉴于此,本实验在无水的条件下,首先将姜黄素、油相、非离子表面活性剂、助表面活性剂按适当比例混合,制备得较稳定的姜黄素自微乳。口服姜黄素自微乳后,在胃液中因胃蠕动和乳化剂作用下自发形成O/W型微乳,微乳可提高姜黄素的水溶性,提高其口服吸收和生物利用度[4]。由于姜黄素自微乳室温下呈液态,不宜携带与服用,因此本实验又筛选适宜的吸收剂,令姜黄素自微乳固化,制成了颗粒剂,使自微乳的携带与服用更加方便。
1 仪器与试药
1.1 仪器 TN-100B型托盘天平(上海精科天平),恒温磁力加热搅拌器(江苏省金坛市荣华机器制造有限公司,85-2型),精密电子天平(上海精密科学仪器有限公司,FA1004N)。
1.2 试药 肉豆蔻酸异丙酯(国药集团化学试剂有限公司,化学纯),聚乙二醇400(天津市北方天医化学试剂有限公司,分析纯),聚氧乙烯蓖麻油EL 35(徳国BASF公司),淀粉(天津市干腌食品公司,食品级),糊精(西安宏昌药业),微晶纤维素(台湾明台化工股份有限公司),葡萄糖(天津市北方天医化学试剂有限公司,分析纯),蔗糖粉(天津中医药大学药物制剂实验室提供),甘露醇、枸橼酸(天津市科密欧化学试剂有限公司,分析纯),山梨酸(天津市北方天医化学试剂有限公司,分析纯),聚乙二醇4000、聚乙二醇6000(天津市科密欧化学试剂有限公司,化学纯),聚乙二醇8000(天津市瑞金物化学品有限公司,化学纯),聚维酮(天津市科密欧化学试剂开发中心),姜黄素标准品(中国药品生物制品检定所,批号0823-9802),其余试剂均为分析纯。
2 实验方法
2.1 姜黄素自微乳的制备称取32g聚氧乙烯蓖麻油EL、8 g聚乙二醇400,置于100mL三角瓶中,37℃水浴加热,以恒温磁力加热搅拌器搅拌30min,加入10g肉豆蔻酸异丙酯,搅拌均匀。精密称取2g姜黄素,少量多次加入三角瓶中,室温搅拌24 h。
2.2 吸收剂的筛选 将吸收剂粉碎,分别过100目筛,备用。称取1.00g姜黄素自微乳,置于小蒸发皿中,少量多次加入吸收剂,以玻棒搅拌均匀,将吸附固化的自微乳过筛,以自由通过14目筛,轻压后可通过60目筛为度,记录加入吸收剂的质量,分别计算各吸收剂的吸收比(固化比=自微乳质量:吸收剂质量),重复3次,计算平均值。
2.3 自微乳颗粒的制备 称取5 g姜黄素自微乳,加入吸收剂搅拌均匀,滴入适量30%聚维酮溶液,制成软材,以14目筛湿法制粒,50℃干燥,整粒,16目筛整粒,密闭保存。
2.4 自微乳颗粒的溶出 分别量取250mL人工胃液,加于溶出杯中,依2010版《中国药典》附录“溶出度测定法”,设定转速为 100 rpm,于 0.5、1、2、3、4、5、6、7、8、9、10min 吸取溶出液3mL,以0.45μm微孔滤膜过滤,弃去初滤液,取续滤液,以人工胃液为空白,于420 nm测定吸光度,以溶出液最大吸光度为100%,求算各时间点相对累积溶出率,以时间为横坐标,相对累积溶出率为纵坐标,绘制累积溶出曲线,以excel软件按式-1进行Weibull概率模型拟合[5],求算Td和T50。

2.5 姜黄素自微乳颗粒的含量测定
2.5.1 供试品溶液的制备 取约20mg姜黄素自微乳颗粒,精密称定,置于50mL量瓶中,加入约40mL甲醇,超声震荡5min,溶液自然冷却至室温,以甲醇稀释至刻度,混匀,精密吸取5mL稀释至10mL,混匀,取适量溶液以0.45μm微孔滤膜过滤,弃去初滤液,取续滤液,以甲醇为空白,于420 nm测定吸光度,外标法计算含量。
2.5.2 线性范围 精密称取2.8mg姜黄素标准品,置于10mL量瓶中,加甲醇稀释至刻度,精密吸取此溶液,分别稀释成浓度为 4.48、3.36、2.24、1.12、0.56 μg·mL-1的溶液,于420 nm测定吸光度,以姜黄素浓度为横坐标,吸光度为纵坐标进行线性回归,建立回归方程。姜黄素在0.26~5.20 μg·mL-1范围内线性关系良好,回归方程为Y=0.1964X-0.0048,相关系数 R2=0.9999。
2.5.3 精密度 以甲醇为空白对照,分别取姜黄素标准品溶液高浓度(4.48 μg·mL-1)、中浓度(2.24 μg·mL-1)、低浓度(1.12 μg·mL-1),以甲醇为空白,于 420 nm 下测定吸光度,连续测定5次,求算RSD。高浓度的RSD为0.15%,中浓度的RSD为0.39%,低浓度的RSD为0.97%。
2.5.4 稳定性 将2.24 μg·mL-1的姜黄素标准品溶液室温放置,分别于 0、2、4、6、8、10 h 取样,以甲醇为空白,于 420 nm测定吸光度,计算RSD。姜黄素标准品溶液在测定条件下10 h内稳定,RSD为1.13%。
2.5.5 回收率 取空白颗粒适量,置于50mL量瓶中,加入姜黄素标准品溶液0.5mL,以甲醇稀释至刻度,超声震荡5min,取适量溶液以0.45μm微孔滤膜过滤,弃去初滤液,取续滤液,以甲醇为空白,于420 nm测定吸光度,外标法测定姜黄素含量,计算回收率和RSD。姜黄素平均加样回收率为100.31%,RSD 为 0.80%。
3 实验结果
3.1 吸收剂的选择 多糖类辅料对姜黄素自微乳有较好的吸附性,糖醇酸类辅料的吸附性次之,聚乙二醇类辅料的吸附性较差,但枸橼酸和山梨酸吸附性最差。固化比详见表1。

表1 吸收剂的固化比
3.2 自微乳颗粒的溶出速率 从每类吸收剂中选择吸收比最小的两种吸收剂制备自微乳颗粒,以人工胃液为溶出介质测定颗粒的溶出速率,经Weibull概率模型拟合,可见微晶纤维素和甘露醇的Td和T50明显小于其他吸收剂,由于纤维素类吸收剂一般对药物都有一定吸附损失,综合考虑以甘露醇作为吸收剂制备姜黄素自微乳颗粒剂较为合适。以甘露醇为吸收剂的姜黄素自微乳颗粒外标法测得姜黄素含量为0.63%。结果如图1和表2所示。

图1 各吸收剂的相对累积溶出百分率
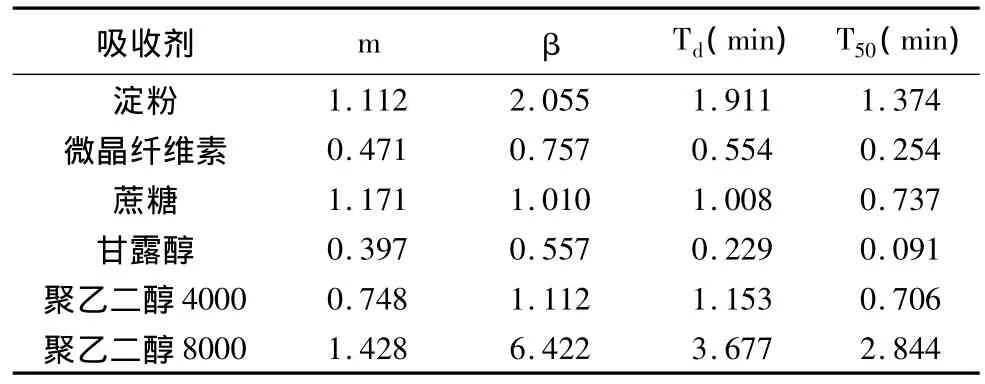
表2 溶出曲线的Weibull概率模型拟合
4 讨论
以糊精作为吸收剂,颗粒的成型性较好,但颗粒硬度较大,崩解缓慢;以淀粉作为吸收剂,颗粒软硬适中,颗粒成型率较高,但崩解速度不及微晶纤维素快。多糖类吸收剂制得的颗粒的溶出液较混浊,不溶性辅料可能会对药物有一定吸附,因此对于姜黄素而言不宜选用多糖类吸收剂。
以柠檬酸为吸收剂时发现柠檬酸吸附自微乳后粘度增大,易结成片状,不易过筛。曾经尝试以聚乙二醇2000为吸收剂,但发现聚乙二醇2000质软,极易互相粘结成球状,难于制剂成型。总体来看聚乙二醇的颗粒成型性不如多糖类和糖醇酸类。
姜黄素对水、对热均不稳定,因此湿法制粒中制软材时的粘合剂使用了30%的PVP乙醇溶液,粘性适中,且PVP有助于颗粒迅速崩解,使颗粒的自乳化时间缩短。以本实验条件下,以甘露醇为吸收剂制备姜黄素自微乳的颗粒,成型良好,颗粒易溶于水,溶出时间短,而且溶液澄清,姜黄素无吸附损失。
[1]国家药典委员会.中华人民共和国药典2010年版(一部)[S].北京:中国医药科技出版社,2010:247.
[2]冯为,胡林峰.姜黄素的研究进展及其抗肿瘤作用概况[J].中国现代药物应用,2011,5(13):117 -118.
[3]张立康,汪小珍,李婉姝,等.姜黄素在大鼠体内药代动力学和生物利用度研究[J].中国药理学通报,2011,27(10):1458-1462.
[4]崔晶,翟光喜,赵宇,等.姜黄素微乳的体内吸收研究[J].中草药,2007,38(3):368 -372.
[5]张莉,夏运岳.用电子表格 Excel计算药物溶出度Weibull分布参数[J].药学进展,2002,26(1):48-50.
