氯化镁醇合物体系Ziegler-Natta催化剂制备过程的在线红外研究
2011-11-09廖翼涛高明智
廖翼涛,高明智
(中国石化 北京化工研究院,北京 100013)
分析测试
氯化镁醇合物体系Ziegler-Natta催化剂制备过程的在线红外研究
廖翼涛,高明智
(中国石化 北京化工研究院,北京 100013)
采用在线红外分析仪分析了氯化镁醇合物体系Ziegler-Natta(Z-N)催化剂制备的全过程:低温反应阶段、升温阶段、加入内给电子体反应阶段和催化剂处理阶段。分析结果表明,为保证催化剂具有良好的颗粒形态,低温反应阶段的初始温度不高于-10℃较适宜;在升温阶段,为消除TiCl4-n(OCH2CH3)n生成速率的突变,当温度在10~20℃之间时应适当放缓升温速率;当在反应体系中加入邻苯二甲酸二异丁酯(DIBP)后,DIBP主要与活化的MgCl2络合生成MgCl2·DIBP络合物,同时生成少量的MgCl2,DIBP,TiCl4三者共同作用物,DIBP未与TiCl4直接进行作用。
在线红外分析;氯化镁醇合物;四氯化钛;邻苯二甲酸二异丁酯;Ziegler-Natta催化剂
催化剂的制备与选取是聚丙烯的关键技术之一,因此聚丙烯催化剂的开发和研究是聚丙烯技术发展的核心[1]。随着聚烯烃行业的不断发展,出现了各种类型的聚烯烃催化剂。从第3代Ziegler-Natta(ZN)催化剂开始,不同结构的内给电子体化合物与MgCl2和TiCl4构成了催化剂的主要组分[2]。在制备过程中这3种组分的存在状态,以及它们之间发生的作用和变化一直是人们关注的问题。利用氯化镁醇合物制备的催化剂是目前应用最广泛的催化体系。
近年来,较多的研究者[3-5]利用IR光谱技术对载体型催化剂进行了分析;郑荣辉等[6]采用IR光谱技术测定了烯烃聚合用Ti-Mg系负载型催化剂制备过程中形成的物种;曹守镜等[7]利用IR光谱分析了MgCl2-C4H9OH-SiCl4-TiCl4体系的高效催化剂,记录了催化剂制备各阶段产物的IR光谱。除了传统的IR光谱分析技术外,一种新型的在线IR分析技术在有机化学等领域开始应用,这种技术能实现对反应过程的实时监测[8]。目前,关于利用此技术分析载体型催化剂制备过程的报道较少。
本工作利用在线IR分析技术,对氯化镁醇合物体系Z-N催化剂制备过程中不同阶段的反应情况进行了实时监测,监测在催化剂表面反应生成的、溶于液相中的物质,根据其IR光谱变化推断固体表面的反应情况。
1 实验部分
1.1 试剂
TiCl4:工业品,纯度大于99.9%,密度1.79 g/mL,河北邢台有色金属冶炼厂;氯化镁醇合物(MgCl2· n EtOH):中国石化催化剂北京奥达分公司;邻苯二甲酸二异丁酯(DIBP):化学纯,北京化工厂;氮气:中国石化北京化工研究院,纯度大于99.999%,H2O的质量分数小于2.0×10-6,O2的质量分数小于2.0×10-6,净化后使用;己烷:工业一级,中国石化燕山石化化工二厂,经净化塔脱水脱氧。
1.2 氯化镁醇合物体系Z-N催化剂的制备
在反应釜内加入70 m L TiCl4,冷却至一定温度,恒温下加入4 g MgCl2·n EtOH并将其与TiCl4反应0.5 h(低温反应阶段);以一定的升温速率升温至40℃(升温阶段);加入1 m L内给电子体DIBP,然后在1.5 h内缓慢升温至130℃并恒温反应2 h(加入内给电子体反应阶段);降温至90℃,沉降一定时间,移走上层液体后,加入70 m L TiCl4,逐步升温至130℃并恒温2 h;抽滤后降温至60℃,再用70 m L己烷洗涤若干次直至IR谱图上无其他杂质峰(催化剂处理阶段)。
1.3 原理与方法
在线红外分析仪是一种能对反应过程进行实时监测的仪器,能实时记录反应过程中体系的IR谱图。在催化剂制备过程中,通过对实时IR谱图中的特征峰进行分析来考察反应过程发生的化学变化。
采用Mettler Toledo公司ReactIR IC10型在线红外分析仪分析氯化镁醇合物体系Z-N催化剂的制备过程。用高纯氮气吹扫分析仪,除去仪器内部水蒸气及其他气体杂质,并用丙酮清洗钻石探头表面,扫描范围650~4 000 cm-1,分辨率8 cm-1,每获取一张IR谱图的扫描次数是256,每分钟获取一张IR谱图[9]。
2 结果与讨论
2.1 催化剂制备全过程的在线IR分析
氯化镁醇合物体系Z-N催化剂的制备可分为4个阶段:低温反应阶段、升温阶段、加入内给电子体反应阶段和催化剂处理阶段。
在氯化镁醇合物体系Z-N催化剂制备过程中,TiCl4与MgCl2·n EtOH的反应是一个剧烈、大量放热的过程,TiCl4取代乙醇并在MgCl2的空位上进行配位,通过双氯桥键与处于不饱和配位的(110)和(100)晶面上的Mg原子形成稳定的复合物。TiCl4与低碳醇反应时,不能完全置换Cl-,只能生成部分取代的氯代钛醇盐(TiCl4-n(OCH2· CH3)n)[10],反应如下:
采用SPSS 18.0软件对数据进行分析处理,计量资料以(均数±标准差)表示,采用t检验;计数资料以(n,%)表示,采用χ2检验,以P<0.05表示差异具有统计学意义。
TiCl4+n CH3CH2O H — →TiCl4-n(OCH2CH3)n+n HCl利用在线红外分析仪检测溶于 TiCl4中的TiCl4-n(OCH2CH3)n的IR特征峰,根据其峰位的变化推断反应体系中的反应情况。
氯化镁醇合物体系Z-N催化剂制备全过程中液相的三维IR谱图的变化见图1。由图1可知,随着反应的进行,在不同时间段出现了不同反应阶段所对应的IR谱图。
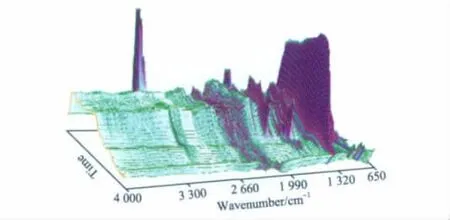
图1 氯化镁醇合物体系Z-N催化剂制备全过程的三维IR谱图Fig.1 3D IR spectra of the whole process for preparation of MgCl2 alcohol complex(MgCl2·n EtOH) system Ziegler-Natta catalyst.
2.1.1 加入DIBP前的在线IR分析
加入DIBP前反应体系的三维IR谱图见图2。从图2可知,加入DIBP前,在反应体系中υC—O的特征峰分裂成了1 104,1 076 cm-1处的两个峰,表明生成了不同结构的TiCl4-n(OCH2CH3)n[11]。
2.1.2 加入DIBP后的在线IR分析
加入DIBP前后反应体系的三维IR谱图见图3;加入DIBP反应5 min后,反应体系的实时IR谱图见图4。由图3和图4可知,未加入DIBP时,在1 686,1 662,1 320,1 298 cm-1处未出现吸收峰;加入DIBP后,在上述4个波数处出现了特征吸收峰,且峰强度随反应的进行而逐渐增强,这表明加入的DIBP与MgCl2和TiCl4开始发生了相互作用。其中,1 686,1 662 cm-1处的特征吸收峰归属于DIBP中υC═O(向低波数方向发生了偏移);1 320,1 298 cm-1处的特征吸收峰归属于DIBP中υC—O(向高波数方向发生了偏移)[12]。

2.1.3 催化剂处理阶段的在线IR分析
经纯净TiCl4处理,反应体系中TiCl4-n(OCH2· CH3)n的含量降至较低,再经己烷多次处理后反应体系的三维IR谱图见图5。在用TiCl4和己烷处理过程中,保证仪器金属探头一直在最低液面内,即可检测到催化剂处理阶段液相体系内的IR吸收。从图5可见,2 959,2 928,1 466,1 379 cm-1处的吸收峰为正己烷的特征峰。可见,此时溶液中只含有大量己烷,不含 TiCl4-n(OCH2CH3)n及其他杂质,说明催化剂表面已基本处理干净。

图5 经己烷多次洗涤后反应体系的三维IR谱图Fig.5 3D IR spectra of the reaction system washed w ith n-hexanemany times.
2.2 低温反应阶段的研究
在低温反应阶段,初始反应温度对TiCl4-n· (OCH2CH3)n吸光度的影响见图6。
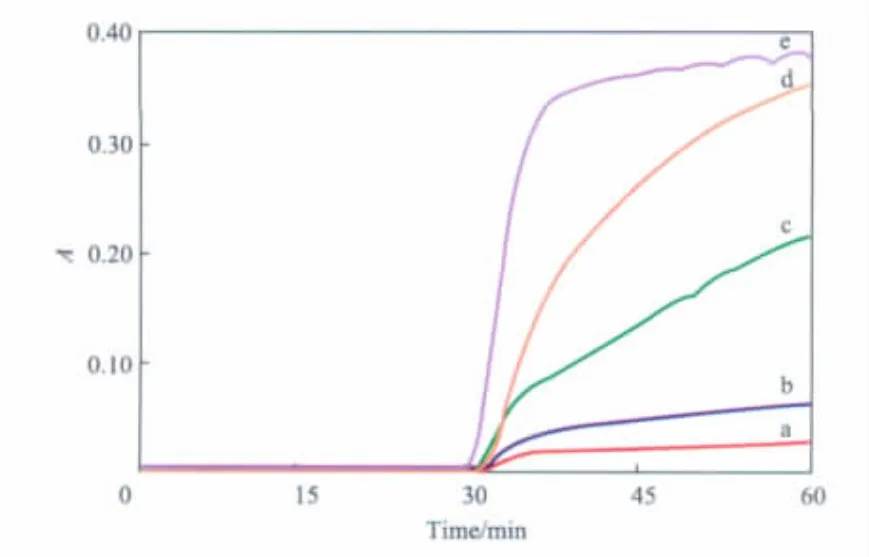
图6 初始反应温度对TiCl4-n(OCH2 CH3)n吸光度的影响Fig.6 The effect of the initial temperature in low temperature reaction step on absorbance(A)of TiCl4-n(OCH2 CH3)n.
吸光度的大小直接反应物质生成速率的快慢。从图6可见,随初始反应温度的升高,TiCl4-n· (OCH2CH3)n的吸光度逐渐增大,即 TiCl4-n· (OCH2CH3)n的生成速率逐渐加快,反应愈加剧烈。特别是当初始反应温度在0℃以上时,在很短的时间内,TiCl4-n(OCH2CH3)n的吸光度就达到了平衡值,即生成速率达到平衡值。氯化镁醇合物体系Z-N催化剂制备的初始反应温度非常重要,TiCl4在球型MgCl2醇合物上的负载过程是放热过程,为使催化剂仍能保持载体的球形形态,反应适宜在低温下进行[13]。因此,为保证球形的粒子不被破碎,同时得到良好的催化剂颗粒形态,初始反应温度选择不高于-10℃较适宜。
2.3 升温阶段的研究
在氯化镁醇合物体系Z-N催化剂制备过程中,控制好升温阶段的升温速率是保持催化剂良好颗粒形态、降低聚合物细粉含量的关键[14]。升温速率对TiCl4-n(OCH2CH3)n吸光度的影响见图7。从图7可见,即使升温速率不同,但升温到40℃时,TiCl4-n(OCH2CH3)n的吸光度都基本趋于恒定,即生成速率基本趋于恒定,反应达到了平衡;除升温速率为2.00℃/m in的曲线外,其他3条曲线在10~20℃之间均出现吸光度突变,也就是TiCl4-n· (OCH2CH3)n的吸光度突然增大(即生成速率加快)。在升温速率为2.00℃/m in的曲线上,可能由于升温速率太快,掩盖了吸光度突变(即速率突变)。产生速率突变时,由于反应的突然加剧会对催化剂的颗粒形态产生影响,因此在升温阶段需控制好升温速率,在温度升高到10~20℃之间时,通过对冷却系统的调节尽量减慢升温速率,最大限度地消除速率突变过程的发生。
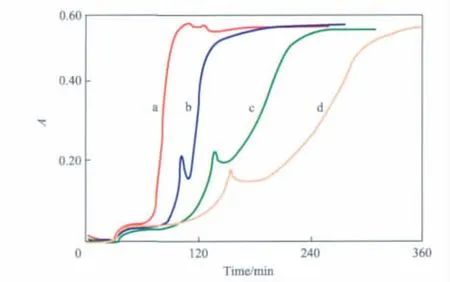
图7 升温速率对TiCl4-n(OCH2 CH3)n吸光度的影响Fig.7 The effect of the heating rate on A of TiCl4-n(OCH2 CH3)n. Reaction conditions:heating for 1 h after reaction,initial temperature-20℃,final temperature 40℃.
2.4 内给电子体结合情况的研究
在催化剂制备过程中各组分之间发生的作用和变化以及各组分的存在状态,一直是人们关注的问题。Yang等[15]用研磨法和化学沉降法制备了单酯和双酯给电子体的催化剂,在利用红外光谱仪对其进行分析时发现,加入DIBP的催化剂中,双酯(υC═O,波数1 732 cm-1)配位在MgCl2上,形成了MgCl2·DIBP表面络合物(υC═O,波数1 685~1 689 cm-1),同时含有少量的 TiCl4双酯络合物(υC═O,波数1 660~1 665 cm-1,为肩峰)。
DIBP主要与MgCl2的(110)或(100)晶面进行络合。由于MgCl2醇合物中的乙醇已经与MgCl2(110)和(100)晶面进行了络合,使得DIBP不能与MgCl2进行络合反应;而无水MgCl2中的MgCl2未与乙醇进行络合,因此DIBP可以与MgCl2进行络合。
2.4.1 DIBP/无水MgCl2反应体系
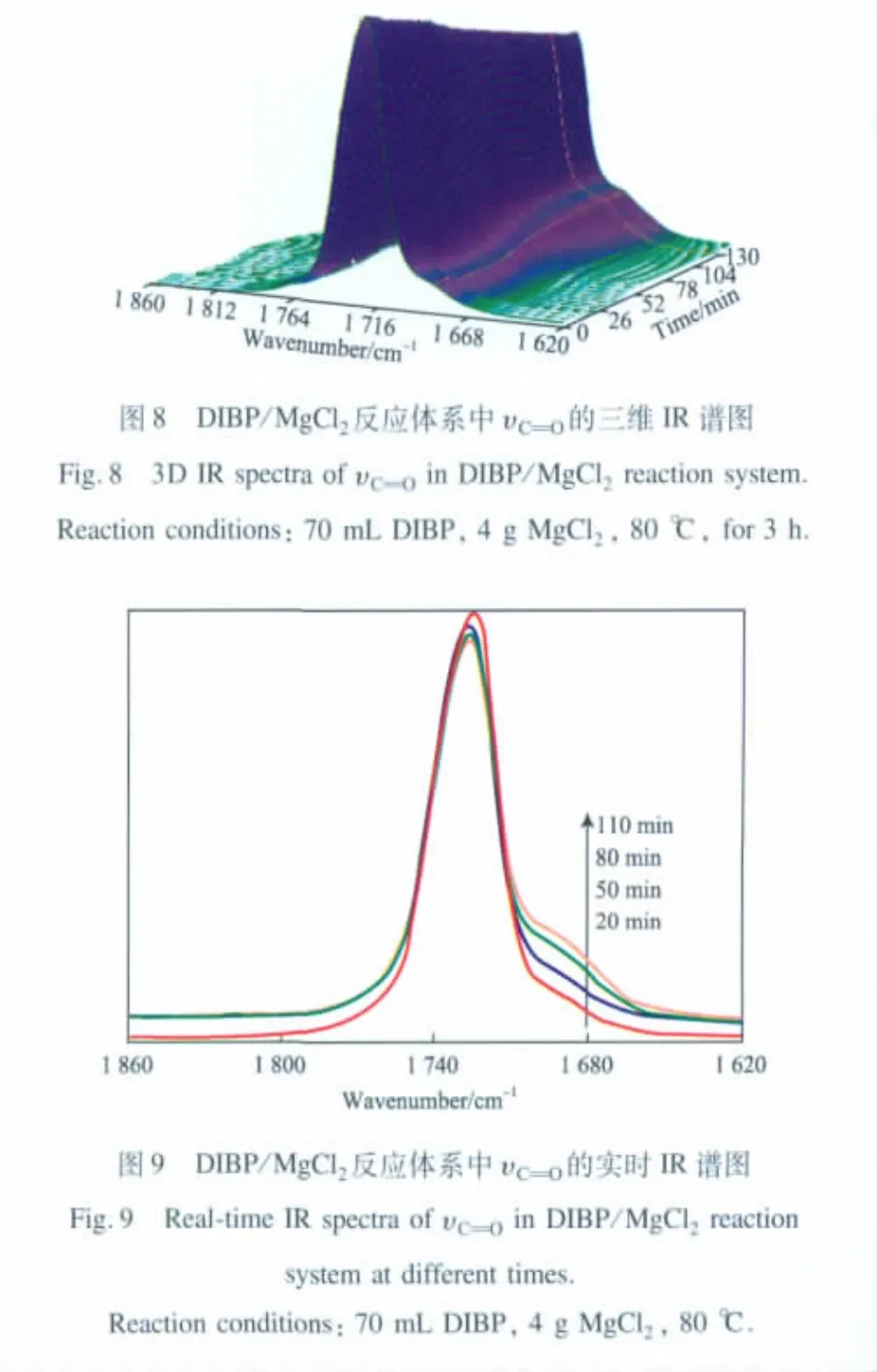
DIBP/无水MgCl2反应体系中υC═O的三维IR谱图及实时IR谱图分别见图8和图9。由图8及图9可知,在20 m in时,纯DIBP中υC═O的特征峰出现在1 725 cm-1处;随反应时间的延长,υC═O的特征峰逐渐向低波数方向偏移,1 725 cm-1处的特征峰强度逐渐减弱,而1 689 cm-1处的特征峰强度逐渐增强,这是因为DIBP与MgCl2不断发生反应生成络合物 MgCl2·DIBP;又由于反应体系中的DIBP过量,因此在IR谱图中的1 725 cm-1处始终有纯DIBP中υC═O的特征峰出现。
2.4.2 TiCl4·DIBP/MgCl2·n EtOH反应体系
TiCl4·DIBP/MgCl2·n EtOH反应体系中υC═O的三维IR谱图和实时IR谱图分别见图10和图11。由图10和图11可知,与 DIBP中 υC═O的特征峰(波数1 725 cm-1)比较,在33 min时(加入MgCl2· n EtOH前),υC═O的特征峰向低波数方向偏移至1 636,1 580 cm1处。由此可见,TiCl4·DIBP络合物中υC═O的特征峰位于1 636,1 580 cm1处。随MgCl2·n EtOH的加入,在1 686,1 662 cm1处迅速出现吸收峰,即体系的反应加剧;从35 min开始,1 636,1 580 cm1处的吸收峰强度迅速减弱。

由图10和图11中的特征吸收峰的变化情况可知,加入 MgCl2·n EtOH之前,先是由 DIBP与TiCl4形成大量的TiCl4·DIBP二酯络合物;再加入MgCl2·n EtOH后,随着TiCl4与MgCl2·n EtOH中的EtOH反应的进行,使得MgCl2活性位外露而被活化,由于DIBP更易于与活化的MgCl2(110)晶面络合,从而导致TiCl4·DIBP二酯络合物的分解,反应体系中逐渐形成了大量MgCl2·DIBP络合物,以及少量的MgCl2,DIBP,TiCl4三者共同作用物。
2.4.3 内给电子体结合情况的讨论
在氯化镁醇合物体系Z-N催化剂制备过程中,加入DIBP后将反应体系在1 750~1 620 cm-1之间的三维IR谱图放大可得到图12。从图12可看出,加入DIBP后,在1 686,1 662 cm-1处的吸收峰强度在短时间内增大到最高值,之后随反应时间的延长,两个峰的强度逐渐降至较小值。
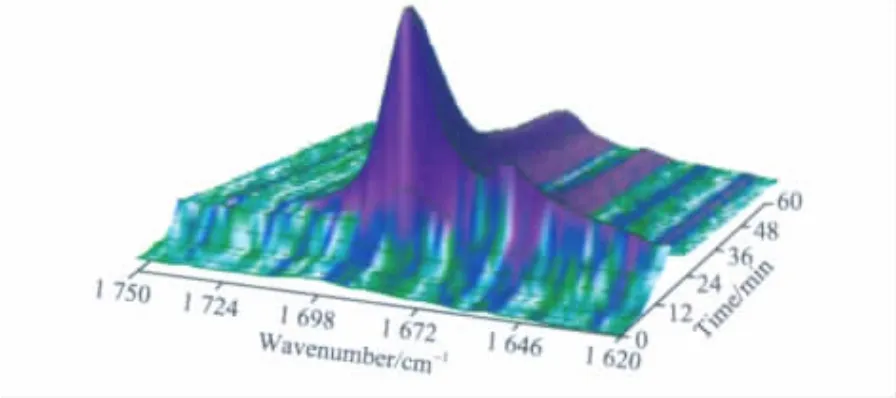
图12 加入DIBP后反应体系放大的三维IR谱图Fig.12 The enlarged 3D IR spectra of the reaction system after adding DIBP.
从图12还可知,1 686 cm-1处的吸收峰较强,而在1 662 cm-1处为弱的肩峰。一般认为加入内给电子体后,由于(110)晶面上的 Mg原子酸性比(100)晶面上的Mg原子酸性大,故MgCl2(110)晶面易于与TiCl4竞争络合DIBP,已负载在(110)晶面上的部分 TiCl4也会被 DIBP取代,生成大量的MgCl2·DIBP络合物。另一方面,图12中1 686 cm-1处的特征峰与图8中纯MgCl2·DIBP络合物在1 689 cm-1处的υC═O特征峰基本一致。因此,图12中1 686 cm-1处的特征峰归属于MgCl2·DIBP络合物中的υC═O。
由图10可看出,TiCl4·DIBP二酯络合物中υC═O的特征峰位于1 636,1 580 cm1处。由此可见,图12中1 662 cm-1处的弱肩峰并非归属于TiCl4· DIBP二酯络合物的 υC═O,而应该归属于 MgCl2,DIBP,TiCl4三者共同作用物中的υC═O。
图12中1 686,1 662 cm-1处的特征峰强度先迅速增强后逐渐减弱。这是由于在线红外分析仪只能检测到溶液体系中的IR吸收,而很难检测到固体表面物质的IR吸收。刚加入DIBP时,由于它本身具有溶剂功能,使得少量的MgCl2溶解于反应体系中,随着反应的进行,DIBP逐渐消耗,溶于其中的络合物又逐渐吸附回MgCl2固体表面。
因此,在氯化镁醇合物体系Z-N催化剂制备过程中,MgCl2,DIBP,TiCl4相互作用的可能情况为:DIBP主要是与活化的MgCl2络合生成MgCl2· DIBP络合物,同时生成少量的MgCl2,DIBP,TiCl4三者共同作用物;因体系中并无TiCl4·DIBP二酯络合物的羰基特征峰,可见DIBP并没有与TiCl4直接进行作用。
3 结论
(1)利用在线红外分析仪对氯化镁醇合物体系Z-N催化剂的制备过程进行了实时监测研究。
(2)在氯化镁醇合物体系Z-N催化剂制备过程的低温反应阶段,为保证催化剂具有良好的颗粒形态,初始温度不高于-10℃较适宜;在升温阶段,当温度升到10~20℃之间时应适当放缓升温速率,以最大限度地消除TiCl4-n(OCH2CH3)n生成速率的突变。
(3)在氯化镁醇合物体系Z-N催化剂制备过程中,当反应体系中加入DIBP后,DIBP主要与活化的MgCl2络合生成MgCl2·DIBP络合物,同时生成少量的 MgCl2,DIBP,TiCl4三者共同作用物,DIBP未与TiCl4直接进行作用。
[1] 李玉芳,伍小明.我国聚丙烯工业的市场前景及发展建议[J].江苏化工,2005,33(4):6-9.
[2] 高明智,李红明.聚丙烯催化剂的研发进展[J].石油化工,2007,36(6):535-542.
[3] 黄文氢,张颖,杨万泰.Ziegler-Natta催化剂的表征研究进展[J].化工进展,2010,29(7):1224-1228.
[4] 费建奇,李刚,荣峻峰,等.新型TiCl4/MgCl2高效聚丙烯催化剂的制备及其结构表征[J].石油化工,2008,37(5):465-469.
[5] 肖士镜,蔡世绵,刘焕勤,等.丙烯聚合载体高效催化剂的研究[J].催化学报,1980,4(1):291-297.
[6] 郑荣辉,曾金龙,曹守镜,等.烯烃聚合Ti-Mg系负载型催化剂的IR光谱[J].福建分析测试,1997,6(1):593-596.
[7] 曹守镜,林瑞霞,曾金龙,等.烯烃聚合高效催化剂化学负载机理和活性中心性质:Ⅰ.红外吸收光谱研究[J].厦门大学学报,1980,(1):70-80.
[8] 齐洪祥.几种在线分析仪表的特点及其在我国石化工业中的应用[J].现代科学仪器,2004,(6):3-5.
[9] 王洪武,张红.在线红外研究H2MDI与PCDL预聚反应动力学[J].聚氨酯工业,2004,24(3):17-19.
[10] 李小红,蒋伟辉.金属氯化醇盐的红外光谱分析[J].广州化学,2008,33(4):43-46.
[11] 李维真.球型乙烯聚合催化剂的制备及性能[J].石化技术,2004,11(2):26-28.
[12] 薛军,高明智,李天益.MgCl2负载TiCl4催化剂中内给电子体对活性组分钛的影响[J].高分子学报,2006,(7):927-930.
[13] 中国石油化工股份有限公司北京化工研究院.烯烃聚合用的球形催化剂组份、制备方法和应用及球形催化剂:中国,1036011C[P].1997-10-01.
[14] 付义,赵增辉.球型MgCl2负载Ziegler-Natta催化剂的制备及影响因素的研究[J].分子催化,2007,21(增刊):2-3.
[15] Yang C B,Hsu C C,Park Y S,etal.Infrared Characterization of MgCl2Supported Ziegler-Natta Catalystsw ith Monoester and Diester as a Modifier[J].Eur Polym J,1994,30(2):205-214.
Study on Preparation of MgCl2Alcohol Complex Supported Ziegler-Natta Catalyst Using Real-Time IR
Liao Yitao,Gao Mingzhi
(Beijing Research Institute of Chem ical Industry,SINOPEC,Beijing 100013,China)
The whole process,including low temperature reaction step,heating step,adding internal donor reaction step and washing step,for preparation of MgCl2alcohol complex supported Ziegler-Natta catalyst,was studied by means of real-time IR.The results showed that the optimum initial temperature in the low temperature reaction step was under-10℃ to get the Ziegler-Natta catalystw ith good shape. In heating step,itwas better to slowdown the heating rate to avoid the sudden change of the forming rate of TiCl4-n(OCH2CH3)n.After adding diisobutyl phthalate(DIBP)as internal donor,MgCl2·DIBP complex compound was produced from DIBP and MgCl2primarily,and a byproduct was also formed from DIBP,MgCl2and TiCl4,but DIBP didn’t reactw ith TiCl4directly on the Ziegler-Natta catalyst.
real-time IR analysis;magnesium dichloride alcohol complex;titanium tetrachloride; diisobutyl phthalate;Ziegler-Natta catalyst
1000-8144(2011)10-1115-06
TQ 426
A
2011-04-26;[修改稿日期]2011-06-26。
廖翼涛(1985—),男,陕西省勉县人,硕士生,电话010-59202642,电邮 ytliao@163.com。联系人:高明智,电邮gaomz.bjhy@sinopec.com。
(编辑 王小兰)
