222例抗肿瘤药致不良反应报告分析
2011-11-06吴洪斌复旦大学附属肿瘤医院药剂科复旦大学上海医学院肿瘤学系上海200032
章 娟,吴洪斌,翟 青(复旦大学附属肿瘤医院药剂科,复旦大学上海医学院肿瘤学系,上海 200032)
药品不良反应(ADR)是在正常用法与用量下与用药目的无关的有害反应。抗肿瘤药具有不同程度的不良反应,不仅影响治疗效果和生活质量,严重时甚至危及患者生命[1]。本文通过对我院2009年1月—2010年12月上报的222例抗肿瘤药的ADR报告进行回顾性分析评价,以了解我院抗肿瘤药ADR发生的特点及规律,加强临床安全用药的指导,做到及早预防、正确处理,进一步提高临床合理用药水平。
1 资料与方法
1.1 资料来源
收集我院2009年1月—2010年12月上报的222例抗肿瘤药ADR报告,均为国家药品不良反应监测中心评价的有效报告。
1.2 方法
对222例抗肿瘤药ADR报告按患者基本情况、原发疾病类型、抗肿瘤药类别、ADR的临床表现和累及器官和(或)系统进行汇总统计分析[2]。
2 结果
2.1 患者基本情况
2.1.1 性别与年龄分布:222例抗肿瘤药ADR报告中,男性63例(占28.38%),女性159例(占71.62%);年龄为24~90岁,平均年龄为54.32岁,中年(41~60岁)患者居多,构成比近60%,见表1。
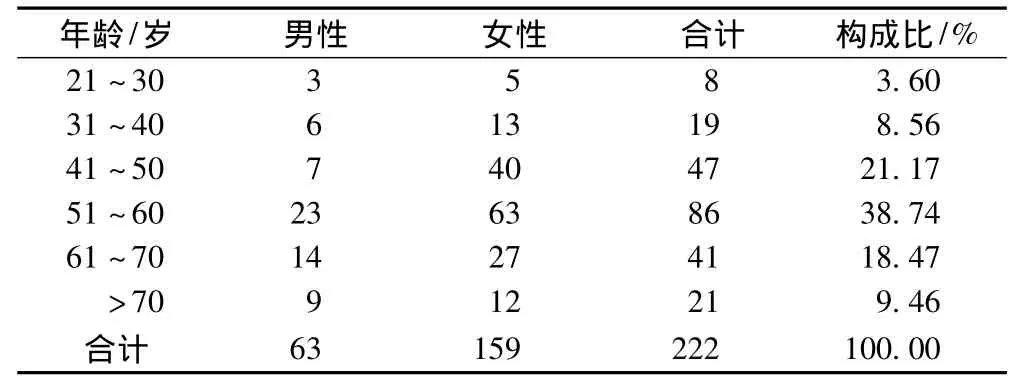
表1 ADR患者性别与年龄分布情况(例)Tab1 Distribution of patients’age and gender of the patients with ADR(cases)
2.1.2 疾病分布:222例抗肿瘤药ADR报告中,原患疾病为消化系统肿瘤有 105例(47.30%),其中大肠癌 83例(37.39%);其次为女性生殖系统肿瘤59例(26.58%),第3位是乳腺癌36例(16.22%),见表2。
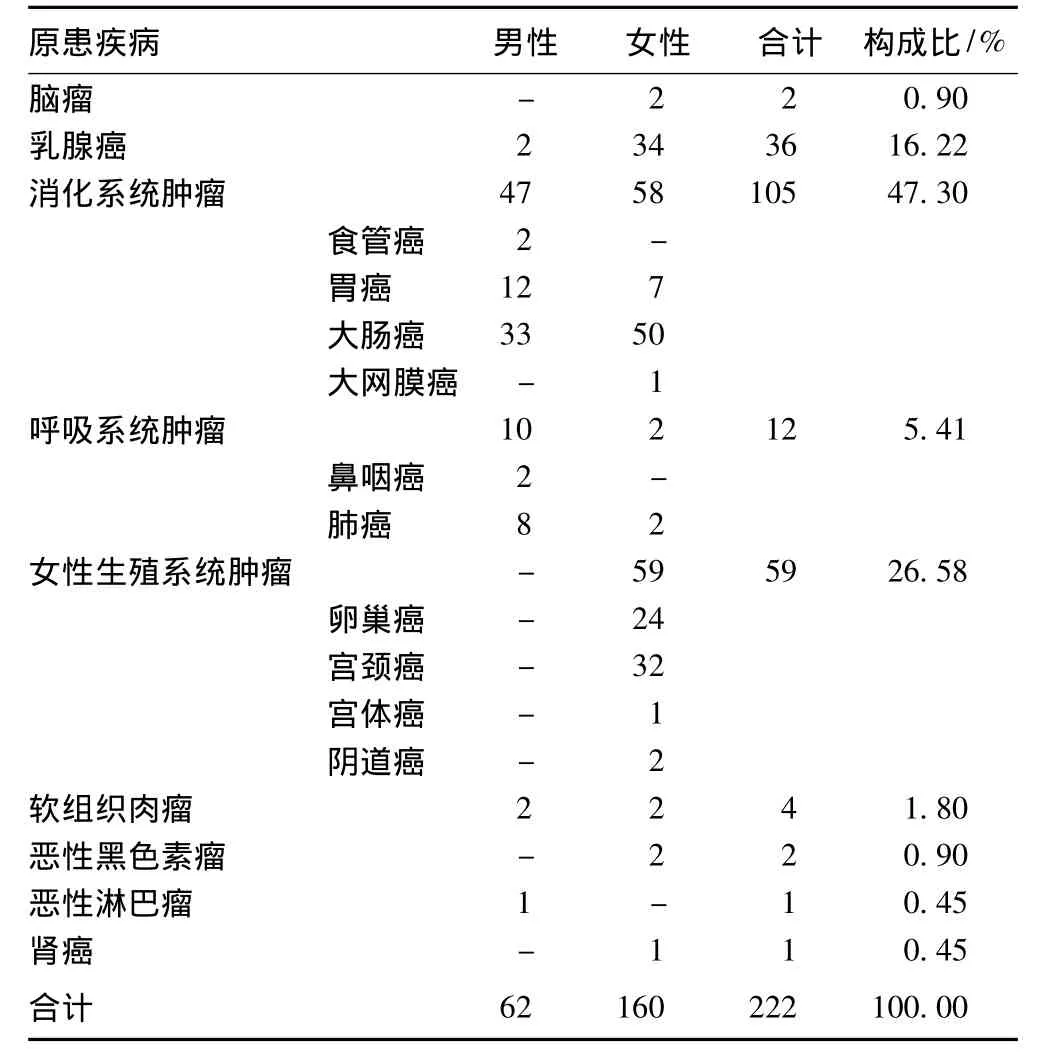
表2 ADR患者原患疾病分布情况(例)Tab2 Distribution of primary diseases of the patients with ADR(cases)
2.1.3 关联性评价:根据卫生部监测中心的ADR关联性评判标准,分为“肯定、很可能、可能、可能无关、待评价、无法评价”。222例抗肿瘤药 ADR报告中评为“肯定”166例(74.77%),“很可能”18例 (8.11%),“可能”32例(14.41%),“可能无关”2例(0.90%),“待评价”4例(1.80%)。
2.2 ADR涉及的抗肿瘤药的种类及构成比
对222例ADR报告中涉及的抗肿瘤药进行分类统计,共涉及到14种抗肿瘤药,居第1位的是铂类药146例(65.77%),其次为紫杉醇类药49例(22.07%),氟嘧啶类药(卡培他滨片)居第3位,共计12例(5.41%),见表3。
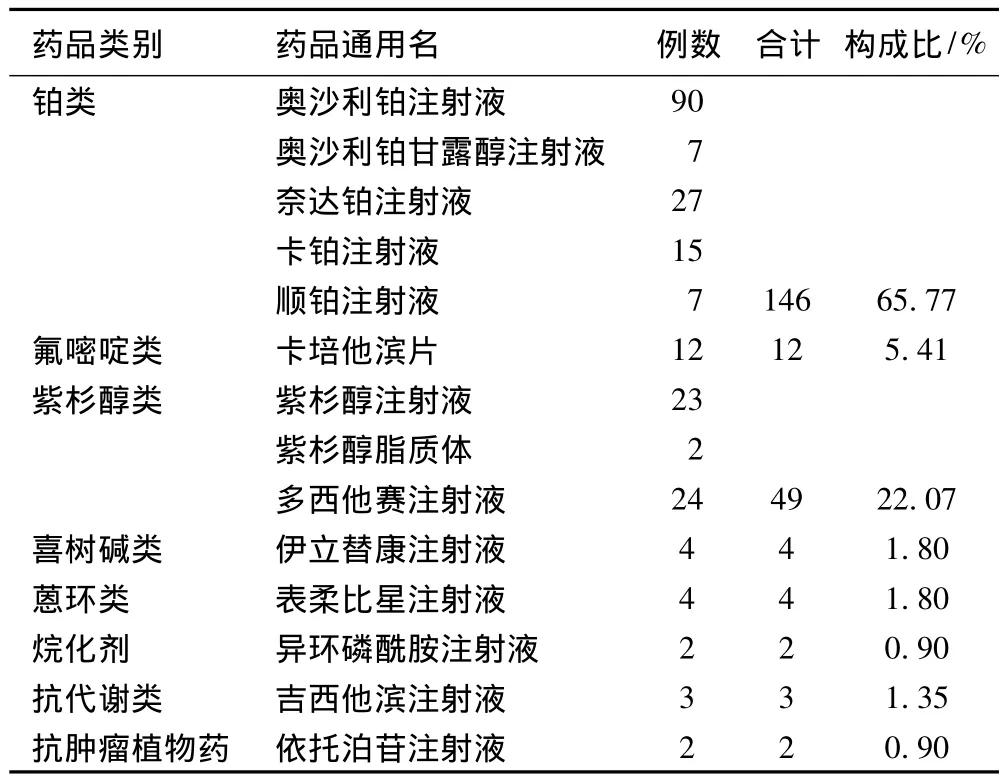
表3 ADR涉及各抗肿瘤药种类及构成比Tab3 Categories and constituent ratio of ADR-involved antitumor drugs
2.3 ADR累及器官和(或)系统及临床表现
222例ADR报告中,219例(98.65%)属一般性ADR,程度均为轻至中度,其中发生率前3位的表现为胸闷、潮红和瘙痒。严重的ADR有3例,包括过敏性休克2例,分别由紫杉醇注射液和注射用盐酸吉西他滨(健择)引起;心脏停搏、昏厥1例,由注射用奥沙利铂引起。经对症及时处理后都好转,对原患疾病没有造成影响。ADR累及的器官和(或)系统主要为神经系统损伤84例(25.53%),循环系统损伤74例(22.50%),皮肤及其附件系统损伤66例(20.06%)。铂类和紫杉醇类药损害器官和(或)系统最多,见表4,ADR累及多个器官和(或)系统的,均分别进行统计,故合计例数>222例。
2.4 发生ADR后再次使用怀疑药品情况
222例ADR中,未再使用怀疑药品83例(37.39%);再次使用怀疑药品发生同样ADR为13例(5.86%);再次使用怀疑药品未发生同样ADR为97例(43.69%);19例(8.56%)是否再次使用怀疑药品情况不明。
3 讨论
3.1 性别与年龄
222例ADR报告中,女性发生率(71.62%)远高于男性(28.38%),这和患者所患疾病有关。我院是上海市唯一的肿瘤专科三级甲等医院,乳腺肿瘤科、妇科肿瘤以及消化道肿瘤科是特色科室,患者多,尤其女性患者较多,所以ADR报告中女性占绝大多数。年龄分布上,多集中于41~60岁的中年人,这个年龄段也是肿瘤的高发阶段,中位年龄在54岁[2,3],近年来恶性肿瘤有逐渐年轻化趋势,所以对青壮年恶性肿瘤患者的ADR监测工作应予以关注。

表4 ADR累及器官和(或)系统及临床表现ADR-involved organs and(or)systems and clinical manifestation
3.2 抗肿瘤药种类
222例ADR报告共涉及抗肿瘤药14种,前3位分别是铂类药(146例),紫杉醇类药(49例),氟嘧啶类药(卡培他滨片12例)。奥沙利铂、卡培他滨是消化道肿瘤尤其是大肠癌的一线治疗药物,疗效明确。紫杉醇、多西他赛、奈达铂、卡铂、顺铂是乳腺癌、妇科肿瘤和头颈部肿瘤的一线治疗药物,此类药物在我院临床应用范围广,使用频率高,用量大,因而其ADR发生的比例也相对较高。同时,铂类和紫杉醇类引起的ADR多表现为神经系统、循环系统和消化系统症状[4-6],如发热、胸闷、头痛、恶心及神经毒性等,并多发生于用药过程中,ADR的关联性易于判定,故这3种药物ADR呈报率相对较高。因此临床选用此类抗肿瘤药时,应对其ADR予以重视,尤其应详细询问患者用药史,给药过程中要密切关注患者用药反应。
3.3 临床表现
222例ADR报告以神经系统损伤最常见(84例次),主要临床表现为头晕、发热、出汗、脸色苍白、口舌麻木、震颤、意识模糊等感觉障碍。抗肿瘤药进入人体后易引起发热,主要通过激活并释放内源性致热源;此类药物引起肿瘤细胞大量坏死脱落也是造成发热等症状的重要原因[5]。发热症状通常于输注过程中发生,停药后体温恢复正常。该反应的临床表现较明显,容易引起临床重视。
循环系统损伤74例次,主要在心脏毒性、血管损伤和骨髓抑制,临床表现为胸闷、胸痛、心悸、气急、晕厥、心脏停搏、白细胞计数减少等,大多数抗肿瘤药均有此类ADR[4]。但222例ADR中,此类损伤占得比例并不是最高,可能存在漏报,因为ADR涉及的大多数为化疗患者,血常规报告未能及时获取,病房中相关ADR上报工作未及时跟进。
消化系统损伤33例次,消化系统是化疗药物引起的早期最常见的毒性[7],主要表现为恶心、呕吐、腹痛、腹泻等症状,这种损伤一般可以在化疗前服用止吐药或者胃黏膜保护剂进行预防。
抗肿瘤药的过敏反应时常发生,程度一般轻至中度,如紫杉醇类药和奥沙利铂的过敏反应发生率高,主要临床表现为瘙痒、皮疹、荨麻疹等,为防止出现严重过敏反应,通常需要在化疗前采取相应的预防措施,如紫杉醇类药化疗前常规使用地塞米松、抗组胺药和西咪替丁;有过敏体质的患者在使用奥沙利铂时也需常规静脉使用地塞米松5~10 mg预防,且在用药期间需密切观察[8-10]。
氟嘧啶类药(卡培他滨)容易出现皮肤色素沉着和手足综合征,手足综合征是由于化疗药物在手足毛细血管部位渗出致周围组织损伤的不良反应,停药后症状逐渐消退,口服大剂量维生素 B6片可减轻症状[11,12]。
222例ADR中,严重的有3例,表现为过敏性休克2例,分别由紫杉醇注射液、注射用盐酸吉西他滨(健择)引起;心脏停搏、昏厥1例,由注射用奥沙利铂引起。紫杉醇过敏反应发生率为39%,其中严重过敏反应发生率2%[9],常发生在用药2~3 min,根据ADR发生过程来看,预防措施也合乎规范,可能由于个体差异等因素导致严重ADR发生;奥沙利铂的ADR主要为神经毒性和过敏反应,神经毒性发生率为82%,过敏反应发生率为12%,仅有1% ~2%的患者出现为3或4级严重症状,该例患者出现心脏停搏、昏厥,视为新的严重的ADR,国内外较罕见,在以后的监测中应引起高度重视[13]。盐酸吉西他滨(健择)引起的过敏反应通常为轻度,非剂量性毒性,常规对症治疗都能有效控制,但也有例外,小于1%的患者可发生严重过敏反应,一旦遇到严重过敏反应的患者,常规处理为静脉给予肾上腺素和地塞米松、苯海拉明等抗过敏药,及时给予氧气吸入,并作相应其他对症处理[14]。
大部分抗肿瘤药在杀伤肿瘤细胞的同时,对正常组织细胞、器官不可避免地产生损害或毒副作用,而这些毒性反应很多是可以预测的,临床使用时要注意密切监测,同时做好相应的防治措施,最大限度地提高疗效,并减少ADR的发生。只有充分地了解抗肿瘤药的不良反应和掌握防治措施,加强ADR的监测,及时上报,尤其注意抗肿瘤药严重的和新的ADR信息的沟通和交流,才能更加合理地使用抗肿瘤药,提高患者的生活质量。
[1]金振波,孙文辉,田德蔷.我院2005—2008年药品不良反应报告回顾性分析[J].中国药学杂志,2009,44(21):1676.
[2]王喆元,吴洪斌,凌云华,等.我院2009年57例抗肿瘤药品不良反应报告分析[J].上海医药,2010,31(11):512.
[3]周际昌.实用肿瘤内科学[M].第2版.北京:人民卫生出版社,2003:343-346,389-393,395-397.
[4]杨 梅,汤致强.抗肿瘤药的不良反应及防治措施[J].中国新药杂志,2008,17(21):1889.
[5]年 华,马明华,徐 泯,等.抗肿瘤药品不良反应报告72 例分析[J].中国新药与临床杂志,2010,29(9):704.
[6]金雪梅.铂类药物的毒性作用与预防措施[J].现代医药卫生,2010,26(21):3294.
[7]王正艳,李向东.紫杉醇导致过敏的防治[J].癌症进展,2009,7(1):114.
[8]周爱萍,王奇璐.抗肿瘤药对消化系统的不良反应及其防治[J].实用肿瘤杂志,2002,17(2):79.
[9]吴洪斌.紫杉醇注射液不良反应的预防及处理[J].中国新药杂志,2002,11(2):168.
[10]吴洪斌,陆 益.多西紫杉醇的不良反应及预防处理[J].药品不良反应杂志,2004,6(4):218.
[11]凌云华,吴洪斌,吴 薇,等.119例口服卡培他滨片不良反应分析[J].中国医院用药评价与分析,2008,8(3):224.
[12]王春敏,吴洪斌.卡培他滨的不良反应及其处理方法[J].中国新药杂志,2003,12(2):138.
[13]姚志东,吴洪斌.奥沙利铂的安全性评价[J].中国新药杂志,2003,12(7):567.
[14]吴洪斌,潘丽琴,刘加葳.吉非替尼不良反应的临床表现及其处理[J].药品不良反应杂志,2003,5(3):176.
