复方苦参注射液联合盐酸羟考酮控释片治疗癌性疼痛的临床观察
2011-11-06关念波中国中医科学院广安门医院肿瘤科北京100053
关念波,林 飞(中国中医科学院广安门医院肿瘤科,北京 100053)
癌性疼痛是疼痛部位需要修复或调节的信息传到神经中枢后引起的感觉,是造成肿瘤晚期患者主要痛苦的原因之一。据WTO统计,世界上大约有超过70%的肿瘤中晚期患者正承受着不同程度的癌性疼痛,疼痛极大地影响其生活质量。临床治疗中,中重度癌性疼痛患者给予阿片类药镇痛已成为标准治疗,但临床工作中发现,单纯通过增大镇痛药剂量有时仍达不到满意效果。复方苦参注射液由苦参、白土苓等中药精制而成,在临床上具有抗肿瘤、镇痛、提高免疫力的功效[1]。本研究观察了我科自2007年1月—2010年1月应用复方苦参注射液联合盐酸羟考酮控释片治疗300例癌性疼痛患者的临床疗效,现报告如下。
1 资料与方法
1.1 一般资料
2007年1月—2010年1月收入我科的晚期癌性疼痛患者,均已经病理学或细胞学确诊。入选患者300例,按入院的顺序随机分为2组,经伦理委员会批准,入组患者签署了知情同意书。
对照组患者150例,其中中度疼痛79例,重度疼痛71例;男性83例,女性67例,平均年龄(68.3±5.6)岁;其原发病组成:肺癌62例,胃癌23例,乳腺癌23例,直肠癌14例,肝癌10例,宫颈癌9例,前列腺癌3例,食管癌3例,卵巢癌2例,恶性淋巴瘤1例,脑瘤0例;其中合并远处转移79例。治疗组患者150例,其中中度疼痛81例,重度疼痛69例;男性85例,女性65例,平均年龄(66.7±5.3)岁;其原发病组成:肺癌61例,胃癌23例,乳腺癌21例,直肠癌15例,肝癌12例,宫颈癌8例,前列腺癌3例,食管癌2例,卵巢癌2例,恶性淋巴瘤2例,脑瘤1例;其中合并远处转移77例。2组患者性别、年龄、病种、体能状况、疼痛程度均具有可比性,差异无统计学意义(P>0.05)。
根据治疗组患者症状及舌苔脉象情况,分为湿浊内阻组及气血亏虚组。湿浊内阻组患者75例,其中中度疼痛39例,重度疼痛36例;气血亏虚组75例,其中中度疼痛42例,重度疼痛33例。2组患者性别、年龄、病种、体能状况、疼痛程度均具有可比性,差异无统计学意义(P>0.05)。
1.2 治疗方法
对照组患者每12 h给予盐酸羟考酮控释片20 mg;治疗组患者于对照组治疗基础上,每日加用复方苦参注射液20 mL+0.9%氯化钠注射液250 mL。2组患者连续治疗1周后按照WHO疼痛分级进行疗效评价,对于治疗癌性疼痛有效者,给予原治疗方案维持治疗30 d,不予减量;治疗无效者,调整治疗方案。
1.3 观察项目
1.3.1 疼痛评估:治疗前疼痛按照 WHO疼痛程度分级(VRS)[3]。0级:无痛。1级(轻度):虽有疼痛但可以忍受,能正常生活,睡眠不受干扰。2级(中度):疼痛明显,不能忍受,要求服用止疼剂,睡眠受干扰。3级(重度):疼痛剧烈不能忍受,需要止疼剂,睡眠受到严重干扰,可伴有植物神经紊乱或被动体位。显效:疼痛减轻Ⅱ度以上;有效:疼痛减轻Ⅰ度;无效:疼痛未减轻或虽有减轻但疗程中又回至原有程度及以上。
1.3.2 生活质量评估:评估肿瘤患者的食欲、精神、睡眠、日常活动、与人交往5项生活质量指标,采用1~5数字评分法,1分为最差,5分为最好[2]。5项指标总分满分为25分,>15分为生活质量良好,≤15分为生活质量差。
1.3.3 不良反应观察:每个疗程治疗前后各检查1次心电图、肝肾功能及血常规。
1.4 统计学方法
采用SPSS 17.0统计分析软件进行数据分析,2组患者治疗前后的变化采用χ2检验或非参数检验,P<0.05表示差异具有统计学意义。
2 结果
2.1 镇痛效果
2组镇痛效果见表1。(1)治疗组与对照组:治疗组癌性疼痛显效125例,有效18例,总有效率95.33%,对照组癌性疼痛显效112例,有效23例,总有效率90.0%,2组间显效率有显著性差异,有统计学意义(P<0.05);总有效率无显著性差异,无统计学意义(P>0.05)。(2)湿浊内阻组与气血亏虚组:湿浊内阻组癌性疼痛显效66例,有效7例,总有效率为97.33%;气血亏虚组癌性疼痛显效59例,有效11例,总有效率为93.33%。2组间显效率有显著性差异,有统计学意义(P<0.05),总有效率无显著性差异,无统计学意义(P>0.05),复方苦参组对湿浊内阻型有更好的疗效趋势。(3)湿浊内阻组与对照组:将治疗组中的气血亏虚组病例剔除掉,湿浊内阻组癌性疼痛显效 66例,有效7例,总有效率为97.33%;对照组癌性疼痛显效112例,有效23例,总有效率90.00%。2组间显效率有显著性差异,有统计学意义(P<0.05),总有效率有显著性差异,有统计学意义(P<0.05)。
2.2 生活质量变化
2组患者治疗前后生活质量变化见表2。(1)治疗组与对照组:治疗组治疗前后生活质量良好率分别为58.7%和86.2%,对照组治疗前后生活质量良好率分别为59.3%和84.7%,2组生活质量改善无显著性差异,无统计学意义(P>0.05)。(2)湿浊内阻组与气血亏虚组:湿浊内阻组治疗前后生活质量良好率分别为60.0%和88.0%,气血亏虚组治疗前后生活质量良好率分别为57.3%和84.0%,2组生活质量改善无显著性差异,无统计学意义(P>0.05)。(3)湿浊内阻组与对照组:湿浊内阻组治疗前后生活质量良好率分别为60.0%和88.0%,对照组治疗前后生活质量良好率分别为59.3%和84.7%,2组生活质量改善无显著性差异,无统计学意义(P>0.05)。
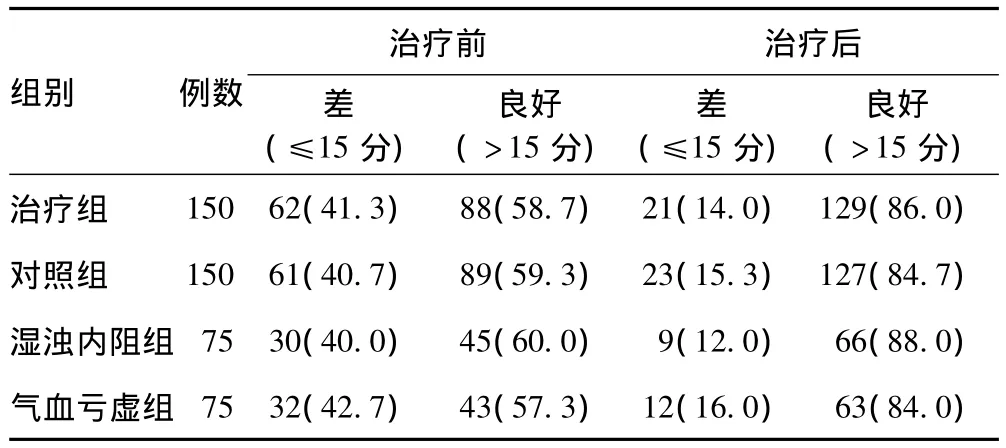
表2 试验患者组间生活质量比较Tab2 Quality of life in two treatment groups
2.3 不良反应
治疗前后心电图、肝肾功能及血常规检查无明显变化。治疗组14例出现腹部不适,8例恶心,5例便秘;对照组22例出现腹部不适,13例有恶心,13例便秘,经对症处理后均消失。
3 讨论
癌性疼痛是肿瘤患者尤其是中晚期终末期肿瘤患者的主要症状之一,癌性疼痛不仅引起患者躯体的不适,同时从心理、生理、精神和社会等多方面干扰和破坏患者的生存质量,即使在发达的国家仍有50%~80%的肿瘤患者没有得到满意缓解[3]。处理好癌性疼痛已成为临床医师所面临的一个棘手问题,有效的镇痛治疗是WHO肿瘤综合规划中4项重点之一。
中医对疼痛的理论概括为2点:不通则痛、不荣则痛。造成不通则痛的常见病因有湿滞、痰阻、血瘀、气郁、寒凝等,造成不荣则痛的病因常见为气血不足、阴阳亏虚。复方苦参注射液主要成分为苦参、白土苓,苦参味苦性寒,有清热燥湿之效,白土苓味甘性淡平,有健脾除湿之效,两者相合,共奏祛湿镇痛之效。痛物质(如PGE2)的存在为肿瘤引起疼痛的主要因素,有学者认为,复方苦参注射液是通过抑制肿瘤浸润或转移的病理产物如PGE2的合成而达到镇痛的作用[5]。动物试验表明,复方苦参注射液有明显的镇痛作用,强度与哌替啶相似,可使小鼠痛阈值显著升高,对肿瘤引起的轻、中度疼痛具有一定的疗效[6]。近期许多临床文献资料报道,复方苦参注射液可明显缓解肿瘤患者的疼痛。虽然复方苦参注射液对癌性疼痛的疗效已经被多篇文献所报道,但对于个体化治疗的泛泛研究是不够的,根据中医辨证分型,更有针对性的治疗才是规范使用中药制剂的正确方法。
本研究为临床应用复方苦参注射液联合盐酸羟考酮控释片治疗癌性疼痛的疗效观察。研究结果显示,治疗组患者癌性疼痛缓解显效率高于对照组,差异有统计学意义(P<0.05),证明复方苦参注射液联合盐酸羟考酮控释片对癌性疼痛具有很好的治疗作用,尤其是在减轻疼痛程度上明显优于单纯使用盐酸羟考酮控释片组。而治疗组中,湿浊内阻组患者癌性疼痛缓解显效率高于气血亏虚组,差异有统计学意义(P<0.05),证明在辨证分型情况下,复方苦参注射液联合盐酸羟考酮控释片对湿浊内阻的癌性疼痛患者较气血亏虚组具有更好的镇痛作用。虽然治疗组和对照组在总有效率上差异没有统计学意义,但是在辨证分型后对比湿浊内阻组与对照组,2组间显效率及总有效率比较均有显着性差异,有统计学意义(P<0.05)。此研究结果证明,复方苦参注射液联合盐酸羟考酮控释片对湿浊内阻型患者组具有更好的效果。
在患者生活质量改善方面,治疗组和对照组在统计学上无显著差异,在辩证分析后虽然湿浊内阻组与气血亏虚组在统计学上依然没有显著差异,但可以看出湿浊内阻组有更好的改善生活质量的趋势,考虑到样本量较小的原因,所以统计学上未见显著差异,有待将来扩大样本量继续深入研究。全组患者血常规、肝功能、肾功能及心电图检查,治疗前后未见影响。总之,复方苦参注射液治疗癌性疼痛的疗效肯定,不良反应轻微。
免除疼痛是患者的基本权利,更是医务人员的神圣职责。随着医学的进步,应对癌性疼痛患者进行个体化的治疗,减轻患者癌性疼痛,提高其生活质量。
[1]陈建清,唐辉华.复方苦参注射液治疗癌痛的疗效观察[J].四川肿瘤学防治杂志,2002,15(4):237.
[2]孙 燕,顾慰萍.癌症三阶梯止痛指导原则[M].第2版.北京:北京医科大学出版社,2002:100-101.
[3]王宏羽.癌症疼痛缓解及姑息性治疗[M].北京:人民卫生出版社,2005:52.
[4]张天泽,徐光炜.肿瘤学[M].天津:天津科学技术出版社,2006:730.
[5]陈旭兰.中医药缓解癌性疼痛的机理探讨[J].中国现代药物应用,2008,2(18):113.
[6]张 彦,蒋红凯,刘小珊,等.苦参碱诱导K562白血病细胞分化和凋亡的实验研究[J].癌症,2008,19(8):756.
[7]张志明.复方苦参注射液治疗癌痛的疗效观察[J].中国医院用药评价与分析,2009,9(4):310.
[8]陈素琼,马玉英,王 伟,等.硫酸吗啡控释片联合复方苦参注射液治疗癌痛的疗效评价[J].中国医院用药评价与分析,2007,7(4):310.
