光学活性1,1'-联-2-萘酚类合成受体的应用研究新进展*
2011-09-24郭志龙汤立军魏恭繁
郭志龙,汤立军,魏恭繁
(渤海大学 化学化工学院,辽宁省功能化合物的合成与应用重点实验室 辽宁 锦州 121013)
光学活性1,1'-联-2-萘酚类合成受体的应用研究新进展*
郭志龙,汤立军**,魏恭繁
(渤海大学 化学化工学院,辽宁省功能化合物的合成与应用重点实验室 辽宁 锦州 121013)
具有光学活性的1,1'-联-2-萘酚及其衍生物由于其本身具有C2对称轴而具有独特的化学性质和手性诱导功能,且在适合结构基团修饰下能产生很强的荧光,在不对称催化和手性客体的荧光识别等方面得到了广泛的应用。在与手性胺、手性醇、糖类、手性阴离子、手性氨基醇和手性氨基酸等手性化合物作用时,该类受体在不同位点接受客体分子,通过光诱导电子转移(PET)及电子交换能量转移(EET)等引起分子内能级变化,使得所有这些相互作用十分灵敏的在其发光强度和能量上反映出来,用光谱仪可监测到这些变化。综述了近年来光学活性1,1'-联-2-萘酚衍生物在手性客体的识别以及作为人工模拟酶对手性α-氨基酸的构型转换两方面的最新应用研究进展。
1,1'-联-2-萘酚;荧光化学传感器;手性识别;构型转换
Abstract:Optically active BINOL and its derivatives have unique chemical properties and chiral inductive function because of the C2symmetric axis.When they are introduced into a suitable functional group,they can produce strong fluorescence,so they are widely applied in asymmetric catalytic reactions and fluorescence recognition of chiral object.This kind of compounds can be used as excellent fluorescent chemosensors because of the alteration can be sensitively reflected by their fluorescence intensity.When interacting with different kinds of chiral compounds such as chiral amines,alcohols,saccharides,chiral anions,amino alcohols and amino acids,an intramolecular energy level changes can be produced by photo-induced electron transfer(PET)and electronic energy transfer(EET)mechanisms,which can be monitored by fluorescence intensity changes.The recent advances of optically active 1,1'-bi-naphthol derivatives as fluorescent chemosensors for chiral object recognition as well as the application of some 1,1'-bi-naphthol derivatives as artificial enzyme for chiral inversion of α-amino acids are summarized.
Key words:1,1'-Bi-2-naphthol;fluorescent chemosensor;chiral recognition;chiral inversion
引 言
具有光活性的1,1'-联-2-萘酚(BINOL)及其衍生物是一类不含手性中心,但具有C2对称轴的阻转异构化合物。两个萘环的转动受到限制使分子具有很好的构造稳定性,具有很强的手性诱导作用。BINOL具有分子的轴不对称性,刚性和韧性等独特的化学性质,因此受到有机合成化学家的普遍青睐。由于其优异的不对称诱导和手性识别能力,以及能够与合适的过渡金属形成配合物,已被作为拆分试剂,诱导试剂,位移试剂,不对称合成的催化剂[1,2]以及高效液相色谱的手性固定相[3]等各个领域。
1 光学活性1,1'-联-2-萘酚类衍生物对手性客体的识别
1.1 手性胺、手性醇及糖类的识别
近些年关于使用光学活性1,1'-联-2-萘酚衍生物对手性胺和手性醇进行对映选择识别的研究已有较多报道,成义祥教授课题组[4]对于近几年的相关研究报道做了较为详细的总结。
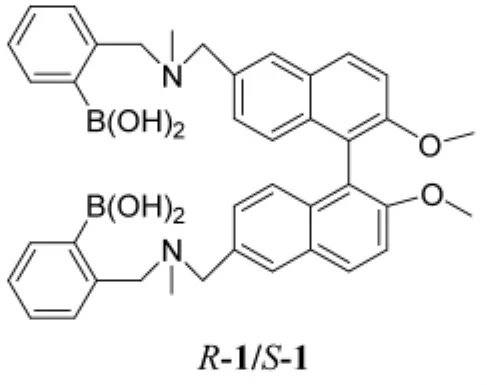
光学纯的糖醇类化合物如D-山梨醇和D-甘露醇作为生物体新陈代谢的重要中间件而广泛应用于药物领域,但是识别这类手性物质的荧光传感器却比较少。赵建章[6]等在总结了近年来关于糖醇的研究报道基础上设计合成了一类6,6’-硼酸取代的1,1'-联-2-萘酚衍生物分子S-1和R-1,并研究了其对一些手性糖类物质的识别。通过在pH=9的体系中的滴定实验验证了二者与D-山梨醇的结合常数分别为 KS=(9.30±1.75)×103M-1,KR=(2.63±1.55)×102M-1,比值约为 KS/KR=35:1。此外发现受体S-1对D-山梨醇和D-甘露醇的选择性为20∶1。这说明由于受体本身的手性特性,可对同类客体有不同的对映选择性和化学选择性。
1.2 手性阴离子的识别
阴离子在生命科学和化学过程中扮演着越来越重要的角色,具有重要生物学意义的阴离子的识别研究越来越受到人们的广泛关注并成为当前超分子化学研究领域的重要课题。何永炳等[7]将包含不同碳原子数的硫脲基团引入1,1'-联-2-萘酚骨架中合成受体了分子2a和2b,研究了它们对扁桃酸阴离子的识别作用。经试验发现受体2a的荧光被猝灭的比例很小,ΔIL/ΔID≈1.04。而在同样的条件下,受体2b被猝灭的比例为ΔIL/ΔID≈3.3,这说明受体2b对扁桃酸阴离子的两种对映体具有很好的对映选择性。经荧光、紫外和核磁光谱验证,此两种受体分子可与客体阴离子形成1∶1结合的配合体,其中2b在加入扁桃酸阴离子后,颜色变化明显,肉眼可见,这说明2b可用来作为扁桃酸阴离子的对映选择比色化学传感器。
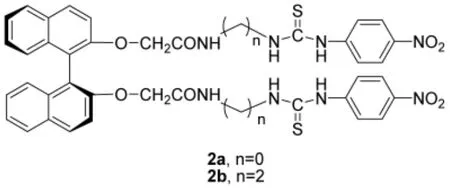
余孝其等[8]直接在1,1'-联-2-萘酚的3,3'位接入咪唑基,合成了受体分子3。使用3对一些α-氨基酸的响应进行了研究,发现3对N-Boc-丙氨酸阴离子有很好的对映选择性识别能力,其结合常数比为(KL/KD=4.5)。

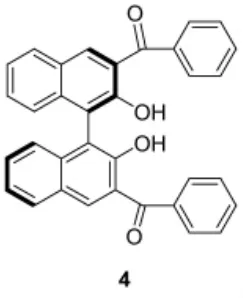
王超杰等[9]合成了一类S型的含有苯甲酰基的1,1'-联-2-萘酚的衍生物受体分子4,并研究了其在氯仿中对各种手性阴离子的识别性能。当在受体溶液中加入S和R型的N-Boc-丙氨酸阴离子的时候,二者对受体的荧光发射强度的猝灭能力明显不同,达到ΔIS/ΔIR=3.12,这表明受体4对N-Boc-丙氨酸阴离子的两种对映体有很好的对映选择性。
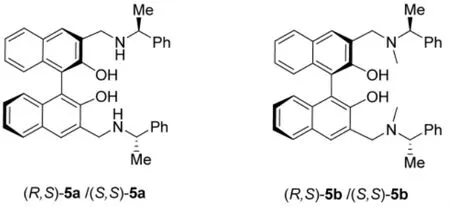
冯小明等[10]合成了一类含有苄基氨甲基的1,1'-联-2-萘酚衍生物分子(R,S)-5a、(S,S)-5a以及它的衍生物分子(R,S)-5b、(S,S)-5b,并用它们对一些外消旋氨基酸衍生物进行了识别研究。当采用混合溶剂(CH2Cl2:hexane=3:7,加 1.2%的 THF),发现在此溶剂体系中,受体(R,S)-5a、(R,S)-5b和(S,S)-5a的荧光强度在加入N-Boc-脯氨酸后得到了很大幅度的增强。其中L-N-Boc-脯氨酸对受体(R,S)-5a的荧光强度的增幅达57倍,而在同样条件下,D-N-Boc-脯氨酸仅使其荧光强度增至6倍。而受体(R,S)-5b对N-Boc-脯氨酸的两种对映异构体的对映选择性却较差。
1.3 手性氨基醇和手性氨基酸的识别
除了养殖环境以外,养殖技术在稻田淡水龙虾的养殖过程中起到至关重要的作用。但是,从我国稻田淡水龙虾养殖的实际情况来看,养殖技术较为落后,主要有以下几个方面的原因:①我国的稻田淡水龙虾养殖工作深受传统龙虾养殖观念的影响,所以对养殖技术的关注度比较低,很难顺应龙虾养殖业的发展潮流;②稻田淡水龙虾养殖技术较为复杂,要想实现对其关键点的综合把握难度较大。
手性氨基酸和手性氨基醇都具有双官能团,1,1'-联-2-萘酚衍生物对它们的识别过程中,两个官能团都可参与同识别位点的结合作用。为了方便叙述与讨论,在此本文将氨基酸及氨基醇的识别进展放在一起讨论。
Pu Lin等[11]在1,1'-联-2-萘酚上引入额外两个醇羟基合成了带有四个羟基的1,1'-联-2-萘酚衍生物分子6a以及它的衍生物6b和6c。与1,1'-联-2-萘酚相比,6a中额外的两个羟基能够加强受体分子与氨基醇的结合能力,从而显著地增强了氨基醇对受体的猝灭效率。作者用R-苯丙胺醇对四种受体的荧光猝灭性质进行了研究,发现,6a的荧光强度被猝灭的最为显著。

Kim等[12]应用带有苯基脲基的化合物7开展了手性1,2-氨基醇的对映选择性识别。在氘代苯中,使受体与2倍量的S或R-氨基醇充分反应,生成希夫碱,利用核磁共振氢谱分析受体对1,2-氨基醇的对映选择性,发现受体7对1,2-氨基醇具有相同的立体选择性,即对R型的氨基醇具有选择性。若将酚羟基变为甲氧基,对映选择性能力显著降低,且改变了立体选择性,即对S型的氨基醇有较好的选择性。
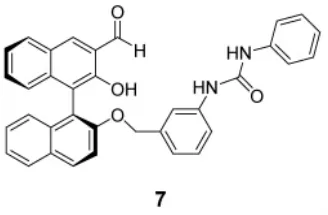
Nandhakumar等[13]在受体7的基础上引入各种取代基,包括吸电子基和供电子基,合成了受体8a~8d。通过考察这些受体与手性氨基醇的对映选择识别,经1H NMR研究发现,连有吸电子基的受体8d对氨基醇的立体选择性的识别略有提高,而连有供电子基的受体8a却略有降低。

Kim等[14]还合成了一类具有吡咯-2-酰胺基的1,1'-联-2-萘酚受体分子9a以及它的衍生物分子9b、9c和9d,并将这些受体用于手性1,2-氨基醇的识别研究。通过1H NMR检测计算出受体与各种氨基醇的相应的KR/KS发现,9a对各种R与S构型氨基醇的对映选择性最好。这说明吡咯-2-酰胺的结构单元是一种非常有效的结合醇羟基的基团,可广泛应用于手性识别的受体分子的合成与应用领域。

Nandhakumar等[15]尝试了在1,1'-联-2-萘酚醛基础上引入脲基、硫脲基和胍基基团,合成3种新型的受体10a、10b和10c,研究了受体对氨基醇的选择性。但实验结果表明,这种氢键供体单元的结构修饰,效果并不很理想。受体10a和10b对氨基醇的对映选择性为(KR/KS=2~4),受体10c为(KR/KS=4~8),这与以往报道的对映选择性能力相近,并无较大提高。

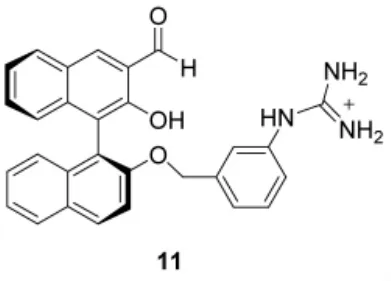
为进一步增强受体与氨基醇间的氢键作用,汤立军等[16]合成了一种新型的胍基1,1'-联-2-萘酚衍生物受体分子11,利用质子化的胍基部分可提供电荷增强的氢键 (Charge Reinforced Hydrogen Bonding,CRHB),大大提高了对手性氨基醇的对映选择性识别能力,比如11对于2-氨基-1-丁醇的两种异构体的对映选择性KR/KS达到了15,这比以往报道的KR/KS介于2~4的中等选择性有很大提高。值得注意的是,尽管11是一个胍盐,但其在CHCl3中具有较好的溶解性,因此识别反应可在CHCl3中进行,方便NMR检测。此外,11还可以用于外消旋氨基醇的萃取拆分,可得到e.e值大于95%的R-氨基醇,使11在手性氨基醇的萃取分离方面具有较好的应用前景。
Ahn等[17]合成了一种基于1,1'-联-2-萘酚骨架的含有C2对称轴的手性分子12,其对外消旋氨基酸的手性识别可以由质子偶合的19F NMR进行检测。受体12对α-位带较大烃基的氨基酸(如色氨酸、苯甘氨酸、苯丙氨酸)的对映选择性要好于α-位带较小取代基的氨基酸(如缬氨酸、亮氨酸)。受体12与氨基酸之间这种通过可逆共价键的形成进行对映选择性识别的报道尚属首次,可广泛应用于外消旋氨基酸对映体的识别及纯度的检验。

2 1,1'-联-2-萘酚类人工模拟酶对手性α-氨基酸的构型转换
磷酸吡哆醛是一种天然辅酶,是维生素B6的辅酶形式,参与氨基酸代谢中的转氨基作用[24,25],可将L-丙氨酸转换成D-丙氨酸。通常L-氨基酸可靠发酵法获得,而D-氨基酸目前尚无法通过发酵法生产。D-氨基酸是手性药物、手性农药、手性食品添加剂的关键中间体,在医药、农药和食品领域有着广泛的应用前景。
Kim教授课题组[26]首次报道了利用人工模拟酶进行的手性α-氨基酸构型转换研究。他们采用7作为磷酸吡哆醛的模拟酶分子,使其在室温及适量的三乙胺存在下,与过量的L-氨基酸作用,形成希夫碱,在分子内共振辅助氢键的作用下,所生成的亚胺在三乙胺的催化作用下可以发生差向异构化,使L-α-氨基酸转变为D-α-氨基酸,并采用NMR跟踪了转变的过程,发现在48h内,大多数L-氨基酸都可以达到转换的平衡。最后利用酸性条件下亚胺的水解反应释放出D-氨基酸。NMR研究发现,受体对于所研究的L-氨基酸具有相同的L到D的转换作用。7可用作外消旋氨基酸的拆分剂并能重复使用,且对于产率和光学纯度无明显降低。
此外Nandhakumar等[18]还用受体8进行了手性氨基酸构型转换的研究。与识别手性氨基醇结果类似,连有吸电子基受体8d对氨基酸的转换效率略高于受体7,而连有供电子基的受体8a略低于7,尽管受体8d这种效率的提高并不显著,但它对以后设计更有效的受体有很好的启发性。
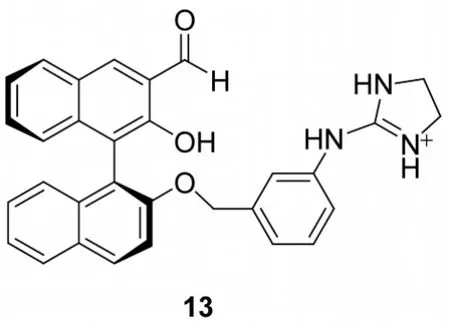
含有胍基的受体11由于可提供电荷加强型氢键(CRHB)而对氨基醇有很好的对映选择性,据此,汤立军等[28]合成了胍基受体13,与前述受体相比,13对大多数的氨基酸均有更好的对映选择性(KD/KL>11),其中对谷氨酸的对映选择性KD/KL达到19/1。13在氯仿中的良好溶解性使得13可作为外消旋α-氨基酸的手性转换试剂和对映选择萃取剂,具有很高的实际应用价值。
3 结语
本文综述了近年来光学活性1,1'-联-2-萘酚衍生物在手性客体的识别以及作为人工模拟酶对手性α-氨基酸的构型转换两方面的最新应用研究进展。在手性分子的识别研究中,如何使主体分子与客体分子具有高度的空间互补性以及合适的结合作用位点,从而提高受体对客体分子的选择性,并能引起受体显著的荧光光谱变化或能量变化,是这类化学传感器分子设计的重点和难点。作为人工模拟酶分子进行手性α-氨基酸的构型转换是光学活性1,1'-联-2-萘酚衍生物的新的应用领域,尽管目前的研究还有很多不完善之处,但是这方面的研究无疑具有重要的理论意义和广阔的应用开发前景。
[1]袁小亚,张政朴.聚合物负载的手性联二萘酚的合成及其在不对称催化中的应用进展[J].有机化学,2007,27(12):1479~1490.[2]王伟,段振华,李宝林.联二萘酚配合物催化的不对称异原子Diels-Alder反应研究进展[J].化学研究,2007,18(2):93~97.
[3]刘天穗,陈亿新,刘军涛,等.柱前衍生化高效液相色谱法拆分1,1′-联-2-萘酚光学异构体[J].精细化工,2007,24(11),1091~1094.
[4]黄辉, 郑立飞, 邹小伟,等.基于1,1′-联-2-萘酚衍生物的手性荧光传感器[J].化学进展,2008,20(4):507~517.
[5]LIN P.Fluorescence of organic molecules in chiral recognition[J].Chemical Reviews,2004,104(3):1687~1716.
[6]LIANG X F,JAMES T D,ZHAO J Z.6,6′-Bis-substituted BINOL boronic acids as enantioselective and chemoselective fluorescent chemosensors for D-sorbitol[J].Tetrahedron 2008,64(7):1309~1315.
[7]Hu C G,He Y B,Chen Z H,et al.Synthesis and enantioselective recognition of an (S)-BINOL-based colorimetric chemosensor formandelate anions[J].Tetrahedron:Asymmetry 2009,20(1):104~110.
[8]LU Q S,LIANG D,ZHANG J,et al.Imidazolium-functionalized BINOL as a multifunctional receptor for chromogenic and chiral anion recognition[J].Organic Letters,2009,11(3):669~672.
[9]XU K X,QIU Z,ZHAO J J,et al.Enantioselective fluorescent sensors for amino acid derivatives based on BINOL bearing benzoyl unit[J].Tetrahedron:Asymmetry 2009,20(14):1690~1696.
[10]HE X,CUI X,LI M S,et al.Highly enantioselective fluorescent sensor for chiral recognition of amino acid derivatives[J].Tetrahedron Letters,2009,50(42):5853~5856.
[11]WANG Q,CHEN X,TAO L,et al.Enantioselective Fluorescent Recognition of Amino Alcohols by a Chiral Tetrahydroxyl 1,1'-Binaphthyl Compound [J].Journal of Organic Chememistry,2007,72(1):97~101.
[12]KIM K M,PARK H,KIM H-J,et al.Enantioselective Recognition of 1,2-Amino Alcohols by Reversible Formation of Imines with Resonance-Assisted Hydrogen Bonds[J].Organic Letters,2005,7(16):3525~3527.
[13]Nandhakumar R,Ryu J,Park H,et al.Effects of ring substituents on enantioselective recognition of amino alcohols and acids in uryl-based binol receptors[J].Tetrahedron 2008,64(33):7704~7708.
[14]NANDHAKUMAR R,SOO A Y,HONG J,et al.Enantioselective recognition of 1,2-aminoalcohols by the binol receptor dangled with pyrrole-2-carboxamide and its analogues[J].Tetrahedron 2009,65(3):666~671.
[15]NANDHAKUMAR R,AHN Y S,YOON H-J,et al.Stereoselective Recognition of Amino Alcohols and Amino Acids by Carbonylurea-and Carbonyguanidinium-based Imine Receptors[J].Bulletin of the Korean Chemical Society,2009,30(12),2938~2942.
[16]TANG L J,CHOI S,NANDHAKUMAR R,et al.Reactive Extraction of Enantiomers of 1,2-Amino Alcohols via Stereoselective Thermodynamic and Kinetic Processes[J].Journal of Organic Chememistry,2008,73(15):5996~5999.
[17]SAMBASIVAN S,KIM D-S,AHN K H,Chiral discrimination of α -amino acids with a C2-symmetric homoditopic receptor[J].Chemical Communications,2010,46:541~543.
[18]SHAW J P,PETSKO G A,RINGE D.Determination of the structure of alanine racemase from Bacillus stearothermophilus at 1.9?resolution[J].Biochemistry 1997,36(6):1329~1342.
[19]WALSH C T.Enzymes in the D-alanine branch of bacterial cell wall peptidoglycan assembly[J].Journal of Biological Chemistry,1989,264(5):2393~2396.
[20]PARK H,KIM K M,LEE A,et al.Bioinspired Chemical Inversion of L-Amino Acids to D-Amino Acids[J].Journal of the American Chemical Society,2007,129(6):1518~1519.
[21]TANG L J,GA H,KIM J,et al.Chirality conversion and enantioselective extraction of amino acids by imidazolium-based binol-aldehyde [J].Tetrahedron Letters,2008,49(48):6914~6916.
Recent Progress in the Application of Optically Active 1,1′-Bi-2-naphthol Synthetic Receptors
GUO Zhi-long,TANG Li-jun,WEI Gong-fan
(College of Chemistry and Chemical Engineering,Bohai University,Jinzhou 121013,China)
TQ 243.13
A
1001-0017(2011)02-0056-05
2010-10-09 *基金项目:辽宁省教育厅资助项目(编号:2008T002)
郭志龙(1983-),男,山西临县人,渤海大学硕士研究生,主要从事功能有机化合物的合成与应用研究。
**通讯联系人
