HPLC 法测定复方银连颗粒中绿原酸的含量
2011-08-07广西北海食品药品检验所北海市536000
夏 莲(广西北海食品药品检验所,北海市 536000)
复方银连颗粒是由金银花、连翘等多味中药组成的临床验方,具有清热、解毒、凉血的功效,临床用于治疗痤疮效果良好。原方以煎剂入药,笔者将其改成颗粒剂,既保持了煎剂吸收较快、作用迅速的优点,又克服了煎剂需临时煎煮、服用量大、携带储存不方便、久置易发霉变质等缺点。本试验采用高效液相色谱(HPLC)法,对复方银连颗粒君药金银花中有效成分绿原酸的含量进行了测定,以为该制剂的质量控制提供参考依据。
1 仪器与试药
Agilent1100型HPLC仪、8453紫外分光光度计(美国安捷伦公司);LG16-W高速微量离心机(北京医用离心机厂);SHZ-DⅢ予华牌循环水真空泵(2 800 r·min-1,巩义市英峪予华仪器厂);BS224S电子分析天平(北京赛多利斯仪器系统有限公司);SB5200DT超声波清洗机(宁波新芝生物科技股份有限公司,工作频率:40 kHz,功率:200 W)。
绿原酸对照品(中国药品生物制品检定所,批号:110715-200815);乙腈(色谱纯,天津市四有科技发展有限公司);磷酸(分析纯,中国医药集团上海化学试剂公司);复方银连颗粒(批号:100901、100903、100906)及其阴性对照颗粒(笔者自制)。
2 方法与结果
2.1 检测波长的选择
参照2010年版《中国药典》(一部)“金银花”项下绿原酸的测定条件[1],并通过绿原酸对照品的紫外扫描结果,选择327 nm为检测波长。
2.2 色谱条件与系统适用性试验
色谱柱:Welchrom C18(150 mm×4.6 mm,5 μm);流动相:乙腈-0.1%磷酸(10∶90);检测波长:327 nm;流速:1.0 mL·min-1;柱温:30℃。分别精密吸取对照品溶液、供试品溶液与阴性对照溶液各10 μL,注入液相色谱仪进行测定。结果表明,绿原酸峰与其他峰分离良好,阴性对照无干扰;理论板数按绿原酸峰计算应不低于3 000。色谱见图1。
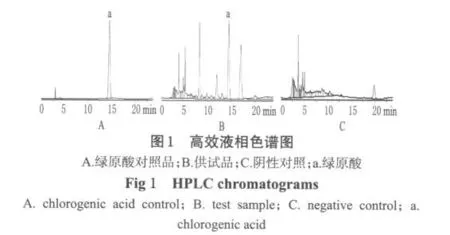
2.3 溶液的制备
2.3.1 对照品溶液 精密称取绿原酸对照品适量,置10 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,制成每1 mL含0.607 mg的对照品溶液。再精密量取0.5 mL,置2 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,制成每1 mL含151.75 μg的对照品溶液。再精密量取1 mL,置2 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,制成每1 mL含75.87 μg的对照品溶液,备用。
2.3.2 供试品溶液 取本品10 g,研细,取约1 g,精密称定,置25 mL量瓶中,加纯净水超声溶解,冷却至室温后定容,摇匀,即得。
2.3.3 阴性对照溶液 按处方量称取缺金银花的其他药材,制成缺绿原酸成分的阴性对照颗粒,并根据“2.3.2”项下方法制成阴性对照溶液。
2.4 线性关系考察
分别精密量取浓度为151.75 μg·mL-1的对照品溶液2、4、6、8、10 μL,注入液相色谱仪,记录色谱图。以峰面积积分值(Y)为纵坐标,进样量(X,μg)为横坐标,进行线性回归,得回归方程为Y=2 970.3X+61.42(r=0.999 6,n=5)。结果表明,绿原酸进样量在0.303 5~1.517 5 μg范围内与峰面积积分值呈良好线性关系。
2.5 精密度试验
精密量取浓度为75.87 μg·mL-1的对照品溶液10 μL,按上述色谱条件注入液相色谱仪,重复进样5次,记录峰面积。结果,平均峰面积为2 369.9,RSD=1.72%(n=5),表明仪器精密度良好。
2.6 重复性试验
取复方银连颗粒细粉(批号:100901)适量,共6份,分别按“2.3.2”项下方法制备供试品溶液,按上述色谱条件测定。结果,样品中绿原酸的平均含量为1.520 mg·g-1,RSD=2.37%(n=6),表明本方法重复性良好。
2.7 稳定性试验
取同一供试品溶液,分别于制备后0、2、4、8、12 h进样10 μL,按上述色谱条件测定。结果,绿原酸峰面积的RSD=1.15%(n=5),表明供试品溶液在12 h内稳定。
2.8 加样回收率试验
取已知含量的复方银连颗粒细粉(批号:100901)6份,每份约0.5 g,精密称定,分别精密加入浓度为0.607 mg·mL-1的绿原酸对照品溶液1.2 mL,按“2.3.2”项下方法制备供试品溶液,按上述色谱条件测定,计算加样回收率,结果见表1。
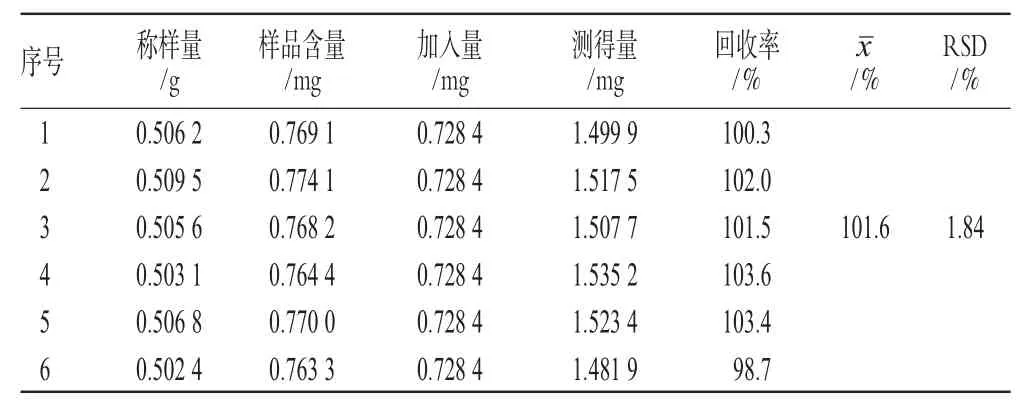
表1 加样回收率试验结果(n=6)Tab 1Results of recovery tests(n=6)
2.9 样品含量测定
分别取3批复方银连颗粒各10 g,研细,取约1 g,按“2.3.2”项下方法制备供试品溶液,并按上述色谱条件测定样品中绿原酸的含量,结果见表2。

表2 样品含量测定结果(n=3)Tab 2Results of content determination of samples(n=3)
3 讨论
3.1 流动相的选择
《中国药典》和某些文献采用不同比例的乙腈-0.4%磷酸溶液[1~5]作为流动相测定绿原酸的含量,但该流动相酸度较大,易损伤柱子,缩短柱子的寿命。因此,笔者通过参考文献[6,7],采用乙腈-0.1%磷酸溶液(10∶90)作为流动相。结果表明,绿原酸的峰分离效果与峰形的对称性等方面与乙腈-0.4%磷酸溶液作流动相时比较无显著差异,故选择该系统作为流动相。
3.2 供试品溶液制备方法的选择
笔者曾对比乙醇超声提取法[5~10]和纯净水超声提取法对供试品制备的影响,结果表明,采用乙醇超声法制备供试品时,绿原酸的提取量仅约为纯净水超声法提取量的69%;同时曾采用乙酸乙酯萃取法[11,12]对供试品进行纯化,结果表明此法虽能除去部分杂质,但绿原酸损耗较高。综合考虑,选择纯净水超声提取法作为供试品的制备方法。
综上,本方法操作简便、可靠,可用于复方银连颗粒的质量控制。
[1] 国家药典委员会编.中华人民共和国药典(一部)[S].2010年版.北京:中国医药科技出版社,2010:205-206.
[2] 张伟敏,蒲云峰,钟 耕.金银花中绿原酸的分析测定方法[J].中国食品添加剂分析测试,2005,9(25):155.
[3] 崔 岚,祝德秋,王晓珉,等.反相高效液相色谱法测定清炎颗粒中绿原酸的含量[J].中国药房,2004,15(6):368.
[4] 张全梅,刘 冰,阿孜古丽.RP-HPLC法测定肺炎合剂中绿原酸的含量[J].中国药房,2008,19(8):205.
[5] 白雪梅,吴健翎,罗 强,等.HPLC法测定四地产金银花中绿原酸的含量[J].河北北方学院学报,2004,21(5):30.
[6] 武 煊,黎晓敏,熊仲良,等.山东和河南及重庆产金银花中绿原酸含量的研究[J].西南农业大学学报(自然科学版),2006,28(3):436.
[7] 杨红娟.金银花质量控制方法的研究[D].沈阳:沈阳药科大学,2003.
[8] 何 刚,刘贤桂,李 樊,等.金银花叶片绿原酸提取及工艺参数优化的研究[J].江西农业大学学报,2008,30(1):136.
[9] 蒋受军,朱 斌.高效液相色谱法测定金银花中绿原酸的含量[J].广西医科大学学报,2002,19(5):695.
[10] 朱 青,李光慧,侯晓明,等.HPLC法测定金银花及利咽止咳冲剂中绿原酸的含量[J].中国实验方剂学杂志,1996,2(5):5.
[11] 朱凯峰.绿原酸提取分离方法研究进展[J].黑龙江医药,2008,6(21):59.
[12] 徐跃成.金银花中绿原酸的提取分离及其抑菌作用研究[D].重庆:重庆大学,2008.
