铕-铽共掺杂的SrF2荧光体的光致发光性能
2011-07-26霍涌前刘启瑞刘晓红张纷飞
霍涌前,刘启瑞,刘晓红,唐 龙,张纷飞,王 潇
(延安大学化学与化工学院,陕西 延安 716000)
SrF2是重要的碱土金属氟化物,具有良好的光学性能,其合成方法有超声合成法[1]、共沉淀法[2]、水热合成法[3]等。Ln3+的发光大多来源于其f-f跃迁,这种跃迁是宇称禁戒的,对光的吸收和发射都很差,使得这类发光材料发光强度一般都比较弱,为了增强Ln3+发光材料的发光强度,常在发光体系中共掺杂稀土离子(如:Ce3+与Eu2+、Ce3+与Tb3+、Er3+与Yb3+、Tm3+与Ho3+等),其发光机理为稀土离子之间的能量传递[4~7]。在Eu3+和Tb3+共掺杂的发光材料中,由于存在Tb3+→Eu3+的能量传递,Tb3+的共掺杂可显著提高掺杂的Eu3+的发光性能,这类共掺杂的发光体系有:硅酸铝钠[8]、钨酸钠[9]、钼酸钙[10]等。目前,国内对于Eu3+和Tb3+共掺杂的SrF2发光材料的研究还很少。
作者采用水热反应法合成了三色荧光体系SrF2:Eu3+,Tb3+发光材料,并且可通过改变激发波长调控材料的黄光强度。
1 实验
1.1 试剂
Sr(NO3)2、NH4F、Eu2O3、Tb4O7(99.99%,上海跃龙稀土新材料有限公司)、DMF、十六烷基三甲基溴化铵(CTABr),均为分析纯。
0.10 mol·L-1Eu(NO3)3和0.10 mol·L-1Tb(NO3)3溶液由Eu2O3和Tb4O7直接称重后,用浓HNO3溶解,除去多余的HNO3后配制而成。
1.2 合成方法
按照适量的配比,分别称取4.148 g Sr(NO3)2、0.7408 g NH4F、1.8222 g CTABr,置于聚四氟乙烯内衬的25 mL高压反应釜内,用移液管移取适量Eu(NO3)3溶液,继续加入8 mL DMF、8 mL蒸馏水,使得混合液总体积约20 mL,密封后放入真空干燥箱,150 ℃恒温反应120 h,然后自然冷却至室温,将所得沉淀物离心分离,依次用蒸馏水、无水乙醇各洗涤3次,在60 ℃下真空干燥,得到SrF2:0.02Eu3+。同法合成SrF2:0.02Tb3+、SrF2:0.02Eu3+,0.02Tb3+系列样品。
1.3 分析测试
样品的物相采用日本岛津公司XRD-7000型全自动X-射线粉末衍射仪测定,Cuκα(λ=0.15418 nm),管电压40 kV,管电流30 mA,步长0.02°,扫描范围2θ:20°~80°,扫描速度为2°·min-1。光致发射光谱和光致发光激发光谱由日本日立公司F-4500型荧光分光光度计测定(激发源为150 W氙灯,分辨率为0.1 nm)。所有测试都在室温下进行。
2 结果与讨论
2.1 SrF2:Eu3+,Tb3+的晶体结构
图1为SrF2:0.02Eu3+、SrF2:0.02Tb3+和SrF2:0.02Eu3+,0.02Tb3+样品的XRD谱图。

图1 铕掺杂(a)、铽掺杂(b)和铕-铽共掺杂(c)氟化锶样品的XRD图谱
通过与标准粉末衍射卡片对比,样品的衍射峰数据与JCPDS(PDF No.06-0262)卡片数据一致,属于立方晶系,即其晶体结构并未因Eu3+、Tb3+的加入而改变。其中的杂质峰可能为样品中残余的表面活性剂所产生。
2.2 SrF2:0.02Eu3+的发光性质(图2)

图2 SrF2:0.02Eu3+材料的激发(a)与发射(b)光谱
图2a是SrF2:0.02Eu3+在594 nm监测波长下的激发光谱,主要由位于260~350 nm范围内强而宽的激发带和位于363 nm、385 nm、397 nm处的弱峰组成,其中样品在260~350 nm处的宽吸收峰可能是由于F-→Eu3+的电荷迁移(CT)带与F-→Sr2+的电荷迁移重叠而形成的。Eu3+的各激发峰分别归属为:363 nm处为7F0→5D4跃迁;385 nm处为7F0→5L7,5G2跃迁;397 nm处为7F0→5L6跃迁。图2b是SrF2:0.02Eu3+在397 nm激发波长下的发射光谱,位于593 nm的黄光峰、614 nm左右的红光肩峰、699 nm的红光峰,分别来自于Eu3+的5D0→7F1、5D0→7F2、5D0→7F4的跃迁。文献报道,当Eu3+处于有严格反演中心的格位时,将以5D0→7F1磁偶极跃迁为主;当Eu3+处于无反演中心的格位时,常以5D0→7F2(约615 nm)的电偶极跃迁发射红光为主。根据593 nm的5D0→7F1与615 nm左右的5D0→7F2跃迁的强度比可知,在SrF2:0.02Eu3+中,Eu3+处于有严格反演中心的格位[11]。该样品发射橙色光。
2.3 SrF2:0.02Tb3+的发光性质(图3)
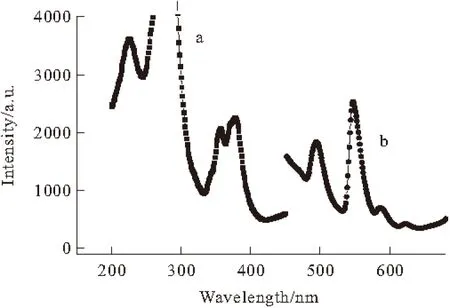
图3 SrF2:0.02Tb3+材料的激发(a)与发射(b)光谱
图3a是SrF2:0.02Tb3+在547 nm监测波长下的激发光谱,其中226 nm对应于Tb3+的 4f8→4f75d1跃迁,264~293 nm处宽峰对应于Tb3+的f→f跃迁,357 nm处为Tb3+的7F6→5L9跃迁,378 nm处为Tb3+的7F6→5G6跃迁。图3b是SrF2: 0.02Tb3+在350 nm激发波长下的发射光谱,其4个峰495 nm、547 nm、586 nm、623 nm分别对应Tb3+的5D4→7F6、5D4→7F5、5D4→7F4、5D4→7F3磁偶极跃迁,其中以547 nm的发射峰最强,样品发射绿光。
2.4 SrF2:0.02Eu3+,0.02Tb3+的发光性质
图4为SrF2:0.02Eu3+,0.02Tb3+在257 nm激发波长下的发射光谱。
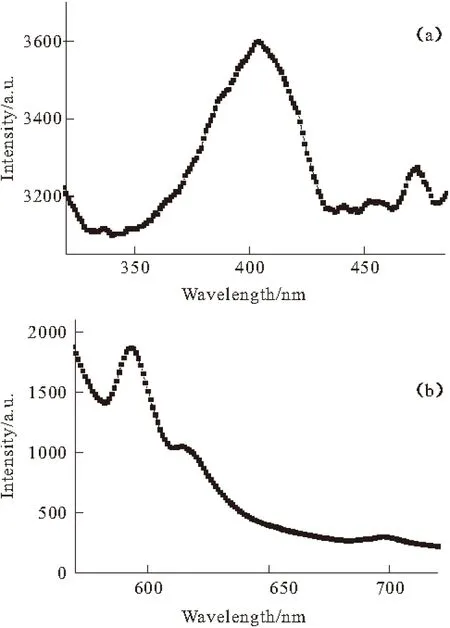
图4 SrF2:0.02Eu3+,0.02Tb3+材料的发射光谱
由图4可知,SrF2:0.02Eu3+,0.02Tb3+在紫、蓝、黄区域均有发射。图4a中第一组宽带发射峰中心位于404 nm,可能对应于Eu2+的d→f跃迁发射[12],Eu2+的产生是由于电子组态共轭的一对稀土离子Eu3+和Tb3+之间的电子转移造成的。
Eu3+(4f6)+Tb3+(4f8)⟺Eu2+(4f7)+Tb4+(4f7)
441 nm蓝光峰为Tb3+的5D3→7F4跃迁,由于5D3→5D4和7F6→7F0的交叉弛豫使蓝光发射相对较弱,456 nm可能为Tb3+的5D3→7F3跃迁,473 nm为Tb3+的5D4→7F6跃迁。图4b中593 nm、614 nm左右红光带肩峰、698 nm分别来自于Eu3+的5D0→7F1、5D0→7F2、5D0→7F4的跃迁。SrF2:0.02Eu3+,0.02Tb3+的发射光谱以404 nm、473 nm、593 nm发射峰较强,其紫、蓝、黄光强度比为100∶91∶52。Eu3+,Tb3+共掺发光材料很少出现此类发光现象。
激发光谱中来自Eu3+的f→f跃迁所产生的激发峰与Tb3+的来自5D3能级的发射峰存在光谱重叠,这为Tb3+→ Eu3+的能量传递提供了可能,而且国内文献报道的Tb3+,Eu3+共掺荧光材料多数是应用能量传递发光机理来合成红光材料。本研究中SrF2:0.02Eu3+,0.02Tb3+的593 nm处Eu3+的5D0→7F1跃迁峰强度增加不大,说明SrF2:0.02Eu3+,0.02Tb3+中基本没有发生Tb3+→ Eu3+的能量传递。
2.5 不同激发波长对SrF2:0.02Eu3+,0.02Tb3+发光性能的影响
SrF2:0.02Eu3+,0.02Tb3+在不同激发波长下的发射光谱见图5。
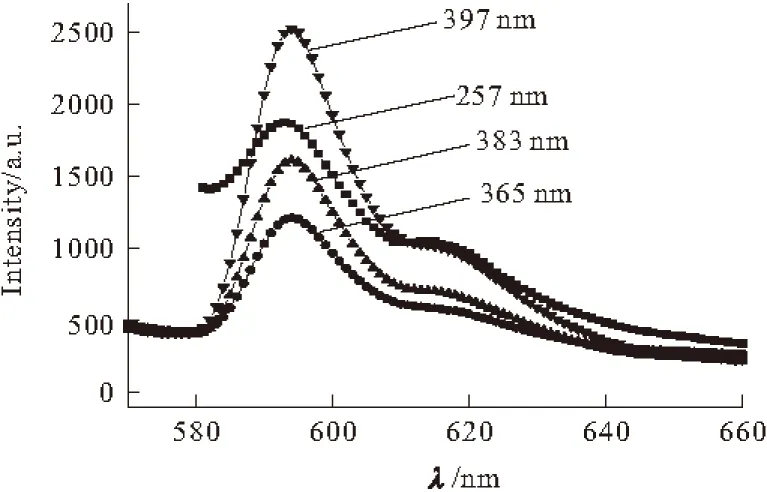
图5 不同激发波长下SrF2:0.02Eu3+,0.02Tb3+的发射光谱
由图5可知,593 nm处Eu3+的5D0→7F1跃迁的发射峰的位置变化不大,但是其发射峰强度变化较大,随着激发波长从257 nm、365 nm、383 nm到397 nm的增加,Eu3+的5D0→7F1跃迁(峰值分别位于593 nm、594 nm、594 nm、594 nm处)的发射峰强度先减小后增大,说明397 nm能够最有效地激发Eu3+到稳定激发态,可能不仅存在电子转移,也有Eu2+→Tb3+和Eu2+→Eu3+的能量传递过程存在。
3 结论
采用水热反应法可在较为温和的条件下合成三色荧光体系SrF2:0.02Eu3+,0.02Tb3+,在257 nm的紫外光激发下,可同时观察到Eu2+、Tb3+、Eu3+的紫、蓝、黄发光峰,峰值分别对应于Eu2+的d→f跃迁、Tb3+的5D4→7F6跃迁和Eu3+的5D0→7F1跃迁发光,在397 nm波长激发下Eu3+的5D0→7F1跃迁发光强度最大,可能不仅存在Tb3+、Eu3+之间的电子转移,也存在Eu2+→Tb3+和Eu2+→Eu3+的能量传递过程。
[1] 许可,徐朗,朱俊杰.超声化学法制备SrF2纳米片自组装微球[J].无机化学学报,2009,25(10):1864-1867.
[2] 吕燕飞,吴希俊,吴大雄,等.乙醇/水混合溶剂沉淀制备纳米SrF2及其粒径控制[J].材料科学与工程学报,2009,27(6):841-844,833.
[3] Zhang Cuimiao,Hou Zhiyao,Chai Ruitao,et al.Mesoporous SrF2and SrF2:Ln3+(Ln=Ce,Tb,Yb,Er) hierarchical microspheres:Hydrothermal synthesis,growing mechanism and luminescent properties[J].J Phys Chem C,2010,114(15):6928-6936.
[4] 万文娇,肖全兰,杨创涛,等.Ca3Sc2Si3O12:Ce3+,Nd3+近红外荧光粉的制备和发光性质[J].硅酸盐学报,2010,38(10):1862-1866.
[5] 于立新,宋宏伟,刘钟馨,等.LaPO4:Ce3+/Tb3+纳米线的合成和发光特性[J].发光学报,2005,26(3):369-374.
[6] Gulnar A K,Sudarsan V,Vatsa R K,et al.CePO4:Ln (Ln=Tb3+and Dy3+) Nanoleaves incorporated in silica sols[J].Crystal Growth & Design,2009,9(5):2451-2456.
[7] 杨创涛,刘关喜,陈清清,等.Li2SrSiO4:Eu2+,Nd3+中Eu2+和Nd3+的光谱性质和能量传递[J].中国稀土学报,2010,28(3):262-265.
[8] 常加忠,王振领,李敏,等.铽-铕共掺杂的硅酸铝钠荧光体的光致发光性能及能量传递[J].中国稀土学报,2009,27(6):750-755.
[9] 李霞,张胤,王喜贵.Na2WO4:Eu3+,Tb3+光致发光材料的发光性质和能量传递[J].稀土学报,2009,30(6):26-29.
[10] Zhang Zhi-jun,Chen Hao-hong,Yang Xin-xin,et al.Preparation and luminescent properties of Eu3+and Tb3+ions in the host of CaMoO4[J].Materials Science and Engineering B,2007,145(1-3):34-40.
[11] 冉营营,赵军伟,孔祥贵.NaYF4:Eu3+纳米粒子和六棱柱的水热控制合成与发光性质[J].发光学报,2010,31(4):556-560.
[12] 周建国,赵凤英,郭宝生,等.含Eu3+,Tb3+硼酸铝磷光体的制备及荧光特性[J].化学研究与应用,2000,12(4):409-412.
