龙须草稀酸预水解过程中糖类组分的溶出规律*
2011-01-24唐杰斌陈克复徐峻李军
唐杰斌 陈克复 徐峻 李军
(华南理工大学制浆造纸工程国家重点实验室∥广东省造纸技术与装备公共实验室,广东广州510640)
美国缅因大学的 Van Heiningen等[1]提出了“集成的林产品生物质精炼”的构想,即在制浆之前提取半纤维素,用以生产生物燃料或者取代石化产品生产可再生且环境友好的化学品.其中溶解浆的生产最符合这一构想,因为溶解浆的生产普遍采用的是预水解-硫酸盐法制浆工艺,预水解的主要目的就是除去原料中的半纤维素.
目前,溶解浆的生产原料主要为棉短绒和针叶木,而我国的棉短绒产量非常有限,木材资源又严重匮乏,因此开发草类原料生产溶解浆具有重要意义.龙须草纤维素含量高,纤维长,强度好,韧度高,被造纸行业称为“群草之冠”[2],是最具开发生产溶解浆潜力的草类原料之一.龙须草原料中,半纤维素的主要组成为木聚糖,木聚糖耐酸能力差,少量的酸就可以加速其水解溶出[3],而且稀酸水解可以除去原料中的难溶灰分,同时可制取可发酵性糖[4].因此,在制备龙须草溶解浆时,采用稀酸预水解.
生物质半纤维素的稀酸水解是一个复杂的过程,很难用精准的动力学模型进行描述[5].Saeman[4]在1945年提出了简单的半纤维素水解动力学模型,此后许多学者对半纤维素稀酸水解动力学进行了研究和修正[5-6].Esteghlalian 等[7]通过对 3种不同的纤维原料的稀酸预处理进行研究,得出了3种原料半纤维素水解的动力学参数.然而,在这些动力学研究中,必须进行一系列假设和复杂的推导,并且这些动力学研究的操作条件相对苛刻,一般是在加入酸后急速升温至最高温度或升温至最高温度后加酸,以时间为变量,近似认为计时前半纤维素未水解.而在工业中,稀酸预水解都会有很长的升温过程,仅时间这一函数不足以描述水解过程中糖类组分的溶出规律;同时这些研究也没有分析水解过程中己糖的变化规律.有关龙须草的稀酸预水解及其规律的研究还未见报道,因此,文中模拟工业上的稀酸预水解过程,考察了龙须草稀酸预水解过程中戊糖和己糖的溶出率随预水解因子(P因子)和稀酸初始质量浓度的变化规律,并在此基础上建立了描述预水解过程中戊糖和己糖溶出规律的经验模型,以期为生产龙须草溶解浆的预水解过程和水解液的资源化利用提供理论依据.
1 实验部分
1.1 原料
龙须草取自河南某纸厂,手工切成长30~50mm的小段,经筛选除杂风干后密封储存备用.
1.2 仪器与设备
主要仪器及设备包括:改装的M/K 609-2-10型蒸煮器(在放液口安装快速转换接头及冷凝管);Dionex ICS-3000型离子色谱仪(IC,CarboPACTM PA1阴离子交换柱,ED检测器);Agilent1100型高效液相色谱仪(HPLC,C18通用型色谱柱,UV检测器).
1.3 稀酸预水解
稀酸预水解在M/K 609-2-10型蒸煮器中进行,其中酸采用的是稀硫酸,在装锅时加入.龙须草装锅量为500g(绝干),液比(固体的质量和液体的体积比)为1∶10.升温阶段从30℃开始,升温速率为2℃/min,升温至指定温度后开始保温并计时,指定保温温度分别为150、160和170℃.预水解过程中间歇取样,每次取液10 mL,取出的样品冷却至室温后检测pH值,然后将样品放入冷冻室内储存备用.
1.4 水解液的检测
水解液及龙须草原料中主要糖组分(包括木糖、葡萄糖、阿拉伯糖、半乳糖)的含量均用离子色谱仪进行检测.龙须草原料糖类组分检测前按照美国可再生能源实验室(NREL)的方法[8]进行两步酸水解处理.水解液中的单糖经稀释过滤后直接检测其含量,而总糖含量测量前还需按照NREL方法的第二步进行处理.水解液中的糠醛(F)和羟甲基糠醛(HMF)含量由高效液相色谱仪测得.IC及HPLC的淋洗条件按文献[9-10]进行.
1.5 戊糖和己糖溶出率的计算
戊糖的量包括水解液中木糖、阿拉伯糖的量和糠醛按物质的量比转化为五碳糖的量.己糖的量包括水解液中葡萄糖、半乳糖的量和羟甲基糠醛按物质的量比转化为六碳糖的量.戊糖溶出率(U)和己糖溶出率(Y)的数学表达式见式(1)和(2):
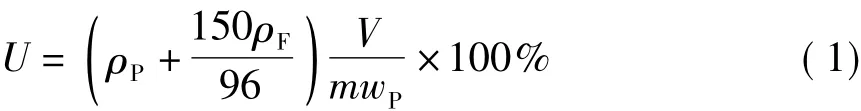

式中:ρP、ρF、ρH、ρHMF分别为水解液中戊糖、糠醛、己糖和羟甲基糠醛的质量浓度,g/L;V为龙须草稀酸预水解液总体积,L;m为每次预水解的龙须草的绝干质量,g;wP、wH分别为龙须草中戊糖、己糖的含量,%.
戊糖残留率(Z)的表达式如下:

2 结果与讨论
2.1 原料中糖组分的测定结果
原料中糖的含量(以龙须草的绝干量为基准计算所占质量分数)分析见表1.

表1 龙须草中糖组分的含量Table 1 Contents of sugars in Eulaliopsis binata %
由表1中可知,龙须草原料中主要的糖组分为葡萄糖、木糖、阿拉伯糖和半乳糖.酸性糖(葡萄糖醛酸和半乳糖醛酸)的含量非常小,总含量不足0.4%,因此文中将主要讨论还原糖(即戊糖和己糖)在预水解过程中溶出率的变化规律.
2.2 溶出率随温度和时间的变化
龙须草稀酸预水解过程中,温度、时间和稀酸初始质量浓度是影响糖类组分溶出的主要因素.固定稀酸初始质量浓度(ρv)为5g/L,研究戊糖和己糖溶出率随温度和时间的变化规律.
2.2.1 保温温度和时间对溶出率的影响
图1为戊糖和己糖溶出率随稀酸预水解保温温度和时间的变化关系.由图1中可知,戊糖和己糖的溶出率随保温温度的提高快速增加,说明高温有助于糖类组分的溶出.在不同温度下,戊糖和己糖的溶出率开始均随水解反应时间的延长而逐渐增大;其中戊糖的溶出率缓慢趋近于100%,后期略有下降.这可能是因为戊糖在溶出过程中,不仅产生了副产物糠醛,还会进一步降解生成一些低分子质量的物质,降解产物含量随着时间的延长逐渐增加,而在戊糖溶出率的计算公式中未将降解产物纳入,因此导致后期溶出率略有下降.
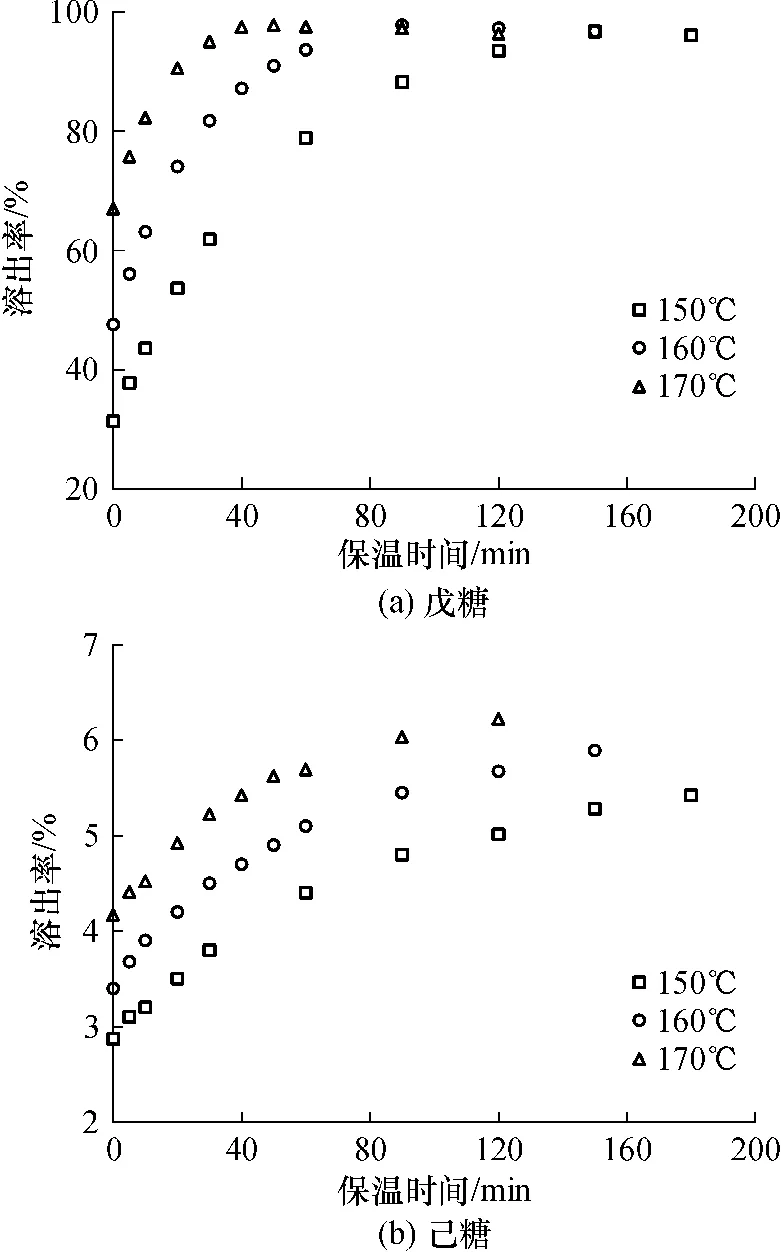
图1 保温温度和时间对戊糖和己糖溶出率的影响Fig.1 Effects of temperature and time on dissolution rates of pentaose and hexose
从图1中还可以看出,保温时间在0 min时,不同温度下的戊糖的溶出率差别很大,己糖亦同,这说明在升温过程中戊糖和己糖都已经开始溶出,由于在相同升温速率下达到不同保温温度的升温时间不同,导致了保温0min时溶出率不同.不同保温温度下戊糖和己糖的溶出率变化速率明显不同.因此,对不同温度下的龙须草进行稀酸预处理时,以时间为单一函数很难描述预处理过程中戊糖和己糖的溶出规律.
2.2.2 戊糖和己糖溶出率随预水解因子的变化规律
Vroom[11]提出的 H因子将制浆过程中的反应温度和时间综合成为一个变量,其数学表达式为

式中:t为反应时间;T(t)为反应温度随反应时间变化的函数;K0为指前因子;E为反应活化能;R为气体常数.
在预水解过程中,同样可以将温度和时间综合成为一个变量,即预水解因子(P因子).P因子由Brasch等[12]于1965年提出,与H因子类似,其数学表达式同式(4).预水解过程中,可以通过控制P因子来控制水解程度[13].目前,研究各种原料预水解的活化能的文献较少,有学者将制浆中的活化能和H因子用于描述预水解中糖的溶出规律,得到了满意的结果.Yoon等[14]发现用于描述云杉硫酸盐法蒸煮过程的活化能和H因子能很好地用于描述火炬松预水解过程中糖的溶出规律;胡会超等[15]将云杉KP法蒸煮过程的H因子进行修正后用于描述竹子高温预水解过程中碳水化合物的溶出,得到了很好的规律;早期,詹怀宇等[13,16]通过对蔗渣高温预水解的大量研究指出,蔗渣预水解过程中戊聚糖的溶出为一级反应,戊聚糖溶出的反应活化能为88.8kJ/mol.文献[13,16]中的预水解工艺与本实验中龙须草的相近,且龙须草与蔗渣同属禾本科植物,主要组分和结构相似.因此,文中尝试采用蔗渣预水解的活化能来对龙须草预水解过程中糖类组分的溶出规律进行探索.戊糖的溶出率随P因子的变化规律如图2所示.

图2 戊糖溶出率随P因子的变化Fig.2 Variation of dissolution rate of pentaose with P factor
由图2中可以看出,通过P因子可以将不同温度下的戊糖溶出率集合到一条趋势线上,戊糖的溶出率随P因子的增大逐渐增加,而且快速趋近于极限值100%;但是在P因子大于95以后,戊糖的溶出率开始出现下降,这与2.2.1节中戊糖溶出率下降的分析相吻合,说明用式(1)计算的溶出率在P因子大于95以后真实度较差,因此在后面的拟合过程中只对P因子小于95的数据进行拟合.
通过对图2中的数据进行直接拟合,发现很难用一个函数式很好地描述戊糖随P因子的变化规律.参考制浆过程中木素脱出动力学的研究方法[13],发现戊糖残留率可以和P因子建立很好的函数关系,如图3所示.由图3中可知,戊糖残留率与P因子之间存在良好的指数关系,其数学表达式为


图3 戊糖残留率随P因子的变化Fig.3 Variation of residual rate of pentaose with P factor
己糖的溶出率随P因子的变化规律如图4所示.由图4中可以看出,己糖的溶出率随着P因子的增大逐渐增加.对图4中数据进行拟合发现,己糖的溶出率与P因子之间存在较好的对数关系,但相关系数r2相对较小.参考戊糖溶出规律的拟合范围,当只对P因子小于95的数据拟合时,r2可以达到0.999,说明己糖的溶出率可以直接用P因子的对数关系表示,其数学表达式为


图4 己糖溶出率随P因子的变化Fig.4 Variation of dissolution rate of hexose with P factor
图4中己糖的溶出率在P因子大于95以后的数值慢慢偏向拟合曲线的下方,这是因为己糖在溶出过程中,不仅会生成副产物羟甲基糠醛,还会进一步降解生成一些低分子质量的物质,P因子越大,降解比例越大.而式(2)没有考虑己糖降解产物,导致P因子大于95后己糖溶出率的偏差越来越大.
2.3 戊糖和己糖溶出率随稀酸初始质量浓度的变化
由2.2中P因子对戊糖和己糖溶出率影响的分析知道,P因子越大,按照式(1)和(2)统计出来的溶出率偏差越大,因此在考察稀酸的初始质量浓度对戊糖和己糖溶出率的影响时,选取的P因子相对较小,分别为42.50(160℃水解30 min)和24.12(150℃水解30 min).在此P因子下稀酸预水解时的稀酸初始质量浓度对戊糖和己糖溶出率的影响如图5(a)和5(b)所示.
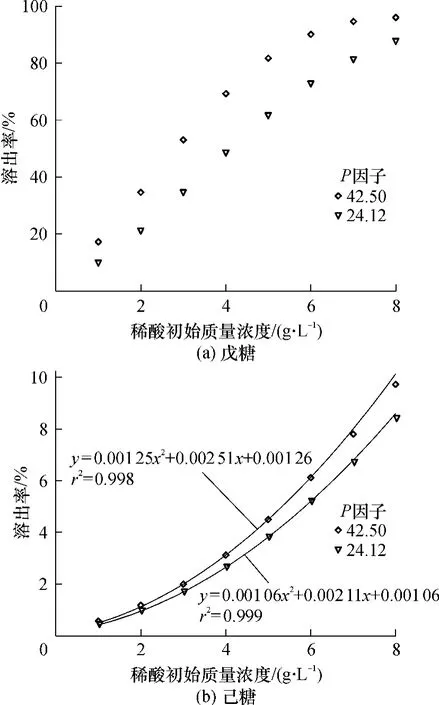
图5 戊糖和己糖溶出率随稀酸初始质量浓度的变化Fig.5 Variations of dissolution rates of pentaose and hexose with initial mass concentration of dilute acid
由图5(a)可知,随着稀酸初始质量浓度的增大,戊糖溶出率逐渐增加,不同的P因子下,溶出率的增加幅度不同.同图2一样,对图5(a)中数据直接拟合,效果不理想.参照图3,用戊糖残留率对(ρv+1)2作图并拟合,发现戊糖残留率与(ρv+1)2也存在着良好的指数关系,如图6所示.
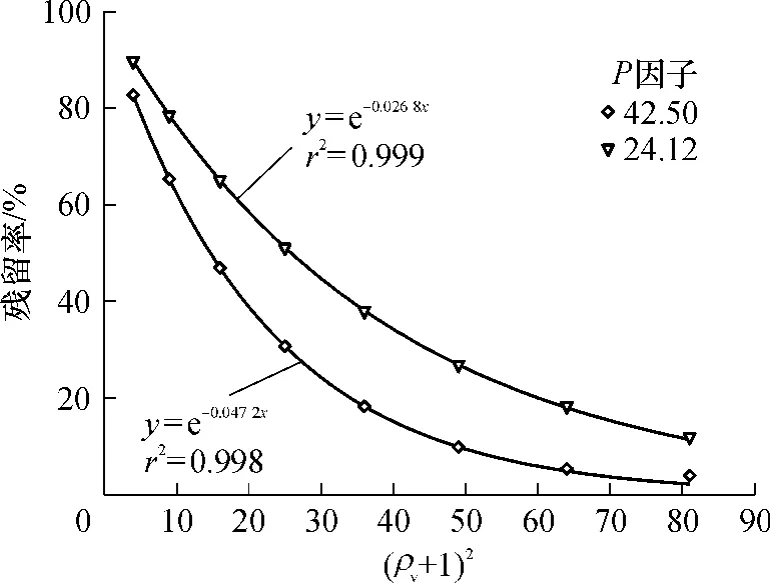
图6 戊糖残留率与(ρv+1)2的关系Fig.6 Relationship between residual rate of pentaose and(ρv+1)2
由图6可知,不同P因子下指数表达式不同.P为42.50时,戊糖残留率为
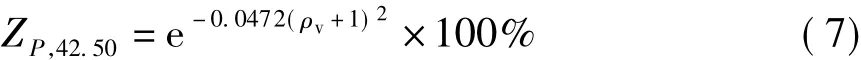
P为24.12时,戊糖残留率为
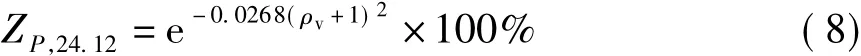
由图5(b)可知,己糖溶出率随着稀酸初始质量浓度的增大逐渐增加,不同的P因子下,溶出率的增加幅度不同.对图5(b)中数据进行拟合发现,己糖的溶出率与稀酸初始质量浓度之间可以用多项式进行表达:P为42.50时,己糖的溶出率 Y=1)2;P为24.12时,己糖的溶出率Y=0.00106+0.00211ρv+0.00106≈0.00106(ρv+1)2.则己糖在P为42.50和24.12下的溶出率分别如式(9)和(10)所示:
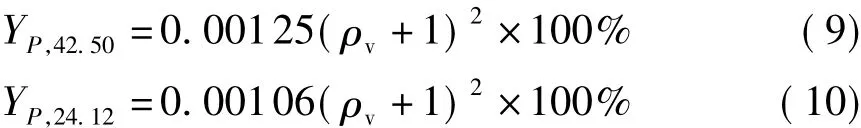
2.4 戊糖和己糖溶出规律经验模型的建立及评价
2.4.1 经验模型的建立
稀酸水解过程中,戊糖和己糖的溶出涉及到传质等比较复杂的物理化学过程,很难推导出严密的戊糖和己糖溶出的数学方程.由前文的分析可知,戊糖残留率与P因子和(ρv+1)2都成Ae-x形式的指数关系,据此笔者将P因子和(ρv+1)2都融合到指数中,则戊糖残留率可以表示为

戊糖溶出率可以表示为

式中:A为常数.
己糖的溶出率与lnP和(ρv+1)2都成正比,因此,己糖溶出率的经验方程可表示为

式中:B为常数.
将实验数据(不同P因子和稀酸初始质量浓度及其对应的戊糖和己糖溶出率)代入相应的式(12)和(13)中进行拟合计算,求得常数A和B以及相应的误差值(见表2).
2.4.2 模型的评价
模型的评价按照文献[17]中纸浆卡伯值预测经验模型准确度的评价方法进行.由该模型计算得到的戊糖溶出率和己糖溶出率与实验测得的溶出率的比较结果如图7所示.从图7(a)可以看出,戊糖溶出率的计算值与测定值之间符合程度的相关系数达到0.983,而溶出率小于95%(图中虚线框以内)的计算值与测定值之间符合程度的相关系数可以达到0.996.从图7(b)中可以看出,己糖溶出率的计算值与测定值之间符合程度的相关系数达到0.981,而溶出率小于6.5%(图中虚线框以内)的计算值与测定值之间符合程度的相关系数可以达到0.998.因此,该经验模型可以用来表达龙须草稀酸水解过程中戊糖和己糖的溶出规律.
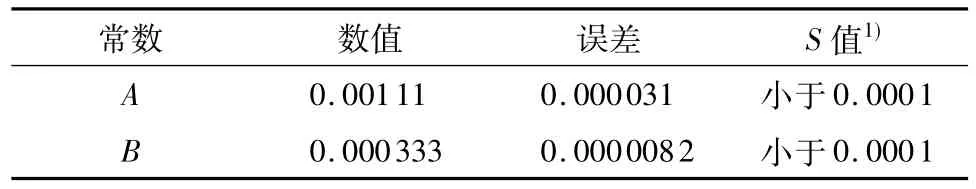
表2 式(12)和(13)中的常数及误差Table 2 Constants and errors in equations(12)and(13)

图7 戊糖和己糖溶出规律模型的评价Fig.7 Evaluation of the models of dissolution laws of pentaose and hexose
这里需要指出的是,图7中戊糖和己糖溶出率后部分(图中虚线框以外)的计算值与测定值之间符合程度的相关系数(λ2)较低,这并不表明在戊糖和己糖溶出率较高时该模型不适合,而是由实验中溶出率的统计式(1)和(2)本身的局限性造成的,具体原因已在2.2节中进行了解释.
3 结语
文中系统地研究了龙须草稀酸预水解过程中保温温度、时间和稀酸初始质量浓度对戊糖和己糖溶出率的影响,得出了戊糖和己糖溶出率与P因子和稀酸初始质量浓度之间的关系,进一步总结出了戊糖和己糖溶出规律的经验方程,即戊糖溶出率U=(1-e-0.00111P(ρv+1)2) ×100% 和己糖溶出率 Y=0.000333(ρv+1)2lnP×100%.它们的建立将为龙须草稀酸预水解过程中半纤维素和纤维素溶出率的控制提供理论依据.
[1] Van Heiningen Adriaan.Converting a kraft pulp mill into an integrated forest biorefinery[J].Pulp and Paper Canada,2006,107(6):38.
[2] 马成战.龙须草与造纸[J].中国林业,1996,47(2):41.Ma Cheng-zhan.Eulaliopsis binata and paper-making[J].Forestry of China,1996,47(2):41.
[3] 杨淑惠.植物纤维化学[M].北京:中国轻工业出版社,2001:230-237.
[4] Saeman J F.Kinetics of wood hydrolysis decomposition of sugars in dilute acid at high temperature[J].Industrial&Engineering Chemistry,1945,37(1)37:42-52.
[5] 余强,庄新姝,袁振宏,等.生物质稀酸水解动力学及其反应器的研究进展[J].化工进展,2009,28(9):1657-1661.Yu Qiang,Zhuang Xin-shu,Yuan Zhen-hong,et al.Kinetics and reactors of lignocellulose hydrolysis with dilute acids[J].Chemical Industry and Engineering Progress,2009,28(9):1657-1661.
[6] 金强,张红漫,严立石.生物质半纤维素稀酸水解反应[J].化学进展,2010,22(4):654-662.Jin Qiang,Zhang Hong-man,Yan Li-shi.Dilute acid hydrolysis reaction of biomass hemicellulose[J].Progress in Chemistry,2010,22(4):654-662.
[7] Esteghlalian Alireza,Hashimoto Andrew G,Fenske John J,et al.Modeling and optimization of the dilute-sulfuric-acid pretreatment of corn stover,poplar and switchgrass[J].Bioresource Technology,1997,59:129-136.
[8] 庄新姝,王树荣,袁振宏,等.纤维素超低酸水解产物的分析[J].农业工程学报,2007,23(2):177-182.Zhuang Xin-shu,Wang Shu-rong,Yuan Zhen-hong,et al.Analysis of cellulose hydrolysis products in extremely low acids[J].Transactions of the CSAE,2007,23(2):177-182.
[9] Liang Li-na,Zhang Ping,Cai Ya-qi,et al.High-performance anion exchange chromatography with pulsed amperometric detection for simultaneous determination of monosaccharides and uronic acids[J].Chinese Journal of Analytical Chemistry,2006,34(10):1371.
[10] 姜聚慧,石起增,陈华军.反相高效液相色谱法测定糠酸和糠醇[J].色谱,2005,23(1):110.Jiang Ju-hui,Shi Qi-zeng,Chen Hua-jun.Determination of furoic acid and furfuryl alcohol by reversed-phase high performance liquid chromatography[J].Chinese Journal of Chromatography,2005,23(1):110.
[11] Vroom K E.The H factor:a means of expressing cooking times and temperatures as a single variable[J].Pulp and Paper Canada,1957,58(3):228.
[12] Brasch D J,Free K W.Prehydrolysis-kraft pulping of pinus radiata grown in New Zealand [J].TAPPI Journal,1965,48(4):245.
[13] 谢来苏,詹怀宇.制浆原理与工程[M].北京:中国轻工业出版社,2005:75-76.
[14] Yoon Sung-Hoon,Macewan Kimberley,Van Heiningen Adriaan.Hot-water pre-extraction from loblolly pine(Pinus taeda)in an integrated forest products biorefinery[J].TAPPI Journal,2008,91(6):27.
[15] 胡会超,詹怀宇,柴欣生,等.基于修正H因子的竹子热水预提取碳水化合物的溶出模型[J].中国造纸,2009,28(11):28-32.Hu Hui-chao,Zhan Huai-yu,Chai Xin-sheng,et al.Degradation models of carbohydrates during bamboo hotwater pre-extraction based on modified H-factor[J].China Pulp & Paper,2009,28(11):28-32.
[16] 陈嘉翔.制浆化学[M].北京:中国轻工业出版社,1990:230-235.
[17] Hatton J V.The potential of process control in kraft pulping of hard-woods relative to softwoods[J].TAPPI Journal,1976,59(8):48.
