锆酸锂的制备、表征及吸附CO2的模拟*
2011-01-24袁文辉梁杰李莉
袁文辉 梁杰 李莉
(1.华南理工大学化学与化工学院,广东广州510640;2.华南理工大学环境科学与工程学院,广东广州510006)
由于温室效应的加剧,如何控制温室气体CO2的排放受到越来越多的关注.燃煤电厂的高温烟道气是CO2长期、稳定、集中的排放源[1].由于烟道气温度较高,常见的方法(如吸收法、低温蒸馏法、吸附法、电化学法和膜分离法等)难以对CO2进行直接、有效的分离[2-6],通常需要将排放气体冷却到300℃以下才能进行吸附分离,存在操作复杂、能耗高等缺点;迄今鲜见工业规模的直接吸收并分离CO2气体的报道[7-8].近年来,国内外研究者对CO2高温吸附剂进行了研究,发现氧化钙在高温下能较好地吸附CO2,但不具备良好的再生能力.进一步的研究发现,Li的硅酸盐(Li4SiO4)及锆酸盐(Li2ZrO3)是高温下最理想的CO2吸附剂.
Nakagawa等[9]以Li2ZrO3为吸附剂应用于CO2的高温吸附,结果发现Li2ZrO3不仅可在400~800℃下使用,而且在吸附/解吸过程中体积变化很小,当在其中加入碳酸锂/钾时,吸附能力有所提高.Ida等[10]发现Li的锆酸盐在400~700℃吸附CO2的能力可达4.5 mmol/g,CO2/N2选择性能优异,可达无穷大.在锆酸锂中掺钾可以显著提高其吸附性能,但会导致其稳定性大幅降低[11].王银杰等[12]用纳米氧化锆和纳米碳酸锂制备了 Li2ZrO3,Pfeiffer等[13]讨论了溶胶-凝胶法制Li2ZrO3的影响因素.Xiong等[14]利用固相反应法制备了Li2ZrO3,并研究了原料ZrO2的尺寸对产品的影响;此外,他还提出了Li2ZrO3吸附CO2的双壳吸附模型.
采用固相法时需要高温下长时间焙烧(850℃下12h)才能得到良好的晶型[14],且固相法在制备过程中易引入杂质,难以控制结晶大小,容易生成大颗粒.采用软化学法制备的晶体通常颗粒细小、规则、均匀,目前用软化学法制备纯Li2ZrO3晶体粉末的报道较少.文中用柠檬酸-乙二醇络合法制备Li2ZrO3超细晶体粉未.对Li2ZrO3样品进行了分析和表征,并对其吸附CO2的性能进行了模型模拟,同时对吸附模型的解法进行了研究.
1 实验部分
1.1 实验方法
采用柠檬酸-乙二醇络合法制备Li2ZrO3粉末.将一定量的LiNO3溶于柠檬酸(CA)+乙二醇+H2O溶液中,在强烈搅拌条件下,按化学计量比加入ZrO(NO3)2,形成无色透明溶液,加热搅拌,待溶剂蒸发后,形成透明凝胶,经干燥得到Li2ZrO3前驱体,将前驱体在一定温度下焙烧一定时间得到的白色粉末即为样品.
1.2 样品表征方法
用D/max-IIIA型X射线衍射仪(XRD,日本理学公司生产)分析样品物相,射线源为Cu Kα.采用STA449型综合热分析仪(TG-DSC,德国NETZSCH公司生产)在80~900℃范围内分析Li2ZrO3超细晶体粉末在升温过程中的质量变化和物相变化,以流量为15cm3/min的N2作为保护气,吹扫气为空气,流量为40cm3/min.进行吸附能力测试时,将吹扫气改为流量为45cm3/min的CO2气体.用LEO 1530 VP型扫描电子显微镜(SEM,德国LEO公司生产)观察粉末的外观形貌.
2 吸附模型的建立
Xiong等[14]提出,当 Li2ZrO3吸附 CO2时,其颗粒形成球形双壳结构.对于纯Li2ZrO3,CO2分子在壳内的传导是整个反应的控制步骤,且其传导规律符合球壳吸附传质方程:

式中:cA为球壳内传质浓度;r为半径;t为吸附时间;DA为扩散系数.
文献中需要测定CO2的分压和操作温度才能求解模型.文中参考 Gabriele等[15]的模型解法,无需测定压力和温度,最终解得吸附质量M与时间和温度的函数关系式:M=F(τ,α),τ=f(t,T),α =g(t,T),然后用自编的VB程序以最小二乘法为原则代入实验数据进行拟合.其中T为热力学温度,τ和α为引入的关于时间和温度的变量.详细求解过程如下.
为简化方程(1),将传质过程看成稳态传质:

设边界条件:r=L(t)时,cA=cA0;r=R(t)时,cA=cA1.L为 Li2ZrO3颗粒半径,R为 ZrO2外壳半径,均为时间t的函数;cA1和cA0分别为ZrO2外壳和内壳处CO2的浓度.
传质过程质量守恒:

式中:V为体积;k为ZrO2的摩尔密度.
由式(2)解得

式中:R0为起始时间时ZrO2外壳半径;y=L/R0.
将式(4)代入式(3)得

解得
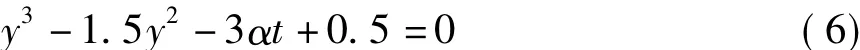
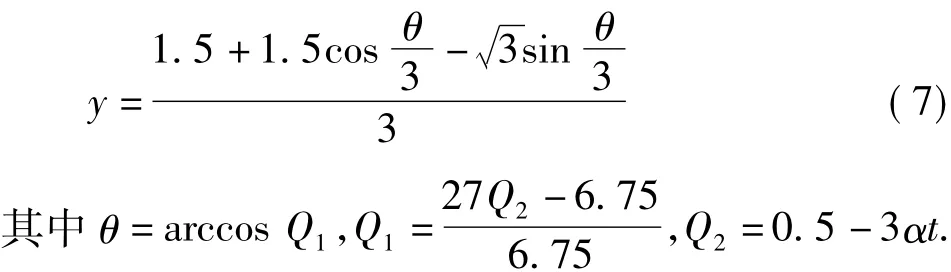
样品相对质量变化

式中:ρ0为Li2ZrO3的密度;Δm为样品质量变化量;m0为样品原始质量;为计算出来的样品相对质量变化;44为CO2的相对分子质量.
由于α和R(t)都不是关于时间的常数,因此引入α系数修正方程[15]:


然后用最小二乘法求τ、α的值,具体如下:设定τ、α初始值满足τmin≤τ≤τmax,αmin≤α≤αmax,目标函数为

式中:zi为实验测得的样品相对质量变化.当φ为最小值时,τ、α即为所求.
3 结果与讨论
3.1 对Li2ZrO3前驱体热分解过程的分析
Li2ZrO3前驱体的TG-DSC曲线如图1所示.在180~220℃范围内样品持续失重,同时出现较小的吸热峰,对应于样品中水分和残留溶剂的挥发.在220~400℃时,样品质量继续下降,且没有明显的吸热或放热,表明前驱体开始分解、氧化的吸热过程与无定形物质形成的放热过程同时进行,热量彼此中和.在400~600℃之间,TG曲线急剧下降的同时,DSC曲线上出现显著的放热峰,表明残余碳的除去以及Li2ZrO3晶体结构的形成.超过600℃后,TG和DSC曲线几乎无变化,表明Li2ZrO3晶体结构基本形成.由此说明,在制备过程中,焙烧温度应该大于600℃才能保证获得完整结晶的Li2ZrO3粉末.

图1 前驱体在空气气氛下的TG-DSC曲线Fig.1 TG-DSC curves of the precursor under air circumstance
3.2 焙烧条件对晶体物相的影响
前躯体分别在不同温度和时间下焙烧后的XRD谱图如图2所示.从图2中可以看出,900℃下焙烧的样品为单斜晶体,800℃以下焙烧才能得到四方晶体,如图2(a)所示.前驱体在800℃下焙烧90min后粉末才出现Li2ZrO3晶体的特征峰,但呈现不完全;随着焙烧时间延长到120和150 min,前驱体进一步氧化分解,Li2ZrO3晶体的特征峰呈现更完全,峰形变得尖锐,杂质减少,如图2(b)所示,其衍射图谱与标准Li2ZrO3晶体的衍射图谱(JCPDS 20-0647)相吻合.
3.3 焙烧条件对晶体外观形貌的影响

图2 样品在不同温度和时间下焙烧后的XRD谱图Fig.2 XRD patterns of the powders calcined at different temperatures for different time
焙烧时间和温度对颗粒中的Li2ZrO3结晶有直接影响.在600℃下焙烧时,即使焙烧时间较长,前驱体焙烧也不完全,仍有大量有机碳,颗粒细小,基本都是由未发育全的初晶构成,显微结构松散,如图3(a)所示.在700℃下焙烧时,前驱体进一步分解,颗粒长大,氧化渐趋完全,随焙烧时间延长,球形颗粒中开始出现方形晶粒,如图3(b)所示.当焙烧温度继续上升到800℃时,球团颗粒减少,说明前驱体焙烧较完全,基本生长成四方晶相的Li2ZrO3,焙烧时间较短时,即使焙烧温度达到800℃,形成的晶粒仍然不够规整,随着焙烧时间延长到150 min,Li2ZrO3氧化渐趋完全,形成的方形晶粒结构均匀、规整、致密,如图3(c)和3(d)所示.
3.4 Li2ZrO3粉体的吸附能力

图3 不同焙烧条件下样品的SEM照片Fig.3 SEM images of the powders calcined in different conditions
将800℃下焙烧150 min的样品分别在不同温度下进行恒温CO2吸附实验,结果见图4.从图4中可以看出,在600℃下恒温30 min时样品质量有较大增幅,相对质量变化21.5%,90min内样品相对质量变化23.7%.观察文献[14]和[15]中的吸附等温线与本实验所得的吸附等温线,发现600℃下实验所得Li2ZrO3的吸附速率具有明显优势,这可能是因为致密规则的方形晶粒具有较大的表面能和热力学不稳定性,有利于气体的快速吸附[16].文中还考察了其它温度下的吸附性能,发现500℃下恒温90min时样品相对质量变化只有6%,前5min曲线斜率依然很大,前期吸附速率较快.实验中还发现,700℃下恒温90min时样品质量无明显增加,这是因为温度太高,因而有利于气体的解吸.由此说明,文中制备的 Li2ZrO3的最佳吸附温度接近600℃,达到最大吸附量时样品相对质量变化为23.7%,相比文献[14]和[15],其吸附速率较快.

图4 不同条件下Li2ZrO3吸附CO2等温线的比较Fig.4 Comparison of adsorption isotherm of CO2on Li2ZrO3in different conditions
3.5 Li2ZrO3吸附模型拟合结果
分别对文中和其它文献中Li2ZrO3的吸附数据进行拟合,用计算机穷举的方式获得最适宜的模型参数.最终解得500和600℃下吸附模型的参数¯α分别为5 ×10-6和 1.8 ×10-5,τ分别为 9.8 和 13.2时,所测相对质量变化zi与模拟计算相对质量变化的最小平方差最小,即实验数据和模型模拟的数据吻合得最好.同理,在解得相应的模型参数后,利用此模型对其它文献的吸附数据的拟合也很好,如图5所示.说明文中建立的模型算法具有拟合精度高、灵活多变、适用范围广的优点,同时也再次证明了双壳模型的科学合理性.
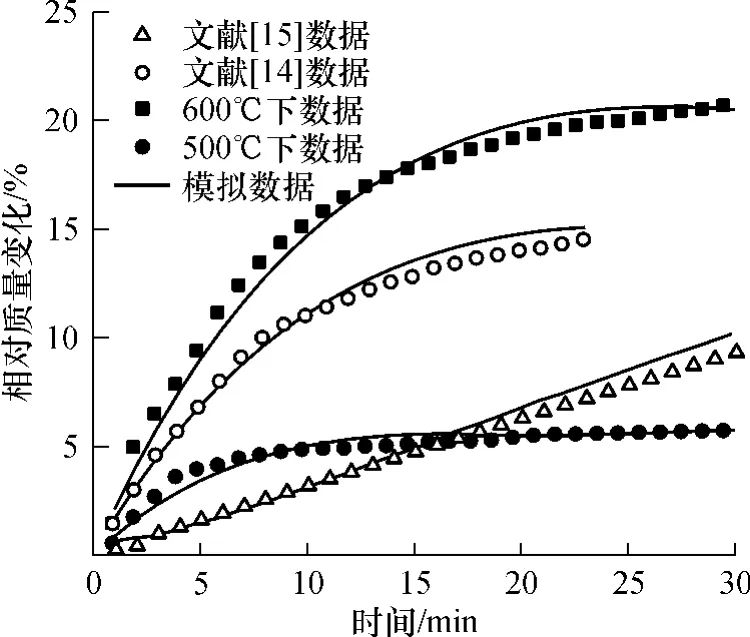
图5 对不同CO2吸附曲线的拟合结果Fig.5 Simulated results of CO2adsorption curves
4 结论
与其它文献报道的Li2ZrO3晶体相比,文中制备的纯Li2ZrO3晶体的粉末粒度小,结构均匀,呈规则四方结构,焙烧温度更低,因而具有更好的吸附速率,其最佳吸附温度为600℃,最大吸附量达样品质量的23.7%,且在此温度下前期吸附速率较快.文中提出的新的模型解法具有适用范围广和灵活的特点,对不同的吸附等温线进行拟合发现,实验数据和模型模拟数据吻合,表明模型及其解法具有合理性.
[1] 袁文辉,王婵月,阎慧静,等.CO2吸附剂掺钾锆酸锂的制备及性能表征[J].华南理工大学学报:自然科学版,2008,36(7):26-37.Yuan Wen-hui,Wang Chan-yue,Yan Hui-jing,et al.Synthesis and property characterization of K-doped Li2ZrO3for CO2adsorption [J].Journal of South China University of Technology:Natural Science Edition,2008,36(7):26-37.
[2] 张小军.全球变暖升温“气候外交”[J].瞭望,2007,17(3):56-57.Zhang Xiao-jun.Global warming“climate diplomacy”[J].Outlook,2007,17(3):56-57.
[3] Xiong Rentian.Novel inorganic sorbent for high temperature carbon dioxide separation[D].Cincinnati:Department of Chemical Engineering of the University of Cincinnati,2003.
[4] 李莉,袁文辉,韦朝海.二氧化碳的高温吸附剂及其吸附过程[J].化工进展,2006,25(8):918-922.Li Li,Yuan Wen-hui,Wei Chao-hai.Adsorbents and adsorptive process for carbon dioxide at high temperature[J].Chemical Industry and Engineering Progress,2006,25(8):918-922.
[5] Yamaguchi T,Niitsuma T,Nair B N,et al.Lithium silicate based membranes for high temperature CO2separation[J].Journal of Membrane Science,2007,294(1/2):16-21.
[6] 李玉龙,张宝真,姚树人.大气中二氧化碳分离技术的研究与现状[J].海军工程学院学报,1995,19(1):87-91.Li Yu-long,Zhang Bao-zhen,Yao Shu-ren.Research on the carbon dioxide removal from atmospheres[J].Journal of the Navakacadeny of Engineering,1995,19(1):87-91.
[7] 夏明珠,严莲荷,雷武,等.二氧化碳的分离回收技术与综合利用 [J].现代化工,1999,19(5):46-48.Xia Ming-zhu,Yan Lian-he,Lei Wu,et al.Separation and recycle techonology and comprehensive utilization for CO2[J].Modern Chemical industry,1999,19(5):46-48.
[8] 胡秀莲,刘强,姜克隽.中国减缓部门碳排放的技术潜力分析[J].中外能源,2007,12(4):1-8.Hu Xiu-lian,Liu Qiang,Jiang Ke-jun.Sectoral technology potential to mitigate carbon emissions in China[J].Sino-Global Energy,2007,12(4):1-8.
[9] Nakagawa K,Ohashi T.A novel method for CO2capture from high temperature gases[J].Journal of the Electrochemical Society,1998,145(4):1344-1346.
[10] Ida J,Lin Y S.Mechanism of high-temperature CO2sorption on lithium zirconate[J].Environmental Science and Technology,2003,37(9):1999-2004.
[11] Ochoa-Fernandez Esther,Ronning Magnus,Yu Xiaofeng,et al.Compositional effects of nanocrystalline lithium zirconate on its CO2capture properties[J].Industrial and Engineering Chemistry Research,2008,47(2):434-442.
[12] 王银杰,其鲁,杜柯,等.K元素的掺杂对锆酸锂材料吸收CO2性能的影响 [J].北京大学学报,2005,41(4):501-505.Wang Yin-jie,Qi Lu,Du Ke,et al.Effect of doping K element on properties of lithium zirconate as CO2-absorbent[J].Acta Scicentiarum Naturalum Universitis Pekinesis,2005,41(4):501-505.
[13] Pfeiffer H,Bosch P,Bulbulian S.Zr alkoxide chain effect on the sol-gel synthesis of lithium metazirconate materials[J].Chemistry and Physics,2002,78(2):558-561.
[14] Xiong Rentian,Ida Junichi,Lin Y S.Kinetics of carbon dioxide sorption on potassium-doped lithium zirconate[J].Chemical Engineering Science,2003,58(19):4377-4385.
[15] Gabriele P,Monica P,Maurizia S,et al.Experimental and modeling studies on high-temperature capture of CO2using lithium zirconate based sorbents[J].Industrial and Engineering Chemistry Research,2007,46(21):6696-6706.
[16] Iwan Alina,Stephenson Hazel,Ketchie William C,et al.High temperature sequestration of CO2using lithium zirconates[J].Chemical Engineering Journal,2009,146(2):249-258.
