HPLC-MS法测定甲磺酸多拉司琼原料药中有关物质和异构体含量
2011-01-09丁素玲江苏奥赛康药业有限公司南京市211112
丁素玲,戴 艳(江苏奥赛康药业有限公司,南京市 211112)
甲磺酸多拉司琼(Dolasetron mesylate)为选择性的5-羟色胺3(5-HT3)受体拮抗药,通过竞争性地阻断消化道黏膜释放的5-HT与5-HT3受体结合,从而具有治疗呕吐的作用[1]。其最早由德国Hoechst Marion Roussel公司研发,1997年在澳大利亚首次上市,商品名Anzement,之后相继在美国、法国、意大利、芬兰(商品名AnZemet)、南非(商品名Zamanon)、德国(商品名Aneme)等地上市,但目前在国内未上市。国内已有厂家对甲磺酸多拉司琼进行研制,但尚未见其中有关物质及异构体(由于本品结构中含有多个手性碳,在合成过程中可能会发生转型,产生异构体)检测方法的文献报道。为了有效控制产品质量,保障临床用药安全,笔者在通过制备方法获得异构体的情况下,建立了以高效液相色谱(HPLC)法和质谱(MS)法同时测定甲磺酸多拉司琼原料药中有关物质及异构体含量的方法。结果表明,本方法准确、专属性好,适用于甲磺酸多拉司琼原料药中有关物质和异构体的检查。
1 仪器与试药
1200系列HPLC仪、6410 Triple Quad液质联用(LC-MS/MS)仪(美国安捷伦科技有限公司)。
甲磺酸多拉司琼对照品(美国Sigma公司,批号:FOC319,纯度:100%);甲磺酸多拉司琼原料药(自制,批号:090501、090601、090602,纯度:均>99.5%);吲哚(南京沐客化学信息有限公司,批号:090301,纯度:98.5%,供系统适用性试验用);甲磺酸多拉司琼异构体(自制,批号:090501,纯度:99.3%);乙腈为色谱纯,其余试剂均为分析纯,水为蒸馏水。
2 方法与结果
2.1 色谱条件
液相条件:采用shim-pack VP-ODS(250 mm×4.6 mm,5µm)为色谱柱;以0.01 mol·L-1甲酸铵溶液(用三乙胺调节pH至7.0)-乙腈(95∶5)为流动相A,以0.01 mol·L-1甲酸铵溶液(用三乙胺调节pH至7.0)-乙腈(27∶73)为流动相B,线性梯度洗脱(0~28 min,A→B由100%∶0→0∶100%,保持10 min;38~40 min,A→B由0∶100%→100%∶0,保持10 min),流速为1.0 mL·min-1;检测波长为210 nm;柱温为35 ℃。
质谱条件:电喷雾电离源(ESI),采用正离子检测模式;毛细管电压为4.0 kV;雾化气温度为350℃;雾化气流速为13.0 L·min-1;雾化气压力为 60.0 psi;扫描范围为 m/z 100~m/z 1 000;选择离子监测(SIM)模式;选择性检测m/z 325离子。
2.2 系统适用性试验
取甲磺酸多拉司琼对照品和吲哚各适量,用流动相B溶解并稀释制成甲磺酸多拉司琼和吲哚浓度分别为10、4µg·mL-1的混合溶液。取该溶液20µL注入液相色谱仪,记录色谱。理论板数以多拉司琼计不低于3 000,与吲哚的分离度(R)大于1.5。色谱见图1。

图1 系统适用性试验高效液相色谱图1.甲磺酸多拉司琼;2.吲哚Fig 1 Chromatograms of test solution for system suitability 1.dolasetron mesylate;2.indole
2.3 方法的专属性考察
2.3.1 破坏性试验。取样品适量,分别经0.1 mol·L-1盐酸溶液、0.1 mol·L-1氢氧化钠溶液、10%过氧化氢溶液、高温(100 ℃水浴,2 h)、强光((4 500±500)lx,4 h)照射破坏。取上述5种破坏性试验溶液各20µL,注入液相色谱仪,记录色谱。结果表明,样品在各强制降解条件下产生的主要降解产物与多拉司琼峰分离较好,表明该方法专属性好,详见图2。
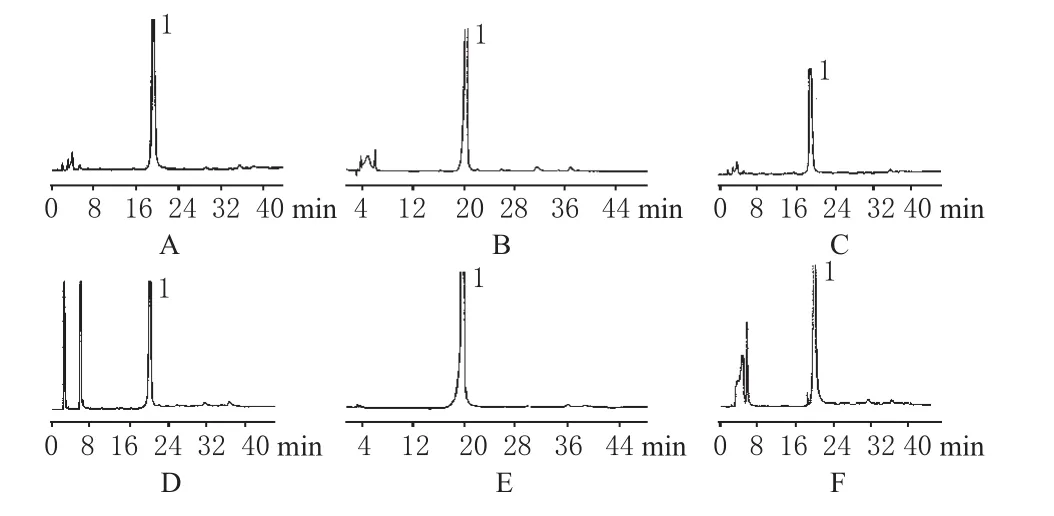
图2 破坏性试验高效液相色谱图A.未破坏样品;B.碱破坏样品;C.酸破坏样品;D.氧化破坏样品;E.光破坏样品;F.高温破坏样品;1.甲磺酸多拉司琼Fig 2 Chromatograms of destroyed testA.samples;B.samples destroyed by alkali;C.samples destroyed by acid;D.samples destroyed by oxidation;E.samples destroyed by light;F.samples destroyed by heat;1.dolasetron mesylate
2.3.2 峰纯度测定。取各破坏性试验溶液20µL,注入液相色谱仪,用二极管阵列检测器(DAD)检测,结果各主峰的紫外吸收光谱完全重合,主峰的纯度因子均大于999.5,提示为单一的色谱峰,峰纯度符合要求。各降解产物及主峰的紫外吸收特征一致。
2.3.3 异构体分离度试验及样品中异构体分析。取甲磺酸多拉司琼对照品和异构体各适量,用流动相B溶解并稀释制成甲磺酸多拉司琼和异构体浓度分别为100、40µg·mL-1的混合溶液;取本品约25 mg,精密称定,置于25 mL容量瓶中,加流动相B溶解并稀释至刻度,摇匀,作为供试品溶液。按“2.1”项下的质谱条件进行试验,结果混合溶液的LC-MS/MS的总离子流扫描Scan(TIC)图和SIM(EIC)图显示在 6.5、7.8 min处各有1峰,主要分子离子峰m/z 325为[M+H]+,与供试品的质荷比m/z相同,判定互为异构体;供试品溶液中未检出异构体。甲磺酸多拉司琼及其异构体离子流色谱详见图3。
2.4 最低检测限
取甲磺酸多拉司琼对照品适量,用流动相B溶解并逐级稀释,照“2.1”项下的色谱条件测定,信噪比为3时,测得甲磺酸多拉司琼的最低检测限为0.5 ng。
2.5 进样精密度试验
取“2.2”项下的溶液,连续进样6次,计算甲磺酸多拉司琼峰面积的RSD,结果为0.45%。

图3 甲磺酸多拉司琼及其异构体离子流色谱图A.甲磺酸多拉司琼对照品+异构体;B.供试品;1.甲磺酸多拉司琼异构体;2.甲磺酸多拉司琼Fig 3 SIM chromatograms of dolasetron mesylate and isomerideA.dolasetron mesylate control+isomeride;B.test sample;1.isomeride of dolasetron mesylate;2.dolasetron mesylate
2.6 样品中有关物质及异构体含量测定
取本品约25 mg,精密称定,置于25 mL容量瓶中,加流动相B溶解并稀释至刻度,摇匀,作为供试品溶液。精密量取供试品溶液1 mL,置于100 mL容量瓶中,加流动相B稀释至刻度,摇匀,作为对照溶液。
取对照溶液20 μL,注入液相色谱仪,记录色谱,调节检测灵敏度,使甲磺酸多拉司琼的峰高约为满量程的10%~25%,保持检测灵敏度不变,再分别量取上述对照溶液及供试品溶液各20 μL,分别注入液相色谱仪,记录色谱。供试品溶液色谱中如显杂质峰,按自身对照法计算,单个杂质含量不得过0.1%,总杂质含量不得过0.3%。结果3批样品中单个杂质含量≤0.05%,总杂质含量<0.1%,异构体未检出,详见表1。

表1 3批样品中有关物质及异构体含量检测结果Tab 1 Results of content determination of related substances and isomeride in 3 batches of samples
3 讨论
3.1 流动相的选择
本文色谱条件是参照文献(《美国药典》30版)[2],结合LCMS/MS方法的流动相特点制定的。经过试验发现,在文献[2]的梯度条件下,基线漂移严重,重现性差。经修改洗脱程序、提高初始流动相A比例、延缓流动相B的升降速率后,筛选出“2.1”项下的梯度洗脱程序,结果较好。
3.2 检测波长的选择
甲磺酸多拉司琼和各主要降解产物在210 nm波长处均有较大吸收,故选择其为有关物质的检测波长。
综上所述,本方法操作简便,结果准确、可靠,适用于甲磺酸多拉司琼原料药的质量控制。
[1] Balfour JA,Goa KL.Dolasetron.A review of its pharmacology and therapeutic potential in the management of nausea and vomiting induced by chemotherapy,radiotherapy or surgery[J].Drugs,1997,54(2):273.
[2] The United States Pharmacopeial Convention.USP30-NF25[S].Rockville:The United States Pharmacopeial Convention,2007:1 986-1 987.
