GC法测定盐酸金刚烷胺片中有关物质含量
2011-01-09宁夏回族自治区药品检验所银川市750004
陈 佩,翟 宇(宁夏回族自治区药品检验所,银川市 750004)
盐酸金刚烷胺片用于治疗帕金森病、药物诱发的锥体外系疾患,也用于防治A型流感病毒所引起的呼吸道感染。《中国药典》2005、2010年版[1,2]中未收载盐酸金刚烷胺片有关物质的测定方法,《美国药典》(USP)[3]和《英国药典》(BP)[4]也只对盐酸金刚烷胺原料药有关物质作了规定。而片剂在制粒、包衣以及贮存过程中均有可能会导致有关物质产生或增加,影响药品的疗效[5]。故本文参考《中国药典》2010年版中盐酸金刚烷胺原料药有关物质的测定方法,建立了气相色谱(GC)法测定盐酸金刚烷胺片中的有关物质含量。该方法灵敏、准确、专属性强,可用于盐酸金刚烷胺片的质量控制。
1 仪器与试药
6890N气相色谱仪及工作站(美国Agilent公司)。
盐酸金刚烷胺标准品(中国药品生物制品检定所,批号:100426-200301,含量:100.0%);金刚烷(美国Chromadex公司,批号:01380-L01,含量:99.9%);41批盐酸金刚烷胺片(国内8家药厂提供,批号略,规格:每片0.1 g);三氯甲烷为分析纯,盐酸、氢氧化钠、双氧水、无水硫酸钠均为优级纯。
2 方法与结果
2.1 色谱条件
色谱柱为HP-5(30 m×0.32 mm,0.25 μm);载气为氮气;氢火焰离子化检测器(FID),进样口温度为200℃,检测器温度为300℃;柱温采用程序升温,初始温度为80℃,保持4 min,然后以12℃·min-1升温至280℃,保持15 min;载气流速为1.0 mL·min-1;溶液进样,进样体积为2 μL。
2.2 溶液的制备
2.2.1 盐酸金刚烷胺标准品溶液。精密称取盐酸金刚烷胺标准品2.000 g,置于分液漏斗中,加5 mol·L-1氢氧化钠溶液20 mL,用三氯甲烷分次振摇提取(15、10 mL),静置分层;取三氯甲烷层,加适量无水硫酸钠振摇脱水,滤过;取滤液置于25 mL容量瓶中,用三氯甲烷稀释至刻度,摇匀,作为标准品贮备溶液。精密量取贮备液1 mL置于10 mL容量瓶中,用三氯甲烷稀释至刻度,摇匀,作为标准品溶液。
2.2.2 盐酸金刚烷胺供试品溶液。取盐酸金刚烷胺片样品20片,精密称定,研细,精密称取适量(约相当于盐酸金刚烷胺1.25 g),置于分液漏斗中,加5 mol·L-1氢氧化钠溶液20 mL,用三氯甲烷分次振摇提取(15、10 mL),取三氯甲烷层,加适量无水硫酸钠振摇脱水,滤过,取滤液置于25 mL容量瓶中,用三氯甲烷稀释至刻度,摇匀,作为供试品溶液。
2.2.3 金刚烷溶液。精密称取金刚烷0.5 g,置于10 mL容量瓶中,加三氯甲烷溶解并稀释至刻度,摇匀。
2.2.4 辅料溶液。按处方量称取辅料(约相当于含盐酸金刚烷胺1.25 g的量),按“2.2.2”项下方法制备辅料溶液。
2.3 系统适用性试验
精密量取“2.2.3”项下金刚烷溶液1 mL,置于100 mL容量瓶中,加盐酸金刚烷胺供试品溶液1 mL,用三氯甲烷稀释至刻度,摇匀,作为系统适用性试验溶液。取此试验溶液及“2.2”项下盐酸金刚烷胺标准品溶液、盐酸金刚烷胺供试品溶液、辅料溶液各2 μL,注入气相色谱仪,记录色谱,见图1。
由图1可知,盐酸金刚烷胺保留时间约为14.1 min,金刚烷保留时间约为11.1 min,盐酸金刚烷胺峰与金刚烷峰(分离度大于20)及其他物质峰的分离度良好。
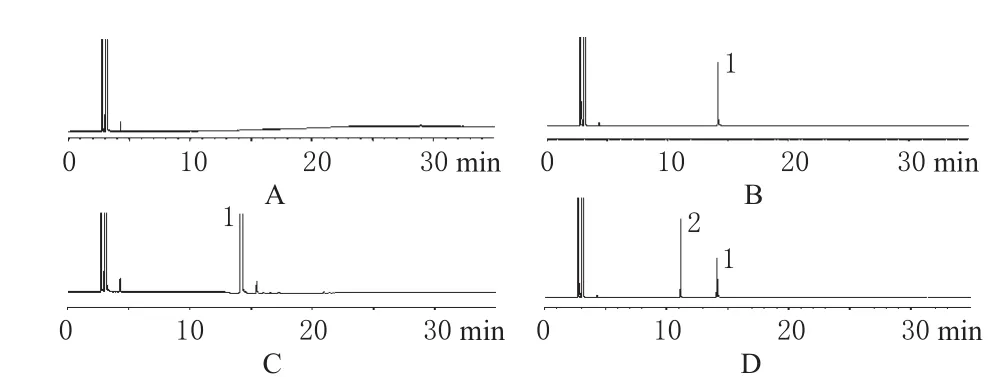
图1 系统适用性试验色谱图A.辅料;B.标准品;C.供试品;D.系统适用性试验溶液;1.盐酸金刚烷胺;2.金刚烷Fig 1 The chromatogram of system suitability testA.blank excipient;B.reference substance;C.test sample;D.solution of system suitability;1.amantadine hydrochloride;2.adamantane
2.4 专属性试验
精密称取盐酸金刚烷胺片细粉适量(约相当于盐酸金刚烷胺1.25 g)共5份,进行如下处理。(1)酸破坏:加0.1 mol·L-1盐酸溶液10 mL使盐酸金刚烷胺溶解,在50℃水浴加热20 min,放置至室温,加0.1 mol·L-1氢氧化钠溶液中和;(2)碱破坏:加1 mol·L-1氢氧化钠溶液10 mL使盐酸金刚烷胺溶解,在80℃水浴加热50 min,放置至室温,加1 mol·L-1盐酸溶液中和;(3)氧化破坏:加双氧水10 mL使盐酸金刚烷胺溶解,放置过夜;(4)高温破坏:在105℃烘箱中加热过夜;(5)光照破坏:在5 000 lx照度下光照过夜。上述5份样品均加入5 mol·L-1氢氧化钠溶液20 mL,用三氯甲烷分次振摇提取(15、10 mL),静置分层;取三氯甲烷层,加适量无水硫酸钠振摇脱水,滤过,取滤液置于25 mL容量瓶中,用三氯甲烷稀释至刻度,摇匀。分别取上述5种溶液,按“2.1”项下的色谱条件测定,记录色谱。结果,各破坏条件下均有不同程度的降解产物生成,但均能与主峰达到完全分离,表明该方法专属性好,详见图2。

图2 专属性试验色谱图A.酸破坏后样品;B.碱破坏后样品;C.氧化破坏后样品;D.高温破坏后样品;E.光照破坏后样品;1.盐酸金刚烷胺Fig 2 The chromatogram of exclusion inspectionA.sample destroyed by acid;B.sample destroyed by alkali;C.sample destroyed by oxidation;D.sample destroyed by high temperature;E.sample destroyed by high light;1.amantadine hydrochloride
2.5 线性关系考察
精密量取“2.2.1”项下盐酸金刚烷胺标准品贮备溶液0.5、1.0、2.0、3.0、4.0、5.0 mL置于5 mL容量瓶中,用三氯甲烷溶液稀释至刻度,摇匀。分别精密量取上述不同浓度溶液2 μL,按“2.1”项下色谱条件进样测定,以各溶液浓度(X,mg·mL-1)为横坐标,峰面积(A)为纵坐标,进行线性回归。结果表明,进样浓度在8.03~80.3 mg·mL-1的范围内,与测定的峰面积呈良好的线性关系:A=6.489×105X+4.060(r=0.999 9,n=6)。
2.6 稳定性试验
取“2.2”项下盐酸金刚烷胺标准品和供试品溶液,分别在0、1、4、12 h进样测定。结果盐酸金刚烷胺标准品溶液放置12 h稳定,盐酸金刚烷胺峰面积的RSD=0.8%;供试品溶液中杂质峰面积未有明显增加,盐酸金刚烷胺峰面积的RSD=1.2%。
2.7 精密度试验
精密量取“2.2.1”项下盐酸金刚烷胺标准品贮备溶液1.0 mL,置于5 mL容量瓶中,用三氯甲烷溶液稀释至刻度,摇匀。连续进样6次,测定。结果,盐酸金刚烷胺峰面积值的RSD=1.1%。
2.8 最低检测限
精密量取“2.2.1”项下盐酸金刚烷胺标准品贮备溶液适量,用三氯甲烷逐步稀释,测定,以盐酸金刚烷胺峰的信噪比(S/N)为3计算,测得其最低检测限为0.22 μg。
2.9 回收率试验
分别精密称取盐酸金刚烷胺标准品1.0、1.25、1.5 g各3份,分置于9个分液漏斗中,分别加入辅料适量,按“2.2.2”项下方法制备成低、中、高3个浓度的溶液各3份。取上述溶液进样2 μL测定,记录色谱。计算盐酸金刚烷胺回收率,结果低、中、高浓度回收率(n=3)分别为92.1%、97.3%、95.5%,RSD分别为2.8%、2.1%、1.9%,表明准确度良好。
2.10 样品中有关物质的含量测定
取盐酸金刚烷胺片样品20片,按“2.2.2”项下方法制备供试品溶液,加入金刚烷溶液。精密量取“2.3”项下系统适用性试验溶液2 μL,注入气相色谱仪,调节检测灵敏度,使主成分色谱峰的峰高约为满量程的20%,金刚烷胺峰与金刚烷峰的分离度应不小于20。精密量取供试品溶液2 μL,注入气相色谱仪,记录色谱。供试品溶液色谱图中如有杂质峰,按归一化法计算,单个杂质峰面积不得大于总峰面积的0.5%,各杂质峰面积的和不得大于总峰面积的2.0%。
对全国8个生产厂家的41批样品按拟定的有关物质方法测定,结果显示,41批样品中均检查出杂质峰,检出率为100.0%,41批样品中总杂质峰的峰面积均在规定限度(2.0%)内,单个杂质峰的峰面积均在规定限度(0.5%)内,结果见表1。
3 讨论
3.1 杂质限度的选择
USP及BP收载的盐酸金刚烷胺原料药采用气相色谱法测定有关物质,限度规定单个未知杂质不得过0.3%,所有杂质总量不得过1.0%;《中国药典》2010年版二部中盐酸金刚烷胺原料药有关物质的限度规定单个杂质峰面积不得大于总峰面积的0.3%,各杂质峰面积的和不得大于总峰面积的1.0%。考虑片剂中有关物质可能增加,故拟定盐酸金刚烷胺片有关物质的限度为:单个杂质峰面积不得大于总峰面积的0.5%,各杂质峰面积的和不得大于总峰面积的2.0%。

表1 41批样品中有关物质含量测定结果Tab 1 Determination results of related substances in 41 batches of samples
3.2 检测方法的选择
笔者曾尝试采用高效液相-紫外分光光度法(HPLC-UV法)和高效液相-蒸发光散射(HPLC-ELSD)法进行测定。但由于盐酸金刚烷胺紫外最大吸收波长为210 nm,属于末端吸收,基线噪音大,故不适合采用HPLC-UV法;盐酸金刚烷胺为水溶性化合物,采用HPLC-ELSD法测定,其在色谱柱上的保留时间短,杂质峰与盐酸金刚烷胺峰不能完全分离。经方法学验证,本文建立的气相色谱法测定盐酸金刚烷胺片的有关物质专属性强、准确,可有效地控制产品质量。
3.3 测定结果分析
盐酸金刚烷胺片厂家编号为2、5、6、7的样品单个杂质量较高,范围在0.11%~0.36%;厂家编号为1、4、8的样品单个杂质量较低,范围在0.03%~0.09%;厂家编号为3的样品单个杂质量总体较低,但有1批较高。说明建立的有关物质测定方法对盐酸金刚烷胺片生产处方的合理性、生产工艺的稳定性均可良好监控。
[1] 国家药典委员会编.中华人民共和国药典(二部)[S].2005年版.北京:化学工业出版社,2005:538.
[2] 国家药典委员会编.中华人民共和国药典(二部)[S].2010年版.北京:中国医药科技出版社,2010:737.
[3] The United States Pharmacopeial Convention.The United States Pharmacopeial[S].Rockville:The United States Pharmacopeial Convention,2009:1 054.
[4] The Recommendation of the Commission on Human Medicines.British Pharmacopoeia[S].London:British Pharmacopoeia Commission Office,2009:262.
[5] 许晋星.RP-HPLC法测定马来酸桂哌齐特片中有关物质的含量[J].中国药房,2009,20(1):59.