微波消解—原子荧光光谱法测定发酵剂中硒的研究
2011-01-08乌尼尔其其格高娃赵源常建军李梅
乌尼尔,其其格,高娃,赵源,常建军,李梅
(内蒙古蒙牛乳业集团股份有限公司,呼和浩特 011500)
微波消解—原子荧光光谱法测定发酵剂中硒的研究
乌尼尔,其其格,高娃,赵源,常建军,李梅
(内蒙古蒙牛乳业集团股份有限公司,呼和浩特 011500)
建立了用氢化物原子荧光法测定发酵剂中的硒,考察了前处理方法和原子荧光仪器对实验结果的影响,最后确定了消解试剂为6:2的硝酸和双氧水,微波消解最高温度为180℃,消解时间为30 min;原子荧光的还原剂为15 g/L的硼氢化钾,载流液为5%的盐酸。用以上最优化条件对发酵剂进行测定,得到硒的检出限为0.1 μg/L,相对标准偏差为0.15%~1.6%,回收率范围为91%~106%。
微波消解;原子荧光;硒;干粉发酵剂
0 引言
硒是人体必需的微量元素,它具有很强的生物活性,它是一种很好的抗氧化剂,能消除体内有机自由基,有抗肿瘤,防衰老,防辐射和增强机体免疫力等多种功能。然而,硒又是一个有毒性的元素,当吸收了3 mg就显示毒性[1]。基于它的两重型,建立一个准确、灵敏的测定方法是很重要的。微量硒的测定方法有:比色法、荧光法、电化学法和原子吸收法等。由于这些方法操作繁琐,灵敏度低,在使用上受到一定限制,而断续流动氢化物发生一原子荧光法已经广泛应用各种试样的测定。
本文采用断续流动氢化物发生一原子荧光法测定发酵剂中微量硒,它具有自动采样、进样量少;线性范围宽及选择的掩蔽剂无毒,操作简单、灵敏度高、准确、快速等特点。
1 实验
1.1 主要仪器与试剂
1.1.1 仪器
北京海光仪器公司产品AEF-2202E原子荧光光度计;高性能硒空心阴极灯;美国CEI微波消解设备;控温加热器。
1.1.2 试剂
硒标准储备液:1 mg/L,国家标准物质中心;硒标准使用液(1 μg/L);硝酸、盐酸、双氧水、氢氧化钾、硼氢化钾、硫尿、抗坏血酸:优级纯;发酵剂样品:某发酵剂公司。
实验中所有器皿均经(1∶1)硝酸溶液浸泡过夜,再用蒸馏水、超纯水冲净后晾干备用。实验中所用水为超纯水(电阻值大于18.2 MΩ)。
1.2 仪器工作条件
光电倍增管负高压280 mV;灯电流60 mA;原子化器高度8 mm载气流量400 mL/min;屏蔽气流量1 000 mL/min;测量方式[2]为标准曲线法。
1.3 样品预处理
微波消解:称取试样发酵剂0.3~0.5 g于消解罐中,再加入2 mL过氧化氢,6 mL硝酸,1 mL超纯水,振摇混合后放置在微波消解设备内,按设定程序消解(表1),消解完毕,冷却后放在控温加热器上继续加热至近干,切不可蒸干。再加5.0 mL浓度为6 mol/L盐酸,继续加热至溶液变为清亮无色并伴有白烟出现,将六价硒还原成四价硒。冷却,用超纯水转移试样消化液于25 mL容量瓶中,加2.0 mL盐酸,5.0 mL质量浓度为50 g/L的硫脲-抗坏血酸混合溶液,再用超纯水定容至刻度,混匀,用原子荧光光度计测定。同时作试剂空白。加标回收实验前处理与实际样品相同,只是多加入适量标样于样品,然后再消化。

表1 微波消解设备升温程序
1.4 标准系列溶液的配置
分别准确吸取1.0,0.5,0.2,0.15,0.1,0.0 mL硒标准使用液(质量浓度为1 μg/L)于25 mL容量瓶中,加2.0 mL盐酸,5.0 mL质量浓度为50 g/L的硫脲-抗坏血酸混合溶液,用超纯水定容,混匀,备用。
1.5 还原剂及载流液的配制
还原剂(质量浓度为15 g/L):称取7.5 g硼氢化钾,2.5 g氢氧化钾,用超纯水溶解于500 mL容量瓶中,定容,混匀,现用现配。
载流液(体积分数为5%):取50 mL盐酸于约有200 mL超纯水的烧杯中,再转移到1000 mL容量瓶中,用超纯水定容,混匀,备用。
1.6 测定
设定好仪器的最佳测定条件,仪器先自动测定标准曲线,然后转入样品空白及样品溶液的测定。
2 结果与讨论
2.1 微波消解试剂配比的确定
首先用单因素法考察消解试剂配比对加标后样品中硒含量的影响,在加标量相同的情况下,由表2可见,选择6 mL硝酸与2 mL双氧水时样品检测出硒的质量分数都大于硝酸与双氧水体积配比为3∶2时,因此微波消解试剂的体积配比定为HNO3∶H2O2=6∶2。
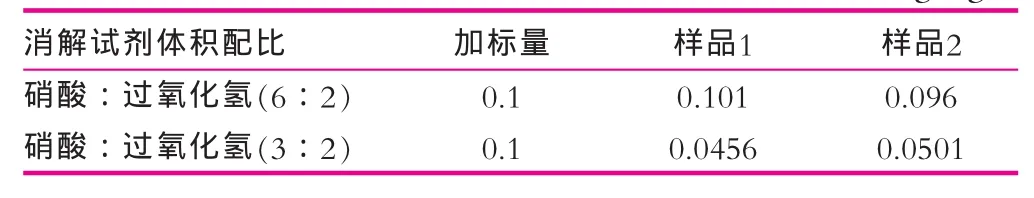
表2 微波消解试剂配比对结果的影响mg/kg
2.2 原子荧光条件的选择
2.2.1 载流液酸度的选择
由重金属离子生成金属氢化物需要一定的酸度,载流液盐酸体积分数过低就会与缓冲液氢氧化钠发生中和反应,不能将硼氢化钾的活性氢全部置换出来;盐酸体积分数过高则会腐蚀原子荧光仪的塑料管路,造成管路泄漏[3],进而影响实验数据的准确性,分别尝试测试3%~25%的盐酸与标准液荧光强度的关系,随着盐酸体积分数的增大,硒的荧光强度会先增加再逐渐趋于稳定,经过对比及实验论证,本文中盐酸体积分数为5%时为最佳条件。
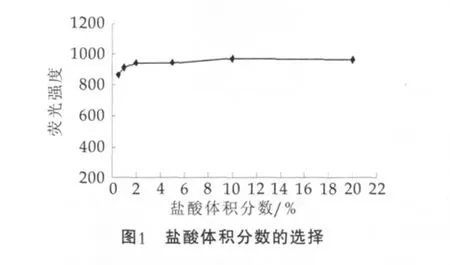
2.2.2 还原剂的质量浓度
由于硼氢化钾的反应活性很高,常温下与水即能发生反应,作为体系中的气态物发生的还原剂,对实验结果的灵敏度、准确度都有非常大的影响,浓度低时气态物难形成,浓度高时产生过多的氢,会引起气液相干扰[4],降低灵敏度,测定质量浓度范围从10 g/L到30 g/L的硼氢化钾对标准液荧光强度的影响,得出硼氢化钾质量浓度为15 g/L时为最佳条件。
2.2.3 线性范围
硒在质量浓度为0~200 μg/L范围内呈线性,回归方程为y=457.79x+28.877,相关系数为0.9992,标准曲线如图2所示。
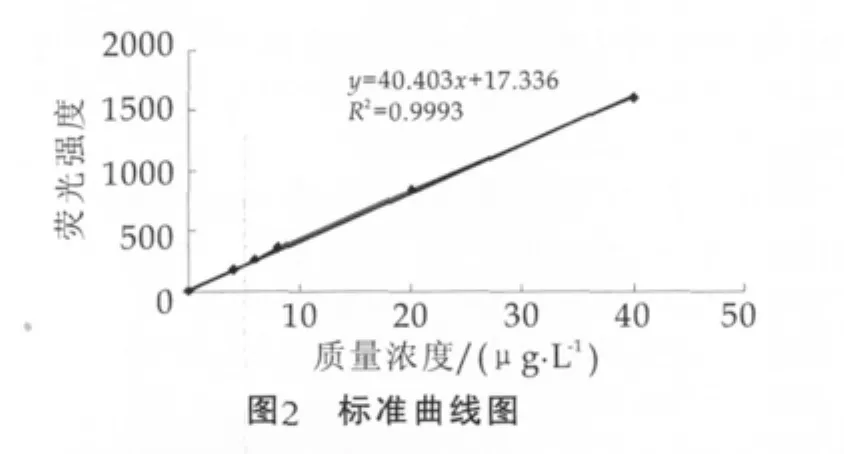
2.3 方法检出限
用空白标准进行20次硒吸光值的连续测定,根据3倍标准偏差[5]与对应的硒工作曲线斜率仪器自动求出该方法硒的检出限为0.1 μg/L。
2.4 精密度实验
分别配制低、中、高3个质量浓度硒标液,每个质量浓度测定6次,计算相对标准偏差,结果如表3所示。
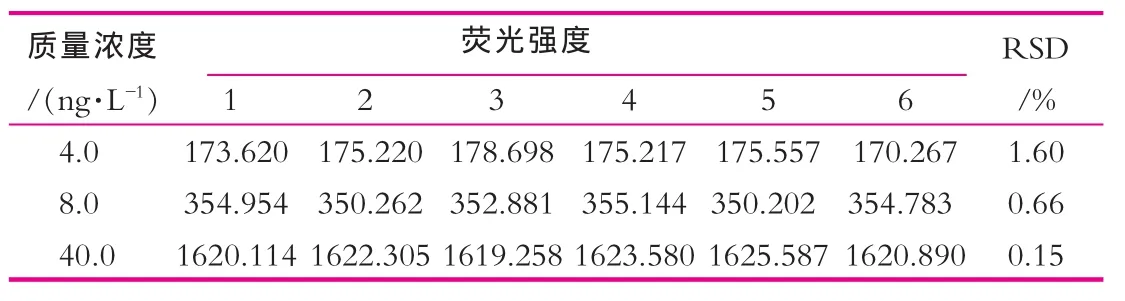
表3 精密度实验
2.5 回收率实验
应用本方法对发酵剂进行低、中、高不同水平加标回收检测[6],结果如表4所示。
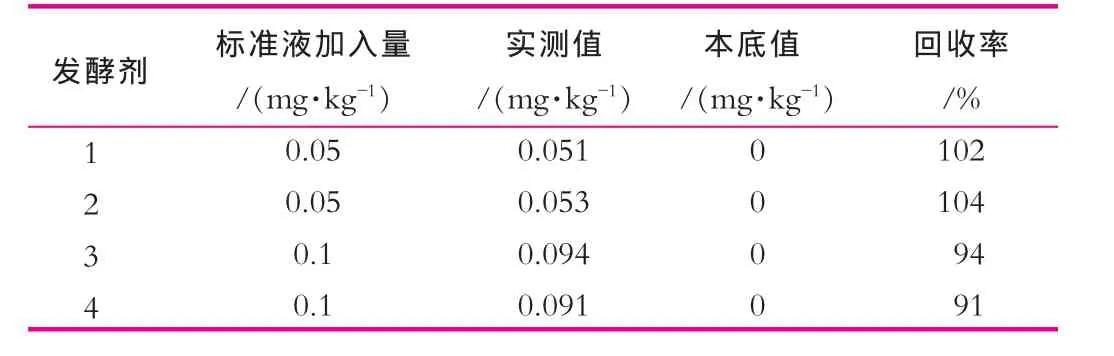
表4 回收率实验
3 结论
(1)本文应用AFS-2202E型双道原子荧光光度计测定发酵剂中硒,测试了各种最佳分析条件,在严格的质量控制条件下,其测定结果是满意的。
(2)用过氧化氢︰硝酸︰超纯水(2︰6︰1,体积比)的比例消解样品,在最佳仪器条件下,能达到很理想的效果。
(3)选择硫脲-抗坏学血酸混合溶液做掩蔽剂,替代铁氰化钾掩蔽剂,避免铁氰化钾遇酸产生极毒的氰化物,危害人体的危险性。
通过实验分析和测试条件优化,建立了原子荧光光谱法分析发酵剂中硒的方法,具有安全,灵敏可靠、简单快捷的优点。
.
[1]吴衔,彭泯.氢化物发生原子荧光法测定天然矿系水中的微量硒[J].分析实验室,2000,19(3):87-88.
[2]邹菁,张平,杨志刚,等.氢化物—无色散原子荧光法测定螺旋藻胶囊中的微量硒[J].分析实验室,1998,17(15):84-86.
[3]张世满.氢化物发生原子荧光法测定生活饮用水中微量硒[J].安徽预防医学杂志,2004,10(1):19-20.
[4]梅光泉.茶叶中的微量元素化学[J].微量元素与健康研究,2004,21 (1):49-52.
[5]CAVA MONTESINOS P J,CERVERA M L.Hydride Generation Atomic Fluorescence Spectmmec Determination of Uhratraces of Selenium and Tellurium in COW’sMilkl[J].J.Anal.Chim.Acta,2003,481(2):291-300.
[6]KUMARS.Trace Element Analytical Chemistry in Medicine and Biology[J].Anal.At Spectrom,1993,8(1):127.
Microwave digestion-atomic fluorescence spectrometry ofSelenium in Ferment
Wunier,Qiqige,Gaowa,ZHAO Yuan,CHANG Jian-jun,LI Mei
(Inner Mongolia Mengniu Dairy Industrial Co.Ltd.,Hohhot 011500,China)
Established using hydride generation atomic fluorescence spectrometry essence of heavy metals like mercury,studied pre-treatment methods and experimental results of atomic fluorescence instruments for the impact of the finalization of the digestion reagent 6:2 nitric acid and hydrogen peroxide microwave digestion maximum temperature of 180℃,digestion time of 25 min;atomic fluorescence of the reducing agent for the 15 g/L of potassium borohydride,carrier liquid for 5%hydrochloric acid.Using the above optimum conditions,the reaction essence was measured to be the detection limit of mercury 0.1 μg/L,the relative standard deviation of 0.15%~1.6%and the recovery ranges from 91%~106%.
Microwave digestion;Atomic fluorescence;Selenium;Ferment
TS252.7
A
1001-2230(2011)06-0062-03
2011-02-23
乌尼尔(1982-),女,本科,研究方向为食品检测。
