三维水网配合物[Ni(phen)2(CO3)]·7H2O的水热合成、晶体结构及其电化学性质*
2010-11-26姚如富
姚如富
(合肥师范学院 化学化工系,安徽 合肥 230601)
近年来,由金属离子和有机建筑模块所构筑的超分子体系在晶体学上展现出新颖和奇特的拓扑构型,使得这些配位分子体系在气体吸附与分离、催化化学、电子传导及分子磁学性质上具有潜在应用前景,因而金属配合物的研究成为当前化学研究的热点之一[1~4]。非共价键作用力,如氢键等分子间相互作用力、π-π堆积作用等成为构筑金属网络的重要驱动力。这些弱的非共价相互作用在生物遗传信息的表达和传递以及超分子自组装等方面具有重要的作用[5]。利用氢键连接构筑模块,设计合成具有特定功能的空穴或孔道状超分子是化学研究的热点之一。通过自组装,得到了氢键构成的分子格子、分子梯子、分子多边形和多面体等各种各样的超分子结构主体,在分子模拟,电化学分析等方面有广泛的应用[6,7]。
螯合配体邻菲啰啉及其衍生物在配位化学的发展中起着重要作用[8,9],由于邻菲啰啉(phen)强烈的螯合配位能力和空间位阻作用,phen在配合物中大多以一配位或二配位的形式存在[10,11]。在金属复合反应中有关螯合配体同金属离子结构形成的混配配合物已有大量报道[12,13]。本文采用水热法合成了一种具有水网结构的配合物[Ni(phen)2(CO3)]·7H2O(1),其结构经IR,元素分析和X-射线单晶衍射表征。相邻的1中,七个结晶水分子和碳酸根通过O-H┈O和C-O┈H氢键作用构成了三维反“S”型的超分子氢键网络。采用循环伏安法,在水溶液中测定了1的电化学性质,结果表明1具有较好的电化学性质,有望在磁电材料方面得以良好的应用。
1 实验部分
1.1 仪器与试剂
Nicolet 380型智能傅立叶变换红外光谱仪(KBr压片);Vario Elemental Ⅲ型元素分析仪;SDT Q600型差示扫描量热仪;Siemens Smart-1000型CCD衍射仪;上海辰华CH. Instrument 650c型电化学工作站。
所用试剂均为分析纯。
1.2 1的合成
在聚四氟乙烯反应釜中加入NiCl2·6H2O 291 mg(0.1 mmol), phen 36 mg(0.2 mmol)和水4.0 mL,搅拌下用0.1 mol·L-1NaOH调至pH 10.0左右;于120 ℃反应3 d得红棕色柱状晶体1(可直接用于X-射线衍射分析),产率85%; IRν: 3 389(OH), 1 589, 1 510, 1 432, 1 277, 1 230, 1 100, 1 060, 1 090, 1 017(C=C, C-N, C-H in phen), 933(CH), 852(phen), 830(CH), 727(phen), 659, 550(Ni-O, Ni-N) cm-1; Anal.calcd for C25H30N4O10Ni: C 49.91, H 4.996, N 9.26; found C 50.10, H 5.001, N 9.02。
1.3 1的晶体结构测定
选取单晶1置衍射仪上,在293(2) K下采用石墨单色化的MoKα射线(λ=0.071 073 nm)作衍射光源,以ω/2θ方式扫描,在2.27 ≤θ≤26.41°内共收集19 844个衍射点,其中独立衍射点为6 238个,可观测点为4 915个。非氢原子坐标由直接法解出,氢原子坐标由差值合成Fourier合成得到,对非氢原子坐标使用全矩阵最小二乘法进行各向异性温度因子修正。1的晶体学数据见表1,部分键长和键角见表2,氢键键长和键角见表3。

表 1 1的晶体学数据Table 1 Crystallographic data of 1
1.4 1的电化学性质测定
在电化学工作站上,在水溶液中,以四丁基溴化铵为支持电解质,Pt电极(213型)为工作电极,Ag/AgCl电极为参比电极,Pt丝电极为辅助电极,以200 mV·s-1的扫描速度在-1.5 V~2.0 V连续循环扫描,测试1在水溶液中的循环伏安曲线。
2 结果与讨论
2.1 1的晶体结构分析
1的分子结构见图1。 由图1可见,Ni处于畸变的八面体配位环境中,Ni2+与2个phen配体提供的4个N原子[(N(1), N(2), N(3), N(4)]和碳酸根提供2个氧原子[O(1), O(2)]形成一个八面体结构,Ni与配位原子形成了两个五元环和一个四元环,使八面体的变形性非常大。O(1), O(2), N(2)和N(3)近似构成八面体的赤道平面,其扭转角为10.41°。 Ni(1)位于该赤道平面上,与该平面的距离为0.000 3 nm。 Ni(1)-N(2)的键长[0.209 26(19) nm]稍短于Ni(1)-N(3)的键长[0.210 31(18) nm], Ni(1)-O(2)的键长[0.207 31(16) nm]稍短于Ni(1)-O(1)的键长[0.204 49(16) nm]。键角分别为:101.57(7)°[N(2)-Ni(1)-N(3)], 91.27(7)°[N(2)-Ni(1)-O(2)], 104.18(7)°[N(3)-Ni(1)-O(1)], 166.14(7)°[N(3)-Ni(1)-O(2)]及63.68(6)°[O(1)-Ni(1)-O(2)]。 phen配位后其键长和键角没有发生多大变化,N(1)和N(2)到phen平面的距离分别为0.004 5 nm和0.029 2 nm; N(3)和N(4)到phen平面的距离分别为0.031 3 nm和0.002 6 nm,中心Ni2+到两个phen平面的距离分别为0.016 2 nm和0.020 5nm,两个phen之间的二面角为77.16°,其与赤道平面的夹角分别为88.13°和86.47°。与镍形成的五元环与其相邻的phen平面之间的二面角分别为3.89°和3.98°。 N(1)和N(4)原子分布在八面体的轴向上,较偏离碳酸根,N(1)和N(4)没有共线[N(1)-Ni(1)-N(4)=169.99°], Ni(1)-N(1)和Ni(1)-N(4)键长分别为0.207 79(19) nm和0.208 87(18) nm。 N(1)和N(4)到赤道平面的距离分别为0.205 70 nm, 0.206 70 nm。

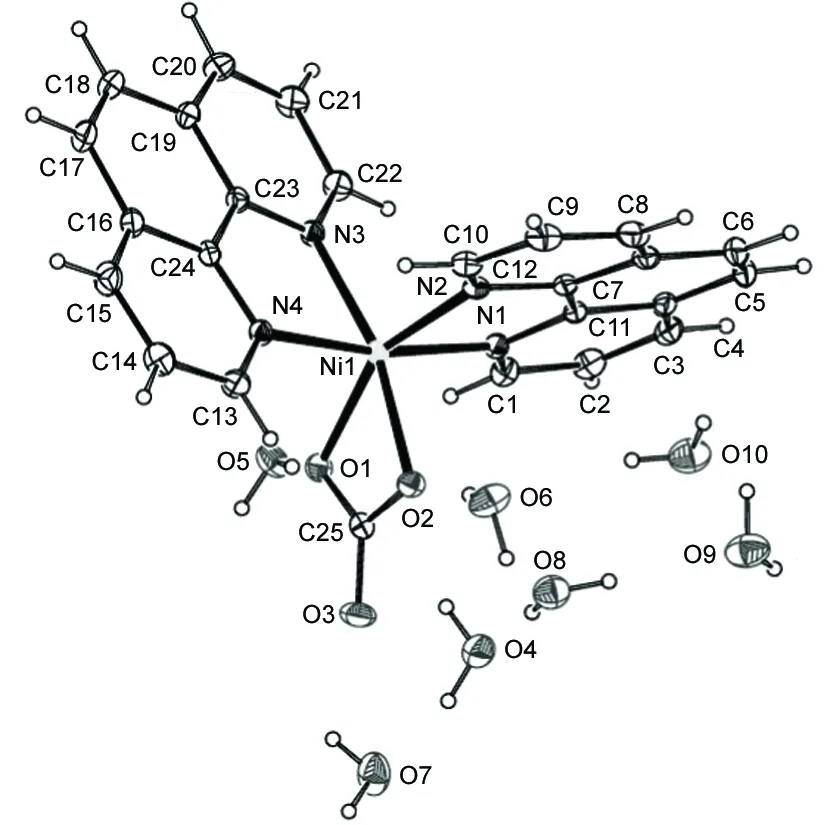
图 1 1的分子结构图

图 2 1分子中的氢键堆积图

图 3 1分子中的二维水网氢键图
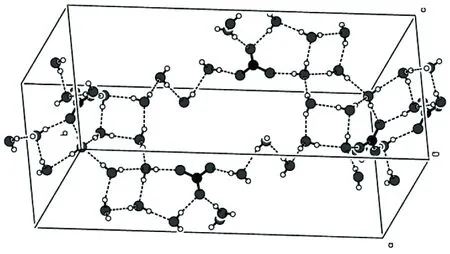
图 4 1分子中的三维水网氢键图

BondLength/nmBondAngle/(°)BondAngle/(°)Ni(1)- O(2)0.204 49(16)O(2)-Ni(1)-O(1)63.68(6)N(1)-Ni(1)-N(2)79.79(7)Ni(1)- O(1)0.207 31(16)O(2)-Ni(1)-N(1)93.95(7)N(4)-Ni(1)-N(2)94.89(7)Ni(1)- N(1)0.207 79(19)O(1)-Ni(1)-N(1)93.48(7)O(2)-Ni(1)-N(3)166.14(7)Ni(1)- N(4)0.208 87(18)O(2)-Ni(1)-N(4)94.65(7)O(1)-Ni(1)-N(3)104.18(7)Ni(1)- N(2)0.209 26(19)O(1)-Ni(1)-N(4)94.93(7)N(1)-Ni(1)-N(3)93.47(7)Ni(1)- N(3)0.210 31(18)N(1)-Ni(1)-N(4)169.99(7)N(4)-Ni(1)-N(3)79.20(7)O(2)-Ni(1)-N(2)91.27(7)N(2)-Ni(1)- N(3)101.57(7)O(1)-Ni(1)-N(2)153.73(7)

表 3 1的氢键键长和键角Table 3 Hydrogen bond lengths ans bond angles of 1
#11-x, -y, 1-z;#2-1+x, y, z;#3x, 1/2-y, 1/2+z;#4x, 1/2-y, -1/2+z;#51+x, 1/2-y, 1/2+z;#6x, y, -1+z
2.2 1的热分析
利用差示扫描量热仪,以10 ℃·min-1的升温速率,在30 ℃~600 ℃内和静态空气条件下对1进行热稳定性研究,结果见图5。从图5可以看出,1的热分解分四步进行。(1)1在110 ℃~180 ℃内失去7个结晶水分子,失重率20.18%,与理论值(20.83%)吻合;(2)随后在260 ℃~310 ℃失重,表明1失去CO2,失重率7.86%(理论值7.27%); (3)1的骨架发生坍塌,在370 ℃~430 ℃内失去2个phen配体,失重率53.98%,与理论值(59.55%)吻合;(4)1一步分解,到550 ℃左右热解完全,推测最终残留物为NiO。

Temperature/℃图 5 1的TG曲线*

Potential/V图 6 1的循环伏安曲线
2.3 1的电化学性质
1的循环伏安曲线见图6。从图6可知,1表现出单电子的准可逆反应,其氧化还原峰非常接近,氧化还原峰分别为0.31 V和-0.40 V,是Ni(Ⅱ)和Ni(Ⅲ)之间的相互转化。该研究对于拓展含有延伸电子共轭体系金属有机化合物的深入研究,探索化合物结构、性质和功能之间的相互关系,开发具有潜在应用价值的磁电功能材料具有一定的指导意义。
3 结论
(1) 合成了镍配合物[Ni(phen)2(CO3)]·7H2O, X-单晶衍射表明,配合物中Ni处于畸变的八面体配位环境中。
(2) 1具有较好的电化学性质,循环伏安法表明,其存在一对氧化还原峰,峰电位分别为0.31 V和-0.40 V。
(3) X-单晶衍射证明在反应过程中配合物分解了空气中的二氧化碳,故该配合物在环境保护以及化学固定二氧化碳方面具有一定的潜在应用价值。
[1] Li D, Clé rac R, Roubeau O,etal. Magnetic and optical bistability driven by thermally and photoinduced intramolecular electron transfer in a molecular cobalt-iron prussian blue analogue[J].J Am Chem Soc,2008,130:252-258.
[2] Lu W, Zhu N, Che C M. Polymorphic forms of a gold(Ⅰ) arylacetylide complex with contrasting phosphorescent characteristics[J].J Am Chem Soc,2003,125:16081-16088.
[3] Kong L Y, Zhu H F, Huang Y Q. Cadmium(Ⅱ) and copper(Ⅱ) complexes with imidazole-containing tripodal polyamine ligands:pH and anion effects on carbon dioxide fixation and assembling[J].Inorg Chem,2006,45:8098-8107.
[4] Hsu M H, Chen R T, Sheu W S,etal. Carbon dioxide fixation by an unprecedented hydroxo lead-chromium carbonyl complex:Synthesis,reactivity, and theoretical calculations[J].Inorg Chem,2006,45:6740-6747.
[5] MacGillivray L R, Arwood J L. Molecular recognition of the cyclic water trimer in the solid state[J].J Am Chem Soc,1997,199:2592-2594.
[6] Liao Y C, Jiang Y C, Wang S L. Discrete water hexamers and template-assisted molecular recognition in an elastic zincophosphate lattice[J].J Am Chem Soc,2005,127:12794-12796.
[7] E Y Choi, L D DeVries, R W Novotny,etal. An interdigitated metalloporphyrin framework:Two-dimensional tessellation,framework flexibility,and selective guest accommodation[J].Cryst Growth Des,2010,10:171-176.
[8] V Gómez, M Corbella, G Aullón. Two temperature-independent spinomers of the dinuclear Mn(Ⅲ) compound{[Mn(H2O)(phen)]2(μ-2-ClC6H4CO2)2(μ-O)](ClO4)2[J].Inorg Chem,2010,49:1471-1480.
[9] C D Zhang, S Liu, C Sun,etal. Assembly of organic-inorganic hybrid materials based on dawson-type polyoxometalate and multinuclear copper-phen complexes with unique magnetic properties[J].Cryst Growth Des,2009,9:3655-3660.
[10] Dhar S, Chakravarty A R. Efficient visible light induced nuclease activity of a ternary mono-1,10-phenanthroline copper(Ⅱ) complex containing 2-(methylthio)ethylsalicylaldimine[J].Inorg Chem,2003,42:2483-2485.
[11] Y Pan, Q Jin, J Chen,etal. Hydrothermal syntheses and characterizations of thioarsenates [Fe(phen)3][As3S6]·dien·7H2O and [Mn2(phen)4(As2S5)]·phen·2H2O:A new coordination mode of the As2S5-anion[J].Inorg Chem,2009,48:5412-5417.
[12] Kari A McGee, Kent R Mann. Inefficient crystal packing in chiral [Ru(phen)3](PF6)2enables oxygen molecule quenching of the solid-state MLCT emission[J].J Am Chem Soc,2009,131:1896-1902.
[13] J Bi, L Kong, Z Huang,etal. Self-encapsulation of [MⅡ(phen)2(H2O)2]2+(M=Co,Zn) in one-dimensional nanochannels of [MⅡ(H2O)6(BTC)2]4-(M=Co,Cu,Mn):A high HQ/CAT ratio catalyst for hydroxylation of phenols[J].Inorg Chem,2008,47:4564-4569.
