高铁酸钾与次氯酸钠联合氧化降解聚乙烯醇的研究
2010-10-25于少明王华林翟林峰
周 俊, 于少明, 王华林, 翟林峰, 刘 涛
(合肥工业大学 化学工程学院,安徽 合肥 230009)
聚乙烯醇(PVA)是一种水溶性高分子化合物,广泛应用于纺织、造纸、涂料等行业[1,2]。据统计,我国纺织行业每年用作上浆剂的PVA大约在3×104t,要产生大量的PVA,其质量浓度为3 g/L左右的退浆废水,若不对其进行处理,将会对生态环境造成严重的危害[3-5]。从20世纪70年代以来,人们就对PVA降解进行了研究。由于PVA的生物降解性较差,传统的生物法难以将其降解完全,文献[6]用活性污泥对 PVA降解,300 d后PVA的去除率为75%。文献[7]用驯化后的微生物降解PVA,其活性受环境的影响较大,PVA的去除效果也不够理想。近年来,化学氧化法用于PVA降解引起人们极大的关注[8,9],文献[9]用 Fenton法降解 0.2 g/L PVA溶液,30 min后COD的去除率为90%。在实际应用中,由于Fenton法要求反应体系pH值在3左右[10],而大多数含PVA的废水呈近中性甚至碱性,因此处理前必须调节废水的pH值。另外,Fenton法只适用于低质量浓度PVA废水的处理[11]。
高铁酸钾是一种强氧化剂,其标准电极电位在酸性介质中为 2.20 V,在碱性介质中为0.72 V,表明其在pH值较宽范围内均具有良好的氧化活性。本文研究了高铁酸钾与次氯酸钠溶液联合氧化降解PVA的方法,取得了较为满意的结果。
1 实 验
1.1 试剂与仪器
试剂:聚乙烯醇(平均聚合度为1 750±50),K2FeO4(自制,纯度为90%~98%),次氯酸钠(自制,质量浓度为 40~ 80 g/L),H3BO3、KI、I2、NaOH和Na2SO3等试剂均为分析纯。
仪器:VECTOR-22傅立叶变换红外光谱仪,UV-9100紫外可见分光光度计,HJ-3控温磁力搅拌器,HHS-2数显恒温水浴锅,TDL-2B离心机以及乌氏黏度计。
1.2 PVA降解实验
取50 mL质量浓度为3.0 g/L PVA溶液于100 mL烧杯中,室温下调节溶液pH值后加入一定量的高铁酸钾固体,快速摇匀;再加入一定量次氯酸钠溶液,反应60 min后加Na2SO3终止反应;离心分离,取上层清液分析其 PVA的质量浓度[12]。
1.3 COD的测定
移取5.00 mL PVA降解实验中的上层清液至50 mL容量瓶中,定容后用重铬酸钾法(CODCr)测定其化学需氧量[13]。
1.4 PVA黏度的测定
移取10.00 mL经砂芯漏斗过滤后的PVA溶液至干燥的乌氏黏度计中,恒温10 min后测定其流过时间t,重复以上操作3次,误差不超过0.3 s。然后用蒸馏水将黏度计清洗3~5次,测定空白样品的流过时间t0,再算出其相对黏度ηr,公式为:
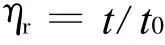
其中,ηr为相对黏度;t为溶液流出时间;t0为溶剂流出时间 。
1.5 红外光谱的检测
取适量PVA降解实验中的上层清液,将其缓慢加热蒸发至近干,再在60℃烘箱中恒温烘干,然后将烘干样与KBr一起研磨、压片,测其红外光谱。
2 结果与讨论
2.1 氧化剂的选择
不同氧化剂对PVA去除效果见表1所列。从表1可知,这3种氧化剂对PVA都有一定的去除能力,但是用高铁酸钾与次氯酸钠联合氧化PVA的去除效果比单独用K2FeO4与NaClO溶液效果好,表明两者具有良好的协同氧化作用。这可能是由于次氯酸钠的存在抑制了FeO42-的分解[14],从而大大提高了K2FeO4溶液的稳定性。

表1 不同氧化剂对PVA去除效果
2.2 高铁酸钾、次氯酸钠投加量的影响
在次氯酸钠的质量浓度为2.5 g/L,氧化时间为60 min时,高铁酸钾投加量对PVA的去除效果如图1所示。从图1可以看出,随着高铁酸钾投加量的增加,PVA的去除率增大;当高铁酸钾投加量为0.32 g/L时,PVA的去除率为98.21%;此后再增大高铁酸钾的投加量,PVA的去除率增加不明显。因此在降解实验中K2FeO4的投加量取0.32 g/L较适宜。
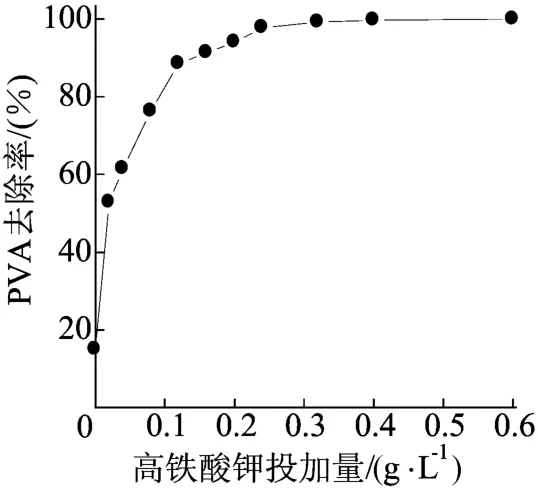
图1 高铁酸钾投加量对PVA去除率的影响
次氯酸钠投加量对PVA去除率的影响结果如图 2所示,此时高铁酸钾的质量浓度为0.32 g/L,氧化时间仍为 60 min。从图 2可看出,PVA的去除率随着次氯酸钠的质量浓度增大而增大,当次氯酸钠的质量浓度为3.92 g/L时,PVA去除率为99.32%,此后,PVA去除率趋于稳定。
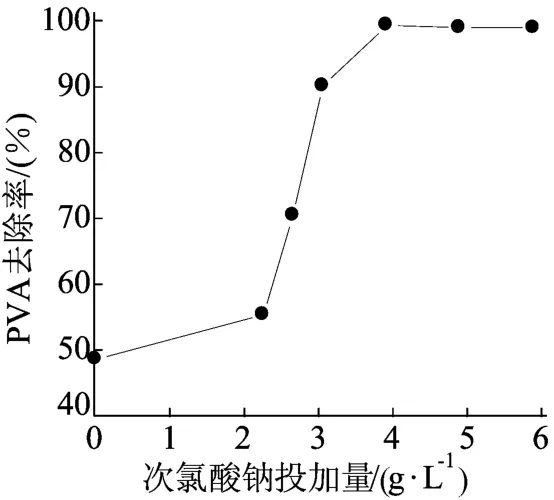
图2 次氯酸钠投加量对PVA去除率的影响
2.3 氧化时间的影响
氧化时间对PVA去除率的影响(高铁酸钾与次氯酸钠质量浓度分别为 0.32 g/L和3.92 g/L)结果如图3所示。由图3可见,高铁酸钾与次氯酸钠联合使用时,不仅对PVA的去除率比两者单独使用时要大许多,且其氧化速度也比两者单独使用时要快许多。从图3中还可以看出,随着时间的延长,3种氧化剂对PVA的去除效果均呈上升的趋势,50 min后PVA的去除率逐渐趋于稳定。
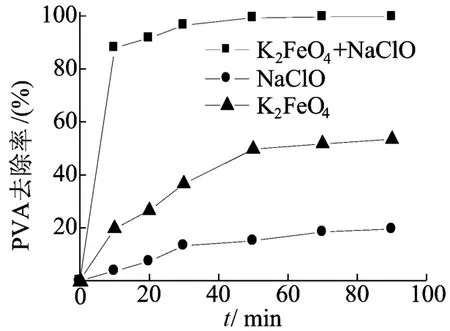
图3 氧化时间对PVA去除率的影响
2.4 pH值的影响
由于高铁酸钾稳定性受溶液pH值影响较大,所以PVA降解前溶液的pH值控制较为重要。实验考察了溶液初始pH值对PVA去除率的影响,结果如图4所示。
从图4中可以发现,次氯酸钠单独作为氧化剂时,PVA初始pH值对其去除率影响不大。高铁酸钾单独作为氧化剂时,当pH<4.6时,PVA的去除率变化较大,当pH>4.6时,PVA的去除率变化逐渐趋于稳定。高铁酸钾与次氯酸钠联合作氧化剂时,PVA的去除率变化趋势与高铁酸钾作为氧化剂时PVA的去除率变化趋势相似,且PVA的去除率值远大于次氯酸钠和高铁酸钾单独作为氧化剂时PVA去除率之和值,表明在实验所用 pH值范围内,高铁酸钾与次氯酸钠对PVA降解均具有良好的协同作用。

图4 pH值对PVA去除率的影响
2.5 PVA初始质量浓度的影响
高铁酸钾与次氯酸钠联合降解初始质量浓度为1.0 g/L和3.0 g/L的PVA溶液,其去除率随氧化时间的变化关系如图5所示。从图5中可以发现,高铁酸钾与次氯酸钠联合降解初始浓度为1.0 g/L和3.0 g/L的PVA效果都较好。对不同初始质量浓度PVA,其CODCr去除率见表2所列。从表2可知,对于初始浓度为 0.5 g/L的PVA,其CODCr去除率较高,表明PVA氧化降解程度较深,溶液中剩余的能与重铬酸钾反应的可还原性物质较少;对于初始浓度为3.0 g/L的PVA氧化后,溶液中剩余的与重铬酸钾反应的小分子还原物质较多,则CODCr去除率不高。

图5 PVA质量浓度对去除效果的影响

表2 不同初始质量浓度PVA的COD去除效果
实验进一步考察了PVA降解过程中溶液相对黏度的变化,结果如图6所示。从图6中看出,在3种氧化剂作用下,PVA溶液相对黏度随氧化时间延长逐渐降低,其中用高铁酸钾与次氯酸钠联合氧化时,PVA溶液的ηr下降得更快,表明此时PVA降解产物的分子量降低速率较快,最终产物分子量较小。

图6 PVA降解中相对黏度的变化
2.6 降解产物分析
PVA及其降解产物的 FT-IR谱图,如图7所示。由图7可以看出,PVA主要的红外吸收峰有3 500~3 000 cm-1O-H伸缩振动吸收宽峰,2 930 cm-1C-H的伸缩振动峰,1 099 cm-1CO伸缩振动峰;氧化后PVA的2 930 cm-1C-H伸缩振动峰消失,而在1 753 cm-1出现了C=O伸缩振动峰,2 457 cm-1、982 cm-1出现了羧基特性峰,表明PVA发生了断链,降解产物主要为羧基化合物。

图7 PVA及其降解产物的FTIR光谱图
3 结 论
(1)高铁酸钾、次氯酸钠对PVA溶液均有一定降解能力,但两者联合使用时,对PVA的氧化降解效果更加显著。
(2)在3.0 g/L,pH值为7.2的PVA溶液中,高铁酸钾与次氯酸钠投加量分别为0.32 g/L、3.92 g/L,反应50 min 时,PVA 的去除率达98%以上,CODCr去除率大于40%。
(3)高铁酸钾与次氯酸钠联合氧化时,通过黏度测定发现PVA逐渐断链成小分子物质,红外光谱分析结果表明最终降解产物主要为羧基化合物。
[1] T okiwa Y,Kawabata G,Jarerat A.A modified method for isolating poly(vinyl alcohol)degrading bacteria and study of their degradation patterns[J].Biotechnology Letters,2001,23:1937-1941.
[2] Kim B C,Sohn C K,Lim S K,et al.Deg radation of polyvinyl alcohol by Sphingomonas sp.SA3 and its symbiote[J].Microbial Biotechnology,2003,30:70-74.
[3] 郭 力,奚旦立,袁海源.含PVA退浆废水处理技术及应用的研究[J].今日科技,2007,(8):45-47.
[4] 张 斌,周永元.浆纱污染与环境保护[J].棉纺织技术,2003,31(7):17-20.
[5] 雷乐成.光助Fenton氧化处理 PV A退浆废水的研究[J].环境科学学报,2000,20(2):139-144.
[6] Ishigaki T,Kawagoshi Y,Ike M,et al.Biodeg radation of a polyvinyl alcohol-starch blend plastic film[J].World Journal of Microbiology&Biotechnology,1999,15:321-327.
[7] Vaclavkova T,Ruzicka J,Julinova M,et al.Novel aspects of symbiotic(polyvinyl alcohol)biodegradation[J].Applied Microbial Biotechnology,2007,76:911-917.
[8] Giroto J A,Guardani R,Teixeira A C S C,et al.Study on the photo-Fenton deg radation of poly viny l alcohol in aqueous solution[J].Chemical Engineering and Processing,2006,45:523-532.
[9] Lei L C,Hu X J,Yue P L,et al.Oxidative degradation of polyvinyl alcohol by the photo chemically enhanced Fenton reaction[J].Journal of Photochemistry and Photobiology A:Chemistry,1998,116:159-166.
[10] 吴耀国,冯文璐,王秋华,等.Fenton法中拓宽pH值范围的方法[J].现代化工,2008,28(2):87-90.
[11] 刘琼玉,李太友.难降解有机污染物的高级氧化技术[J].江汉大学学报(自然科学版),2002,19(2):56-58.
[12] 束嘉秀,董亦斌,张慧芬.分光光度法直接测定水中聚乙烯醇(PVA)含量的研究[J].昆明理工大学学报(理工版),2003,28(5):127-130.
[13] 奚旦立,孙裕生,刘秀英.环境监测[M].北京:高等教育出版社,1995:389-391.
[14] 贾汉东,鲍改玲,孙红宾.次氯酸根对高铁酸盐溶液的稳定作用[J].无机盐工业,2002,34(5):4-5.
