阴/阳离子诱导高铁酸钾去除二级出水中的磷
2021-10-27王洪波王一凡张运波王宁陈飞勇
王洪波王一凡张运波王宁陈飞勇
(1.山东建筑大学 市政与环境工程学院,山东 济南250101;2.山东建筑大学 资源与环境创新研究院,山东 济南250101)
0 引言
人类排放的含磷工业废水和生活污水对全球磷循环产生了显著的影响[1]。水中过量的磷会促使藻类的大量生长和繁殖,从而造成富营养化和藻毒素的分泌。富营养化会导致生态失衡,而藻毒素则直接威胁人类和水生生物的健康[2]。根据GB/T 18918—2002《城镇污水处理厂污染物排放标准》[3],总磷(Total Phosphorus,TP)排放量要求<1 mg/L,城市污水厂二级出水中的磷超过废水标准的情况时有发生,因此,污废水排放前有效去除磷对于控制水体富营养化至关重要。
目前已经提出并应用于控制磷污染的方法很多,包括强化生物处理法、化学沉淀法和吸附法[4]。其中,化学方法存在着成本高、化学污泥含量高、处理困难、产生二次污染等不足;生物法运行条件相对严格,但存在效果不稳定、出水易出现不达标等问题[5];吸附法通常利用大比表面积的吸附材料吸附去除水溶液中的磷[6],虽然操作简单、无二次污染,但传统混凝剂吸附的磷很容易解析到介质中,吸附剂的抗干扰性、解析以及再生方面仍然存在一些问题[7],而且磷的去除效率受吸附剂特性和磷污染物初始浓度的限制[8],在实际使用过程中成本较高,故其实际应用较少。
综上所述,寻找一种具有高效除磷能力的环保型化学药剂具有重要意义。高铁酸钾是一种具有强氧化性的多功能绿色化学絮凝剂[9],在水处理过程中同时用作氧化剂、消毒剂和混凝剂。与传统的化学沉淀和生物除磷手段相比,高铁酸钾的强氧化性能将各种形态的磷氧化成P5+,随后与高铁酸钾的还原产物反应生成磷酸铁沉淀。此外,高铁酸钾的还原产物对磷具有良好的络合和吸附作用,且与硫酸亚铁、硝酸铁、氯化铁和硫酸铝相比,高铁酸钾产生的污泥量要少得多[10]。高铁酸钾的氧化性在污水处理过程中还发挥着预处理作用[11],如对复杂水质环境中的抗生素、重金属等污染物进行预处理,有利于后续的处理工艺和出水水质,这一系列优势都是普通絮凝剂所不具备的。在实际的二级出水中,磷并不是单独存在的,而是以磷酸盐的形态和有机物共存,故高铁酸钾的氧化作用对水中有机物的去除具有重要意义[12]。高铁酸钾不仅可以氧化和去除水中的有机物,还可以生成具有良好除磷性能的新铁氧化物。实验发现,用高铁酸钾处理二级出水时,水中磷含量降低的同时,微污染物(如抗生素等)含量也出现降低,证明了水环境中除磷以外的其他有机物同时得到了处理[13]。高铁酸钾作为一种高效的水处理剂,对水中污染物的协同处理是其最突出的特点,这也是选择高铁酸钾除磷的重要原因。
高铁酸钾除磷是一个多步骤的过程,包括高铁酸钾氧化污染物后还原转化为水解产物氢氧化铁;水解产物在结合磷的同时发挥混凝和絮凝作用。高铁酸钾对磷的去除效率取决于氧化pH值、混凝pH值和反应时间,除磷过程不产生对人类和环境有害的衍生物。此外,铁与磷元素的质量比也会影响磷的去除效率。关于高铁酸钾去除污水中磷的研究已有报道,但鲜有关于还原剂(阴离子和阳离子)对高铁酸钾去除废水中磷的影响的报道。将还原剂引入高铁酸钾除磷体系有两个原因:(1)发现Fe2+被氧化后形成的原位Fe3+比直接投加的Fe3+具有更好的吸附能力[13],因此可以假设加入还原剂能够提高高铁酸钾的反应活性,促进高铁酸钾的氧化性能并增强吸附除磷效果;(2)从经济角度考虑,高纯度固体高铁酸钾至今未大规模生产,成本相对较高,如果添加还原剂可以显著提升处理效果,可以减少高铁酸钾的投加量,降低成本,具有一定的实际指导意义。在对阴/阳离子还原剂选择的过程中,从现有的常用絮凝剂中考虑,使用铁盐作为阳离子还原剂,观察价格较低的铁盐对高铁酸钾处理效果的影响。选择本身对高铁酸钾的稳定性几乎没有影响的I-,能够更好地控制变量,观察处理效果的变化。
文章以二级出水为研究对象,采用阴/阳离子诱导的高铁酸钾进行实验,评价不同种类磷的处理效果,研究还原剂种类、质量比和pH值等因素对处理效果的影响。
1 材料与方法
1.1 材料
实验药品包括四水氯化亚铁FeCl2·4H2O(天津光复精细化工研究所,纯度>99.7%)、六水氯化铁FeCl3·6H2O(天津光复精细化工研究所,纯度>99.7%)、碘化钾KI(天津科密欧化试剂有限公司,纯度>99.0%)。四水氯化亚铁和碘化钾密封保存在干燥黑暗的环境中。高铁酸钾(浙江大学实验室配制,纯度93%)存放在低温干燥的环境中,每次实验前使用铬酸盐滴定法[14]和分光光度法[15]检查纯度。10%抗坏血酸溶液现用现配,最多冷藏保存7 d,钼酸铵溶液也是现用现配,最多冷藏保存15 d,其他试剂均使用优级纯。
所有试剂均用超纯水配制。高铁酸钾和四水氯化亚铁均在干燥环境中称重,10 min内使用,防止因称重时间过长导致Fe2+氧化。采用干抛法,将两者同时加入反应烧杯中,利用定时六联搅拌仪调节搅拌转速和时间。
1.2 方法
1.2.1 磷去除实验
用于实验的二级出水来自山东建筑大学再生水站。在每个烧杯中加入400 mL的二级出水作为样品进行实验。二级出水水质特征见表1。将高铁酸钾固体粉末投加至20 mg/L,还原剂按与高铁酸钾的质量比为1∶1、1.5∶1和2∶1投加。单独使用高铁酸钾实验组的质量浓度为20 mg/L。通过加入氢氧化钠或盐酸调节pH值在5.2~10.2范围内。混凝沉淀实验通过MY3000-6N 6#桨可编程混凝实验搅拌仪(武汉市梅宇仪器有限公司)进行。按以下步骤操作:混合物以350 r/min搅拌20 s,以140 r/min搅拌15 min,再以70 r/min搅拌15 min,最后静置10 min。
沉淀后取上清液,经0.45μm水系滤膜过滤。对过滤后的样品进行TP、溶解性总磷(Soluble Total Phosphorus,DTP)和可溶性正磷酸盐(Soluble Orthophosphate,SOP)的检测,每个样品进行3次平行实验。将实验中生成的沉淀物离心并冷冻干燥后进行表征分析。
1.2.2 分析方法
利用UV-3200紫外分光光度计(上海美谱达仪器有限公司)在700 nm下,通过钼酸铵分光光度法测定过滤上清液中TP、DTP和SOP的浓度[16]。利用FEI Quanta 400 FEG扫描电镜(Scanning Electron Microscope,SEM,赛默飞世尔科技(中国)有限公司)观察沉淀产物颗粒形态。使用ESCALAB 250Xi X射线 光 电 子能 谱 (X-ray Photoelectron Spectroscopy,XPS,赛默飞世尔科技(中国)有限公司)分析沉淀物表面元素的状态。用SmartLab X射线衍射(X-Ray Diffraction,XRD,日本理学株式会社)对内部原子和分子的组成、结构和形态进行分析。使用Nexus 410傅里叶变换红外光谱(Fourier Transform Infrared Spectroscopy,FTIR,美国尼高力仪器公司)研究固体样品的结构和官能团组成。
2 结果与讨论
2.1 阳离子还原剂(氯化亚铁)的作用
高铁酸钾对TP、DTP和SOP的去除率如图1所示。相同pH值时,在Fe2+存在的情况下,3种形式磷的去除率均高于单独使用高铁酸钾的去除率。当pH值范围为5.2~8.2时,添加还原剂Fe2+可显著提高含磷污染物的去除率,而在pH=7、Fe6+∶Fe2+=1∶1.5的条件下,可使TP的去除率提高约37%,DTP和SOP的去除率分别提高约13%和14%。式(1)和(2)[17]分别说明了高铁酸钾还原和Fe2+氧化以及随后与磷酸盐沉淀的反应机理。
除磷过程中,每去除一单位磷消耗1.5单位的含Fe2+混凝剂和1单位的高铁酸钾混凝剂。并且在高铁酸钾还原过程中,一些低价磷可能被氧化成正磷酸盐,以磷酸盐沉淀的形式进一步去除。此外,在氧化过程中,转化生成Fe3+或氢氧化铁等新的铁物种,均为有效的混凝剂[18]。混凝剂表现出较强的吸附和絮凝特性,为难溶性含磷中间体的去除提供了协同作用。
根据图1中DTP与SOP残余量对比可知,高铁酸钾的存在能够有效氧化非正磷酸盐部分的磷,且添加Fe2+实验组与单独使用高铁酸钾实验组相比,更有效地降低了DTP和SOP的残余量。在实验过程中观察到,与高铁酸钾/Fe2+组合相比,单独使用高铁酸钾时,形成的絮体更松散,沉淀性能较差。这一现象表明Fe2+和高铁酸钾组合在吸附沉淀能力方面具有优势。此外,Fe2+被高铁酸钾氧化形成原位Fe3+,与传统Fe3+相比,其与磷具有更强的结合力[13]。KRALCHEVSKA等[19]发现原位形成纳米颗粒的情况下,在吸附剂形成过程中,磷酸盐能被吸附在其表面;并且磷酸盐可以取代铁盐水解形成的部分羟基,形成碱性磷酸铁络合物,从而改变铁盐的水解路径。FYTIANOS等[20]研究表明:铁盐不仅可以在水中形成磷酸铁的沉淀,而且对P和OH-有很强的亲和力,从而可能在溶液中形成其他不溶性的络合物。因此,磷酸盐可以与铁盐反应,抑制铁盐的水解。总之,当高铁酸钾被分解时,氧化铁/羟基氧化铁纳米颗粒的形成受到磷酸盐吸附的影响,从而限制了纳米粒子的生长和随后的聚集。因此,原位生成的氧化铁/羟基氧化物纳米粒子具有更大的比表面积,显著增加了纳米粒子对磷酸盐吸附的有效面积。而Fe2+的添加可促进高铁酸钾分解形成更多原位Fe3+,进而提高处理效果。LEE等[21]报道了高铁酸钾通过双电子转移自衰变为Fe4+和H2O2,Fe4+进一步与H2O2反应生成Fe2+和O2,Fe2+被未分解的高铁酸钾氧化成Fe3+和Fe5+。基于这些机理,添加的Fe2+可以直接与高铁酸钾的部分发生氧化还原反应,形成更多的氧化性·OH和具有更高活性的Fe4+和Fe5+,从而提高了高铁酸钾对污水中非正磷酸盐的去除效果。加入的还原剂与高铁酸钾发生反应,势必会导致高铁酸钾与磷反应的量降低,但高铁酸钾自身的氧化反应速率极快,反应的速率常数在102~105mol/(L·s)范围内变化,能快速起到氧化效果,并且在高铁酸钾分解还原过程中,高铁酸钾并非直接转化为Fe3+,而是通过1电子转移、2电子转移和氧原子转移生成Fe4+和Fe5+等中间价态[22],这些价态同样具有极强的氧化性,且其反应速率比高铁酸钾高2~3个数量级[23]。由于高铁酸钾、Fe5+、Fe4+三者的快速氧化效果,故还原剂的投加所导致的高铁酸钾氧化磷作用减弱这一问题不会产生主导性影响。另外,水中的磷最终以沉淀的形式去除,这一结果是基于两种过程产生的:(1)非正磷酸盐氧化后形成的磷酸根离子与高铁酸钾还原后产生的Fe3+结合;(2)高铁酸钾还原产生的Fe3+进一步水解形成具有网状结构的水解产物,压缩电中和胶体杂质扩散层进行絮凝。还原剂的主要作用是促进高铁酸钾分解,生成更多具有吸附或共沉淀能力的铁氧化物,促进这两种过程,进而减少高铁酸钾的使用量,降低成本。
由图1可看出,当高铁酸钾与Fe2+质量比为1∶2和1∶1.5时,能获得最佳的磷去除效果。但质量比为1∶2时,最佳除磷效果的取得是在pH=8.2条件下,这一条件要求对水质的pH值进行调整,增加了水处理成本。质量比为1∶1.5时,在pH值为5.2~8.2较宽范围内均能取得较高的磷去除率,更贴近实际应用。故在中性pH值时,高铁酸钾与Fe2+质量比为1∶1.5为最佳投药条件。
高铁酸钾、Fe3+和高铁酸钾/Fe2+对TP的去除率如图2所示。高铁酸钾、高铁酸钾/Fe2+和Fe3+均对磷有一定的去除效果。在相同总铁投加量(300μmol/L)条件下,TP的去除效率:高铁酸钾/Fe2+>高铁酸钾>Fe3+。在高铁酸钾/Fe2+组合的情况下,每摩尔铁可处理12.4 mg/L的磷;在单独使用高铁酸钾的条件下,每摩尔铁可处理11.5 mg/L的磷;单独使用Fe3+时,每摩尔铁可处理11 mg/L的磷。显然,Fe2+的加入不仅降低了高铁酸钾的量,而且提高了高铁酸钾对TP的去除效率。这是因为Fe2+增加了溶液中新生成的Fe3+的量,从而增强了对磷酸盐的吸附和络合能力。

图2 300μmol/L的Fe条件下高铁酸钾/Fe3+和高铁酸钾/Fe2+分别对TP的去除率图
2.2 阳离子还原剂(氯化铁)的作用
为了验证Fe3+可作为高铁酸钾的还原剂使用,研究Fe3+对高铁酸钾自分解过程的影响。向pH值为10±0.05的100 mg/L的高铁酸钾溶液中分别投加不同量的Fe3+。高铁酸钾分解趋势如图3所示。Fe3+的加入可以促进高铁酸钾分解,且Fe3+增加能明显提升高铁酸钾分解速率。这一现象证明了Fe3+对于高铁酸钾在溶液中的自分解具有催化作用。这是由于Fe3+可以通过增加高铁酸钾分解的一阶非均质衰减速率常数来催化高铁酸钾的分解[24]。故Fe3+可以作为高铁酸钾的还原剂参与反应。
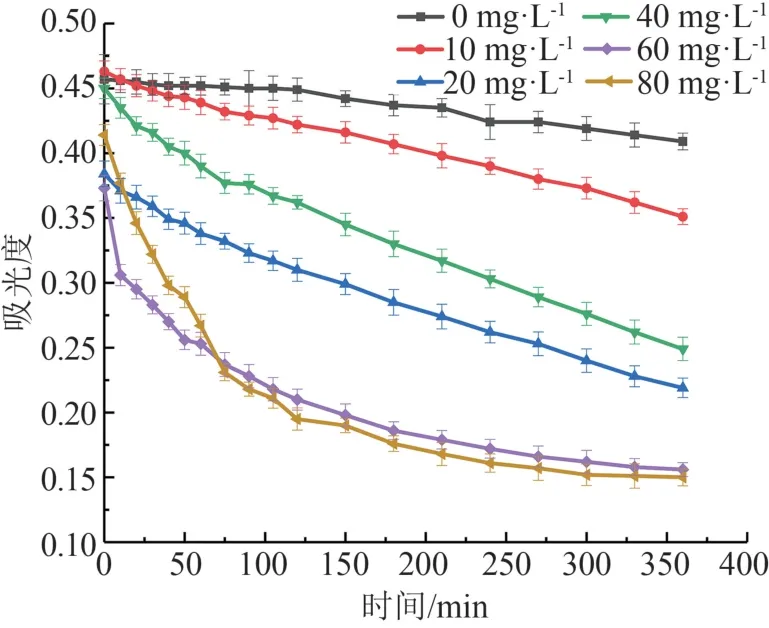
图3 Fe3+质量浓度对高铁酸钾分解的影响图
为了研究铁离子的诱导作用,采用常规混凝剂FeCl3进行了实验。与Fe2+的实验相似,在高铁酸钾用量不变的情况下,通过改变质量比和控制Fe3+的质量浓度进行Fe3+诱导高铁酸钾实验。高铁酸钾对TP、DTP和SOP的去除率如图4所示。
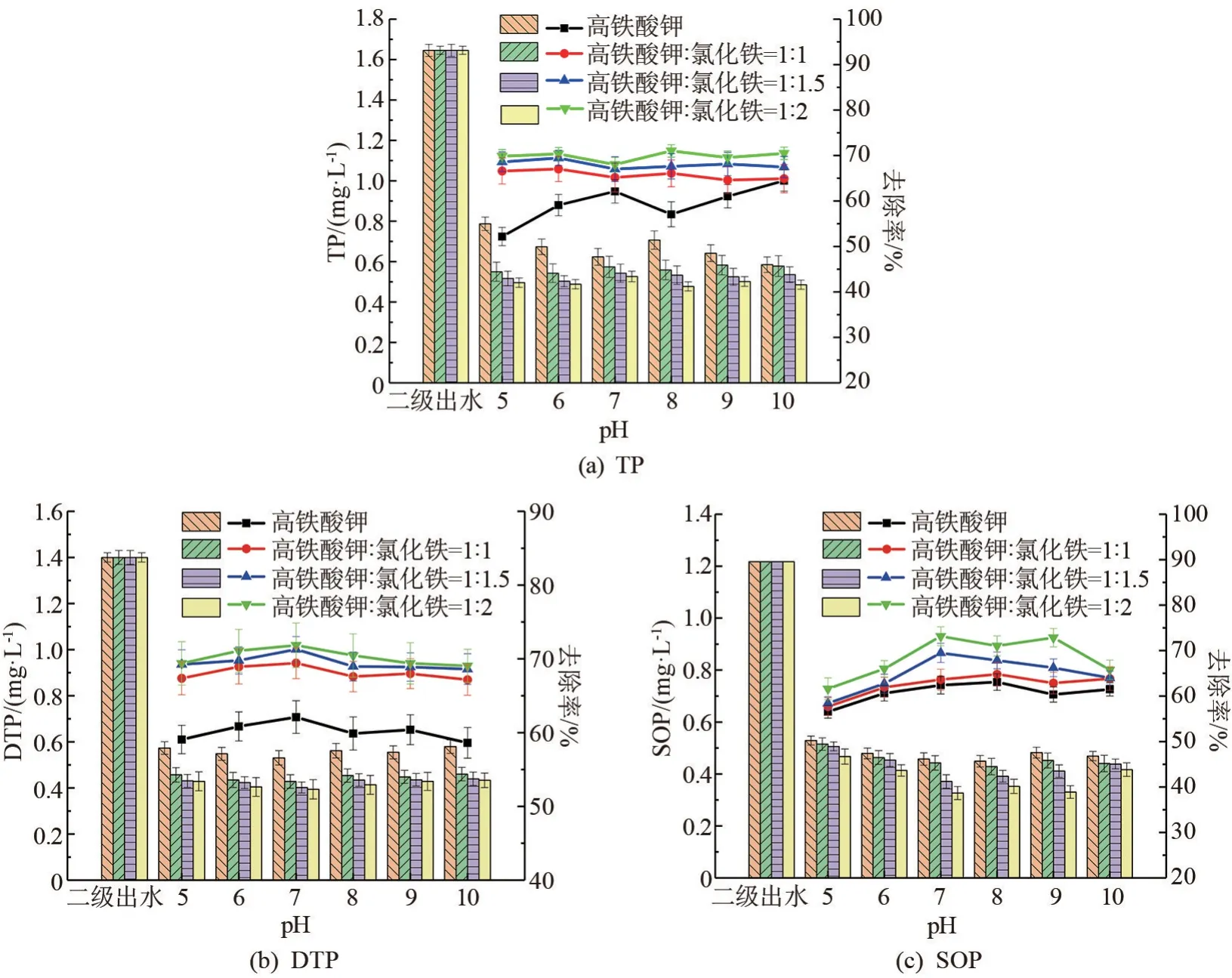
图4 不同高铁酸钾/Fe3+质量比条件下高铁酸钾对TP、DTP和SOP的去除率图
磷的去除率随Fe3+/高铁酸钾质量比和pH值的变化而变化,而TP、DTP、SOP的去除率随Fe3+投加量的增加而提高。Fe3+/高铁酸钾组合的最大TP去除效率最高为75%,低于使用Fe2+/高铁酸钾组(>90%),但在相同条件下高于单独使用高铁酸钾实验组。这可能是因为:(1)氯化铁的加入增加了总铁物种的质量浓度,从而增强了磷的吸附和络合作用;(2)Fe3+本身可以催化高铁酸钾的自分解,进一步加速反应速率[25]。DTP、SOP均在pH=7处取得最高去除效果,这是因为在高pH值环境下,OH-同P竞争与Fe3+结合的机会,通过磷酸铁化学沉淀手段去除的磷减少,且碱性环境高铁酸根离子氧化性减弱,对非正磷酸盐氧化效果降低,从而使除磷效果下降。而在低pH值环境时,氢氧化铁的形成受到限制,导致絮凝作用的减弱。
2.3 阴离子还原剂(碘化钾)的作用
高铁酸钾对TP、DTP和SOP的去除率如图5所示。I-的加入并未产生预期的强化高铁酸钾除磷效果。在相同条件下,磷的去除率均低于单独使用高铁酸钾实验组的去除率。较低的去除效率表明I-不是一种有效的高铁酸钾诱导还原剂。这可能是由于I-消耗了部分本应用于去除污染物的氧化剂(高铁酸钾、高铁酸钾分解中间产物Fe4+和Fe5+)。同时,I-作为一种共存的竞争性阴离子,可以减弱Fe3+的吸附效应。此外,由于I-没有像Fe3+那样增加溶液中的总铁,所以I-的投加未能有效地促进吸附和絮凝效果。因此,I-/高铁酸钾比Fe2+/高铁酸钾、Fe3+/高铁酸钾去除TP的效果要差。
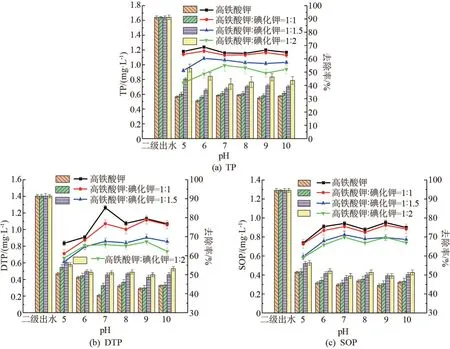
图5 不同高铁酸钾/I-质量比条件下高铁酸钾对TP、DTP和SOP的去除率图
2.4 沉淀物表征
Fe2+和高铁酸钾联用实验后产生的沉淀产物(高铁酸钾与Fe2+的质量比为1∶1.5,下同)的SEM结果如图6所示。沉淀产物的粒径大小、形态结构各异。实验所用原水为中水站二沉池出水,水质复杂且污染物种类繁多,导致了析出物的形态和结构的多样性。从放大图中可以看到大量球形纳米颗粒,与2.1节中推测高铁酸钾还原形成的原位Fe3+纳米颗粒相对应。

图6 沉淀物的SEM图
对处理后生成的沉淀产物进行XPS分析,如图7所示。沉淀物中的主要元素是铁、氧和磷。图7(b)为反应沉淀中磷的XPS高分辨谱,表示磷元素的存在状态。其中,P峰主要由两个峰组成(133.06 eV和133.84 eV),分别对应P和P,均为磷元素的最高价态+5价,P 2p3/2的结合能为132.28 eV,表明其以P的形式存在于沉淀产物中[26]。窄扫描光谱的O 1s(如图7(c)所示)由4个峰(530.75、531.54、532.12和532.67 eV)组成,分别代表氧以O2-、—OH(羟基)、H2O和P—O形式存在[27]。从占比可知,沉淀产物中主要以氢氧化物和磷酸盐沉淀为主,且O 1s为531.48 eV的结合能对应于P。图7(d)中Fe 2p1/2、2p3/2的结合能分别为724.78和711.38 eV,表明铁以Fe3+状态在沉淀中占主导地位。磷、氧、铁的存在价态及存在形式进一步证实了高铁酸钾对磷的去除机理:通过将各种价态磷氧化为+5价再与Fe3+结合生成磷酸铁沉淀,以及高铁酸钾被还原后产生的氢氧化铁吸附两种主要过程进行去除。
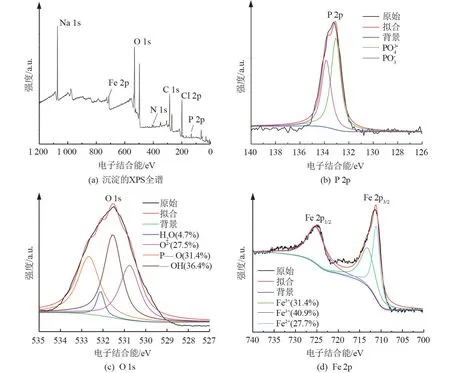
图7 沉淀物的XPS谱图
去除污染物后的沉淀产物的FTIR谱图如图8所示。图中,分别在1 047.40、1 384.27、1 635.05、3 426.12 cm-1处出现了明显的吸收峰,并且在2 852.44和2 922.24 cm-1处出现了肩峰。很显然,在3 426.12 cm-1处出现的特征吸收峰可归因于O—H的伸缩振动[26],说明沉淀物中含有少量H2O和其他含羟基结构的化合物。约在1 384 cm-1处出现P—O—H的特征吸收峰,说明沉淀物中存在磷,证明其得到了去除。在1 047 cm-1处出现的峰位与溶解性磷酸盐的峰位不同[28],显示了一些峰位的移动,可能是因为磷酸盐与羟基氧化铁发生了络合作用。在900 cm-1处为P的对称性伸缩振动吸收峰,在725 cm-1和549 cm-1处为P的非对称弯曲振动吸收峰[29],522 cm-1处还存在(P)—O—H的振动吸收峰[30],在870 cm-1处出现了一个肩峰,可能是PO中的P—O(H)键的振动峰。由结果可知,利用Fe2+协同高铁酸钾去除磷的过程中,低价态的磷被氧化为P5+,以P的形式与Fe3+结合形成磷酸铁沉淀。
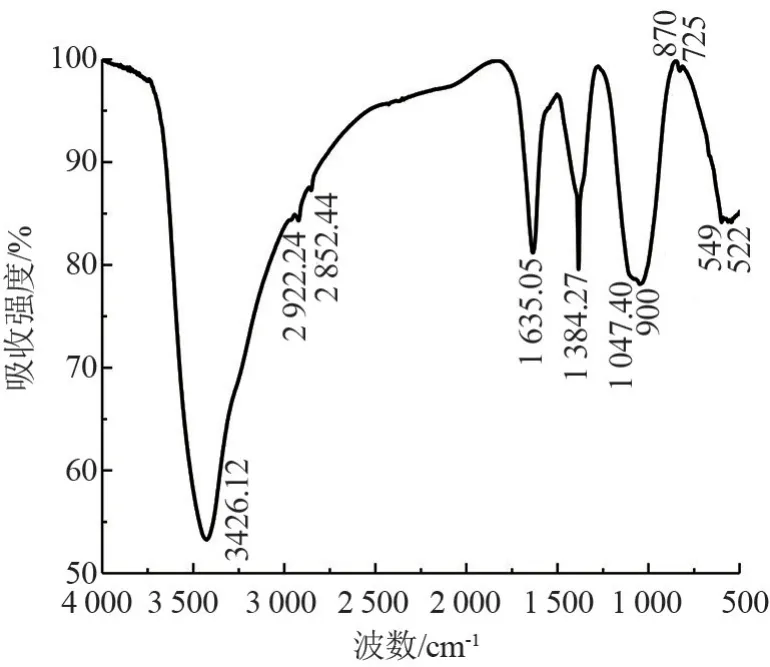
图8 沉淀物的FTIR谱图
Fe2+与高铁酸钾联用处理后所得沉淀物的XRD谱图如图9所示。根据JCPDS衍射卡中序号30-0659的标准图谱,图9中在2θ为20.72°、35.17°和45.42°位置的峰可归属为沉淀中磷酸铁的特征峰,说明原水中不同价态的磷大多被氧化为P5+(P),然后与高铁酸钾分解产生的Fe3+反应,形成磷酸铁沉淀。其中,峰位出现部分轻微偏移,分析可能是由于试验所用原水为中水,含有的杂质类型较多且复杂,在絮凝沉淀过程中包裹在沉淀物表面,进而引起峰位偏移。根据JCPDS 08-0155显示,2θ为21.53°、29.77°和31.05°处的特征衍射峰为含磷复合物,而根据JCPDS衍射卡中的序号22-0283,2θ为27.33°和29.74°处的峰表明实验中形成了一些复杂的含磷难降解配合物,如Fe2.5PO4(OH)4.5和Fe1.6H2PO4(OH)3.8[20]。这些络合物在沉淀阶段,相互吸附形成较大的网状结构,通过网捕卷扫作用,将部分杂质去除。此外,Fe2+与高铁酸钾反应,加速了从Fe6+向Fe4+和Fe5+转移,其反应速率比Fe6+高2~3个数量级,使高铁酸钾氧化效果得到强化。因此,在这个复杂的过程中,可能会发生单电子、双电子或三电子的转移,导致不同价态的铁中间体的混合物生成。这些配合物在絮凝阶段可进行网捕卷扫、吸附和电子中和,因此,最终改善污染物的去除,特别是含磷物种的去除。

图9 沉淀物的XRD谱图
3 结论
通过研究可以得到以下结论:
(1)还原剂Fe2+的加入诱导强化高铁酸钾去除二级出水中90%的TP,Fe2+与高铁酸钾的氧化还原反应促使原位Fe3+及Fe3+产物的增加,而Fe3+又能快速反应生成Fe(OH)3胶体,通过网捕卷扫和吸附电中和等手段,进一步去除复杂难溶性中间产物,使磷物种的去除率得到提高。Fe2+的加入既辅助增强了氧化效果,又强化了絮凝效果,同时提高了高铁酸钾的经济可行性,降低了成本。
(2)与Fe2+相比,I-的加入不能增强磷的絮凝和吸附,反而由于竞争氧化性导致磷的去除率较低,约为60%。
(3)沉淀中的磷大部分以磷酸铁的形式存在,Fe2+的存在促进了高铁酸钾对磷的去除。在反应过程中,高铁酸钾将不同价态磷氧化为P5+,生成P,与高铁酸钾分解产物反应生成磷酸铁沉淀。
