测定直接胆红素方法的分析
2010-07-30唐礼新邱春红
唐礼新 邱春红
胆红素是血红素的代谢产物,主要在肝脏内经结合作用转化排泄,它在血清中以未结合胆红素(即游离胆红素)、结合胆红素(即单葡萄糖醛酸和双葡萄糖醛酸胆红素之和)及δ-胆红素(清蛋白共价连接胆红素) 3种形式存在。临床上测定血清胆红素是黄疸性疾病诊断与鉴别诊断的重要指标,对了解疾病的发展、转归有重要意义[1-3]。本文对Siemens Healthcare Diagnostics inc.生产的试剂盒进行评价和探讨,现报道如下。
1 材料与方法
1.1 仪器
Dimension RXL全自动生化分析仪。
1.2 试剂
试剂盒由Siemens Healthcare Diagnostics inc.生产;试剂Ⅰ成分:0.5%亚硝酸钠、0.5mol/L盐酸;试剂Ⅱ成分:0.45%对氨基苯磺酸、1.09%盐酸。
1.3 原理
重氮化对氨基苯磺酸是通过亚硝酸钠和对氨基苯磺酸在低pH的环境中结合而生成的。用0.05mol/L的HCL稀释样本。先记下空白读数以消除非胆红素色素的干扰。加入重氮化对氨基苯磺酸,结合的胆红素会转化成重氮基胆红素。
1.4 方法
主要分析参数设置测定方法:主波长540nm,副波长700nm,样品体积31μL,试剂体积R1为30μL,R2为60μL,读取终点ΔA。试验过程全部由Dimension RXL全自动生化分析仪完成。
2 结 果
2.1 精密度
按美国临床实验室标准化委员会(NCCLS)评价方案,取低、中、高3个不同浓度的DBIL样品上、下午双份测定,连续测20d,再每天测1次,共测20d,结果见表1。
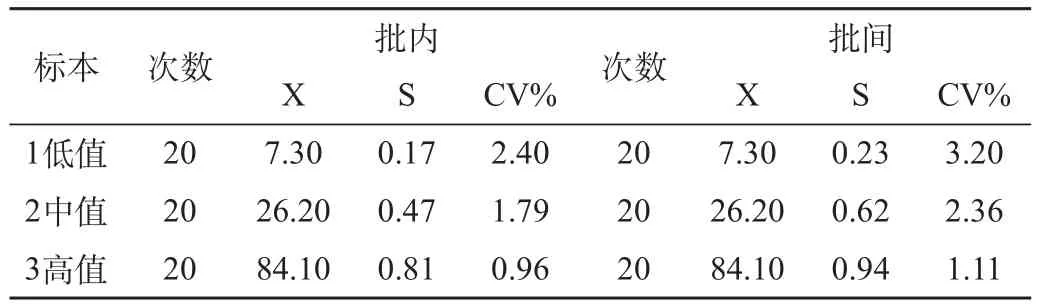
表1 批内和批间精密度测定结果(μmol/L)
2.2 线性和回归分析[2]
按NCCLS的评价方案,选择低浓度(31.4μmol/L)和高浓度(360.0μmol/L)的混合血清2份,然后把这2份样品等量混匀产生中间值,再分别将中间值和低值、中间值和高值等量混匀,共产生5个不同值的样品。在Dimension RXL全自动分析仪上用本法从低值到高值,然后从高值到低值测定,求得均值为Y,以理论值为X进行回归分析,回归方程为:Y=0.9914X+0.075,r=0.9998。结果表明DBIL在350μmol/L内仍保持良好的相关性。
2.3 回收试验
取1份DBIL含量为6.4μmol/L的血清0.8mL,加入DBIL含量为56.3μmol/L的血清0.2mL,计算浓度。结果测定浓度为16.32和16.98μmol/L,回收率为104.10%。
2.4 干扰试验
2.4.1 血红蛋白干扰试验
取1份新鲜混合血清(DBIL为26.6μmol/L)分别加入不同浓度的血红蛋白,用本法测定DBIL。结果血红蛋白<3.2g/L时,对测定结果无显著干扰,但当血红蛋白浓度≥5g/L时,测定值出现负数,表明血红蛋白浓度≥5g/L时,严重干扰DBIL的测定。
2.4.2 脂血干扰试验
取1份新鲜混合血清(DBIL为26.6μmol/L)分别加入不同浓度的脂肪乳,用本法测定DBIL。结果三酰甘油<8mmol/L时对测定结果无显著干扰。
2.4.3 抗坏血酸干扰试验
取1份新鲜混合血清(DBIL为6.6μmol/L)分别加入不同浓度的抗坏血酸,用本法测定DBIL。结果抗坏血酸<1.5g/L时对测定结果无显著干扰。
2.5 方法学比较
选择含量在5~350μmol/L的临床标本80份测定DBIL,按NC-CLS(EP9-P)的评价方案作方法学比较,结果见表2。
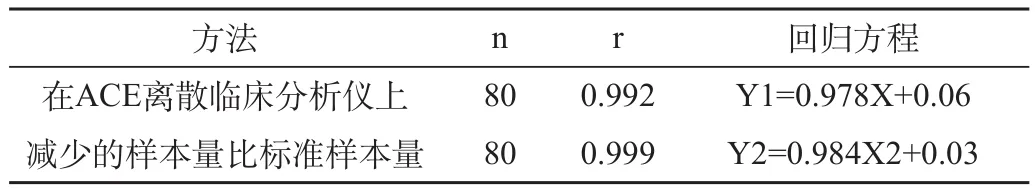
表2 两种方法测定DBIL的相关性比较
3 讨 论
目前如何准确可靠地测定血清胆红素是大家一致关注的问题,由于胆红素极易氧化,导致标准品制备困难,即使各厂家试剂配方相同,但由于校准液的问题,测定结果之间差异也较大。如果统一使用由Doumas等[4]提出的采用二牛磺酸胆红素作为DBIL测定的校准物,各种方法测定结果会得到很大改善,这与文献报道相一致[5]。本研究使用的测定试剂,经实验证明其稳定性好、抗干扰能力强,准确度和精密度良好,测定线性满足临床要求,值得推广应用。
[1]叶应妩,王毓三,申子瑜.全国临床检验操作规程[M].3版.南京:东南大学出版社,2006:452.
[2]杨昌国,许叶,张抗.线性评价和干扰试验中NCCLS评价方案的应用[J].临床检验杂志,1999,17(3):184.
[3]韩志钧.临床化学常用项目自动分析法[M].沈阳:辽宁科学技术出版社,2005:1066.
[4]Doumas BT,Perry BW,Sasse EA,et al.Standardization in billirubin assays; Evaluations of selected methods and stability of bilirubin solutions[J].Clin Chem,1973,19(9):984-993.
[5]Young DS.Effects of Preanalytical Variables on Clinical Laboratory Tests[M].3rd ed. Washington,DC:AACC Press,2007:175.
