掺Fe3+A-TiO2粉末的水热法制备及其光催化降解甲基橙
2010-07-13张一兵郑敏蒋荣彬江雷
张一兵,郑敏,蒋荣彬,江雷
1.上饶师范学院,江西 上饶 334001;2.中科院化学研究所,北京 100080
甲基橙广泛应用于生产和科学实验中,常用作酸碱指示剂和生物染色。由于应用广泛,对环境造成一定污染。利用光催化技术降解有机污染物受到人们的日益重视,它处理有机染料废水的氧化能力强、无二次污染、设备简单、操作条件容易控制。
TiO2是良好的光催化剂,它存在三种晶型:金红石型、锐钛矿型和板钛矿型,其中以锐钛矿型的TiO2拥有最好的光催化活性。因为锐钛型 TiO2容易转化为最稳定的金红石型,所以工业上有效合成单一的锐钛型TiO2的技术至关重要,制备高产量、纯净的锐钛型 TiO2的工作困难。TiO2半导体光催化剂,以其活性高、稳定、无毒、价廉的特点,能将环境污染物完全降解为CO2和H2O,且不造成二次污染,而得到广泛研究[1-2]。其主要原理是利用TiO2受光激发产生的高活性电子空穴对附着在表面的H2O、O2等氧化为·OH、H2O2、O2-等强氧化剂而将污染物氧化降解[3]。然而由于TiO2只能被波长等于或小于387 nm的光所激发,而这部分光只占太阳光的小部分(小于5%),因此不能充分利用太阳光[2]。如何使TiO2利用可见光进行光催化是人们热切期盼的,为此人们积极从事这方面研究[4-7]。Zhu等人[8]研究发现,以水热法制备TiO2能将金属离子深度而均匀地掺入TiO2中,这样能有效地利用可见光,提高TiO2催化活性。研究表明,金属离子掺杂有望在TiO2表面上引入缺陷结构,成为电子或空穴的捕获阱并延长·OH的寿命从而可有效提高光催化效率。Choi等[9]系统报道了21种金属离子对TiO2的掺杂效果,其中以Fe(Ⅲ)掺杂为最佳。目前,掺铁TiO2纳米材料的制备方法主要有化学沉淀法、溶胶-凝胶法及水热法等。
本文以硫酸钛为原料,在加入添加剂的关键技术下,通过优化反应条件(时间、质量浓度及添加剂用量等),用水热法简易地制备了的掺Fe3+A-TiO2粉末,并研究了以它为光催化剂对甲基橙溶液进行降解的最佳条件。
1 实验部分
1.1 主要试剂与仪器
Ti(SO4)2固体和 FeCl3固体(AR,SCRC国药集团化学试剂有限公司),BaCl2及无水乙醇(AR,北京化工厂);X-射线衍射(XRD):Dmax/2500,Rigaku,Japan;电子显微扫描仪(SEM):Jeol,JMS-6700F;透射电镜 TEM(TEM):Jeol,JMS-100CXⅡ;高压反应釜(内衬聚四氟乙烯内杯,240℃,RD-100型,中国石油化工科学研究院);WFH-203三用紫外分析仪(上海精科实业有限公司),UV-1201单光束紫外可见分光光度计(北京瑞利分析仪器公司)。实验中各种化学试剂均为分析纯。
1.2 掺Fe3+A-TiO2粉末的制备
在一定量的Ti(SO4)2固体中加入蒸馏水形成溶液后,慢慢加入一定量的添加剂及不同量(物质的量的比)的FeCl3固体,磁力搅拌下形成0.15 mol·L-1的Ti(SO4)2溶液,溶液稍静置后倒入100 mL不锈钢(内杯为聚四氟乙烯)的洁净的高压釜,溶液的最大体积不超过高压釜体积的75%,烘箱从环境温度开始升温到达170 ℃后加热反应4 h,反应完毕切断电源使烘箱自然降温,冷却至室温后取出玻璃基板,经去离子水洗(以 BaCl2溶液检验 SO42-的存在)、无水乙醇洗后,自然干燥后对产物进行表征,用X-射线衍射进行产物的晶相分析;产物的形貌用电子显微扫描仪SEM和透射电镜TEM观察。
1.3 光催化降解甲基橙的方法
配置一定质量浓度的甲基橙溶液250 mL,取少量溶液测定其吸光度A0,于母液中加入一定量自制的A-TiO2粉末,置于暗箱中,光照下,调节恒温磁力搅拌器快速搅拌后,开始反应,同时记录时间。进行多组平行实验,每隔一段时间取出少量的溶液,测剩余甲基橙的吸光度At。因为吸光度与甲基橙的质量浓度成正比,所以催化降解率的计算按下面的公式:

其中A0正比于甲基橙的初始质量浓度,At正比于降解t时间后剩余甲基橙的质量浓度。
2 结果与讨论
2.1 XRD与SEM分析
图1a表示了170 ℃下反应4 h所得产物粉末的XRD图,从中发现,存在25.41°、38.01°、48.01°、54.71°、63.11°的吸收峰,这是锐钛矿型TiO2晶体的特征峰,其中(101)峰最强,说明本工作合成的掺Fe3+TiO2为锐钛矿型。分析图1a可知,除了(101)吸收峰最强外,还存在较弱的(004)、(200)、(105)、(211)和(204)吸收峰,这些都符合钛矿型TiO2晶体标准XRD图。图1b和1c是TiO2粉末的SEM图和TEM图。从二图可以发现,产物粉末是由生成的掺Fe3+TiO2微米球形成的,球径约2~3 μm,它由TiO2纳米晶体自组装而成。TiO2纳米晶体呈现八面体结构,平整的三角形表面边长约100~200 nm,晶体长约1~1.5 μm。
2.2 甲基橙溶液最大吸收波长的确定
配制10 mg·L-1的甲基橙溶液。以蒸馏水作为参比溶液,在不同的波长λ下,测其吸光度A0,结果表1。从表1中可以看出,溶液的最大吸收波长为465 nm,此时的吸光度为 0.795。在本实验中,测定甲基橙的吸光度时均将波长定为465 nm。
2.3 锐钛矿型TiO2光催化最佳条件的确定
2.3.1 光源对光催化降解甲基橙的影响
向3份质量浓度均为10 mg·L-1的甲基橙溶液中各加0.0500 g掺Fe3+5%的A-TiO2,18 ℃下分别在可见光(40 W白炽灯)和波长分别为254 nm、365 nm的紫外光源下进行光照降解。反应4 h后,结果见表2。从表2可以发现,用波长365 nm的紫外光光催化降解甲基橙溶液的效果比用可见光和波长为254 nm的紫外光光催化降解甲基橙的效果要好。这是因为在紫外光照下是由光子激发引起 TiO2价带上电子跃迁的,因此使用能量与TiO2禁带宽度相近的365 nm的紫外光照射效果最佳。所以,本实验选用的光源是波长为365 nm的紫外光。

表1 甲基橙的不同波长的吸光度Table 1 Absorbances of methyl orange under different wave length

表2 光源对光催化降解甲基橙的影响Table 2 Degeneration of methyl orange affected by light sources
2.3.2 A-TiO2掺 Fe3+量不同对光催化降解甲基橙的影响
取5份10 mg·L-1甲基橙溶液各50 mL,各加入0%、2%、5%、8%、10%(物质的量的比)的掺Fe3+A-TiO20.0500 g,365 nm的紫外光照下,18 ℃下反应4 h后检测剩余甲基橙质量浓度,结果见表3。从表3看出,掺Fe3+的TiO2对甲基橙的降解率比不掺Fe3+的降解率更高,甲基橙的降解率随着掺Fe3+量的增加而先增后减,当掺Fe3+5%时降解率最大(57.8%)。掺Fe3+有助于提高TiO2的催化性能,这可能因为:Fe3+是电子的有效接受体,减少了光生电子-空穴对的复合,使电子-空穴对得到有效分离,从而使 TiO2表面产生更多的·OH自由基,提高甲基橙的降解率[10]。掺Fe3+量低于5%时,不能使电子-空穴对得到有效分离,使得TiO2表面产生的·OH自由基较少,降解率低。高于 5%会导致金属离子成为电子和空穴的复合中心,从而降低了TiO2的催化性能,掺杂质量浓度过大会使空穴和电子向表面的迁移中遇到更多的捕获,从而降低了量子效率。因此,本实验选择的TiO2最佳掺Fe3+量为5%。

图1 所得掺Fe3+A-TiO2粉末的XRD图(a)、SEM图(b)和TEM图(c)Fig.1 XRD patterns(a) and SEM image(b)and TEM) imange(c) of as-prepared TiO2 powders
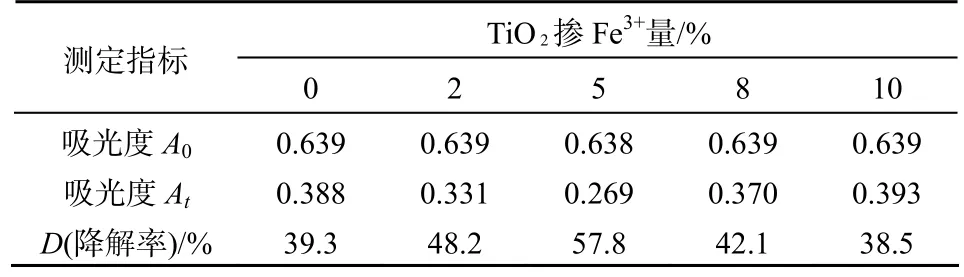
表3 TiO2掺Fe3+量不同对光催化降解甲基橙的影响Table 3 Degeneration of methyl orange affected by the different amount of Fe3+-doped TiO2
2.3.3 TiO2用量对光催化降解甲基橙的影响
取50 mL、10 mg·L-1甲基橙溶液6份,各加入0.0300 g、0.0500 g、0.0700 g和 0.0900 g掺 Fe3+5%A-TiO2,18 ℃下365 nm光照反应4 h后检测剩余甲基橙质量浓度,结果见表4。表4表明,随着TiO2量的增加甲基橙的降解率逐渐增大,当 TiO2达0.0500 g时,甲基橙的降解率最大(57.8%),继续增加TiO2的量,甲基橙的降解率又减小。原因可能是当TiO2用量较小时,光源产生的光子不能被完全转化为化学能,使得光子没有被充分利用,降解率降低;适当的TiO2用量可增加反应物与催化剂的接触面积,产生较多的活性自由基而提高降解效率;而添加量过多会造成较强的光散射,增大电子一空穴的复合几率,催化效果反而降低;因此,不同的反应物体系存在着最佳投加量[11]。本实验选择掺Fe3+5%的TiO2用量为0.0500 g。

表4 掺Fe3+5%的TiO2用量对光催化降解甲基橙的影响Table 4 Degeneration of methyl orange affected by the the mass of TiO2
2.3.4 光照时间对光催化降解甲基橙的影响
在50 mL、10 mg·L-1甲基橙溶液中加0.0500 g掺Fe3+5%A-Ti02,18 ℃下365 nm光照反应,每隔1 h测试溶液中甲基橙质量浓度,结果见表5。分析表5可以发现,随着光照时间的增长甲基橙的降解率增大,光照4 h时甲基橙的降解率最大(57.8%)。继续增加反应时间,甲基橙的降解率反而降低。这可能是:反应开始时甲基橙降解不完全降解率较低,延长反应时间降解率增大,当时间过长时甲基橙降解形成的自由基有足够的时间再结合形成甲基橙或者形成吸光度较大的物质,反而使降解率减小。本实验选择的最佳光照时间为4 h。

表5 反应时间对催化降解甲基橙的影响Table 5 Degeneration of methyl orange affected by reaction time
2.3.5 甲基橙初始质量浓度对光催化降解甲基橙的影响
分取 5、7、10、12、14 mg·L-1的甲基橙溶液各50 mL,各加掺Fe3+5% A-TiO20.0500 g,18 ℃下365 nm紫外光照反应4 h,每隔一定时间取出反应溶液测定吸光度,结果得表6。分析表6可知,随着甲基橙质量浓度的增加降解率逐渐增大,当质量浓度达到 10 mg·L-1时,甲基橙降解率达最大(51.4%),继续增加甲基橙质量浓度,其降解率反而降低。原因可能是:当甲基橙初始质量浓度较低时,降解绝对量占居主导地位,故在较低质量浓度时,随质量浓度的增加,甲基橙的降解率升高。但当甲基橙初始质量浓度达到一定值时,甲基橙自身质量浓度占主导地位,降解的绝对量虽然增大,但是降解率反而下降[12]。所以本实验选择甲基橙溶液的最佳质量浓度为10 mg·L-1。

表6 甲基橙初始质量浓度对降解甲基橙的影响Table 6 Degeneration of methyl orange affected by its initial concentration
3 结论
(1)以Ti(SO4)2溶液为主要材料,在加入添加剂的关键技术下,通过优化反应条件用水热法简易地制备了掺Fe3+TiO2纳米材料,XRD表征其为锐钛矿型TiO2,即掺Fe3+A-TiO2;
(2)SEM和TEM表征结果说明,产物粉末是由生成的掺 Fe3+A-TiO2微米球形成的,球径约 2~3 μm,它由 TiO2纳米晶体自组装而成。TiO2纳米晶体呈现八面体结构,平整的三角形表面边长约100~200 nm,晶体长约1~1.5 μm;
(3)水热法制备掺Fe3+A-TiO2的优化条件是:在0.15 mol·L-1Ti(SO4)2水溶液加入适量的添加剂FeCl3固体于170 ℃恒温反应4 h;
(4)优化了以自制的掺 Fe3+A-TiO2光催化甲基橙溶液的条件:甲基橙溶液的初始质量浓度 10 mg·L-1、掺 Fe3+5%(物质的量比)A-TiO2投放量0.0500 g、18 ℃下365 nm紫外光照射反应4 h,甲基橙降解率达到57.8%。
[1]XIE Yibing, YUAN Chunwei.Characterization and photocatalysis of Eu3+-TiO2sol in the hydrosol reaction system[J].Materials Reseach Bulletin.2004, 39: 533 -544.
[2]甘礼华, 刘明贤, 张霄英, 等.掺铁TiO2-活性炭复合材料的制备及其光催化活性[J].同济大学学报: 自然科学版, 2008, 36(4): 538-542.GAN Lihua, LIU Mingxian, ZHANG Xiaoying, et al.Synthesis and photocatalytic activity of Fe-doped TiO2-activated carbon composite materials response to visible light[J].Journal of Tongji University:Natural Science, 2008, 36(4): 538-542.
[3]张万忠, 刘景民, 周智敏.纳米 TiO 的研究与应用进展[J].石油化工, 2007, 36(11): 1184-1190.ZHANG Wanzhong, LIU Jingmin, ZHOU Zhimin.Research progress in preparation and application of nano-titania[J].Petrochemical Technology, 2007, 36(11): 1184 -1190.
[4]张晓勇, 晁明举, 梁二军, 等.钒掺杂纳米TiO2薄膜的结构和光吸收性能[J].无机材料学报, 2009, 24(1): 34 -38.ZHANG Xiaoyong, CHAO Mingjv, LIANG Erjun, et al.Microstructure and photo-absorption property of V-doped nano-TiO2thin films[J].Journal of Inorganic Materials, 2009, 24(1): 34 -38.
[5]杨贞妮, 刘强, 朱忠其, 等.钒掺杂TiO2粉体的制备及性能[J].粉末冶金材料科学与工程, 2009, 14(1): 63-66.YANG Zhenni, LIU Qiang, ZHU Zhongqi, et al.Preparation and properties of V-doped TiO2powders[J].Materials Science and Engineering of Powder Metallurgy, 2009, 14(1): 63-66.
[6]胡普查, 肖举强, 展宗城, 等.纳米掺氮 TiO2可见光降解环境内分泌干扰物BPA研究[J].环境科学与技术, 2009, 32(3): 46-49.HU Pucha, XIAO Juqiang, ZHANG Zoncheng, et al.Visible light degradation of bisphenol A in water using N-doped TiO2nano-powder[J].Environmental Science & Technology, 2009, 32(3):46-49.
[7]周文芳, 朱忠其, 张瑾,等.微波化学法合成可见光响应氮掺杂纳TiO2光催化剂[J].功能材料, 2009, 2(40): 212-215.ZHOU Wenfang, ZHU Zhongqi, ZHANG Jin, et al.Visble-light-induced nitrogen-doped TiO2nanocrystal photocatalysts synthesized by microwave chemical method[J].Journal of Functional Materials,2009, 2(40): 212-215.
[8]ZHU Jiefang, ZHENG Wei, HE Bin, et al.Characterization of Fe–TiO2photocatalysts synthesized by hydrothermal method and their photocatalytic reactivity for photodegradation of XRG dye diluted in water[J].Journal of Molecular Catalysis A:Chemical , 2004, 216(1): 35-43.
[9]CHOI W, TERMIN A, HOFFMANN M R.The role of metal iron dopants in quantnm-sized TiO2: correlation between photoreactivity and charge carrier recombination dynamics[J].Journal of Physical Chemistry, 1994, 98(51): 13669-13679.
[10]梁喜珍, 余荣清.光催化降解甲基橙的研究[J].化工时刊, 2007,21(10): 21-24.LIANG Xizhen, YU Rongqing.Study on photocatalytic degradation methyl orange[J].Chemical lndustry Times, 2007, 21(10): 21-24.
[11]刘鑫, 刘福田.V、La共掺杂对纳米TiO2光催化降解甲基橙的研究[J].陶瓷学报, 2007, 28(2): 104-107.LIU Xin, LIU Futian.Research on photo-catalytic activity of V-La codoped nano-TiO2for methyl orange degradation[J].Journal of Ceramics, 2007, 28(2): 104-107.
[12]王敏, 王里奥, 张文杰, 等.FeVO4光催化剂降解甲基橙研究[J].功能材料, 2009, 40(2): 201-203.WANG Min, WANG Li’ao, ZHANG Wenjie, et al.Photocatalytic degradation of methyl orange using FeVO4photocatalyst[J].Journal of Functional Materials, 2009, 40(2): 201-203.
