正交试验优选清肝利胆胶囊醇提工艺
2010-05-22澜兰艾则孜帕依曼亥米提于宁新疆医科大学第一附属医院药剂科乌鲁木齐市830054新疆维吾尔自治区药物研究所乌鲁木齐市830004
澜兰·艾则孜,帕依曼·亥米提,于宁(1.新疆医科大学第一附属医院药剂科,乌鲁木齐市 830054;.新疆维吾尔自治区药物研究所,乌鲁木齐市 830004)
清肝利胆胶囊是以藏医理论组方的现代藏药复方制剂,处方来源于藏药临床经验方,笔者已按中药、天然药物6(2)类完成了所有临床前的研究工作,现进行临床研究工作。本品处方由川西獐芽菜、波梭瓜子、唐古特乌头、角茴香、兔耳草、苦买菜、诃子、甘草、大黄、金钱草、木香等12味药材组成,具有祛湿除黄、清肝利胆和清热解毒的功效。方中各药分别被2005年版《中国药典》(一部)、《部颁标准·藏药分册》和《藏药标准》收载。由于处方中大黄含蒽醌类有效成分[1],唐古特乌头和角茴香含有生物碱[2],兔耳草、苦买菜和川西獐芽菜含有黄酮和皂苷类[3~5],这些有效成分均有祛湿除黄、清肝利胆和清热解毒等药理作用[1~5],因此,根据各药材有效部位和有效成分的理化性质,对这8味药材选用乙醇提取。为将本方开发成可供临床使用的工艺稳定、质量可靠的现代藏药复方制剂,笔者特对该复方进行了醇提工艺研究,优选出了合理可行的提取工艺。
1 材料
1.1 仪器
Libror AEG-200型电子天平(日本岛津公司);SPD-10AVP型高效液相色谱(HPLC)仪,包括LC-10ATVP二元高压泵、SPD-10AVP紫外检测器、CTO-10ASVP柱温箱、SCL-10AVP系统控制器(日本岛津公司);BS110S型电子天平(北京赛多利斯仪器有限公司);KQ-100DE型数控超声波清洗器(昆山市超声仪器有限公司);DHG-9023A型恒温箱(扬州三发电子有限公司)。
1.2 试药
大黄素、大黄酚对照品(中国药品生物制品检定所,批号分别为0756-200110、0796-200208);甲醇为色谱纯,HPLC用水为超纯水,乙醇为药用规格,其余试剂均为分析纯。
2 方法与结果
2.1 大黄总蒽醌的含量测定[6~8]
2.1.1 色谱条件:用十八烷基硅烷键合硅胶为填充剂,色谱柱为Shimadzu VP-ODS柱(250 mm×4.6 mm,5µm),流动相为甲醇-0.1%磷酸溶液(85∶15),检测波长为254 nm,柱温为35℃,流速为1.00 mL·min-1。理论塔板数按大黄峰计算应>3000。
2.1.2 对照品溶液的制备:称取大黄素、大黄酚对照品各适量,用甲醇(色谱纯)制成含大黄素4µg·mL-1和大黄酚8µg·mL-1的对照品溶液。
2.1.3 供试品溶液的制备:称取本品约1.0 g,置于100 mL锥形瓶中,加8%盐酸20 mL,超声处理5 min,再加三氯甲烷20 mL,加热回流1 h,放冷,置分液漏斗中,用少量三氯甲烷洗涤容器,并入分液漏斗中,分取三氯甲烷层,酸液再用三氯甲烷提取2次,每次10 mL,合并三氯甲烷液,减压回收溶剂至干,残渣加适量甲醇微热使溶解,转移至50 mL量瓶中,用少量甲醇分次洗涤容器,合并洗液至同一量瓶中,并稀释至刻度,摇匀,用微孔滤膜(0.45 μm)滤过,取续滤液,即得。
2.1.4 阴性对照溶液的制备:称取按处方比例除大黄以外的其它醇提药材,按清肝利胆胶囊醇提制备工艺制成阴性样品,按“2.1.3”项下方法制成阴性对照溶液。
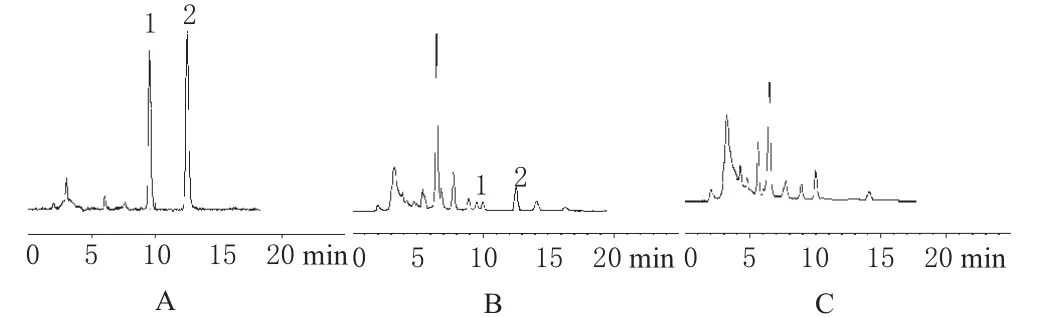
图1 高效液相色谱图A.对照品;B.供试品;C.阴性对照;1.大黄素;2.大黄酚Fig 1 HPLC chromatogramsA.reference substance;B.test sample;C.negative control;1.emodin;2.chrysophanic acid
2.1.5 系统适用性试验:取上述对照品、供试品、阴性对照溶液,照“2.1.1”项下色谱条件注入液相色谱仪。经计算,大黄素的理论塔板数 n=5.54(tR/Wh/2)2=12971,分离度 R=2(tR2-tR1)/(W1+W2)=1.65,拖尾因子fs=W0.05h/2d1=0.97;大黄酚的理论塔板数 n=5.54(tR/Wh/2)2=13103,分离度 R=2(tR2-tR1)/(W1+W2)=6.31,拖尾因子fs=W0.05h/2d1=0.96,均符合2005年版《中国药典》的规定。在供试品的色谱图中,对照品峰位与阴性对照没有峰重叠,说明该法专属性良好。色谱见图1。2.1.6 线性关系考察:称取大黄素、大黄酚对照品适量,加甲醇(色谱纯)分别制成每1 mL含大黄素7.68µg和含大黄酚102µg的贮备溶液。分别精密量取上述大黄素对照品溶液2.5、5、7.5、10、12.5 mL,大黄酚对照品溶液0.5、1、2、3、4 mL,置25 mL量瓶中,加甲醇至刻度,摇匀,即得。分别精密吸取上述溶液10 μL,注入液相色谱仪,记录峰面积。以进样浓度(C,μg·mL-1)为横坐标,峰面积积分值(A)为纵坐标,进行线性回归,得大黄素回归方程为A=33319C+1536.1(r=0.9996),大黄酚回归方程为A=39750C+22239(r=0.9993)。结果表明,大黄素、大黄酚检测浓度分别在0.768~3.84、2.04~16.32 μg·mL-1范围内与各自峰面积积分值呈良好线性关系。
2.2 乙醇浸出物量的测定
精密量取乙醇提取液100 mL,置已干燥至恒重并称重的蒸发皿中,水浴蒸发干,于105℃烘箱干燥3 h至恒重,取出,迅速置干燥器中冷却,称重,重复3次,求得乙醇浸出物量。
2.3 正丁醇萃取物量的测定
精密量取乙醇提取液200 mL,加正丁醇萃取3次,第1次30 mL,第2、3次分别为20 mL,全部置已干燥至恒重并称重的蒸发皿中,水浴蒸发干,于105℃烘箱干燥3 h至恒重,取出,迅速置干燥器中冷却,称重,重复3次,求得正丁醇萃取物量。
2.4 三氯甲烷萃取物量的测定
精密量取乙醇提取液200 mL,加三氯甲烷萃取3次,第1次30 mL,第2、3次分别20 mL,全部置已干燥至恒重并称重的蒸发皿中,水浴蒸发干,于105℃烘箱干燥3 h至恒重,取出,迅速置干燥器中冷却,称重,重复3次,求得三氯甲烷萃取物量。
2.5 正交试验[9,10]
根据单因素和预试验结果,固定提取次数,选择乙醇浓度(A)、提取时间(B)和乙醇用量(C)为考察因素,采用正交试验设计。结合常用分析方法和目前能够得到有效成分对照品的情况,确定总蒽醌(即大黄素含量与大黄酚含量)、正丁醇萃取物量、三氯甲烷萃取物量和乙醇浸出物量为指标,综合评分(权重系数分别为0.5、0.2、0.2、0.1),优选最佳乙醇提取工艺。因素水平见表1。
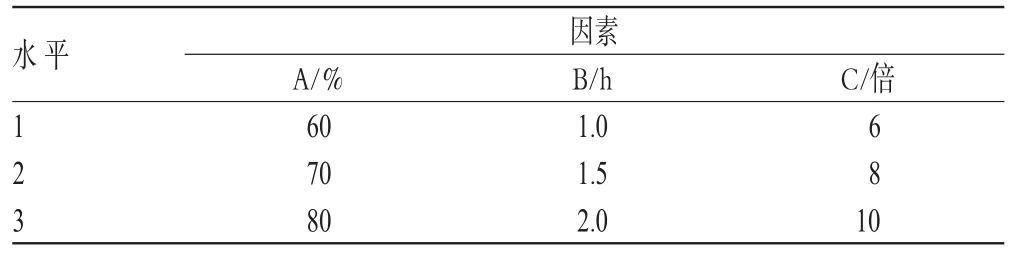
表1 因素水平Tab 1 Levels and factors
综合评分=(总蒽醌/最大总蒽醌)×50%+(正丁醇萃取物量/最大正丁醇萃取物量)×20%+(三氯甲烷浸出物量/最大三氯甲烷萃取物量)×20%+(乙醇浸出物量/最大乙醇浸出物量)×10%。
按处方比例称取各味醇提药材,滤液定容,分别测定大黄总蒽醌、正丁醇萃取物量、三氯甲烷萃取物量、乙醇浸出物量。正交试验结果见表2。
由表2可知,各因素对综合评分的影响大小顺序为:A(乙醇浓度)>B(提取时间)>C(加醇量);每个因素三个水平之间的趋势为 A3>A2>A1,B2>B3>B1,C2>C3>C1;直观分析得提取工艺为A3B2C2,即加8倍量80%乙醇回流提取2次,每次1.5 h。采用方差分析进一步优化,结果见表3。
由表3可知,A因素的影响具有显著性(P<0.05),B和C因素的影响均无显著性(P>0.05)。结合直观分析结果,以A3B2C2组合为佳,即加8倍量80%乙醇提取2次,每次1.5 h。据此条件对川西獐芽菜、波梭瓜子等8味药材进行验证试验,结果与正交试验结果一致,说明筛选出的最佳醇提工艺可行、合理、稳定。
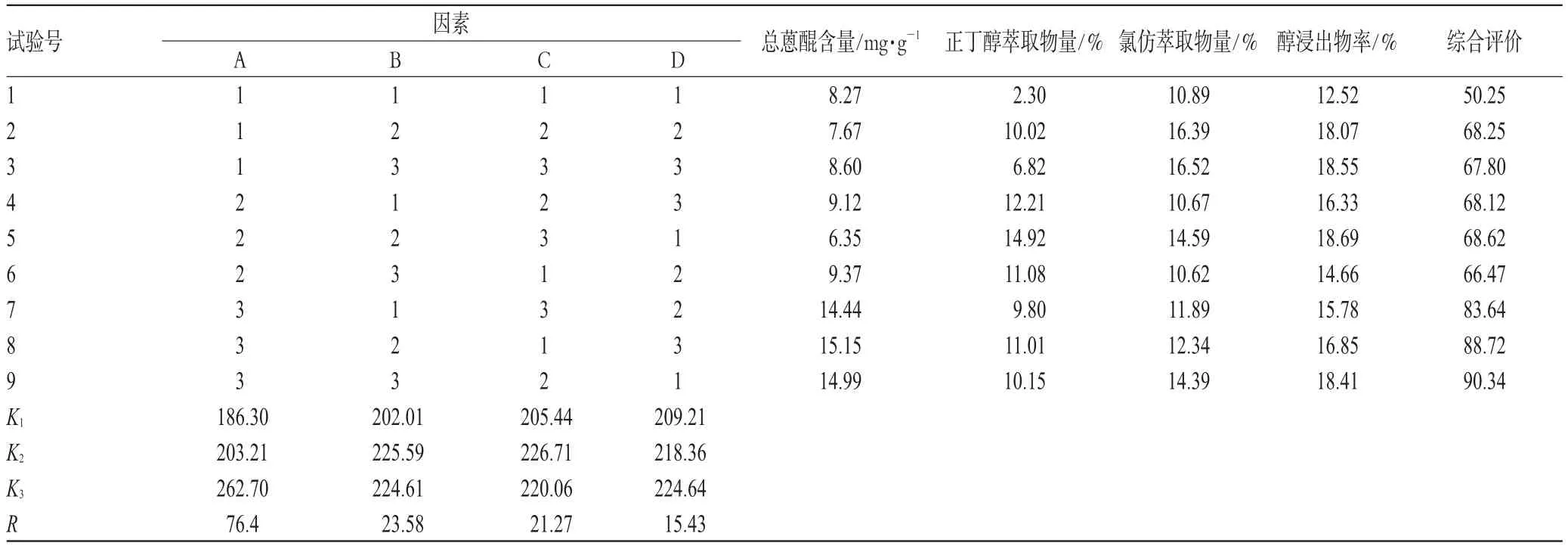
表2 正交试验结果Tab 2 Results of orthogonal experiment
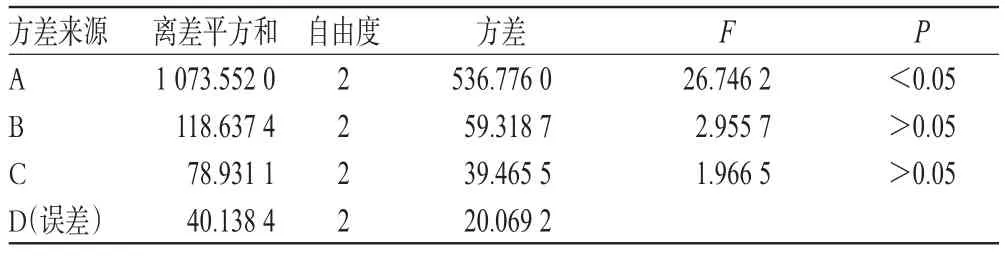
表3 方差分析结果Tab 3 Results of variance analysis
3 讨论
本研究建立了以HPLC法测定清肝利胆胶囊中总蒽醌含量的方法,为进一步完善清肝利胆胶囊的质量控制标准提供了准确、简便、可行的测定方法。
根据处方中甘草等其余药材的药理作用、有效成分和有效部位选定水提取法,选择加水用量、提取次数和提取时间为因素进行正交试验,最终确定最佳水提工艺为加8倍量水提取3次,每次1 h。按上述工艺进行重复试验3批,测定每步工艺指标,证明本研究优选得的水提工艺合理、稳定、可行。故醇提工艺和水提工艺共同构成了清肝利胆胶囊的提取工艺。
[1]国家药典委员会编.中华人民共和国药典(一部)[S].2005年版.北京:化学工业出版社,2005:17、41、59、129、212.
[2]西藏自治区卫生厅编.藏药标准[S].1979年版.西宁:青海人民出版社,1979:39、43、82、118、133.
[3]陈耀祖,张惠迪,张所明,等.藏药短穗兔耳草化学成分的研究[J].高等学校化学学报,1989,24(3):260.
[4]马继元,王峥涛,齐树合.羽叶苦买菜的化学成分研究[J].中国药科大学学报,1998,29(3):167.
[5]纪兰菊,保 怡,陈桂琛.15种獐芽菜属植物中主要药用成分的高效液相色谱测定[J].西北植物学报,2004,24(7):1298.
[6]刘永刚,薄少英,李 夏,等.HPLC测定复方胆痛胶囊中大黄素和大黄酚的含量[J].中国新药杂志,2006,15(19):1674.
[7]李元辉.HPLC法测定不同产地大黄中4种蒽醌类化合物含量[J].中药研究与信息,2005,7(6):17.
[8]杨立伟,龙 飞.HPLC法测定消炎清热胶囊中黄芩苷的含量[J].中国药房,2008,19(21):1632.
[9]张传平.中药研究中正交试验设计运用存在的问题讨论[J].陕西中医学院学报,2001,24(4):54.
[10]王小琳,张玉杰,石任兵.正交实验设计优选牛蒡子的提取工艺[J].北京中医药大学学报,2003,26(4):64.
