复方心安软胶囊质量标准研究
2010-05-22李华李明钟雪梅晁衍明第三军医大学军职干休所重庆市400038山东肥城市桃园中心卫生院肥城市7609
李华,李明,钟雪梅,晁衍明(.第三军医大学军职干休所,重庆市 400038;.山东肥城市桃园中心卫生院,肥城市 7609)
复方心安软胶囊由丹参、三七、银杏叶、川芎、甘草等8味中药组成,具有活血化瘀、行气止痛、改善微循环等功效。可用于气滞血瘀引起的胸痹、胸闷、心悸及多种中风后遗症。该制剂为颗粒剂改剂型而来,原质控标准没有含量测定项目。为更好地控制该制剂质量,本研究对该制剂中丹参、三七、银杏叶等3味药进行薄层定性鉴别研究,以丹参有效成分丹参素钠为指标成分进行了含量测定研究[1,2]。结果表明,所建标准可用于本制剂的质量控制。
1 仪器与试药
1100型高效液相色谱(HPLC)仪,包括DAD检测器、ChemStation色谱工作站(美国Agilent公司);LGJ-18型冷冻干燥机(北京四环科学仪器厂);Laborota 4000型旋转蒸发仪(德国Heidolph公司);SHB-95型循环水式真空泵(郑州华中仪器厂);AE 163型十万分之一电子分析天平(瑞士Mettler Toledo公司);KQ-500B型超声波清洗器(江苏省昆山市超声仪器有限公司)。
复方心安软胶囊(中国人民解放军海军总医院制剂室提供,批号:080610、080727、080822、080923、081010);丹参素钠、丹参酮ⅡA、人参皂苷Rb1、三七皂苷R1、银杏内酯A、银杏内酯B对照品(中国药品生物制品检定所,批号分别为110855-200101、110766-200214、110704-200220、110745-200312、865-9601、0862-200004);乙腈(色谱纯,美国Fisher公司);水为超纯水(Milli-Q纯水仪制得),其余试剂均为分析纯。
2 方法与结果
2.1 定性鉴别
2.1.1 丹参的TLC鉴别[3]取本品内容物0.5 g、不含丹参的阴性样品0.5 g,分别加乙醚20 mL,超声5 min,滤过,滤液挥干,残渣加乙酸乙酯2 mL使溶解,作为供试品溶液及阴性对照溶液;另取丹参酮ⅡA加乙酸乙酯制成每1 mL含0.5 mg的溶液,作为对照品溶液。吸取上述3种溶液各5 μL,分别点于同一硅胶G薄层板上,以甲苯-醋酸乙酯(19∶1)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,于105℃加热20 min。结果,供试品色谱中,在与对照品色谱相应的位置,显相同颜色的斑点;阴性对照无干扰。丹参的TLC见图1。
2.1.2 三七的TLC鉴别 取本品内容物0.5 g、不含三七的阴性样品0.5 g,分别加甲醇20 mL,加热回流20 min,放冷,滤过,滤液蒸干,残渣加水10 mL,微热使溶解,加水饱和的正丁醇振摇提取3次,每次20 mL,合并正丁醇提取液,用氨试液提取2次,每次20 mL,弃去氨液,正丁醇液蒸干,残渣加甲醇2 mL使溶解,作为供试品溶液及阴性对照溶液;另取人参皂苷Rb1和三七皂苷R1对照品,加甲醇制成每1 mL各含1 mg的混合溶液,作为混合对照品溶液。吸取上述3种溶液各5 μL,分别点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲醇-水(15∶40∶22∶10)10℃以下放置12 h的下层溶液为展开剂,展开,取出,晾干,喷10%硫酸乙醇溶液,于110℃加热10 min,置紫外光灯(365 nm)下检视。结果,供试品色谱中,在与混合对照品色谱相应的位置上,显相同颜色的斑点;阴性对照无干扰。三七的TLC见图2。
2.1.3 银杏叶的TLC鉴别 取本品内容物0.5 g、不含银杏叶的阴性样品0.5 g,分别加乙酸乙酯超声提取2次,每次30 mL,蒸干,残渣加15%乙醇5 mL溶解,置已处理好的聚酰胺柱上,用5%乙醇40 mL洗脱,收集洗脱液,蒸去乙醇,残渣加1 mL丙酮溶解,作为供试品溶液及阴性对照溶液;另取银杏内酯A和银杏内酯B对照品,加丙酮制成每1 mL各含0.65 mg的混合溶液,作为混合对照品溶液。吸取上述3种溶液各5 μL,分别点于同一硅胶G薄层板(含4%醋酸钠的羧甲基纤维素钠溶液为黏合剂)上,以甲苯-乙酸乙酯-丙酮-甲醇(10∶5∶5∶0.6)为展开剂,15℃展开,取出,晾干,醋酐蒸汽中熏10 min,于140℃加热30 min,置紫外光灯(365 nm)下检视。结果,供试品色谱中,在与混合对照品色谱相应的位置上,显相同颜色的斑点;阴性对照无干扰。银杏叶的TLC见图3。

图1 丹参的TLC1.供试品;2.阴性对照;3.丹参酮ⅡA对照品Fig 1 TLC of S.Miltiorrhiza1.samples;2.negative sample;3.tanshinone reference substance

图2 三七的TLC1.供试品;2.阴性对照;3.混合对照品Fig 2 TLC of P.notoginseng1.samples;2.negative sample;3.mixture control

图3 银杏叶的TLC1.供试品;2.阴性对照;3.混合对照品Fig 3 TLC of G.biloba1.samples;2.negative sample;3.mixture control
2.2 定量分析[2]
2.2.1 对照品溶液的制备 取丹参素钠对照品适量,精密称定,加甲醇制成浓度为50.0 μg·mL-1的溶液,摇匀,即得。
2.2.2 供试品溶液的制备 取样品约0.5 g,精密称定,置具塞锥形瓶中,精密加入50%甲醇50 mL,密塞,称重,超声处理30 min,放冷,再称重,用上述溶剂补足失重,摇匀,滤过,取续滤液,即得。
2.2.3 阴性对照溶液的制备 按处方比例及工艺条件制备缺丹参的阴性样品,按“2.2.2”项下方法制备阴性对照溶液。
2.2.4 色谱条件与系统适用性试验 色谱柱:Nova-pak ODS(250 mm×4.6 mm,5 μm);流动相:甲醇-0.5%磷酸二氢钾溶液(0.1%磷酸溶液调pH至4.0,15∶85);流速:1.0 mL·min-1;检测波长:280 nm;进样量:10 μL。理论塔板数按丹参素钠峰计算应不低于4000。在上述色谱条件下取丹参素钠对照品溶液、供试品溶液和阴性对照溶液各10 μL进样,结果表明样品中其它成分对丹参素钠的测定无干扰。色谱见图4。

图4 高效液相色谱图A.对照品;B.供试品;C.阴性对照;1.丹参素钠Fig 4 HPLC chromatogramsA.reference substance;B.sample;C.negative control;1.sodium danshensu
2.2.5 标准曲线的制备 精密称取丹参素钠对照品5.0 mg,置25 mL量瓶中,加50%甲醇溶解并稀释至刻度。精密吸取上述溶液0.5、1、1.5、2、3、5 mL,置10 mL量瓶中,加50%甲醇至刻度,摇匀。按上述色谱条件取10 μL进样,记录色谱图。以检测浓度(X)为横坐标,峰面积积分值(Y)为纵坐标,制备标准曲线,得回归方程为Y=12.126X-17.329(r=0.9996)。结果表明,丹参素钠检测浓度在10.0~100.0 μg·mL-1范围内与峰面积积分值呈良好的线性关系。
2.2.6 精密度试验 精密吸取对照品溶液,按照上述色谱条件连续进样5次,测定峰面积。结果,RSD=0.88%,表明仪器精密度良好。
2.2.7 重复性试验 取同批次样品,按照“2.2.2”项下方法制备6份供试品溶液,测定并计算其含量。结果,丹参素钠平均含量为每粒2.06 mg,RSD=2.05%,表明方法重复性良好。
2.2.8 稳定性试验 取同一供试品溶液,于室温下放置,在不同时间段(0、2、4、8、16、24、48 h)按上述色谱条件进样测定。结果,RSD=1.95%,表明供试品溶液在48 h稳定性良好。
2.2.9 加样回收率试验 精密称取已知含量的样品约0.5 g(含丹参素钠为每粒1.98 mg)6份,分别精密加入不同质量的丹参素钠对照品,每个质量平行2份,按照“2.2.2”项下方法制备供试品溶液,测定并计算其含量和加样回收率,结果见表1。
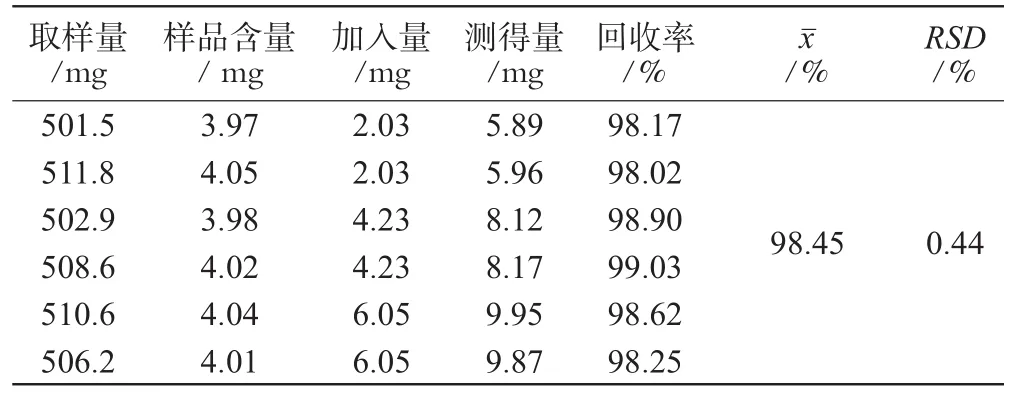
表1 加样回收率试验结果(n=6)Tab 1 Results of recovery tests(n=6)
2.2.10 样品含量测定 取5批样品,分别按照“2.2.2”项下方法制备供试品溶液,测定并计算其含量,结果见表2。

表2 样品含量测定结果(n=3)Tab 2 Content determination of samples(n=3)
3 讨论
试验中考察了冷浸、超声及加热回流3种提取方法,结果表明,冷浸48 h提取含量最高,超声法次之,加热回流提取含量最少。但超声法耗时短、方法简便且杂质较少,故本试验选择此提取方法。
本试验参考文献[4~6]的流动相:甲醇-1%冰醋酸(15∶85)、甲醇-水-冰醋酸(3∶96∶1)及甲醇-0.5%冰醋酸梯度洗脱[6],结果发现以甲醇-0.5%磷酸二氢钾溶液(0.1%磷酸溶液调pH值至4.0,15∶85)为流动相时,丹参素钠与其它组分即能达到较好分离,且柱效高、耗时短。
[1]国家药典委员会编.中华人民共和国药典(一部)[S].2005年版.北京:化学工业出版社,2005:52.
[2]李红磊.丹参酮复合丹酚酸复合微乳的制备[C].南方医科大学毕业论文集,2006:29.
[3]崔淑云,王登旭.益肝康口服液的制备及质量标准研究[J].中国药房,2008,19(3):192.
[4]侯利强,邢俊生,高亚强,等.高效液相色谱法测定甲亢灵颗粒中丹参素的含量[J].中国现代药物应用,2008,2(3):8.
[5]邹蔼珍.乐脉颗粒的质量标准研究[J].中国药房,2005,16(15):1178.
