胺类萃取剂高效分离Hf(Ⅳ)与W(Ⅵ)的方法研究
2010-01-26凡金龙张生栋卢嘉春张自禄丁有钱常永福
凡金龙,张生栋,卢嘉春,刘 杰,张自禄,丁有钱,常永福
1.中国原子能科学研究院 放射化学研究所,北京 102413; 2.西北核技术研究所,陕西 西安 710024
对某些环境样品中长寿命、超痕量的放射性核素182Hf(t1/2=8.90×106a)[1]进行分析,可用于指示核反应的过程信息。由于182Hf半衰期长且含量极低,因此,用通用的质谱技术或者放射性测量方法无法进行分析测量。加速器质谱(AMS)的丰度灵敏度高,是分析182Hf的合适方法之一[2-3]。解决样品中大量天然同质异位素182W的干扰问题是实现AMS准确测定182Hf的关键。
化学分离是AMS分析测定182Hf中去除182W干扰的有效手段之一。尽管有关Hf(Ⅳ)与W(Ⅵ)的化学分离已有很多报道[4-9],但多数没有给出W(Ⅵ)的去污因子。为开展182Hf的AMS测量及分析工作,近来报道了溶剂萃取、离子交换或多种分离组合的方法来分离Hf(Ⅳ)与W(Ⅵ),其中有些Hf(Ⅳ)回收率高(>95%),但对W(Ⅵ)的去污因子不高(103~104)[3,10];有些对W(Ⅵ)的去污因子较高(约106),但分离步骤烦琐,导致Hf(Ⅳ)回收率偏低(70%)[11]。基于样品中182Hf含量极低,所设计的流程既要保证Hf(Ⅳ)的高收率又要实现对W(Ⅵ)的高去污。
伯胺N1923在H2SO4介质中可富集Zr(Ⅳ),柠檬酸存在下可抑制W(Ⅵ)的萃取,HCl可将有机相中的Zr(Ⅳ)反萃下来[12-13];而叔胺TOA在HCl介质(少量H2O2存在)中优先萃取W(Ⅵ)而很少萃取Hf(Ⅳ),两者具有很高的分离因子(1.6×106)[10]。因此,本工作拟以N1923和TOA为萃取剂,探索并建立一个更加简便、高效的Hf(Ⅳ)与W(Ⅵ)的分离方法,为样品中182Hf含量的分析提供基础。
1 实验部分
1.1 分离流程的基本设想
根据文献[10,12-13]结果,设想将分离流程分为两部分,先研究伯胺N1923在H2SO4介质中萃取Hf(Ⅳ),然后研究叔胺TOA在HCl介质中萃取W(Ⅵ),并通过反萃剂将这两种胺类萃取剂萃取Hf(Ⅳ)和W(Ⅵ)的过程有机地结合起来。
1.2 试剂与仪器
N1923萃取剂,上海有机化学研究所;TOA萃取剂,美国Fluka公司;Hf(Ⅳ)载体溶液(10 g/L):分别取一定量光谱纯HfO2用HF-H2SO4溶解,经氨水沉淀后,分别转化为3 mol/L H2SO4和6 mol/L HCl溶液备用;W(Ⅵ)载体溶液(5 g/L):一定量Na2WO4·2H2O用超纯水溶解配制;175,181Hf指示剂:一定量光谱纯HfO2在西安脉冲反应堆辐照3 h,热中子注量率为1×1013/(cm2·s),按上述方法转化为溶液备用;187W指示剂:一定量光谱纯WO3在西安脉冲反应堆辐照3 h,热中子注量率为1×1013/(cm2·s),用0.1 mol/L NaOH溶液溶解后备用;裂变产物溶液:140Ba-140La、141,144Ce、147Nd、95Zr-95Nb、103Ru、137Cs,西安脉冲反应堆生产;实验用水为美国Millipore公司生产的超纯水,电阻率18.2 MΩ·cm;HNO3、HCl、HF、H2SO4、30% H2O2均为优级纯;其它试剂均为分析纯。
测试系统由美国ORTEC公司生产的阱式GWL-250-15-S型HPGe探测器和DSPEC-PLUS数字化多道谱仪组成,其中HPGe探测器的能量分辨率为2.30 keV(1.332 MeV);LD5-2A型低速离心机,调速范围0~5 000 r/min,北京医用离心机厂;HY-4调速多用振荡器,调速范围0~3 000 r/min,金坛市华峰仪器有限公司。
1.3 萃取实验
向10 mL塑料萃取管中加入3 mL含一定量指示剂及载体的水相溶液,用等体积一定浓度的N1923或TOA萃取剂进行萃取,在室温(18±1) ℃下机械振荡20 min(已达萃取平衡),离心分相,两相各取2 mL于γ测量管中分别测量放射性计数率。按式(1)—(3)计算各核素的分配比(D)、萃取率(E)及去污因子(DF);对于出现第三相的情况,按式(4)计算各核素的分配比(D)。
(1)
(2)
(3)
(4)
式中,Ci,o和Ci,a分别为萃取平衡后有机相和水相分析液中i核素的放射性计数率,s-1;Cfeed和Cproduct分别为料液和产品液中杂质核素的总放射性计数率,s-1;Ci,i为萃取前每2 mL初始水相中i核素的放射性计数率,s-1。
1.4 测量
将萃取后的水相、有机相分别移取于γ测量管中,在距离HPGe探测器相同的几何位置进行测量。测量的核素及其主要γ射线能量和强度列于表1。
2 结果和讨论
2.1 伯胺N1923对Hf(Ⅳ)与W(Ⅵ)的萃取行为研究
2.1.1H2SO4浓度对Hf(Ⅳ)及裂片核素萃取的影响 不同H2SO4浓度(0.4~8 mol/L)中,5% N1923-二甲苯对Hf(Ⅳ)及裂片核素的萃取行为示于图1。由图1可知,在0.4~4 mol/L范围内,Hf(Ⅳ)、Zr(Ⅳ)、Nb(Ⅴ)萃取率(Y)均大于99%,

表1 核素及其主要γ射线能量和强度[14]Table 1 Nuclides and their main gamma-ray energies and intensities [14]

图1 H2SO4浓度对N1923萃取Hf(Ⅳ)及某些裂片核素的影响Fig.1 Effect of H2SO4 concentration on the extraction of Hf (Ⅳ) and some fission products with N1923水相(Aqueous phase):示踪量Hf (Ⅳ)及裂片核素(Tracer amount of Hf (Ⅳ) and some fission products);有机相(Organic phase):5% N1923-二甲苯(Xylene)★——181Hf,▼——95Zr,▲——95Nb,■——141Ce,○——147Nd,△——140La,●——103Ru,◆——140Ba,□——137Cs
而后,Nb(Ⅴ)萃取率迅速下降,5 mol/L后,Hf(Ⅳ)、Zr(Ⅳ)萃取率迅速下降,两者萃取行为基本一致;其它裂片核素(141Ce、147Nd、140La、103Ru、140Ba)在c(H2SO4)=3~8 mol/L范围内萃取率较低(<8%),随着H2SO4浓度的进一步降低,萃取率迅速增大;Cs(Ⅰ)在实验浓度范围内几乎不被萃取。由此可见,3~5 mol/L H2SO4可以作为Hf(Ⅳ)、Zr(Ⅳ)与其它裂片核素优化的分离条件。Hf(Ⅳ)的萃取机理可能与Zr(Ⅳ)相似,以络阴离子形式与N1923铵盐阳离子形成离子缔合物而被萃取[12]。对于Nb(Ⅴ)的干扰,可以通过萃取前在水相添加H2O2来掩蔽[12]。
2.1.2H2SO4中柠檬酸(Cit)质量浓度对Hf(Ⅳ)与W(Ⅵ)萃取的影响 在定量萃取Hf(Ⅳ) 的介质(3.6 mol/L H2SO4)中,Cit质量浓度对5% N1923-二甲苯萃取Hf(Ⅳ)与W(Ⅵ) 的影响示于图2。由图2可知,无论Cit存在与否,Hf(Ⅳ)萃取率都大于99%,但加入Cit可明显抑制W(Ⅵ)的萃取。在3.6 mol/L H2SO4-0.05 kg/L Cit介质中,W(Ⅵ)的萃取率仅为6.6%,两者分离效果最优。文献[13]仅讨论了1~4 mol/L H2SO4中,0.1 mol/L Cit对W(Ⅵ)的萃取结果。

图2 柠檬酸质量浓度对N1923萃取Hf(Ⅳ)与W(Ⅵ)的影响 Fig.2 Effect of citric acid mass concentration on the extraction of Hf (Ⅳ) and W(Ⅵ) with N1923c(H2SO4)=3.6 mol/L水相(Aqueous phase):ρ(Hf)=ρ(W)=100 mg/L;有机相(Organic phase):5% N1923-二甲苯(Xylene)
2.1.3萃取剂浓度对Hf(Ⅳ)与W(Ⅵ)萃取的影响 在优化的Hf(Ⅳ)与W(Ⅵ)分离水相(3.6 mol/L H2SO4-0.05 kg/L Cit)中,萃取剂N1923的体积分数(φ(N1923)=1%~8%)对两者萃取的影响示于图3。由图3可知,在选取的萃取剂浓度范围内,Hf(Ⅳ)萃取率均大于99%;W(Ⅵ)的萃取率随萃取剂浓度的增大而增加的趋势不明显,即使在较高萃取剂体积分数(8%)下,其萃取率也小于9%。由此可见,水相中Cit的掩蔽是导致W(Ⅵ)不易被萃取的主要原因。

图3 φ(N1923)对Hf(Ⅳ)与W(Ⅵ)萃取的影响Fig.3 Effect of φ(N1923) on the extraction of Hf (Ⅳ) and W (Ⅵ)水相(Aqueous phase):3.6 mol/L H2SO4-0.05 kg/L Cit,ρ(Hf)=ρ(W)=100 mg/L;有机相(Organic phase):N1923-二甲苯(Xylene)
2.1.4HCl浓度对Hf(Ⅳ)与W(Ⅵ)负载有机相反萃的影响 不同HCl浓度(2~8 mol/L)对负载有Hf(Ⅳ)与W(Ⅵ)的5% N1923-二甲苯的反萃率(Y′)示于图4。由图4可知,一次反萃即可保证Hf(Ⅳ)完全反萃至水相;而至少90%的W(Ⅵ)也被反萃。酸浓度高有利于两者的分离,但HCl是强腐蚀性挥发性酸,浓度过高对操作环境不利。

图4 HCl浓度对Hf(Ⅳ)与W(Ⅵ) 负载有机相反萃的影响Fig.4 Effect of HCl concentration on the back extraction of Hf (Ⅳ) and W (Ⅵ) from organic phase有机相(Organic phase):5% N1923-二甲苯(Xylene),ρ(Hf)=ρ(W)=10 mg/L
以上研究结果表明,萃取水相的选择是影响Hf(Ⅳ)与裂片核素及W(Ⅵ)分离的主要因素;而萃取剂及HCl反萃剂的浓度对Hf(Ⅳ)与W(Ⅵ)分离的影响较小。
2.2 叔胺TOA对Hf(Ⅳ)与W(Ⅵ)的萃取行为研究
2.2.1HCl浓度对萃取的影响 不同HCl浓度(2~10 mol/L)中,0.3 mol/L TOA-二甲苯/环己烷对Hf(Ⅳ)与W(Ⅵ) 的萃取行为示于图5。由图5可知,W(Ⅵ)萃取率随着HCl浓度增大而逐渐增大至接近最大值;而Hf(Ⅳ)萃取率只有在HCl浓度大于6 mol/L才迅速增大。因此,在6 mol/L HCl介质中,Hf(Ⅳ)与W(Ⅵ)分离效果最优,此条件同Maji[10]研究结果一致。本研究表明,尽管Maji选用的环己烷稀释剂的萃取性能略好,但当HCl浓度大于2 mol/L时,萃取出现第三相,给操作及测量带来不利。进一步的实验表明,在不加Hf(Ⅳ)与W(Ⅵ)的情况下,依然出现第三相,而且随着酸浓度及萃取剂浓度增大,第三相越明显(有机相分层界面下层的体积增大)。因此,第三相的出现可能是由于TOA-环己烷萃取HCl所致。相反,在本实验浓度范围内,以二甲苯为稀释剂不会出现第三相,相分离很好。
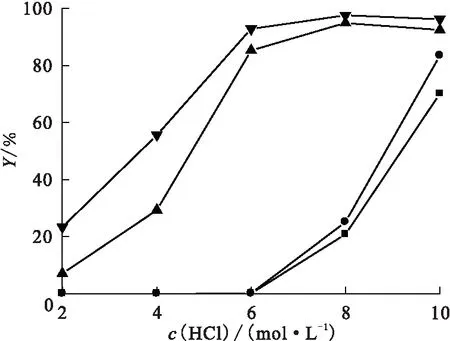
图5 HCl浓度对TOA萃取Hf(Ⅳ)与W(Ⅵ)的影响Fig.5 Effect of HCl concentration on the extraction of Hf (Ⅳ) and W (Ⅵ) with TOA 水相(Aqueous phase):ρ(Hf)=ρ(W)=10 mg/L;有机相(Organic phase):0.3 mol/L TOA-二甲苯/环己烷(Xylene/cyclohexane)■——Hf(TOA-二甲苯(Xylene)), ●——Hf(TOA-环己烷(Cyclohexane)), ▲——W(TOA-二甲苯(Xylene)),▼——W(TOA-环己烷(Cyclohexane))
2.2.2TOA萃取W(Ⅵ)机理的初步探索 以lgD对lgc(TOA)作图示于图6。由图6得直线斜率接近1,由此表明在此体系中,TOA铵盐阳离子与W(Ⅵ)络阴离子生成1∶1的离子缔合物而被萃取。而TOA对Hf(Ⅳ)的萃取机理已有文献[15]报道为阴离子交换过程,TOA铵盐阳离子与Hf络阴离子形成2∶1的离子缔合物(R3NH)2·HfCl6而被萃取。

图6 lg D对lg c(TOA)图Fig.6 Plot of lg D vs lg c(TOA) 水相(Aqueous phase):ρ(W)=10 mg/L,6 mol/L HCl;有机相(Organic phase):TOA-环己烷(Cyclohexane)

图7 H2O2质量分数对TOA萃取Hf(Ⅳ)及W(Ⅵ)的影响Fig.7 Effect of H2O2 mass fraction on the extraction of Hf(Ⅳ) and W(Ⅵ) with TOAc(HCl)=6 mol/L水相(Aqueous phase):ρ(Hf)=ρ(W)=10 mg/L;有机相(Organic phase):0.3 mol/L TOA-二甲苯(Xylene)
2.2.3H2O2浓度对萃取的影响 酸性介质中加入H2O2,W(Ⅵ)可形成更稳定的络阴离子[16]。因此,本工作研究了6 mol/L HCl中,H2O2质量分数(w(H2O2)=0.5%~5%)对两者萃取行为的影响,结果示于图7。由图7可知,H2O2存在与否,Hf(Ⅳ)的萃取率都小于0.1%,但随着H2O2的加入,W(Ⅵ)萃取率明显提高。6 mol/L HCl-1% H2O2中0.3 mol/L TOA-二甲苯对W(Ⅵ)的萃取率可达98%,有利于Hf(Ⅳ)与W(Ⅵ)的分离;而且在此介质中,0.3 mol/L TOA-环己烷对W(Ⅵ)具有相同的萃取结果。这说明H2O2对W(Ⅵ)萃取的影响远大于稀释剂效应。本研究弥补了Maji[10]对H2O2浓度没有量化的不足。
2.2.4改性剂对第三相及W(Ⅵ)萃取的影响 以辛醇为改性剂,对环己烷作为稀释剂出现第三相的消除及W(Ⅵ)萃取的影响列于表2。由表2可知,要使萃取不出现第三相,有机相辛醇的体积分数不得小于3%,但此条件不利于W(Ⅵ)的萃取。因此,对TOA萃取分离Hf(Ⅳ)与W(Ⅵ)建议使用二甲苯作为稀释剂。

表2 不同体积分数的辛醇作为改性剂时TOA-环己烷萃取W(Ⅵ)的行为Table 2 Extraction behavior of W (Ⅵ) with TOA in cyclohexane together with various octanol as phase modifier
注(Note):水相(Aqueous phase):6 mol/L HCl-1% H2O2,ρ(W)=10 mg/L;有机相(Organic phase):0.3 mol/L TOA-环己烷-辛醇(Cyclohexane and octanol)
2.3 N1923和TOA溶剂萃取分离Hf(Ⅳ)与W(Ⅵ)
2.3.1分离流程 在上述研究的基础上,确立了N1923和TOA多步溶剂萃取分离Hf(Ⅳ)与W(Ⅵ)的流程(图8)。在N1923萃取及洗涤步骤,相比(有机相与水相体积之比)选择1∶2,反萃步骤相比为1∶1,TOA萃取步骤相比为2∶1。
2.3.2流程的化学回收率及去污因子测定 以187W为示踪剂,监测了流程各分离步骤结束后W(Ⅵ)的去污因子(DF),结果列于表3。由表3可知,N1923溶剂萃取过程对毫克量级W(Ⅵ)的去污因子在103量级。TOA第一次萃取,对W(Ⅵ)的去污因子在102量级,但随着萃取水相W(Ⅵ)浓度的降低,TOA对W(Ⅵ)的萃取率会发生突降,两次萃取后再增加萃取次数,对W(Ⅵ)的去污已不明显。TOA三次萃取,对W(Ⅵ)的去污因子大于104。
分别以181Hf、187W为示踪剂,测定了不同Hf(Ⅳ)、W(Ⅵ)混合载体量情况下全流程的化学回收率及总去污因子,结果列于表4。由表4可知,Hf(Ⅳ)载体量在微克至毫克范围内,流程的化学回收率(R)均大于90%;而全流程对W(Ⅵ)的去污因子随W(Ⅵ)载体量的变化较明显,主要原因是随着萃取水相W(Ⅵ)浓度的降低,TOA对W(Ⅵ)的去污已不明显。

图8 Hf(Ⅳ)与W(Ⅵ)分离流程示意图Fig.8 Schematic diagram of the separation of Hf(Ⅳ) from W(Ⅵ)

No分离步骤(Separationstep)DF1N1923萃取(Extraction)32×1012第一次洗涤(Thefirstscrubbing)16×1023第二次洗涤(Thesecondscrubbing)18×1024反萃(Backextraction)15×1035TOA第一次萃取(Thefirstextraction)20×1056TOA第二次萃取(Thesecondextraction)22×1077TOA第三次萃取(Thethirdextraction)44×107
3 结 论
(1) 在3.6 mol/L H2SO4-0.05 kg/L Cit介质中,5% N1923-二甲苯萃取可富集Hf(Ⅳ),实现与较低价态元素(一价、二价及三价的稀土)及W(Ⅵ)的有效分离。由于柠檬酸可阻止毫克量级W(Ⅵ)在强酸介质中形成钨酸沉淀,N1923溶剂萃取有利于对高浓度W(Ⅵ)的去污。

表4 流程的化学回收率及去污因子Table 4 Recovery of Hf(Ⅳ) and decontamination factor of W(Ⅵ) by the separation procedure
注(Note):1) 计数率的统计不确定度小于10%(The statistical uncertainty of the counting rate is less than 10%)
(2) 在HCl介质中,W(Ⅵ)络阴离子与TOA铵盐阳离子生成1∶1的离子缔合物而被萃取。在6 mol/L HCl-1% H2O2介质中,0.3 mol/L TOA-二甲苯可优先定量萃取W(Ⅵ)而与Hf(Ⅳ)有效分离。TOA溶剂萃取适用于对低浓度W(Ⅵ)的去污,否则水相易形成钨酸沉淀而导致分离变坏。
(3) N1923和TOA溶剂萃取过程通过6 mol/L HCl反萃剂巧妙结合,无需额外的介质转换操作。该方法既可有效富集Hf(Ⅳ)(回收率大于90%),又可高效去除W(Ⅵ)(去污因子为4.4×107),有望用于AMS测量182Hf前样品的制备。
致谢:感谢西安脉冲反应堆潘孝兵、于青玉在制备辐照靶方面提供的帮助。
[1] Vockenhuber C, Oberli F, Bichler M, et al. New Half-Life Measurement of182Hf: Improved Chronometer for the Early Solar System[J]. Phys Rev Lett, 2004, 93(17): 172501/1-172501/4.
[2] Vockenhuber C, Bichler M, Golser R, et al.182Hf, A New Isotope for AMS[J]. Nucl Instrum Methods Phys Res, Sect B, 2004, 223-224: 823-828.
[3] Qiu J, Jiang S, He M, et al. Measurement of Hf-182 With HI-13 AMS System[J]. Nucl Instrum Methods Phys Res, Sect B, 2007, 259(1): 246-249.
[4] Ward T E, Haustein P E. NewKπ=8-Isomer in182Hf [J]. Phys Rev C, 1971, 4(1): 244-246.
[5] Shishkin S V, Shishkina T V, Buklanov G V, et al. Separation of Carrier Free W-178 From Alpha-Particle Activated Hafnium With TBP Impregnated Resin[J]. Czech J Phys, 2003, 53: A425 -A427.
[6] Schumann D, Dressler R, Taut S, et al. On-Line Separation of Short-Lived Tungsten Isotopes From Tantalum, Hafnium and Lutetium by Adsorption on Ion Exchangers From Aqueous Ammonia Solution[J]. J Radioanal Nucl Chem Lett, 1996, 214(1): 1-7.
[7] Szeglowski Z, Guseva L I, Lien D T, et al. On Line Ion Exchange Separation of Short-Lived Zr, Hf, Mo, Ta and W Isotopes as Homologs of Transactinide Elements[J]. J Radioanal Nucl Chem, 1998, 228(1-2): 145-149.
[8] Kleine T, Münker C, Mezger K, et al. Rapid Accretion and Early Core Formation on Asteroids and the Terrestrial Planets From Hf-W Chronometry[J]. Nature, 2002, 418: 952-955.
[9] Kleine T, Mezger K, Münker C, et al.182Hf-182W Isotope Systematics of Chondrites, Eucrites, and Martian Meteorites: Chronology of Core Formation and Early Mantle Differentiation in Vesta and Mars[J]. Geochim Cosmochim Acta, 2004, 68(13): 2 935-2 946.
[10] Maji S, Lahiri S, Wierczinski B, et al. Separation of Trace Level Hafnium From Tungsten: A Step Toward Solving an Astronomical Puzzle[J]. Anal Chem, 2006, 78(7): 2 302-2 305.
[11] 姜 涛,杨通在,仇九子,等.加速器质谱测量用HfF4样品的制备研究[J].核技术,2007,30(8):660-664.
[12] 石毓英,李成文,秦光荣.N1923萃取锆性质的研究及其应用[J].分析测试通报,1992,11(1):25-29.
[13] 石毓英,秦光荣.N1923分离富集钽铌[J].分析测试通报,1990,9(3):68-72.
[14] Firestone R B, Shirley V S. Tables of Isotopes[M]. 8thed. Wiley-inter Science: University of California, March, 1996: 2 629-7 959.
[15] Yang X J, Christian P. Separation of Hafnium and Zirconium From Ti- and Fe-Rich Geological Materials by Extraction Chromatography[J]. Anal Chem, 1999, 71: 1 706-1 711.
[16] Fritz J S, Topping J J. Chromatographic Separation of Vanadium, Tungsten and Molybdenum With a Liquid Anion-Exchanger[J]. Talanta, 1971, 18: 865-872.
