合成磁共振成像多定量值联合应用可提高干燥综合征的诊断准确率
2024-11-20夏弘毅孙其安陈铖陆璐焦志云李郑

摘要:目的 "探讨合成磁共振成像(MAGiC)在干燥综合征(SS)诊断中的的可行性及临床应用价值。方法 "前瞻性收集2023年2~10月于扬州大学附属医院就诊的SS患者36例作为SS组,选取同期38例健康志愿者作为对照组(HC组),分别对两组患者双侧腮腺行T1WI、T2WI及MAGiC扫描,对MAGiC图像进行后处理,生成T1、T2及质子密度(PD)mapping 3组定量序列。由2位医师分别测量双侧腮腺的T1、T2及PD值,采用组内相关系数(ICC)评估观察者间及观察者内的一致性。采用Pearson或Spearman检验比较双侧腮腺MAGiC各定量值的相关性。采用独立样本t检验或Wilcoxon秩和检验比较双侧腮腺SS组与HC组间MAGiC各定量值的差异。对MAGiC定量值差异具有统计学意义的计数资料绘制ROC曲线,采用Z检验比较曲线下面积。结果 "一致性分析结果显示双侧腮腺T2、PD值的ICC均gt;0.800,双侧腮腺T1值最低,ICC均gt;0.700。相关性分析结果显示双侧腮腺两组间MAGiC各定量值均具有高度相关性(rgt;0.8)。两组T1、T2值差异均有统计学意义(Plt;0.001),PD值差异均无统计学意义(Pgt;0.05)。MAGiC T1与T2值联合诊断的准确率(84.35%)及曲线下面积(0.88)最高,与T1值的差异有统计学意义(P=0.026)。结论 "MAGIC技术可以定量评估SS腮腺病变,MAGiC多定量值联合应用可提高诊断准确率。
关键词:MAGiC;腮腺;定量MRI;干燥综合征
The combined application of multiple quantitative values of synthetic magnetic resonance imaging can improve the diagnostic accuracy of sjogren's syndrome
XIA Hongyi, SUN Qi'an, CHEN Cheng, LU Lu, JIAO Zhiyun, LI Zheng
Department of Radiology, Affiliated Hospital of Yangzhou University, Yangzhou 225000, China
Abstract: Objective To explore the feasibility and clinical application value of MAGiC technique in the diagnosis of Sjogren's syndrome (SS). Methods A total of thirty-six SS patients from the Affiliated Hospital of Yangzhou University from February to October 2023 were selected as the SS group, and thirty‑eight healthy volunteers from the same period were selected as the control group (HC group). T1WI, T2WI and MAGiC scanning were performed on bilateral parotid glands of the two groups, respectively. After post-processing of MAGiC images, three sets of quantitative sequences T1, T2, proton density (PD) mapping were generated. The obtained T1, T2 and PD values of the bilateral parotid glands were measured by two physicians, and intra-group correlation coefficient (ICC) was used to evaluate inter-observer and intra-observer consistency; the correlation of quan titative values of MAGiC in bilateral parotid glands was compared by Pearson or Spearman test; and the independent samples t test or Wilcoxon rank sum test was used to analysis the differences in quantitative values of MAGiC between the bilateral parotid gland SS group and HC group. ROC curves were plotted for counting data with statistically significant differences in MAGiC quantitative values, and Z-test was used to compare the area under the curve. Results The results of consistency analysis showed that both T2 and PD values of the bilateral parotid gland had ICCgt;0.800, while T1 values of the bilateral parotid gland were lower (ICCgt;0.700). Correlation analysis showed that the quantitative values of MAGiC were highly correlated between the two groups (rgt;0.8). The analysis results between the two groups showed that T1 and T2 values were statistically significant (Plt;0.001), while PD values were not statistically significant (Pgt;0.05). The accuracy (84.35%) and area under the curve (0.88) of the combination of MAGiC T1 and T2 values were the highest, and the difference with T1 values was statistically significant (P=0.026). Conclusion MAGiC technology can quantitatively evaluate SS parotid gland lesions, and the combined application of multiple quantitative values of MAGIC technology can improve the diagnostic accuracy.
Keywords: MAGiC; parotid; quantitative MRI; sjogren's syndrome
干燥综合征(SS)是一种系统性的自身免疫性疾病,主要累及涎腺及泪腺[1-3] 。SS患病率女性明显高于男性,不同国家和地区有所不同。随着磁共振成像技术的发展,MRI已广泛用于涎腺病变的评估。MRI具有软组织分辨率高、多参数、多对比成像等特点,且MRI无电离辐射,具备多种特殊成像技术[4]。近年来,MRI检查技术在SS患者腮腺病变诊断中已得到一定应用,不仅可以通过常规MRI检查反映腮腺不可逆的脂肪浸润,还可以通过功能MRI检查显示腮腺导管的变化及腮腺血流动力学的变化[5-7]。但是目前国内外磁共振定量等成像技术扫描时间长,一次扫描仅可获取单一定量数据,缺乏多定量数据联合评估腮腺病变。
合成磁共振成像(MAGiC)是一种多对比度一站式驰豫定量技术,可通过一次多动态多回波序列获取多种对比度图像及多种定量数据,且扫描时间缩短,具有临床应用可行性[8-9],且目前国内外未见有将MAGiC技术用于SS腮腺病变研究。本研究旨在比较SS患者与健康志愿者腮腺MAGiC多定量参数的差异,探讨MAGiC技术在SS诊断中的的可行性及临床应用价值。
1 "资料与方法
1.1 "一般资料
本研究为前瞻性研究,收集2023年2~10月在扬州大学附属医院行腮腺MR检查的SS患者36例作为SS组,另选取同期38例健康志愿者作为对照组(HC组)。其中SS组36例双侧共71个腮腺,HC组38例双侧共76个腮腺。本研究已获得扬州大学附属医院伦理委员会批准同意(备案编号:MR-32-23-032636)。
纳入标准:依据 2016年美国风湿病学会/欧洲抗风湿病联盟临床诊断标准首次确诊的SS的患者[10];未进行任何相关治疗;无头颈部肿瘤史和放疗史,无糖尿病病史;未应用抗乙酰胆碱药物。排除标准:存在磁共振检查禁忌证;存在显著运动伪影、硬件伪影等,不能满足图像测量分析;剔除一侧或双侧腮腺急性肿大患者,影响对解剖结构的观察。
1.2 "仪器与方法
采用GE Architect 3.0T 超导MR成像仪及19通道头颈联合线圈。
横断面T2WI采用水脂分离成像(IDEAL)序列,扫描范围包括双侧腮腺上下缘及病变范围,TR 3250 ms,TE 85(10.2~122.7) ms,矩阵 288×256,FOV 20 cm× " 20 cm,层厚3 mm,层间隔1 mm。
冠状面T2WI采用IDEAL序列,扫描范围包括双侧腮腺前后缘及病变范围,TR 2500 ms,TE 72(10.1~121.2)ms,矩阵 288×256,FOV 22 cm×22 cm,层厚 " " 4 mm,层间隔0.5 mm。
横断面T1WI采用快速自旋回波(FSE)序列,扫描范围包括双侧腮腺上下缘及病变范围,TR 754 ms,TE Min Full(14.5~29.1)ms,矩阵 288×256,FOV 20 cm×20 cm,层厚3 mm,层间隔1 mm。
横断面MAGiC序列采用多延迟回波序列,扫描范围包括双侧腮腺上下缘及病变范围,自动设置TR值,TE 11.4(5.7~34.2)ms,Eff.TE2 68.4(39.9~69)ms,自动设置TI值,矩阵288×256,FOV 20 cm×20 cm,层厚 " " " "3 mm,层间隔1 mm。
1.3 "感兴趣区(ROI)设定及测量
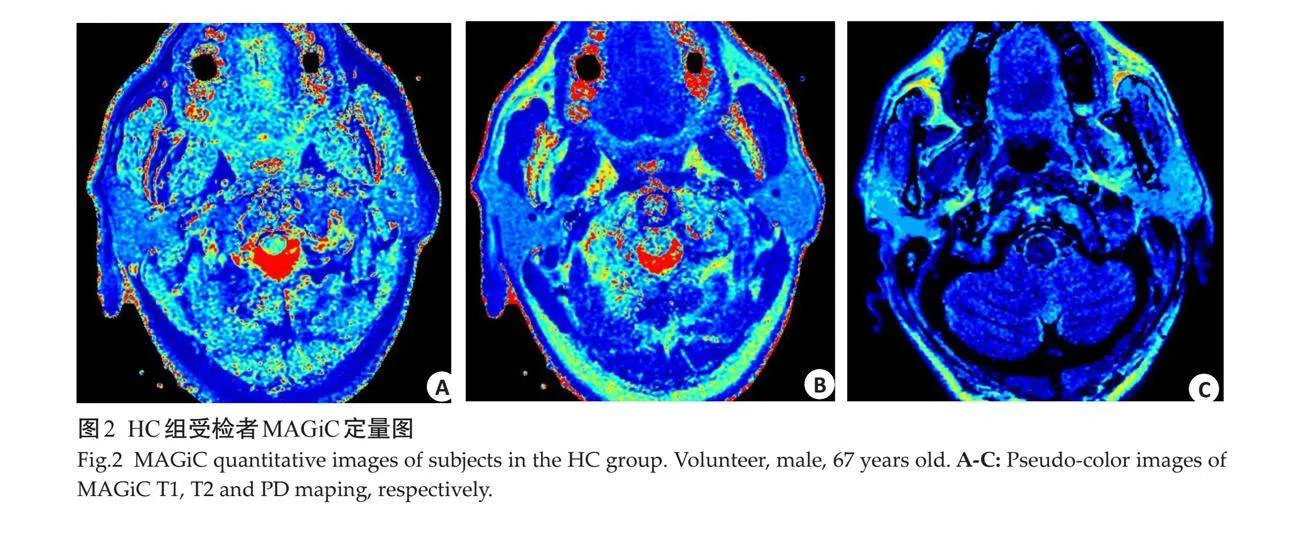
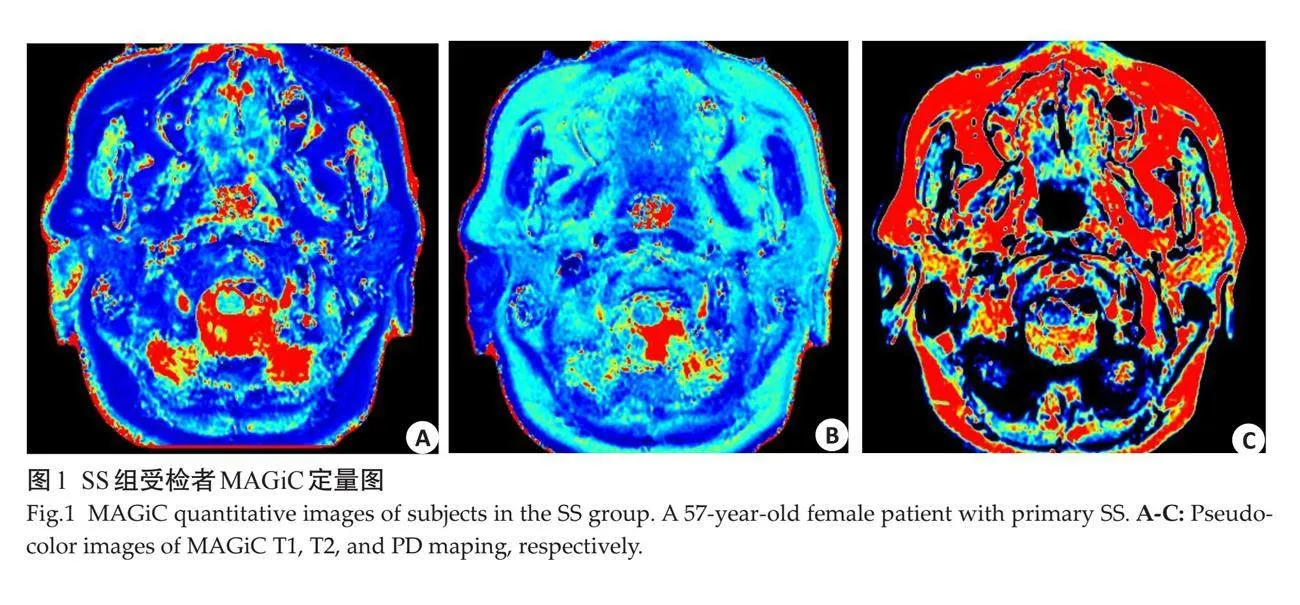
使用扫描仪图像编辑模块(MAGiC,version 100.0.0)进行图像后处理生成 T1 mapping、T2 mapping、PD mapping三组定量图谱,每组定量序列自动生成伪彩图(图1~2)。在MAGiC合成T2图像上选择双侧腮腺最大层面,沿腮腺内缘勾画感兴趣区,尽量避开腺体内大血管、导管,获得ROI的T1、T2、PD值。测量分别由2位放射科医师独立完成,并在间隔至少2周后重复测量数据。具有高度相关性的双侧腮腺定量数据取双侧平均值用于统计分析。
1.4 "统计学分析
采用SPSS26.0和MedCale19.4.0软件进行统计分析。采用Shapiro-Wilk检验行正态性分析,符合正态性分布的数据以均数±标准差表示,不符合正态分布的数据以中位数(上下四分位数)表示。采用组内相关系数(ICC)分析MAGiC定量值测量的观察者内及观察者间一致性,ICClt;0.5表示一致性较差,0.5≤ICC≤0.75为一致性中等,ICCgt;0.75为一致性较好。SS组与HC组双侧腮腺MAGiC各定量值相关性检验比较,符合正态分布采用Pearson检验,不符合正态分布采用Spearman检验。SS组与HC组MAGiC各定量值差异比较,符合正态分布采用独立样本t检验,不符合正态分布采用Wilcoxon秩和检验。将MAGiC定量值差异具有统计学意义的计数资料绘制ROC曲线,采用Z检验比较曲线下面积(AUC),并评估MAGiC各定量值联合对SS的诊断效能。以Plt;0.05为差异有统计学意义。
2 "结果
2.1 "MAGiC定量参数一致性比较
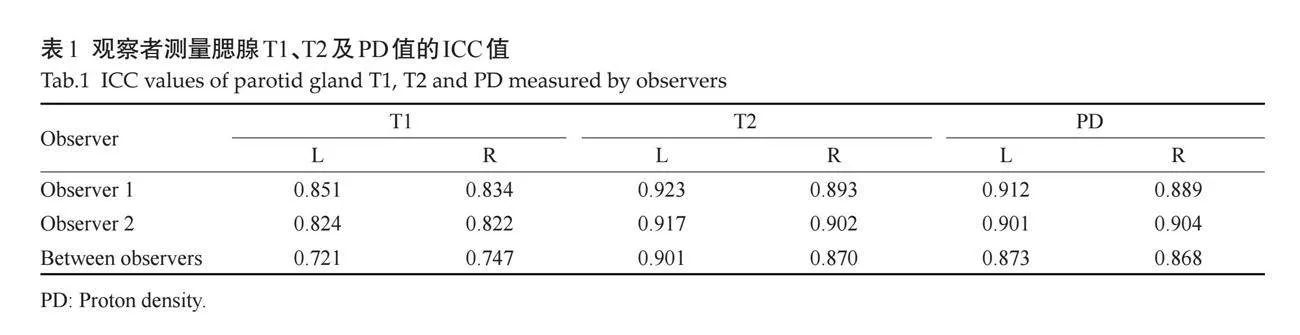
双侧腮腺T2、PD值的ICC均gt;0.800,双侧腮腺T1值最低,但ICC均gt;0.700(表1)。
2.2 "SS组与HC组双侧腮腺MAGiC各定量值相关性分析
双侧腮腺两组间MAGiC各定量值均具有高度相关性(r均gt;0.8),其中SS组T2定量值相关性最高 " " "(r=0.893,Plt;0.001,表2)。
2.3 "SS组与HC组间MAGiC各定量值差异比较
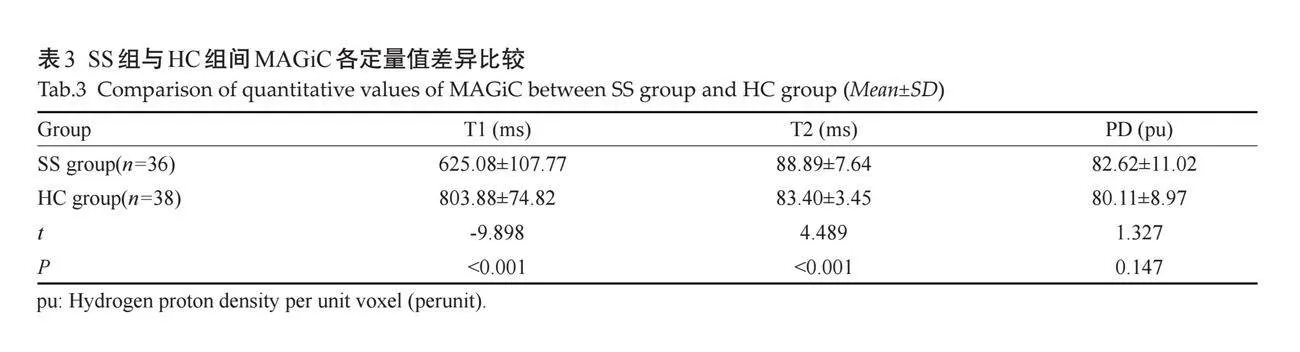
SS组与HC组腮腺T1、T2值的差异有统计学意义(Plt;0.001),PD值的差异无统计学意义(Pgt;0.05,表3)。
2.4 " 定量参数诊断SS的效能
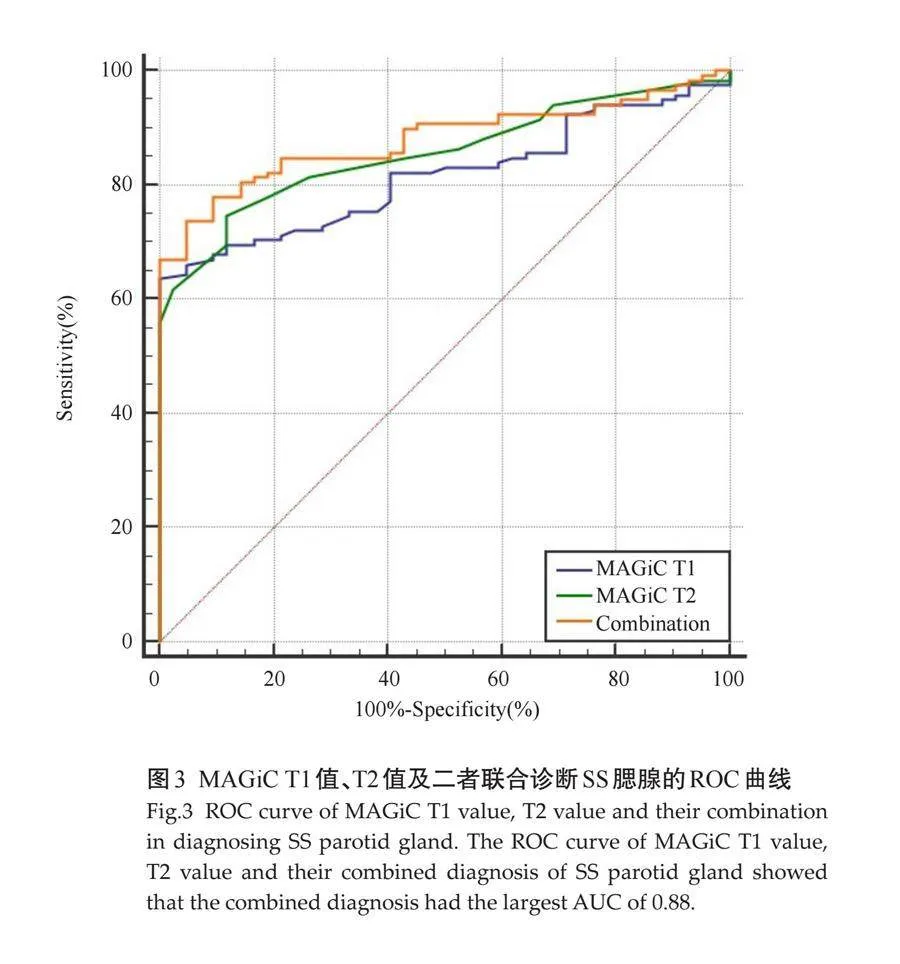
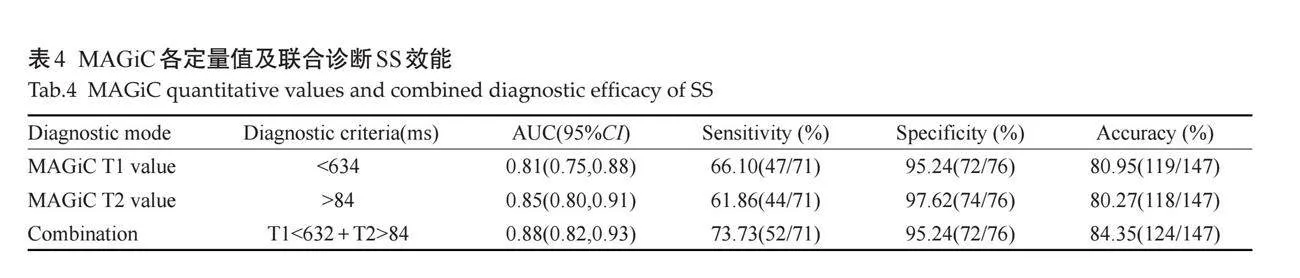
MAGiC T1与T2值联合诊断的准确率及AUC最高,其中与单纯MAGiC T1值的差异有统计学意义 " " " " " (P=0.026),与单纯MAGiC T2值的差异无统计学意义(P=0.298)。MAGiC T1与T2值的AUC之差为0.041(P=0.298),MAGiC T1与T2值的诊断价值差异无统计学意义(表4、图3)。
3 "讨论
MAGiC技术是一种基于多延迟多回波序列的新的定量扫描技术,它能够量化弛豫时间和质子密度,并通过后处理平台自动重建不同对比度和定量弛豫率图。既往研究表明,MAGIC图像在整体质量、解剖形态以及病变检测能力上与常规序列相当[11]。多参数定量能够无创、定量评估SS患者腮腺实质的状态[12-13],本研究旨在通过MAGiC成像评估SS患者的腮腺损伤。本研究发现,SS患者两侧腮腺实质之间的T1值、T2值、PD值差异无统计学意义,这提示SS患者双侧腮腺的损伤程度是一致的,推测是因为SS是一种系统性疾病,主要以干燥症状和免疫介导的腺体损伤为特征。由于SS涉及全身的免疫反应,炎症细胞不会特异性的针对某一腺体,而是累积双侧腮腺,因此患者双侧腮腺间的定量参数差异无统计学意义。
本研究中SS患者腮腺的T1值和T2值与健康志愿者间存在差异,而PD值的差异无统计学意义,这说明MAGiC序列测得的T1值和T2值能够反映SS累积的腮腺损伤。ROC曲线提示T1值和T2值在鉴别SS患者和健康志愿者的AUC值分别为0.81、0.85,但是差异无统计学意义,提示这两种参数在评价SS腮腺损伤方面具有相似的效能。T1 mapping反映的是组织的纵向弛豫时间,它是一种敏感的磁共振成像技术,用于评估组织的生物因素的物理性质。这些性质包括大分子浓度、组织的水分子含量以及脂肪含量等生物因素,它们对T1值的大小有直接影响。不同的生物因素在不同的组织类型和疾病状态下可能会发生变化,因此T1值可以反映这些生物因素的变化,且国内外目前未见T1值用于SS腮腺损伤方面的研究。本研究结果显示,SS患者腮腺实质的T1值显著高于健康志愿者。SS是一种以唾液腺浸润为特征的慢性炎症性疾病[14-17]。在SS中,唾液腺的持续性炎症会导致腺体组织的破坏和唾液腺的浸润。这种浸润过程通常伴随着腺泡的增生和腺泡细胞被脂肪浸润物所替代[18]。因此,本研究推测SS患者腮腺区T1值降低可能是因为炎症状态下,组织内的水分子可能增多,而脂肪浸润导致组织中脂肪含量的增加。这些变化可能会减少组织中的大分子浓度并影响其生物物理性质,进而导致T1值降低。
T2 mapping是一种基于多回波自旋回波序列的MRI技术,它提供了组织的T2弛豫时间信息,因此被认为是一种无创、高分辨率的定量成像方法。目前,T2 mapping已广泛应用于医学影像学领域,主要用于评估心肌损伤、肌肉病变和肝脏纤维化等多种疾病[19-21]。已有研究发现,T2值的增加是早期心肌损伤的重要迹象,可以敏感地反映心肌细胞的水肿和炎症状态;随着炎症细胞浸润的程度增加,组织的T2值也会相应地上升[22]。本研究结果显示,SS患者的T2值明显高于健康志愿者,与目前文献报道[23]一致。SS是一种以腺体炎性浸润为特征的慢性免疫性疾病,因此我们推测T2值的升高可能与SS患者腺体的淋巴细胞浸润有关,淋巴细胞是炎症反应的主要细胞类型,在SS患者的腮腺组织中常能发现淋巴细胞浸润现象,这可能是SS患者腮腺T2值增高的一个重要因素。此外腮腺实质的炎症反应可能导致组织水分子的增加和局部水肿,这些因素也可能增加T2值。综上,本研究认为SS患者腮腺T2值的升高可能是由于腮腺实质的炎症反应、组织水肿以及淋巴细胞的浸润等因素共同作用所致。这些因素反映了SS患者腮腺组织的炎症状态,也强调了T2 mapping作为一种有用的生物标志物在评估SS患者腮腺损伤中的重要性。
近年来,MRI检查技术在SS腮腺病变诊断中不断成熟,不仅可以提供常规影像学资料,还可以提供灌注、血流、定量等信息,因此在SS诊断中得到广泛应用[24-31]。但既往研究表明常规MRI及MR腺导管成像诊断SS的敏感度较低,诊断效能欠佳[32-34]。MAGiC T1、T2值对于SS腮腺损伤的诊断均具有较高的准确性,其多定量参数成像可为MRI常规成像无形态学改变提供一定的临床诊断价值。本研究结果显示以MAGiC T1、T2值联合诊断SS的准确率最高,其最佳阈值分别为MAGiC T1值632 ms、T2值84 ms。T1值可反应病变组织脂肪的存在,T2值诊断病变的水肿和炎症较常规MRI更为敏感,二者联合诊断可获得更佳的诊断SS效能,因此可以采用MAGiC技术诊断SS腮腺病变,从而提高诊断的准确性。
综上所述,尽管目前T2 mapping等定量检查技术可评估SS腮腺病变,但在不增加扫描时间基础上,MAGiC技术可一站式获取多定量数据,且T1、T2值多定量联合诊断准确率更高,可在SS患者腮腺病变诊断中推广。本研究局限性在于样本量较少,数据存在偏倚;未纳入脂肪分数等定量数据联合分析;对照组为健康对照组,但是未纳入有口干、眼干等临床症状但未被诊断为SS的疑似SS患者,因此后续有待进一步开展大样本、结合脂肪分数、扩散系数等多定量技术的研究。
参考文献:
[1] " van Ginkel MS, Glaudemans AWJM, van der Vegt B, et al. Imaging in primary sjögren's syndrome[J]. J Clin Med, 2020, 9(8): 2492.
[2] " Fox PC. Autoimmune diseases and Sjogren's syndrome: an autoimmune exocrinopathy[J]. Ann N Y Acad Sci, 2007, 1098: 15-21.
[3] " Fox RI. Sjögren's syndrome[J]. Lancet, 2005, 366(9482): 321-31.
[4] " Rao Y, Xu N, Zhang Y, et al. Value of magnetic resonance imaging and sialography of the parotid gland for diagnosis of primary Sjögren syndrome[J]. Int J Rheum Dis, 2023, 26(3): 454-63.
[5] " Jousse-Joulin S, Coiffier G. Current status of imaging of Sjogren's syndrome[J]. Best Pract Res Clin Rheumatol, 2020, 34(6): 101592.
[6] " "Ding C, Xing X, Guo Q, et al. Diffusion-weighted MRI findings in Sjögren's syndrome: a preliminary study[J]. Acta Radiol, 2016, 57(6): 691-700.
[7] " 韦洁勤, 张 "静, 陆力坚, 等. 干燥综合征腮腺导管MRS与CT及X线造影对比研究[J]. 中国临床新医学, 2015, 8(3): 193-7.
[8] " 李方正, 李 "芹, 郑召龙, 等. 合成MRI临床应用的研究进展[J]. 放射学实践, 2022, 37(3): 402-6.
[9] " "孙其安, 李 "郑, 何 "玲, 等. MAGiC技术在颈椎间盘退行性改变中的应用价值[J]. 放射学实践, 2023, 38(1): 70-5.
[10] "Shiboski CH, Shiboski SC, Seror R, et al. 2016 American college of rheumatology/european league against rheumatism classification criteria for primary sjögren's syndrome: a consensus and data‑driven methodology involving three international patient cohorts[J]. Arthritis Rheumatol, 2017, 69(1): 35-45.
[11] "崔 "峰, 王 "聪, 王 "娅, 等. MAGiC技术的基本原理及临床研究进展[J]. 临床放射学杂志, 2021, 40(12): 2434-7.
[12] "冯倩倩, 储 "晨, 王凤仙, 等. MR T2* mapping技术评估干燥综合征涎腺病变[J]. 中国医学影像技术, 2019, 35(10): 1467-71.
[13] "冯倩倩, 储 "晨, 王振伟, 等. 体素内不相干运动MR成像在诊断干燥综合征腮腺病变的应用研究[J]. 临床放射学杂志, 2020, 39(6): 1074-9.
[14] "纪权书, 丁长伟. 干燥综合征腮腺MRI的研究进展[J]. 磁共振成像, 2020, 11(4): 311-4.
[15] Zhou QQ, Zhang W, Yu YS, et al. Comparative study between ZOOMit and conventional intravoxel incoherent motion MRI for assessing parotid gland abnormalities in patients with early‑or mid-stage sjögren's syndrome[J]. Korean J Radiol, 2022, 23(4): 455.
[16] "何思慧, 张剑勇, 贾二涛. 原发性干燥综合征炎症发病机制[J]. 中国免疫学杂志, 2023, 39(12): 2679-83.
[17] "Takagi Y, Sasaki M, Eida S, et al. Comparison of salivary gland MRI and ultrasonography findings among patients with Sjögren's syndrome over a wide age range[J]. Rheumatology, 2022, 61(5): 1986-96.
[18] McCoy SS, Baer AN. Neurological complications of sjögren's syndrome: diagnosis and management[J]. Curr Treatm Opt Rheumatol, 2017, 3(4): 275-88.
[19] Módis LV, Aradi Z, Horváth IF, et al. Central nervous system involvement in primary sjögren's syndrome: narrative review of MRI findings[J]. Diagnostics, 2022, 13(1): 14.
[20] "中华医学会风湿病学分会. 干燥综合征诊断及治疗指南[J]. 中华风湿病学杂志, 2010, 14(11): 766-8.
[21] "贾斯齐, 颜春龙, 金宇华, 等. 磁共振T2 mapping技术在心脏疾病中的应用研究进展[J]. 磁共振成像, 2023, 14(6): 145-50.
[22] "曾飘娥, 周 "延, 刘剑羽. 功能MRI在肌肉损伤中的应用进展[J]. 国际医学放射学杂志, 2019, 42(2): 189-92.
[23] "金明丽, 潘志华, 蒋 "颖, 等. T2值定量评估不同肝纤维化分期大鼠肝脏铁沉积[J]. 中国介入影像与治疗学, 2022, 19(2): 110-4.
[24] "Muntean DD, Bădărînză M, Stefan PA, et al. The diagnostic value of MRI-based radiomic analysis of lacrimal glands in patients with sjögren's syndrome[J]. Int J Mol Sci, 2022, 23(17): 10051.
[25] "冯倩倩, 储 晨, 王凤仙, 等. T2 mapping在干燥综合征腮腺损伤早期评估中的应用[J]. 医学影像学杂志, 2020, 30(1): 27-30.
[26] "Liu SM, Chen WW, Wang M, et al. Quantitative analysis of parotid gland secretion function in Sjögren's syndrome patients with dynamic magnetic resonance sialography[J]. Korean J Radiol, 2019, 20(3): 498-504.
[27] "张 "楠, 刘 "辉, 乔 "薇, 等. 唾液腺超声评分联合核素显像对干燥综合征具有较高的诊断价值[J]. 分子影像学杂志, 2022, 45(3): 323-9.
[28] "邢晓菲, 丁长伟. 酸刺激前后扩散加权成像评价干燥综合征患者腮腺功能[J]. 中国临床医学影像杂志, 2016, 27(10): 706-9.
[29] Ogura I, Sasaki Y, Oda T, et al. Magnetic resonance sialography and salivary gland scintigraphy of parotid glands in sjögren's syndrome[J]. Chin J Dent Res, 2018, 21(1): 63-8.
[30] Su GY, Xu XQ, Wang YY, et al. Feasibility study of using intravoxel incoherent motion MRI to detect parotid gland abnormalities in early‑stage Sjögren syndrome patients[J]. Magn Reson Imaging, 2016, 43(6): 1455-61.
[31] "Kami YN, Sumi MS, Takagi Y, et al. Arterial spin labeling imaging for the parotid glands of patients with sjögren's syndrome[J]. PLoS One, 2016, 11(3): e0150680.
[32] Ren YD, Li XR, Zhang J, et al. Conventional MRI techniques combined with MR sialography on T2‑3D‑DRIVE in Sjögren syndrome[J]. Int J Clin Exp Med, 2015, 8(3): 3974-82.
[33] "Kojima I, Sakamoto M, Iikubo M, et al. Diagnostic performance of MR imaging of three major salivary glands for Sjögren's syndrome[J]. Oral Dis, 2017, 23(1): 84-90.
[34] Niemelä RK, Takalo R, Pääkkö E, et al. Ultrasonography of salivary glands in primary Sjogren's syndrome. A comparison with magnetic resonance imaging and magnetic resonance sialography of parotid glands[J]. Rheumatology, 2004, 43(7): 875-9.
(编辑:郎 "朗)
