深度学习联合C-TIRADS在甲状腺4a类结节风险分层管理的应用
2024-10-30何美情张均高燕华张茜茜韩磊李艳川



摘要:目的" 探讨深度学习联合中国超声甲状腺影像报告和数据系统(C-TIRADS)在甲状腺4a类结节风险分层管理的应用。方法" 纳入陕西省人民医院2018年12月~2022年10月收治的179例甲状腺结节患者,依据病理结果分为良性组(n=76)与恶性组(n=103),所有患者均予以超声检查,按照C-TIRADS指南标准、深度学习进行观察诊断。利用多因素Logistic回归分析获取独立预测指标;利用ROC曲线评估预测变量准确性。结果" 多因素Logistic分析显示,甲状腺结节图像特征的结构、方位、边缘、回声、局灶性强回声及年龄是独立预测甲状腺结节性质的指标(Plt;0.05)。以病理结果为金标准,深度学习联合C-TIRADS与病理结果完全符合率为96.65%,Kappa值为0.932,一致性好;联合诊断甲状腺4a类结节的符合率、特异度、阳性预测值显著高于深度学习、C-TIRADS(Plt;0.05)。联合诊断疾病的敏感度、阴性预测值高于深度学习(Plt;0.001),但与C-TIRADS的差异无统计学意义(Plt;0.05)。ROC曲线分析显示,C-TIRADS、深度学习及联合诊断的AUC分别为0.873、0.819、0.967;与Az=0.5相比,差异有统计学意义(Plt;0.001)。结论" C-TIRADS在甲状腺4a类结节风险分层管理中敏感性较高,结合深度学习辅助诊断能够准确进行甲状腺结节良恶性鉴别,具备较高诊断效能。
关键词:甲状腺结节;中国超声甲状腺影像报告和数据系统;深度学习;恶性风险;指南;诊断
The application of deep learning combined with C‑TIRADS in the risk stratification management of thyroid nodules classified as 4a
HE Meiqing1, ZHANG Jun1, GAO Yanhua1, ZHANG Xixi1, HAN Lei1, LI Yanchuan2
1Department of Ultrasound, 2Department of Obstetrics, Shaanxi Provincial People's Hospital, Xi'an 710068, China
Abstract: Objective To explore the application of deep learning combined with the Chinese thyroid imaging reporting and data system (C-TIRADS) in the risk stratification management of thyroid nodules classified as 4a. Methods A total of 179 patients with thyroid nodules treated at Shaanxi Provincial People's Hospital from December 2018 to October 2022 were included, divided into benign (n=76) and malignant groups (n=103) based on pathological results. All patients underwent ultrasound examination and were diagnosed using C‑TIRADS guidelines and deep learning. Multiple factor Logistic regression analysis was used to obtain independent predictive indicators; the accuracy of predictive variables was assessed using the ROC curve. Results Multiple factor Logistic analysis showed that the structural, directional, edge, echo, focal strong echo, and age characteristics of thyroid nodule images are independent indicators for predicting the nature of thyroid nodules (Plt;0.05). With pathological results as the gold standard, the complete consistency rate of deep learning combined with C-TIRADS with pathological results was 96.65%, and the Kappa value was 0.932, indicating good consistency; the consistency rate, specificity, and positive predictive value of the combined diagnosis for thyroid nodules classified as 4a were significantly higher than those of deep learning and C‑TIRADS (Plt;0.05). The sensitivity and negative predictive value of the combined diagnosis for the disease were higher than those of deep learning (Plt;0.001), but the difference with C‑TIRADS was not statistically significant (Pgt;0.05). ROC curve analysis showed that the AUCs for C‑TIRADS, deep learning, and combined diagnosis were 0.873, 0.819, and 0.967, respectively; compared with Az=0.5, the differences were all statistically significant (Plt;0.001). Conclusion C-TIRADS has a high sensitivity in the risk stratification management of thyroid nodules classified as 4a, and combined with deep learning for auxiliary diagnosis, it can accurately distinguish between benign and malignant thyroid nodules, with high diagnostic efficacy.
Keywords: thyroid nodules; Chinese thyroid imaging reporting and data system; deep learning; malignant risk; guidelines; diagnosis
甲状腺结节属于常见甲状腺疾病,发病率为19%~67%,且伴随1%~2%的甲状腺癌发病率,常为甲状腺乳头状癌[1-2] 。其恶性结节较为少见,但一旦延误诊治可能发生转移进展,故甲状腺结节病理性质鉴别尤为重要。随着超声设备持续改进,甲状腺结节检出率显著增加,其良恶性鉴别也得到了临床普遍关注[3]。现阶段国内外已发布多项指南,2009年一项研究提出了甲状腺影像报告和数据系统(TIRADS),有利于提高超声鉴别诊断效能[4]。随后韩国学者提出的K-TIRADS[5]、美国放射学会(ACR)提出的ACR-TIRADS[6]相继出现,ACR-TIRADS影响较大,不过分类设计参数、评分足23个,应用相对不方便。中文版TIRADS(C-TIRADS)[7]由2020年中国专家委员会公布,其临床应用尚未普及,但应用较为便捷,涉及的基本参数为6个,有助于提高医师工作效率。研究显示,C-TIRADS可能是一种临床上适用于诊断甲状腺结节的工具[8]。诸多研究结果更证明了C-TIRADS在甲状腺结节中诊断价值较高[9-11]。但甲状腺结节超声图像会表现出边缘模糊、形状不规则、钙化点阴影等问题,图像质量易受到回声干扰与斑点噪声影响,以致诊断结果具有主观差异性,受限于医师临床经验。深度学习在医学图像领域占据重要地位,可直接提取原始数据中有用特征进行学习,能够计算样本数据层次特征,生成较高层次抽象特征;且在超声图像领域中,基于卷积神经网络的结节分类模型相较于深度置信网络更为成功,可应用于超声图像甲状腺结节良恶性鉴别[12]。既往研究发现,C-TIRADS联合人工智能可有效鉴别诊断甲状腺结节,准确性相对较高[13]。但其尚未分析深度学习、C-TIRADS及联合诊断与病理结果的一致性,且未突出深度学习在甲状腺4a类结节诊断中效能分析。为进一步提高疾病诊断准确性,本研究旨在与病理结果对照,评估深度学习联合C-TIRADS在甲状腺4a类结节风险分层管理中效能分析,比较联合诊断与单一诊断的检出情况,从而探讨两者对疾病的诊断价值。
1" 资料与方法
1.1" 一般资料
纳入陕西省人民医院2018年12月~2022年10月收治的179例甲状腺结节患者,依据病理结果分为良性组(n=76)与恶性组(n=103)。179例患者中,女性125例,男性54例,年龄21~78(48.17±12.62)岁。纳入标准:经手术切除得到确切病理学结果;经影像学评估为甲状腺4a类结节;病理资料全。排除标准:既往存在甲状腺相关有创操作史者;影像学图像不完整或缺失者;合并甲状腺功能亢进者;病理结果不明确;临床资料不全。本研究获得医院伦理委员会批准[审批号:2024伦审第(R083号)]。
1.2" 方法
1.2.1" 超声检查" "采用RS80A超声诊断仪,受检者取仰卧位,嘱咐其暴露颈部,以枕垫肩,再行超声观察,频率为3~12 MHz。于甲状腺体表处放置探头,L3-12A线阵探头。记录结节位置、形态、大小与回声、边界、成分等。选取并储存能够反映典型病变特征的图像。
1.2.2" C-TIRADS指南" "由2位医师观察图像,根据C-TIRADS指南予以分类,如结果不一致,需进行共同讨论。该指南中超声特征涉及5个阳性指标,依次为实性、可疑微钙化、垂直位、极低回声、不规则/边界模糊/甲状腺外侵犯。以及彗星尾伪像的1个阴性指标,阳性指标分别赋值1分,阴性指标赋值-1分,合计结节各类超声特征即为总分。其中5分为C-TIRADS 5,恶性率gt;90%,高度恶性;3~4分为C-TIRADS 4c,恶性率为50%~90%,高度可疑恶性;2分为C-TIRADS 4b,中度可疑恶性,恶性率10%~50%;1分为C-TIRADS 4a,低度可疑恶性,恶性率2%~10%;0分为C-TIRADS 3,恶性率lt;2%,可能良性;-1分为C-TIRADS 2,恶性率为0,良性;无结节为C-TIRADS 1;经活检证实恶性的结节为C-TIRADS 6。
1.2.3" 深度学习" "图像选取和处理:从超声数据库中选取3562张甲状腺图像,图像要求包括:存在正常甲状腺组织供对照;同一视角、同一区域图像中,选择代表性的图像;甲状腺结节图像完整、清晰;图像中无血流信号叠加;甲状腺结节病理诊断明确。得到超声图像后予以深度学习模型训练,分为原始训练集、验证集、测试集。预处理期间,裁剪图像外部分,并转为灰度图像,裁剪至224×224像素,由1位医师标注图像中甲状腺结节位。
数据增强:原始训练集含恶性结节图像、良性结节图像,其中良性结节图像较多,可对恶性结节予以数据重采样,以扩充训练集,确保数据集平衡,采样率为1:1。
神经网络模型:因在学习数据充足时,卷积神经网络表现相对稳定,且为人工智能识别领域重要技术,可用于本研究甲状腺结节图像分类。基于U型卷积神经网络,对图像中任一像素进行区别,再通过设置训练集、验证集,对病变图像进行自动提取,针对性观察图像中关键特征,获取结节分类结果,最后对人工智能评估结果进行统计分析。
1.2.4" 深度学习联合C-TIRADS" "根据C-TIRADS指南标准对甲状腺结节进行分类,后按照深度学习所获取的诊断结果,将诊断为“可能恶性”的分类上调1级,将诊断为“可能良性”的分类下调1级,C-TIRADS 5类不再上调,C-TIRADS 2类不再下调。
1.3" 统计学分析
采用SPSS26.0进行统计学分析。计量资料以均数±标准差表示,组间比较采用t检验;计数资料用n(%)表示,组间比较采用χ2检验;利用多因素Logistic回归分析获取独立预测指标;以病理结果为金标准,利用ROC曲线评估预测变量准确性;利用Kappa进行一致性分析;以Plt;0.05为差异有统计学意义。
2" 结果
2.1" 两组基本资料对比
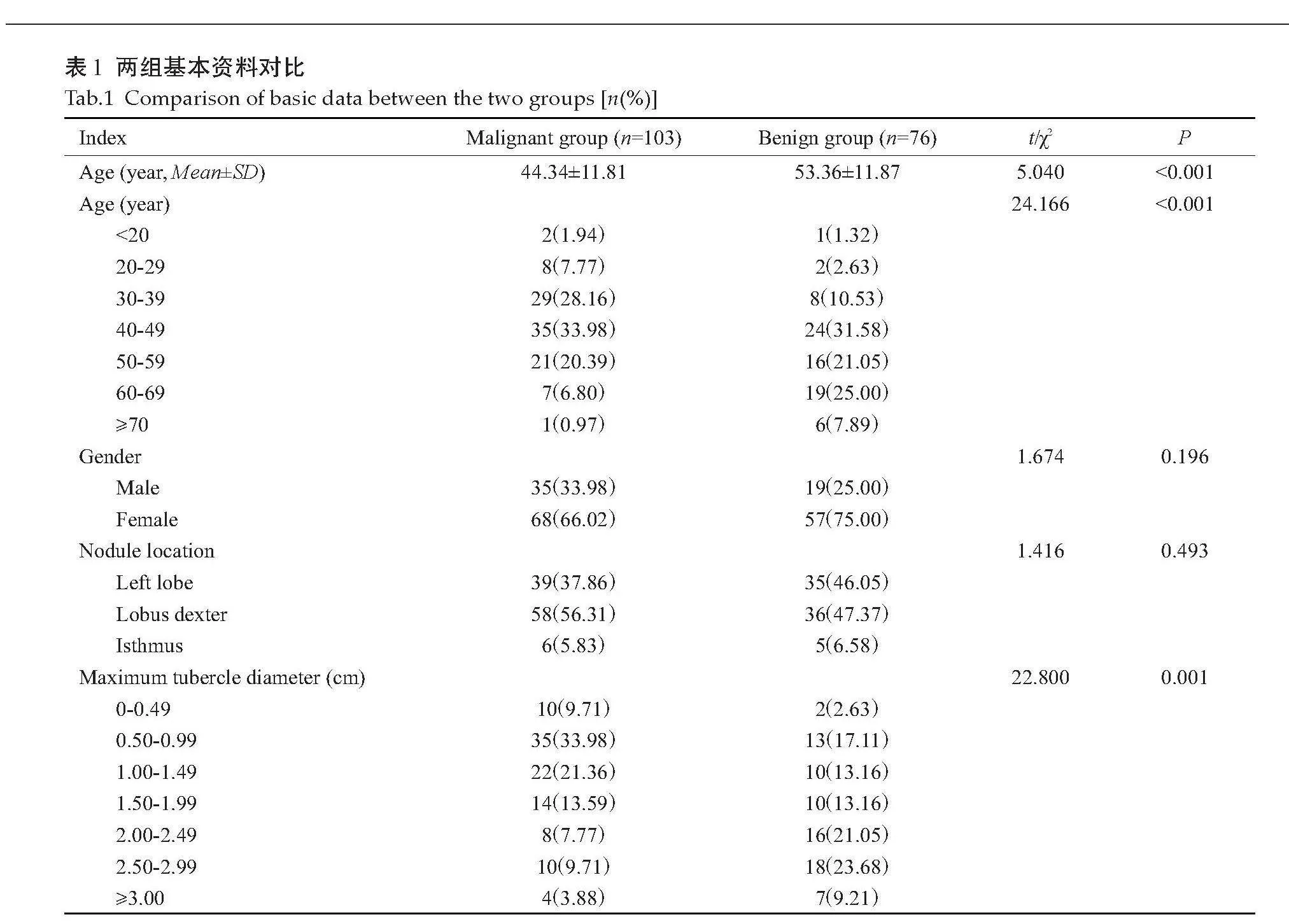
恶性组年龄、结节最大径与良性组的差异有统计学意义(Plt;0.05);恶性组性别、结节部位与良性组的差异无统计学意义(Pgt;0.05,表1)。
2.2" 两组甲状腺结节图像特征对比
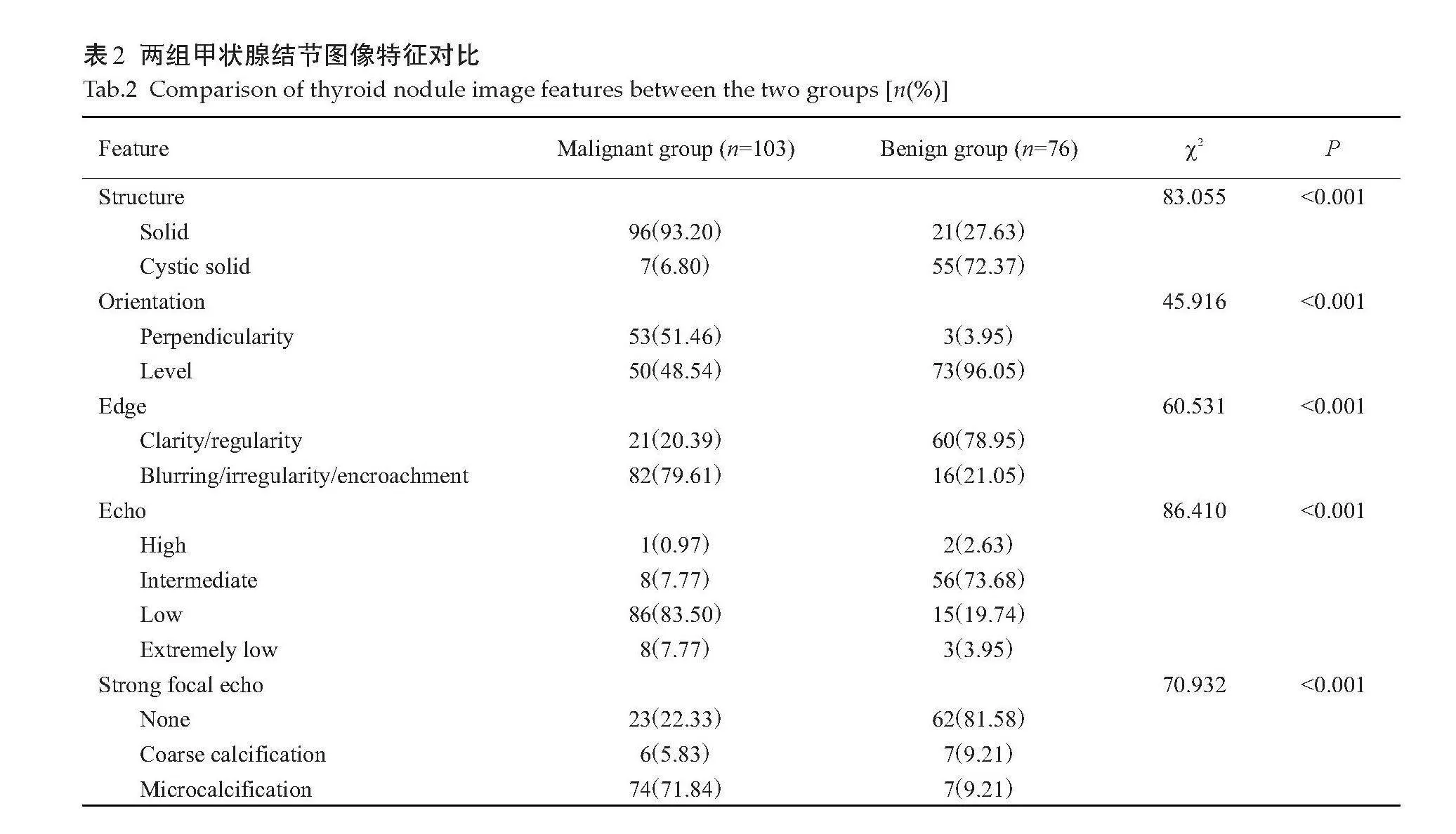
恶性组图像特征的结构、方位、边缘、回声、局灶性强回声与良性组比较,差异均有统计学意义(Plt;0.001,表2)。
2.3" Logistic回归分析独立预测指标
甲状腺结节图像特征的结构、方位、边缘、回声、局灶性强回声及年龄是独立预测甲状腺结节性质的指标(Plt;0.05,表3)。
2.4" 深度学习及C-TIRADS诊断甲状腺4a类结节的测定结果
C-TIRADS与病理结果完全符合率为87.71%(157/179),Kappa=0.748,一致性良好;深度学习与病理结果完全符合率为81.01%(145/179),Kappa=0.622,一致性良好;深度学习联合C-TIRADS与病理结果完全符合率为96.65%(173/179),Kappa=0.932,一致性好。C-TIRADS诊断甲状腺4a类结节的符合率与深度学习的差异无统计学意义(P=0.081);深度学习联合C-TIRADS诊断甲状腺4a类结节的符合率高于深度学习(Plt;0.001)和C-TIRADS(P=0.002,表4)。
2.5" 深度学习及C-TIRADS诊断甲状腺4a类结节的结果比较
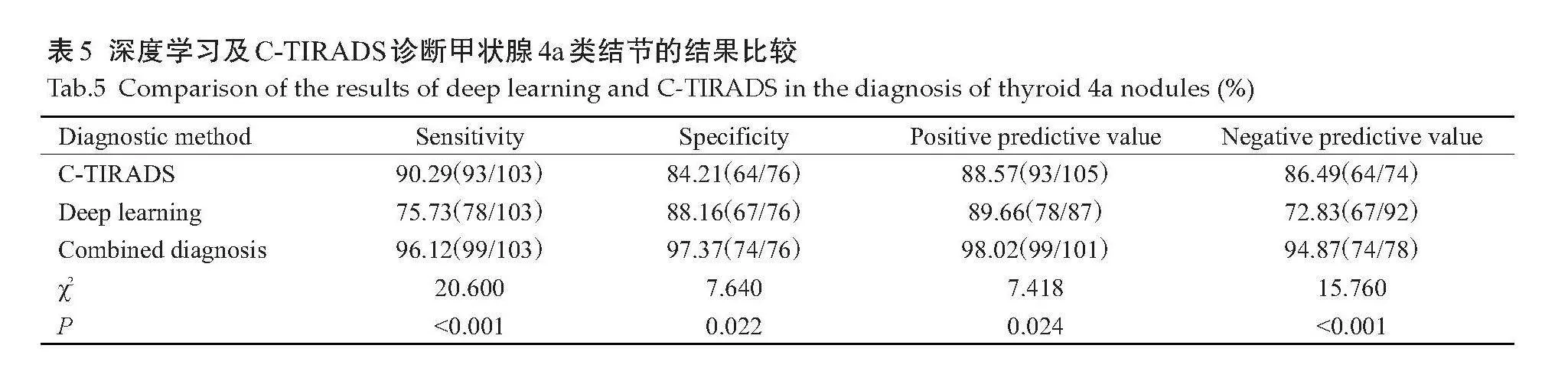
深度学习联合C-TIRADS诊断甲状腺4a类结节的敏感度、阴性预测值高于深度学习(Plt;0.001),但与C-TIRADS的差异无统计学意义(Pgt;0.05);联合诊断疾病的特异度、阳性预测值高于深度学习、C-TIRADS(Plt;0.05,表5)。
2.6" 深度学习及C-TIRADS诊断甲状腺4a类结节的诊断效能分析
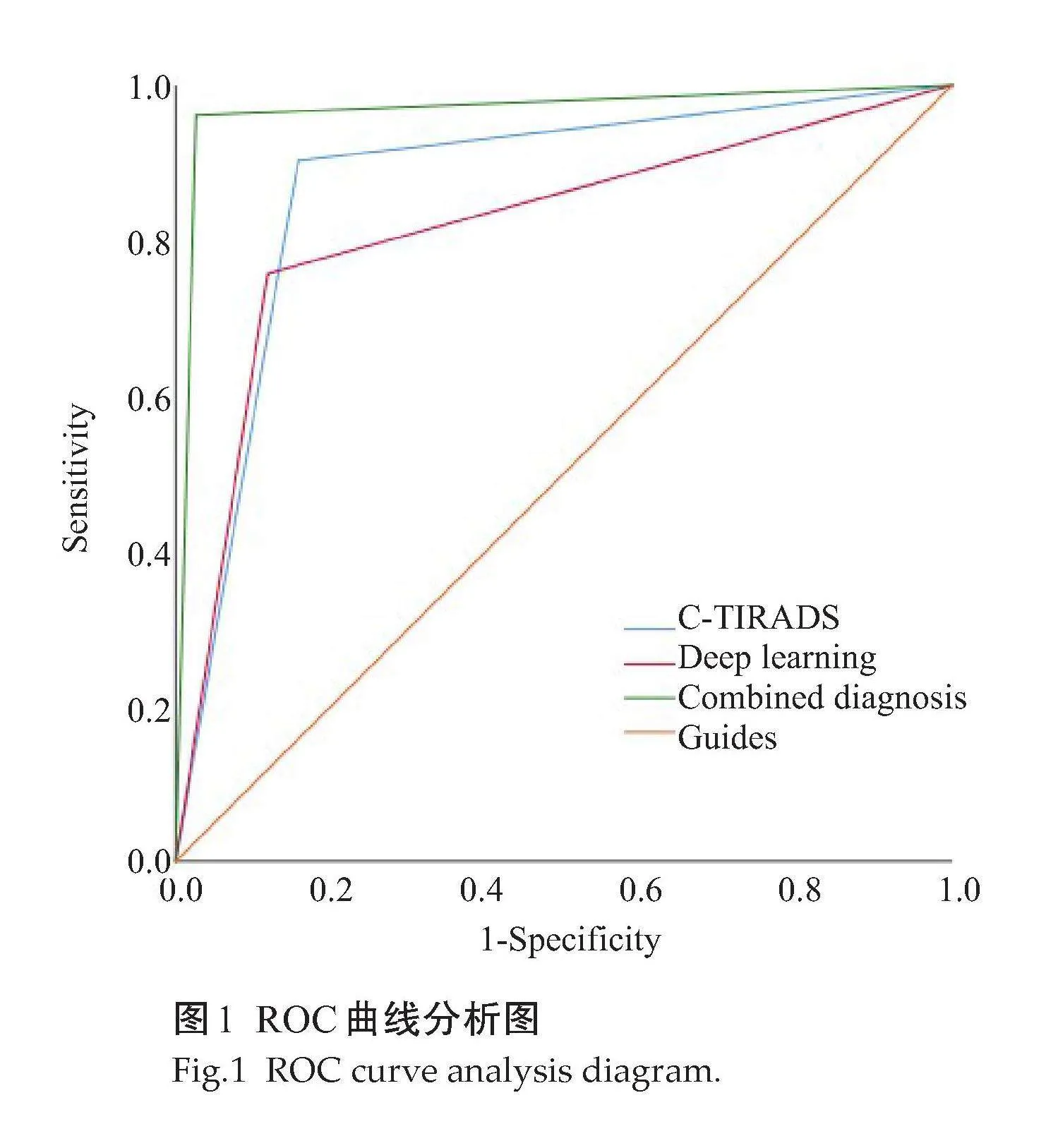
C-TIRADS、深度学习及联合诊断的AUC分别为0.873、0.819、0.967;与Az=0.5相比,均有统计学意义(Plt;0.001,表6、图1)。
2.7" 病例分析
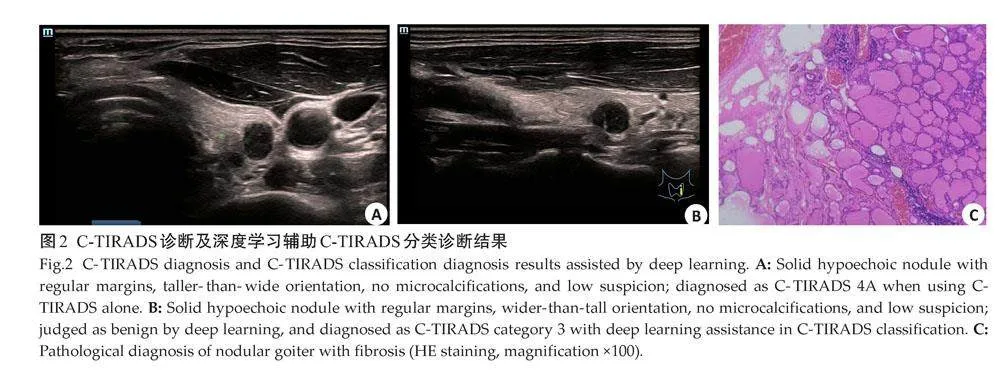
患者男性,48岁,病理诊断为结节性甲状腺肿伴纤维化。单独应用C-TIRADS诊断为C-TIRADS 4a,属于低度可疑恶性,后联合深度学习所获取的诊断结果,进行再次分类。深度学习判断为良性,深度学习辅助C-TIRADS分类诊断为C-TIRADS 3类,提示两者联合后诊断为可疑恶性的甲状腺结节数量减少(图2)。
3" 讨论
C-TIRADS综合了甲状腺结节超声诊断的国际标准,其最佳诊断点为4a,相较于K-TIRADS、ACR-TIRADS更为简便、实用,且准确度、敏感度均最高,可靠性更强,整体诊断价值较好。这可能是因K-TIRADS主要针对1.0 cm以上结节,对于1.0 cm以下结节研究较少,存在一定局限性;ACR-TIRADS可显示恶性分层中加权意义,但分类设计参数较多,多分类间易有重叠,计算内容增加,易出现归类困惑的现象,存在临床应用不便的问题[14]。也有研究指出,C-TIRADS涉及5个恶性征象,由危险分层与超声特征间联系所得[7]。其计分方法为按项计数,无复杂权重计算,恶性特征相同类别仅赋予1分,操作相对简化,能减少诊断医师评分时间。以上均提示C-TIRADS在甲状腺结节恶性危险分层中表现良好,具有较高诊断效能[15-17]。
本研究多因素Logistic回归分析显示:甲状腺结节图像特征的结构、方位、边缘、回声、局灶性强回声及年龄是独立预测甲状腺结节性质的指标。其原因为:(1)结构:C-TIRADS选择实性为恶性指标,其相较于低回声敏感度更高,属恶性征象之一。如存在囊实混合回声,且以实性为主,提示其存在微钙化,血流信号丰富,故还需观察囊实性结节实性部分的钙化、回声、血流情况等特征,高度警惕其恶性可能。(2)方位、边缘:垂直位包括纵切面、横切面任一切面表现出垂直位,相较于单一切面敏感度和准确性更高,而边缘模糊/不规则/甲状腺外侵犯作为C-TIRADS认可的恶性指标,特异度较高,均具备恶性风险预测价值[18-19]。但关于C-TIRADS是否将边缘模糊、垂直位纳入危险因素,仍存在争议[20-22],尚需进一步验证。(3)回声:C-TIRADS恶性征象之一不涉及低回声,仅为极低回声,可能因恶性结节纤维组织增生明显,声阻抗差改变较大,恶性风险增加,导致回声更低[23]。本研究恶性结节中低回声占比高达83.50%,应需重视。(4)局灶性强回声:恶性结节较为牢靠的恶性征象之一包含微钙化[24],特异性较高,但与结节无关的微钙化样也需注意,亦有恶性可能。另有研究表明:年长患者甲状腺结节恶性概率相较于年轻者更低[25],这与本研究结果类似,提示年龄结合甲状腺结节图像特征对于初步评估甲状腺结节性质具有一定价值。然而甲状腺结节于C-TIRADS 4a类中仍发现重叠交叉的图像,尚存在一定的诊断困难[26]。
目前,以深度学习为主的人工智能鉴别诊断快速发展中[27],在医学领域越来越受到重视,适用于解决大数据问题[28]。其能够用于超声甲状腺结节诊断,通过卷积神经网络对图像进行深度学习、建模、训练、客观定量分析,拥有良好的诊断性能[29]。有研究回顾性收集超声图像6321张,将其投入深度学习模型,予以验证和训练,结果显示深度学习诊断甲状腺结节的敏感度及特异度较高,图像诊断时间极短,未来有望应用于医学影像学,辅助超声医师行实时诊断,提高医师的诊疗效率[30]。本研究以病理结果为金标准,深度学习联合C-TIRADS诊断甲状腺4a类结节的符合率、特异度、阳性预测值显著高于深度学习、C-TIRADS;深度学习联合C-TIRADS诊断疾病的敏感度、阴性预测值显著高于深度学习,但与C-TIRADS的差异无统计学意义;ROC曲线分析显示,C-TIRADS、深度学习及联合诊断的AUC分别为0.873、0.819、0.967,与Az=0.5相比,差异均有统计学意义。有研究显示,良恶性诊断界值为4a类时,人工智能结合C-TIRADS相较于C-TIRADS准确性明显上升,为避免过度诊疗,可在确保诊断准确性的基础上大量降低细针穿刺抽吸活检[13]。本研究中C-TIRADS、深度学习及联合诊断的Kappa值分别为0.748、0.622、0.932,提示C-TIRADS、深度学习一致性良好,两者联合则能降低不同医师的诊断主观差异性,有助于提升甲状腺4a类结节诊断准确率及效率,一致性更好。但本研究深度学习模型的诊断效能相对不足,可能是由于超声图像原始数据训练集较少,后续还需收集更多图像,提高模型诊断性能,加强对模型的训练学习测试[31]。此外,本研究还存在一定局限性:深度学习模拟训练所需图像,需人工标记甲状腺结节位置,人力物力花费较大;所选恶性结节比例略高,可能出现选择偏倚,对结果造成一定影响,未来尚需多中心大样本量验证。
综上所述,C-TIRADS在甲状腺4a类结节风险分层管理中敏感性较高,结合深度学习辅助诊断能够准确进行甲状腺结节良恶性鉴别,具备较高诊断效能,可保证恶性结节得到及时治疗。
参考文献:
[1]" "Seo S, Park S, Lee DN, et al. Increased incidence of thyroid cancer in occupational radiation epidemiology: attribution to screening among radiation workers[J]. Radiat Res, 2021, 195(4): 397-400.
[2]" "董洪伟, 苗重昌, 杜" 丰, 等. 声触诊组织成像量化技术联合C-TIRADS与K-TIRADS对甲状腺结节的诊断效能比较[J]. 中南医学科学杂志, 2023, 51(5): 703-6.
[3]" " 李" 健, 殷延华, 戚建国, 等. 甲状腺结节超声恶性风险分层方法对甲状腺结节良恶性的鉴别诊断价值: 中美指南对比分析[J]. 中国全科医学, 2022, 25(9): 1077-81.
[4]" "Horvath E, Majlis S, Rossi R, et al. An ultrasonogram reporting system for thyroid nodules stratifying cancer risk for clinical management[J]. J Clin Endocrinol Metab, 2009, 94(5): 1748-51.
[5]" "Kwak JY, Han KH, Yoon JH, et al. Thyroid imaging reporting and data system for US features of nodules: a step in establishing better stratification of cancer risk[J]. Radiology, 2011, 260(3): 892-9.
[6]" "Tessler FN, Middleton WD, Grant EG, et al. Re: ACR thyroid imaging, reporting and data system (TI-RADS): white paper of the ACR TI-RADS committee[J]. J Am Coll Radiol, 2018, 15(3 Pt A): 381-2.
[7]" "Zhou JQ, Yin LX, Wei X, et al. 2020 Chinese guidelines for ultrasound malignancy risk stratification of thyroid nodules: the C-TIRADS[J]. Endocrine, 2020, 70(2): 256-79.
[8]" "Jin Z, Pei SF, Shen H, et al. Comparative study of C‑TIRADS, ACR‑TIRADS, and EU‑TIRADS for diagnosis and management of thyroid nodules[J]. Acad Radiol, 2023, 30(10): 2181-91.
[9]" "Chen QF, Lin MN, Wu SZ. Validating and comparing C-TIRADS, K-TIRADS and ACR-TIRADS in stratifying the malignancy risk of thyroid nodules[J]. Front Endocrinol, 2022, 13: 899575.
[10]" Ma Y, Huo XG, Kong SS, et al. A review about C-TIRADS, ACR-TIRADS, and K‑TIRADS combined with real‑time tissue elastography to diagnose thyroid nodules[J]. Discov Med, 2023, 35(174): 1-10.
[11]" Cai YF, Yang RX, Yang SH, et al. Comparison of the C-TIRADS, ACR-TIRADS, and ATA guidelines in malignancy risk stratification of thyroid nodules[J]. Quant Imaging Med Surg, 2023, 13(7): 4514-25.
[12]" 林" 岚, 张" 格, 吴水才. 深度学习算法在甲状腺超声图像结节良恶性分类中的应用[J]. 医疗卫生装备, 2020, 41(6): 93-8.
[13]" 李" 潜, 丁思悦, 郭兰伟, 等. 甲状腺结节超声恶性危险分层中国指南(C-TIRADS)联合人工智能辅助诊断对甲状腺结节鉴别诊断的效能评估[J]. 中华超声影像学杂志, 2021, 30(3): 231-5.
[14]" 毛" 森, 赵鲁平, 李小花, 等. 2020中国超声甲状腺影像报告和数据系统在甲状腺结节鉴别诊断中的应用价值[J]. 中华医学杂志, 2021, 101(45): 3748-53.
[15] Hu Y, Xu SY, Zhan WW. Diagnostic performance of C-TIRADS in malignancy risk stratification of thyroid nodules: a systematic review and meta-analysis[J]. Front Endocrinol, 2022, 13: 938961.
[16] Jin Z, Zhu YQ, Lei Y, et al. Clinical application of C-TIRADS category and contrast-enhanced ultrasound in differential diagnosis of solid thyroid nodules measuring ≥1 cm[J]. Med Sci Monit, 2022, 28: e936368.
[17]" Zhou Y, Li WM, Fan XF, et al. Comparing diagnostic efficacy of C-TIRADS positive features on different sizes of thyroid nodules[J]." Int J Gen Med, 2023, 16: 3483-90.
[18]" 高" 源, 邓大同, 刘" 彧, 等. 2020版C-TIRADS在甲状腺结节诊断和处理中的应用价值[J]. 安徽医科大学学报, 2022, 57(3): 497-9.
[19]" 吴秀艳, 蔡雪珍, 刘舜辉, 等. 甲状腺结节超声恶性危险分层指南对甲状腺乳头状癌的诊断价值: C-TIRADS与ATA指南比较[J]. 中国医学影像学杂志, 2024, 32(1): 34-41.
[20]" Ha EJ, Na DG, Baek JH, et al. US fine-needle aspiration biopsy for thyroid malignancy: diagnostic performance of seven society guidelines applied to 2000 thyroid nodules[J]. Radiology, 2018, 287(3): 893-900.
[21] Ramundo V, di Gioia CRT, Falcone R, et al. Diagnostic performance of neck ultrasonography in the preoperative evaluation for extrathyroidal extension of suspicious thyroid nodules[J]. World J Surg, 2020, 44(8): 2669-74.
[22]" 张" 帆, 陈" 文, 薛" 恒. 纵横比对于不同大小甲状腺乳头状癌的超声诊断价值研究[J]. 中国超声医学杂志, 2020, 36(1): 8-10.
[23]" Xu Y, Qi XJ, Zhao X, et al. Clinical diagnostic value of contrast-enhanced ultrasound and TI-RADS classification for benign and malignant thyroid tumors: one comparative cohort study[J]. Medicine, 2019, 98(4): e14051.
[24] Kim PH, Suh CH, Baek JH, et al. Diagnostic performance of four ultrasound risk stratification systems: a systematic review and meta-analysis[J]. Thyroid, 2020, 30(8): 1159-68.
[25] Kikuchi S, Takeshita T, Shibata H, et al. New evidence about thyroid cancer prevalence: prevalence of thyroid cancer in younger and middle-aged Japanese population[J]. Endocr J, 2013, 60(4): 501-6.
[26]" "张" 娜, 闫凤芝, 李" 娅, 等. 超声弹性成像联合超声引导下针吸技术在甲状腺C-TIRADS 4a类结节诊断中的应用[J]. 中国超声医学杂志, 2023, 39(9): 1066-9.
[27] Tessler FN, Thomas J. Artificial intelligence for evaluation of thyroid nodules: a primer[J]. Thyroid, 2023, 33(2): 150-8.
[28]" Li HL, Weng J, Shi YJ, et al. An improved deep learning approach for detection of thyroid papillary cancer in ultrasound images[J]. Sci Rep, 2018, 8(1): 6600.
[29] Yu X, Wang HJ, Ma LY. Detection of thyroid nodules with ultrasound images based on deep learning[J]. Curr Med Imaging Rev, 2020, 16(2): 174-80.
[30]" 王洪杰, 于" 霞, 高" 强. 基于深度学习的甲状腺结节自动识别方法在超声图像中的应用[J]. 中国医疗设备, 2019, 34(10): 72-4, 78.
[31]" 陈" 飞, 郑力基, 易小林, 等. 基于深度学习和图像融合诊断甲状腺结节良恶性的研究[J]. 广东医学, 2022, 43(8): 925-29.
(编辑:熊一凡)
收稿日期:2024-06-06
基金项目:陕西省重点研发计划项目(2023-YBSF-465);西安市科技局项目(22YXYJ0108),陕西省人民医院2023年科技发展孵化基金项目(2023YJY-75)
作者简介:何美情,副主任医师,E-mail: hemeiqing1331@126.com
通信作者:李艳川,副主任医师,E-mail: liyanchuan2008@163.com
