小儿手术前应用咪达唑仑口服溶液减少术前焦虑及术后躁动的效果
2024-05-19刘洋
刘洋


【摘要】 目的:观察手术前给予小儿咪达唑仑对术前焦虑和术后躁动的影响。方法:将2022年1月—2023年1月100例在泉州市第一医院接受手术治疗的患儿纳入研究,依照随机数字表法分为对照组和观察组,各50例。对照组术前30 min口服葡萄糖,观察组术前30 min口服咪达唑仑口服溶液。观察患儿服药前(T0)、入室前3 min(T1)、麻醉诱导后30 min(T2)的生命体征指标[心率(HR)、平均动脉压(MAP)]、术前焦虑情况[改良耶鲁术前焦虑量表(m-YPAS)]、术后躁动情况[小儿麻醉苏醒期躁动(PEAD)量表]及不良反应。结果:观察组T1、T2时的MAP和HR均较T0时均更低,T1时,观察组的MAP、HR均低于对照组,T2时,观察组的MAP、HR均高于对照组,差异均有统计学意义(P<0.05);服药后观察组m-YPAS各项评分均下降,且各项评分均低于对照组,差异均有统计学意义(P<0.05);术后,观察组PEAD各项评分均低于对照组,差异均有统计学意义(P<0.05)。结论:术前给予患儿咪达唑仑可缓解术前焦虑和术后躁动,并能提升麻醉质量,有助于稳定患儿生命体征,并且不增加不良反应发生风险。
【关键词】 咪达唑仑 小儿手术 术前焦虑 术后躁动
由于儿童身心尚未发育完全,术前焦虑一直是困扰麻醉医师和患儿家长的问题,有调查结果显示,小儿术前焦虑发生率近60%[1-2]。陌生的环境、疾病引发的不适、对治疗的恐惧、与父母分离均是术前焦虑的重要因素,焦虑情绪可导致患儿出现难以控制的哭闹、逃跑、易激惹等现象,并伴有心理应激,导致麻醉效果受到影响,增加术后并发症发生风险,例如苏醒期躁动、疼痛加剧、谵妄、睡眠障碍等,不利于术后康复[3-4]。研究显示,小儿手术前给予适当的镇静药物,可缓解患儿术前焦虑,提升麻醉质量与术后康复效果[5]。咪达唑仑是一种镇静催眠药物,具有较好的抗惊厥、抗焦虑、镇静效果,并且起效迅速,对苏醒时间影响不大,但静脉给药可能会加重患儿的抗拒心理,咪达唑仑口服溶液因添加了微甜的佐剂,更容易被患儿接受[6-7]。基于此,为进一步缓解小儿术前焦虑,提升麻醉质量,本研究将为2022年1月—2023年1月在泉州市第一医院接受手术治疗的患儿应用咪达唑仑进行术前镇静,观察其对术前焦虑、术后躁动及各阶段生命体征变化的影响,现报道如下。
1 资料与方法
1.1 一般资料
选取2022年1月—2023年1月在本院接受手术治疗的患儿100例。(1)纳入标准:①有手术适应证,择期进行手术治疗;②既往无手术史;③发育正常,无智力低下或情感障碍;④对本次研究所用药物无过敏反应。(2)排除标准:①合并神经系统疾病、凝血功能障碍、传染病;②近90 d内存在哮喘、感冒等呼吸系统疾病;③父母一方已故或父母双亡;④近1年内经历特殊事件,包括亲人过世、更换幼儿园、更换住所等。按照随机数字表法将患儿分为对照组和观察组,各50例。本研究已通过本院医学伦理委员会审批,患儿家属充分了解研究内容后自愿签署知情同意书。
1.2 方法
两组患儿术前常规检查、禁食禁水,麻醉诱导前30 min,在父母陪伴下将患儿接到手术室等候区,给予对照组患儿5%葡萄糖(生产厂家:佛山昊朗药业有限责任公司,批准文号:国药准字H20013100,规格:500 mL︰25 g)0.5 mg/kg;给予观察组患儿咪达唑仑口服溶液[生产厂家:宜昌人福药业有限责任公司,批准文号:国药准字H20213321,规格:0.2%(10 mL∶20 mg)]0.5 mg/kg,最大剂量均不超过15 mg。同时连接生命体征监测仪器,30 min后患儿与父母分离,进入手术室佩戴面罩吸氧(5 L/min),采用5%七氟烷(生产厂家:上海恒瑞医药有限公司,批准文号:国药准字H20213735,规格:120 mL)进行麻醉诱导,待呼之不应、睫毛反射消失后开放静脉通路,常規气管插管行机械通气。两组术中维持麻醉均采用七氟烷0.6~0.8 MAC,新鲜气体流量2 L/min,泵注瑞芬太尼(生产厂家:江苏恩华药业股份有限公司,批准文号:国药准字H20143315,规格:2 mg)0.1~0.3 μg/(kg·min)。
1.3 观察指标及判定标准
(1)生命体征指标:观察患儿服药前(T0)、入室前3 min(T1)、麻醉诱导后30 min(T2)的生命体征指标,包括心率(heart rate,HR)、平均动脉压(mean arterial pressure,MAP)。(2)术前焦虑:服药前、服药后15 min采用改良耶鲁术前焦虑量表(modified Yale preoperative anxiety scale,m-YPAS)评估患儿的术前焦虑程度,包括语言(1~4分)、发声(1~6分)、情感表达(1~4分)、机警状态(1~4分)、父母作用(1~4分)5个维度,分数与患儿的焦虑程度呈正相关。(3)术后躁动:从患儿苏醒后起,每5分钟通过小儿麻醉苏醒期躁动量表(pediatric anesthesia emergence delirium scale,PEAD)评估1次患儿躁动情况,共评估6次,取最高评分。PEAD包括5个条目,①服从指令;②行为有目的性;③关注环境;④不安;⑤哭闹,均采用5级评分法。(4)不良反应:记录两组患儿用药后的相关不良反应,包括头晕、恶心等。
1.4 统计学处理
本次研究所得数据均使用SPSS 23.0统计学软件完成分析。计量资料用(x±s)表示,组间比较用独立样本t检验,组内比较用配对t检验;计数资料以率(%)表示,比较用字2检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组基线资料对比
对照组:男30例,女20例;年龄3~7岁,平均(5.01±1.24)岁;体重18~35 kg,平均(25.78±3.57)kg;美国麻醉师协会(American society of anesthesiologist,ASA)分级:Ⅰ级22例,Ⅱ级28例。观察组:男32例,女18例;年龄3~8岁,平均(5.14±1.18)岁;体重17~34 kg,平均(25.12±4.01)kg;ASA分级:Ⅰ级20例,Ⅱ级30例。两组基线资料比较,差异均无统计学意义(P>0.05),具有可比性。
2.2 两组各阶段生命体征对比
两组T0时的MAP和HR比较,差异均无统计学意义(P>0.05);观察组T1、T2时的MAP和HR均较T0时更低,T1时,观察组的MAP、HR均低于对照组,T2时,观察组的MAP、HR均高于对照组,差异均有统计学意义(P<0.05);对照组T1时MAP和HR均高于T0时,T2时MAP和HR均低于T0时,差异均有统计学意义(P<0.05);两组T2时的MAP和HR均低于T1时,差异均有统计学意义(P<0.05)。见表1。
2.3 两组术前焦虑情况对比
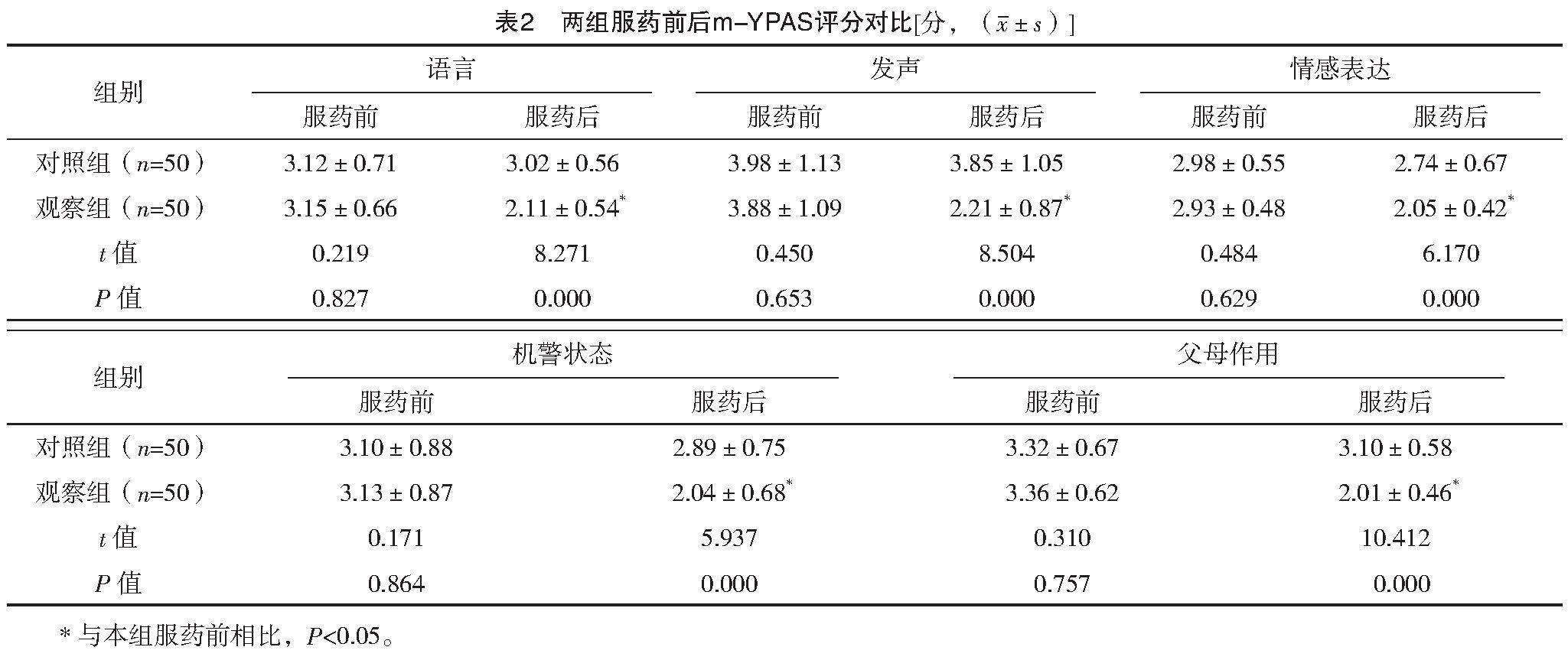
服药前,两组m-YPAS各项评分比较,差异均无统计学意义(P>0.05);服药后观察组m-YPAS各项评分均下降,且各项评分均低于对照组,差异均有统计学意义(P<0.05)。见表2。
2.4 两组术后躁动情况对比
术后,观察组PEAD各项评分均低于对照组,差异均有统计学意义(P<0.05),见表3。
2.5 两组不良反应发生情况对比
服药后,对照组患儿未出现不良反应,观察组发现有1例恶心、1例头晕,不良反应发生率为4.00%(2/50),两组对比,差异无统计学意义(字2=0.510,P=0.475)。
3 讨论
多数儿童对医院环境较为恐惧,尤其是需要与父母暂时分离的手术患儿,围手术期可能会出现更为剧烈的应激反应,在心理方面主要表现为焦虑、惊恐等,难以配合治疗,手术前患儿需独自进入手术室,易出现哭闹、挣扎甚至逃跑的情况,强烈的负性情绪会影响麻醉诱导配合度,并影响麻醉效果和手术安全性,部分患儿术后苏醒期可出现不同程度的躁动[8-10]。苏醒期躁动多表现为躁动不安、兴奋异常,多与定向障碍并存,伴有多种不恰当行为,例如无意识动作、无理性言语、哭喊、妄想等,严重者可导致意外伤害,引发不良后果,不利于术后康复[11-13]。因此,为保障手术安全和进程顺利,应在小儿术前给予相应的镇静措施,既往传统的术前镇静多采用药物注射,因患儿多对注射抱有抗拒心理,一定程度可加重术前焦虑,因此应尽量采用其他给药方式,口服具有痛苦小、起效快的特点,患儿与家长接受度较高[14-15]。
本次研究为观察组患儿应用咪达唑仑,取得较好效果。咪达唑仑是一种水溶性苯二氮?类药物,广泛用于术前镇静,其镇静、抗惊厥、抗焦虑、顺行性遗忘作用均较好,经口服给药后作用迅速。本次研究结果显示,观察组患儿T1时的MAP、HR均较对照组更低,而T2时的MAP、HR均较对照组更高(P<0.05),提示术前30 min给予患儿咪达唑仑口服液可稳定患儿生命体征,避免大幅度波动。分析原因为咪达唑仑可作用于脑干网状结构、大脑边缘系统,抑制去甲肾上腺素能神经元作用,以降低身心压力造成的肾上腺素增加,从而减轻紧张、焦虑感,因此患儿进入手术室时体征较为平稳,未见明显紧张、惊恐情绪[16]。此外,患儿术前与父母分离时易导致哭闹,可导致过度呼吸、喉痉挛等影响正常呼吸的生理反应,一定程度上会影响吸入式麻醉的效果,对心率、血压造成较大影响,不利于术中体征平稳[17]。儿童的心理承受能力较为低下,就医过程中长时间处于焦虑状态,因此会更为抗拒陌生的给药措施,既往选用的肌注、滴鼻等术前镇定方式均会引发患儿身心不适,部分患儿甚至出现强烈挣扎和逃跑的情况,既为医护人员增加了工作量,又不利于患儿治疗的顺利开展[18]。本研究结果显示,观察组患儿服药后m-YPAS评分明显下降,且明显低于对照组,推测是因为患儿对口服液的接受度较高,患儿用药过程未出现激烈情绪,有助于增强药物镇静效果。咪达唑仑口服溶液具有一定甜味,用药期间不引发惊恐情绪,尤其在术前禁食禁水后,患儿接受度普遍较高,一定程度上可以缓解其抗拒心理,对改善焦虑状态有积极影响。
术后苏醒期躁动是全麻手术常见的并发症,患儿苏醒期出现易激惹、倔强不合作、手脚挣扎乱动等情况,严重者可导致手术切口出血、引流管脱落等,而躁动时的情绪与思维障碍可长期留存在记忆中,造成精神创伤,严重者可导致术后精神障碍或人格改变[19]。术前紧张和术中机体应激反应是导致术后苏醒期躁动的危险因素,降低患儿术前焦虑程度,减小术中应激可减少术后苏醒期躁动发生风险。本研究中观察组患儿术后PEAD各项评分均低于对照组(P<0.05),提示该组患儿苏醒期躁动程度明显较轻。推测是因为患儿术前口服咪达唑仑后,焦虑程度得到明显改善,有利于提升麻醉质量,咪达唑仑可抑制神经元活动,降低神经元兴奋性,避免插管、切除病灶、改变体位等手术操作激活下丘脑-垂体-肾上腺皮质系统,降低手术应激,因此围手术期体征较为平稳,有助于减少术后躁动[20]。在本次研究中,观察组仅2例患儿发生头晕、恶心的不良反应,且程度较轻,未影响治療顺利进行,与对照组比较差异无统计学意义(P>0.05),提示术前采用咪达唑仑口服液安全性良好。
综上所述,为行手术治疗的患儿术前应用咪达唑仑口服溶液,可有效降低术前焦虑,有助于稳定患儿生命体征,减少术后躁动发生风险,并且安全性有保障。
参考文献
[1]吕真洁,朱晓琳,王珊,等.基于mYPAS的学龄前患儿术前焦虑特征的潜在类别分析[J].全科护理,2022,20(17):2418-2422.
[2]黄丹辉,王远胜,黄俊伟,等.全麻下腹腔镜小儿手术苏醒期躁动发生危险因素分析[J].医学理论与实践,2020,33(22):3800-3801.
[3]周思易,徐韬,卞勇,等.口服咪达唑仑复合经鼻艾司氯胺酮用于小儿术前镇静的ED90及临床效果[J].国际麻醉学与复苏杂志,2022,43(6):596-600.
[4]冯雨.右美托咪定和咪达唑仑对小儿静脉吸入复合麻醉苏醒期躁动的影响[J].中外医学研究,2020,18(1):43-45.
[5]孙东燕,姜雪丽,刘清兰,等.术前镇静治疗在小儿短小手术的效果观察[J].中国社区医师,2021,37(27):67-68.
[6]伍金红,李文献,吕培培,等.口服和静脉注射咪达唑仑用于小儿术前镇静的效果分析[J].国际麻醉学与复苏杂志,2021,42(5):487-490.
[7]王丽娟.咪达唑仑滴鼻在小儿疝气手术七氟烷麻醉中的应用[J].中国民康医学,2019,31(1):67-69.
[8]侯丕红,李金生,颜玲玲.右美托咪定与咪达唑仑术前滴鼻对腺样体切除术患儿术前镇静和苏醒期躁动的影响[J].山西医药杂志,2019,48(1):53-56.
[9]姚圣杰,王敏燕,王蛮蛮.右美托咪定滴鼻镇静麻醉在配合小儿心脏超声检查中的应用[J].中国妇幼保健,2020,35(3):568-570.
[10]吴雄志,王宣,徐四七,等.咪达唑仑口服溶液比右美托咪定喷鼻更有效缓解儿童术前焦虑[J].中国临床药理学与治疗学,2023,28(6):666-670.
[11]胡先平,宮庆娟,郭冠东.右美托咪定滴鼻应用于小儿全身麻醉对苏醒期躁动的影响[J].现代中西医结合杂志,2019,28(11):1225-1227.
[12]徐净.氟比洛芬酯复合咪达唑仑口服液减少小儿OSAHS手术后苏醒期躁动的临床观察[J].贵州医药,2022,46(9):1397-1398.
[13]王瑞玉,张奉超,杜冰,等.预先静脉给予咪达唑仑对全麻手术患儿术后不良行为改变的改善作用观察[J].山东医药,2021,61(18):65-68.
[14]李玉梅,郑雪松,张燕飞.右美托咪定与咪达唑仑对小儿麻醉苏醒期躁动影响的研究[J].中国卫生标准管理,2021,12(14):111-114.
[15]赵丹.咪达唑仑与氟比洛芬酯对全麻苏醒期躁动及疼痛改善疗效的比较[J].山西卫生健康职业学院学报,2021,31(3):81-83.
[16]蓝海燕.咪达唑仑联合艾司氯胺酮口服对小儿术前镇静的影响:一项随机对照双盲试验[D].温州:温州医科大学,2021.
[17]王延庆.观察咪达唑仑、右美托咪定对七氟醚全身麻醉术后躁动的作用[J].中国医药指南,2020,18(5):163-164.
[18]吕娜.右美托咪定与咪达唑仑对小儿泌尿外科手术麻醉效果和血流动力学的影响比较[J].空军医学杂志,2019,35(1):60-64.
[19]贾苗,吴小乐,范从海,等.不同剂量右美托咪定与咪达唑仑滴鼻在小儿腺样体切除术中的应用效果[J].广西医科大学学报,2019,36(11):1801-1805.
[20]廖小杰,王向东.右美托咪定和咪达唑仑对小儿静脉吸入复合麻醉苏醒期躁动的影响观察[J].中国医学创新,2021,18(6):165-168.
