核心素养导向下“5E教学模式”在高中化学教学中的应用
2024-04-21张磊
摘 要:5E教学模式是以学生综合能力培养为核心的教学模式之一,将其引入高中化学课堂教学,对于教学模式的创新有促进作用.文章据此对5E教学模式内涵进行了介绍,论述了其在课堂当中的实践应用策略.
关键词:核心素养;5E教学模式;高中化学
中图分类号:G632 文獻标识码:A 文章编号:1008-0333(2024)03-0090-03
5E教学模式的应用重点在于对学生探究意识、归纳能力、合作交流能力的培养,通过导入、探究、解释、迁移、评价5个环节实施教学流程,为学生营造探究学习环境,有助于其化学核心素养的提升.研究5E教学模式在化学课堂中的应用具有现实意义[1].
1 5E教学模式介绍
所谓5E教学模式,就是将教学过程分为5个阶段:第一,引入阶段,为学生创设熟悉的学习环境,激发其求知欲望;第二,探究阶段,要求学生将已有知识作为基础,根据学生身心发展规律,为其设置合作学习活动,引领学生主动参与学习过程,培养其动手和动脑能力;第三,解释阶段,由教师对证据、结论二者之间关系进行解释,增强学生整理信息、归纳总结和表达能力;第四,迁移阶段,也是分析结果和结论应用阶段,有助于学生举一反三能力的培养;第五,评价阶段,要求学生探究学习过程,设置差异化实验方案,选择不同的实施路径,获得学习结论.教师利用评价环节,引导学生之间互相学习和交流.在以上5个环节的应用之下,打造一体化化学课堂,辅助学生探究学习,以学生为中心,突出其对知识的主动建构能力培养,完成课程标准的要求.
2 核心素养下5E教学模式在高中化学教学中的应用策略
2.1 应用于基础理论讲解
对于电化学领域当中的知识和生活当中的电镀、氯碱工业的相关内容,教师在课堂上运用5E教学模式,可以带领学生利用变换电极的方式,对电解原理进行探究,渗透电解氯化钠溶液、电镀铜等实验,结合电解池构成条件、离子放电顺序等展开教学.
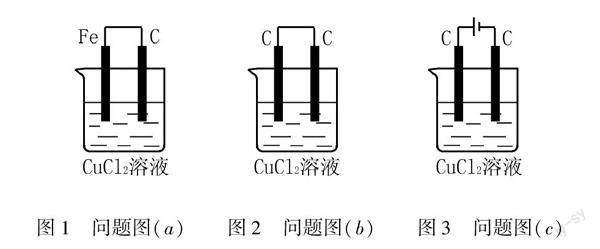
第一,引入教学.笔者利用信息技术展示图片,提出问题:“图1当中装置名称是什么?装置能量转化形式是什么?”“如图2所示,若将铁棒换成石墨棒,是否会有电流产生?尝试说明理由?”“如图3所示,如果电解质溶液、电极不改变情况之下,连接电源以后会有怎样的现象出现?能量转化是怎样的?”导入环节创设实验情境,抛出系列问题,鼓励学生积极思考,根据学生的回答,教师将理论知识引入课堂[2].和电源的负极连接的碳棒叫做阴极,和正极连接的碳棒为阳极.随后抛出探究问题:“若将条件更改,将碳更换成铁会有怎样现象出现?”
第二,探究教学.教师可以为学生提供实验所需装置和药品,鼓励学生参与实验探究,观察实验现象,总结结论.某学生在探究过程当中发现两个电极都是铁,质量相等,CuCl2溶液为电解质,没有电源时,实验过程两极会析出红色固体,在实验以后将电极取出,待其干燥以后称量,可以看出阴阳极质量
相等.另一学生发现两个电极都是铁,质量相等,CuCl2溶液为电解质,且有电源的情况下,阴极析出红色固体,实验后将电极取出,待干燥后称量,阴极的质量增大,阳极质量减小.
第三,解释阶段.学生给出结论内容如下:针对前者,两个电极都参加了反应,由于电池并非原电池,加上两极材料相同,红色固体的析出原因是铁和氯化铜溶液之间发生反应;针对后者,阳极铁棒参加反应.此时学生可能产生疑惑:“反应过程都存在电解质溶液和电源,但是阴极和阳极现象不同,是否为电极材料原因?”对此,教师及时给予解释:“无论是石墨,还是金,又或者铂都属于惰性电极,电极本身不会参加反应,由于阴极周围有铜离子,因此能够析出铜单质,导致阴极质量增加;对比而言,铜、铁、铝则属于活性电极,本身也会参与反应,阳极质量减小”.学生深度思考以后,可能还会存在疑问:“以上实验现象由于电极材料差异,导致反应现象不同,那电解质溶液不一样的时候,反应现象是否也会不同?”继续探究阶段,将两极使用质量相同的石墨,利用NaCl溶液作为电解质,向其中添加适量酚酞,阴极会出现无色无味的气体,将其收集以后并点燃,火焰为淡蓝色,在上方罩干燥烧杯,内壁有水珠生成,阴极溶液变红,阳极产生有刺激性气味的气体,能够使湿润碘化钾试纸变蓝.对于实验现象进行解释,说明反应过程形成了碱性物质、氢气和氯气,水电离出氢离子,最后变成氢气,氢氧根有剩余.若将电解质溶液变为Na2SO4溶液,剩余操作和以上相同,阴极的反应现象也和学生描述情况相同,阳极产生气体,能够使带火星木条复燃.电解质溶液改变以后,有氢气和氧气生成,氢离子和氢氧根源自水.最后教师要求学生根据阳极放电的顺序,判断出阳极活性最大,氯离子次之,之后是氢氧根和硫酸根,阴极的放电顺序表明铜离子的活性高于氢离子,高于钠离子.
第四,迁移阶段.由教师提问:“水为弱电解质,为了增强其导电性,是否可以经常向其中加入Na2SO4或者NaCl?”激发学生思考,学生根据所学知识,结合放电顺序,了解Na2SO4溶液的电解实质是电解水,反应原理不变;但是电解NaCl溶液,就会产生氯气,电解原理发生变化.
第五,评价阶段.教师组织学生进行自主评价、小组互评,相互交换意见,随后设计铁上镀铜实验,检验学生对于化学理论的掌握情况[3].
教学过程中围绕电化学领域理论讲解需求,设置化学实验,将电极材料、电解液等更换,组织学生参与探究学习.经过观察现象,产生疑问,在教师的引领下循序渐进探索化学实验的实质,迁移所学知识,达到学以致用,层层深入,发挥5E教学模式的应用优势.
2.2 应用于化学概念教学
离子反应属于高中化学课程当中关键概念之一,通过这部分内容的学习能够引领学生从全新视角对于化学反应形成认识.对于离子反应实质探究教师可利用5E教学模式展开教学.
第一,引入环节.教师可以选择学生熟悉的三国人物诸葛亮作为导入素材,“七擒孟获过程当中,诸葛亮遇到了麻烦,因为蜀军误饮哑泉水,所以不能言语,为什么水会致哑?之后遇到一老叟,经过其指点以后,应用安乐泉水,转危为安,安乐泉水的成分是什么?”鼓励学生查阅资料,回答问题.用趣味化情境,为学生自主探究提供材料,使其通过自主学习,总结哑泉水当中含有重金属离子“铜离子”,饮用的“药”能够沉淀铜离子.
第二,探究环节.教师为学生提供实验药品和装置,组织其参与实验,验证猜想.学生①向试管当中滴加1 mL浓度为1 mol/L氯化铜溶液,随后滴加同等浓度硫酸钠溶液1 mL,观察实验现象.学生②向试管当中滴加1 mL浓度为1 mol/L氯化铜溶液,之后滴加同等浓度氢氧化钠溶液2 mL,观察实验现象.
第三,解释阶段.学生①可以观察到试管当中没有沉淀,此试管内可能无化学反应发生,随后添加钡离子,产生硫酸钡沉淀,说明原溶液中硫酸根未参加反应.对于铜离子是否参加反应进行检验,添加足量氢氧化钠,产生沉淀,说明原溶液中铜离子也没有参加反应.检验氯离子,向溶液当中添加硝酸根,产生氯化银沉淀,说明原溶液中氯离子未参加反应.最终得出结论,离子反应概念即为溶液内离子浓度发生变化的反应.学生②观察到有蓝色沉淀氢氧化铜生成,判断铜离子和氫氧根发生反应,得出结论,离子反应是水溶液内有离子参加的化学反应.
第四,迁移阶段.抛出问题,使用相同药品能否根据其他现象证明离子反应发生与否?学生结合以往所学的知识,共同参与导电实验设计,利用小灯泡亮度变化判断反应发生情况.学生①向烧杯内添加1 mL浓度为1 mol/L的氯化铜溶液,再添加同等浓度的硫酸钠溶液1 mL,观察小灯泡亮度变化不够明显;学生②向烧杯内添加1 mL浓度为1 moL/L的氯化铜溶液,再添加同等浓度的硫酸钠溶液2 mL,观察小灯泡亮度变暗;学生③向烧杯当中加入1 mL浓度为1 mol/L氢氧化钠溶液,之后滴加酚酞,发现溶液变红,继续滴加1 mL浓度为1 mol/L的盐酸溶液,发现小灯泡亮度逐渐变暗,溶液颜色逐渐褪去;学生④向烧杯当中滴加1 mL浓度为1 moL/L的盐酸溶液,再滴加1 mL碳酸钠溶液,可以看到小灯泡亮度变暗,有气泡产生.此时教师提出问题,学习离子反应以后,是否能够将复分解反应发生条件总结出来?学生根据所学知识,将知识迁移应用,说出“复分解反应条件为有水、气体或沉淀生成”.以离子浓度变化角度分析,水、气体和沉淀生成过程,离子浓度减小,就是发生了离子反应[4].
第五,评价阶段.在教师的组织下,学生根据实验现象总结离子反应.同时,教师要注意启发引导,提示学生从其他方面对离子反应进行证明,按照离子浓度变化与否来证明是否发生反应也可以.由此可见,教学过程可以通过多种方法设置探究活动.
以上教学过程运用5E教学方法,通过导入环节引用历史典故,发挥多学科融合教学优势,调动学生学习兴趣,启发其进入探究讨论环节.学生之间各抒己见,利用不同方法完成探究,解释阶段条理清晰,能够利用多种方式总结结论,高效率学习,感受化学知识的魅力.
3 结束语
综上分析,在核心素养理念的指导下,教师可以选择5E教学模式为学生讲解基础理论、化学概念等知识,以学生为主体,突出学生探究能力培养.因为教学模式存在特定理论框架,能够循序渐进引导学生关注探究过程,在教师的指导下,合作完成探究任务,有助于学生集体荣誉感的培养和合作意识的增强,进而提高其化学素养.
参考文献:
[1] 李思瑶,王海燕,徐爱菊.运用“5E学习环”教学模式培养高中生化学学科核心素养[J].中学教学参考,2020(35):3.
[2] 马长燕.核心素养导向下教学模式在高中有机化学教学中的应用:以“乙醇”为例[J].科普童话·新课堂(中),2021(09):114-115.
[3] 王惠娥,陈欣.基于5E教学模式的重要概念教学实践与探索[J].福建基础教育研究,2018(2):3.
[4] 石启英,魏燕,乔成芳.基于化学核心素养的“化学概念”5E教学模式设计[J].商洛学院学报,2022,36(6):8.
[责任编辑:季春阳]
收稿日期:2023-10-25
作者简介:张磊(1983.12-),男,江苏省镇江人,本科,中学一级教师,从事高中化学教学研究.