肿瘤标志物联合HER-2在原发性胃癌患者中的诊断效能
2024-04-07张娟张东英王琴
张娟,张东英,王琴
1.徐州医科大学附属邳州医院病理科,江苏徐州 221300;2.徐州医科大学附属邳州医院检验科,江苏徐州 221300
胃癌是临床中比较常见的一种恶性肿瘤,对患者生命健康有着极大的威胁。目前,胃镜检查与病理组织活检是诊断胃癌的常用方式,前者通过向胃部置入胃镜,观察胃部状况,以此判断胃部病变程度。在胃镜检查过程中,多数患者均会产生恐惧、焦虑等不良情绪,影响了检查结果[1]。由于早期胃癌诊断方式有限,加之症状并不明显,导致多数患者确诊时已达中晚期。随着医学检验技术的不断发展与进步,血清肿瘤标志物检测日益普遍[2]。除此之外,人表皮生长因子受体2(Human Epidermal Growth factor receptor 2, HER-2)作为一种生长因子,能够发挥跨膜酪氨酸激酶活性,在正常组织中微量表达,但在肿瘤细胞中多呈高表达,为此,对原发性胃癌诊断有着一定的价值[3]。基于此,本文为了探讨肿瘤标志物联合HER-2的诊断价值,现选取2017年6月—2023年1月期间徐州医科大学附属邳州医院收治的60例原发性胃癌患者进行研究。现报道如下。
1 对象与方法
1.1 研究对象
选取本院接受治疗的60例原发性胃癌患者选为观察组,以同期进行健康查体的60名体检者为参照组。观察组:男33例,女27例;年龄33~61岁,均值(50.34±3.67)岁。参照组:男32例,女28例;年龄34~61岁,均值(50.95±3.82)岁。两组以上数据对比,差异无统计学意义(P均>0.05),具有可比性。本研究通过医学伦理委员会的审批(2023-08-005),所有研究对象或者家属均自愿签订知情同意书。
1.2 纳入与排除标准
纳入标准:①观察组外科术后病理检查(金标准)确诊原发性胃癌,符合《中国临床肿瘤学会胃癌诊疗指南》[4]中有关诊断标准;②凝血功能正常;③可正常沟通,意识清楚;④临床资料齐全。排除标准:①伴有严重感染者;②合并其他恶性肿瘤者;③伴有严重肝、肾等器官功能异常者;④近期服用过生长激素、补充性激素者;⑤处于妊娠期或者哺乳期女性。
1.3 方法
肿瘤标志物检验:采集空腹静脉血5 mL,经离心处理后取上层清液待测,离心率3 000 r/min,离心时间10 min,采用UniCel Dxl 800免疫分析系统检测糖类抗原19-9(Carbohydrate Antigen 19-9, CA19-9)、糖类抗原125(Carbohydrate Antigen 125, CA125)、糖类抗原72-4(Carbohydrate Antigen 72-4, CA72-4)、癌胚抗原(Carcinoembryonic Antigen, CEA)。
HER-2水平检验:利用胃镜提取胃黏膜样本,用浓度为3.7%的甲醛溶液进行固定,以BenchMark GX全自动多功能免疫组化染色系统检测HER-2水平。
1.4 观察指标
统计比较两组肿瘤标志物与HER-2水平,以及肿瘤标志物诊断、HER-2诊断、肿瘤标志物联合HER-2诊断的准确度、灵敏度、特异度。灵敏度=真阳性例数/(真阳性例数+假阴性例数)×100%。特异度=真阴性例数/(真阴性例数+假阳性例数)×100%。准确度=(真阳性例数+真阴性例数)/总例数×100%
肿瘤标志物阳性判定标准[5]:CA19-9>35 U/mL;CA125>35 U/mL;CA72-4>6.9 U/mL;CEA>5 ng/mL。其中1项指标为阳性即肿瘤标志物诊断阳性。
HER-2阳性判定标准[6]:HER-2>15 ng/mL。
1.5 统计方法
将研究数据输入统计学软件SPSS 24.0中检验分析,符合正态分布的CA19-9、CA125、CA72-4、CEA、HER-2水平以(±s)表示,给予t检验;诊断结果及诊断效能为计数资料,以例数(n)和率(%)表示,给予χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者CA19-9、CA125、CA72-4、CEA、HER-2水平对比
观察组CA19-9、CA125、CA72-4、CEA、HER-2水平明显高于参照组,差异有统计学意义(P均<0.05)。见表1。
表1 两组患者CA19-9、CA125、CA72-4、CEA、HER-2水平对比(±s)
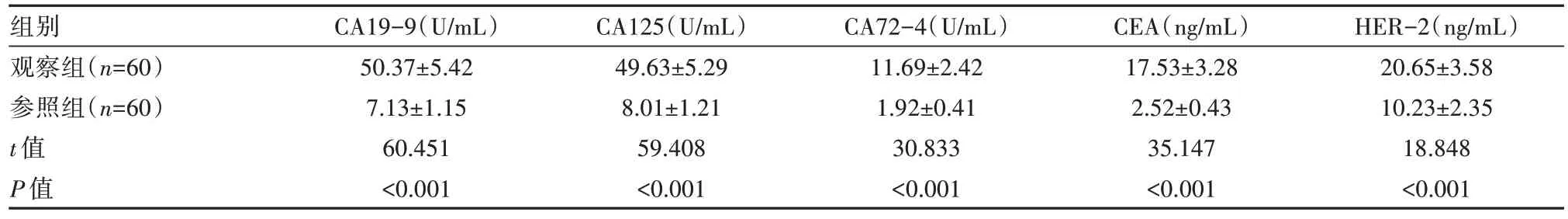
表1 两组患者CA19-9、CA125、CA72-4、CEA、HER-2水平对比(±s)
注:CA19-9:糖类抗原19-9,CA125:糖类抗原125,CA72-4:糖类抗原72-4,CEA:癌胚抗原,HER-2:表皮生长因子受体2。
组别观察组(n=60)参照组(n=60)t值P值HER-2(ng/mL)20.65±3.58 10.23±2.35 18.848<0.001 CA19-9(U/mL)50.37±5.42 7.13±1.15 60.451<0.001 CA125(U/mL)49.63±5.29 8.01±1.21 59.408<0.001 CA72-4(U/mL)11.69±2.42 1.92±0.41 30.833<0.001 CEA(ng/mL)17.53±3.28 2.52±0.43 35.147<0.001
2.2 肿瘤标志物联合HER2诊断原发性胃癌的结果与诊断效能
肿瘤标志物诊断原发性胃癌假阴性8例,假阳性3例,HER-2诊断原发性肺癌假阴性9例,假阳性4例,肿瘤标志物与HER-2联合诊断原发性胃癌的假阴性1例,假阳性2例,见表2。经计算,肿瘤标志物联合HER-2诊断的准确度、灵敏度明显高于肿瘤标志物诊断、HER-2诊断,差异有统计学意义(P均<0.05);在特异度方面,肿瘤标志物诊断、HER-2诊断、肿瘤标志物联合HER-2诊断比较,差异无统计学意义(P均>0.05),见表3。

表2 肿瘤标志物与HER-2诊断原发性胃癌的结果(n)
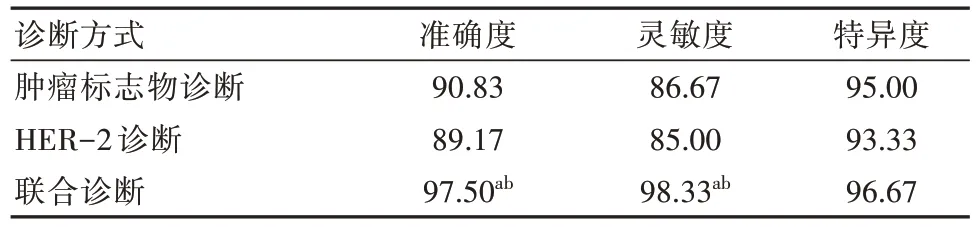
表3 不同方法诊断原发性胃癌的诊断效能(%)
3 讨论
胃癌是一种出现在胃黏膜上皮的恶性肿瘤,诊断方式主要有胃镜检查、CT检查、超声检查等,但都存在一定的局限性[7-8]。为此,在临床中,应积极探索有效的诊断胃癌的方式,从而尽早确诊病情,尽早给予治疗,以此提高患者预后。
HER-2是一种主要分布在细胞膜上的细胞原癌基因,少数分布在细胞质中[9]。在病理状态下,HER-2可抑制肿瘤细胞凋亡,且有助于增强肿瘤细胞侵袭力、促进肿瘤心血管再生[10-11]。有关研究发现,HER-2检验对诊断癌症原发病灶有着十分积极的作用,但对早期病症的诊断具有一定的局限性[12-13]。除此之外,血清肿瘤标志物检验也是诊断恶性肿瘤的常用方式,具有操作简单、快捷、痛苦小等优势[14]。在血清肿瘤标志物检验中,CA19-9是一种含有黏液的大分子糖蛋白,与肿瘤大小、淋巴转移、浸润深度等关系密切,是诊断胃癌及预测预后的重要指标[15]。CA125是一种较为常用的肿瘤标志物,当患上胃癌后,CA125呈高表达[16]。CA72-4也是一种含有黏液的大分子糖蛋白,对诊断胃癌进展有着十分积极的作用[17]。CEA是一种广谱肿瘤标志物,通过检验其水平可判断是否存在肿瘤倾向[18]。
本文研究表明:观察组CA19-9为(50.37±5.42)U/mL,CA125为(49.63±5.29)U/mL,CA72-4为(11.69±2.42)U/mL,CEA为(17.53±3.28)ng/mL,HER-2为(20.65±3.58)ng/mL均高于对照组(P均<0.05),与其他文献报道结论一致[19]。肿瘤标志物与HER-2联合诊断原发性胃癌的灵敏度与准确率分别为98.33%和97.50%,高于肿瘤标志物和HER-2单一诊断原发性胃癌的效能(P均<0.05),与文献报道结论相符[20]。在原发性胃癌诊断中,相较于单一检验来说,肿瘤标志物联合免疫组化指标检验的价值更高,有助于提高诊断阳性率,且能够对病情严重程度予以判定,为临床诊断与治疗提供了可靠的参考依据。
综上所述,肿瘤标志物联合免疫组化指标诊断原发性胃癌的价值更高,且通过对肿瘤标志物的检测,可准确判断病情严重程度。
