成人脓毒症休克患者院内死亡风险的早期预测及简易评分表构建
2024-03-21牟青松任香凝陆金帅
牟青松,任香凝,陆金帅,张 静△
(1.新疆医科大学研究生学院,乌鲁木齐 830017;2.新疆维吾尔自治区人民医院急诊科,乌鲁木齐 830001)
脓毒症是由感染引起的器官功能障碍,可进展为致命的脓毒症休克,其死亡率高达40%[1]。尽管诊断和治疗方法已得到改进,但脓毒症的发生率和死亡率依旧居高不下,并且脓毒症患者出院后1年内再入院率为65.0%,成为全球健康领域的主要挑战之一[2]。因此,对于脓毒症休克患者预后因素的早期筛查与早期干预具有重要临床意义。然而,在脓毒症休克患者的预后预测方面,虽然多生物标志物联合检测相较于单一指标更为精确,但在临床应用中受到操作复杂性的限制。因此,利用评分系统来评估脓毒症患者的严重程度和预后逐渐成为一种趋势。在实际的临床环境中,预测脓毒症休克患者的预后仍是一大挑战[3-4]。随着脓毒症-3.0(Sepsis3.0)标准的更新[5],尚无评分系统能够很好地适应新的诊断标准,以及准确且便捷地预测脓毒症患者的预后。因此,本研究旨在通过探讨更多可能的预后影响因素,构建一个新的、简化的早期评分系统,以期在保证操作简便的同时,提高对脓毒症休克患者预后的早期预测效能,为早期干预和临床决策提供依据。
1 资料与方法
1.1 一般资料
采用回顾性分析方法,本研究详细审查了2021年1月至2022年7月新疆维吾尔自治区人民医院急诊重症监护室(emergency intensive care unit,EICU)接受治疗的脓毒症休克患者的医疗记录。应用明确的纳入和排除标准,最终选定247例患者为研究对象,男139例(56.3%)、女108例(43.7%)。纳入标准:(1)年龄≥18岁;(2)符合Sepsis3.0的脓毒症休克诊断标准[5]。排除标准:(1)妊娠期妇女;(2)住院期间选择放弃治疗的患者;(3)临床资料不全或缺失关键数据的患者;(4)重症监护室(intensive care unit,ICU)住院时间少于24 h的患者;(5)恶性肿瘤、血液病、结缔组织病等疾病患者。本研究遵循医学伦理学标准,并经新疆维吾尔自治区人民医院伦理委员会批准(批件号:KY2022072217)。
1.2 方法
1.2.1临床资料收集
利用医院电子病历信息系统,本研究全面收集了患者的人口统计学资料和住院24 h内的临床数据、常用评分及实验室资料(24 h内如有多次结果取最差值)。(1)人口统计学资料:如年龄、性别;(2)临床资料:如基础生命体征(体温、心率、呼吸频率、收缩压、舒张压等)和基础疾病(高血压、糖尿病、冠状动脉粥样硬化性心脏病等);(3)实验室资料:如血液学参数[白细胞计数、血红蛋白、血小板计数、血小板分布宽度(platelet distribution width,PDW)等],生化参数[乳酸、肌酐、总胆红素、清蛋白、B型钠尿肽(B-type natriuretic peptide,BNP)、肌酸激酶、肌钙蛋白I(cardiac troponin I,cTnI)、肌钙蛋白T(cardiac troponin T,cTnT)、AST、ALT、镁离子等],感染相关参数[C反应蛋白(C-reactive proten,CRP)、降钙素原、白细胞介素-6(interleukin-6,IL-6)等];(4)血气分析参数:二氧化碳分压(partial pressure of carbon dioxide,PCO2)、氧分压;(5)凝血功能参数:活化部分凝血活酶时间(activated partial thromboplastin time,APTT)、D-二聚体;(6)常用评分:格拉斯哥昏迷量表(Glasgow coma scale,GCS)、序贯器官功能衰竭评估(sepsis-related organ failure assessment,SOFA)、快速序贯器官功能衰竭评估(quick sequential organ failure assessment,qSOFA)。
1.2.2样本量计算
本研究采用Cox比例风险回归模型的样本量估算公式:
n=自变量数量×(5~20)/患病率
①
依据国内外文献报道,脓毒症休克患者短期死亡率约为50%,本研究死亡率为50.6%(125/247)。本研究共筛选出18个相关性较明确的变量,取死亡率50%计算所需样本量为180~720,最终纳入247例。根据患者在院内的情况,分为存活组(n=122)和死亡组(n=125)。
1.2.3终点指标定义
(1)患者痊愈并出院;(2)患者在住院期间死亡。
1.3 统计学处理
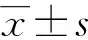
2 结 果
2.1 患者临床资料比较
本研究共纳入247例患者,存活组122例占49.4%,死亡组125例占50.6%。两组患者住院时间、呼吸频率、心率、乳酸、降钙素原、白细胞计数、CRP、IL-6、血小板计数、BNP、肌酸激酶、cTnT、cTnI、清蛋白、总胆红素、AST、PCO2、肌酐、尿素氮、D-二聚体、qSOFA评分、GCS评分和SOFA评分差异有统计学意义(P<0.05),其他指标差异无统计学意(P>0.05),见表1。
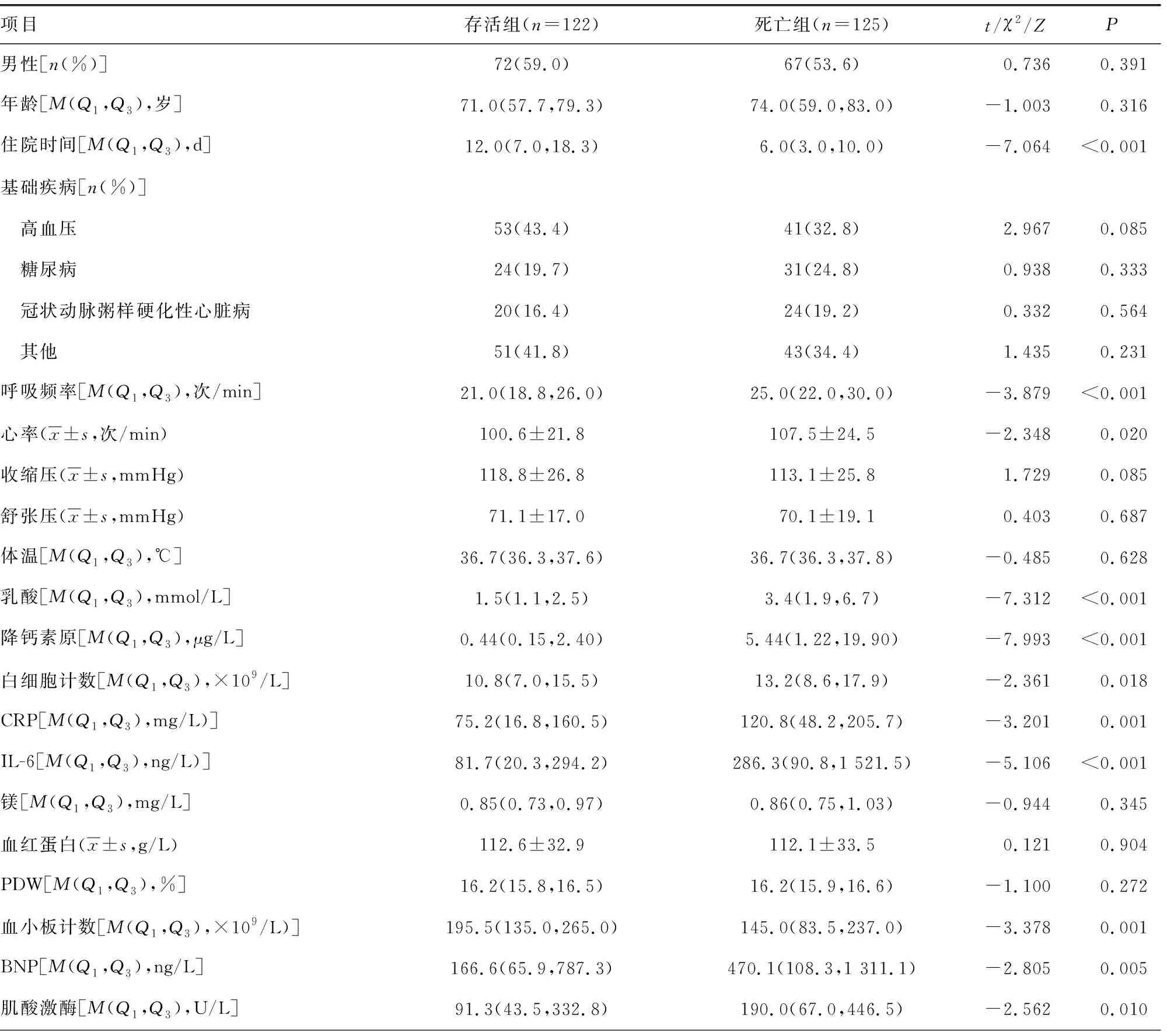
表1 两组临床资料比较
2.2 脓毒症休克患者院内预后的单因素分析
单因素分析结果显示,脓毒症休克患者院内预后的影响因素为呼吸频率、心率、GCS评分、qSOFA评分、SOFA评分、白细胞计数、血小板计数、D-二聚体、乳酸、降钙素原、IL-6、cTnI、总胆红素、清蛋白、AST、ALT、肌酐、尿素氮(P<0.05),见表2、3。
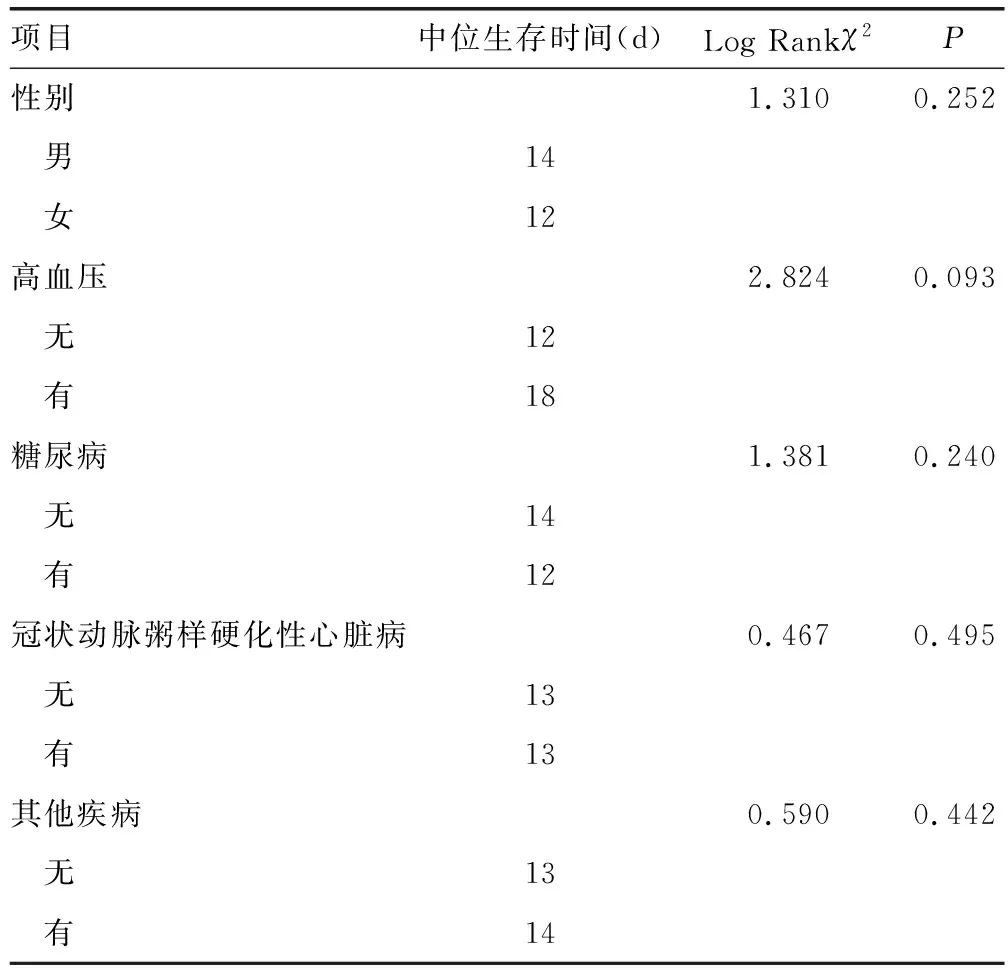
表2 影响脓毒症休克患者预后的分类变量单因素分析
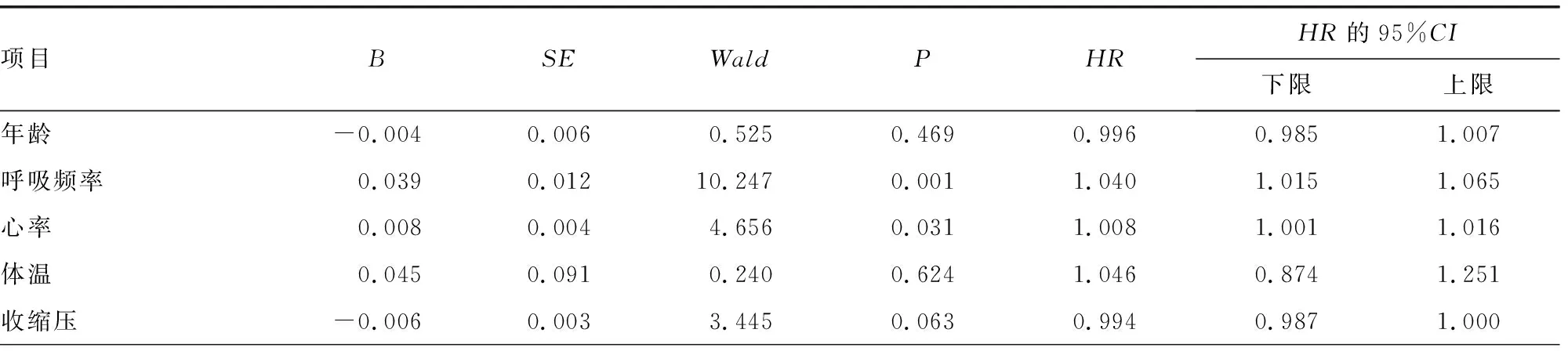
表3 影响脓毒症休克患者预后的连续变量单因素分析
2.3 脓毒症休克患者院内预后的多因素分析
将单因素分析中P<0.05的因素纳入多因素分析,结果显示:GCS评分(HR=0.929,95%CI:0.875~0.985,P=0.014)、qSOFA评分(HR=1.475,95%CI:1.094~1.989,P=0.011)、乳酸(HR=1.096,95%CI:1.049~1.145,P<0.001)、降钙素原(HR=1.009,95%CI:1.000~1.018,P=0.048)、清蛋白(HR=0.958,95%CI:0.922~0.996,P=0.029)是脓毒症休克患者院内预后的独立影响因素,见表4。
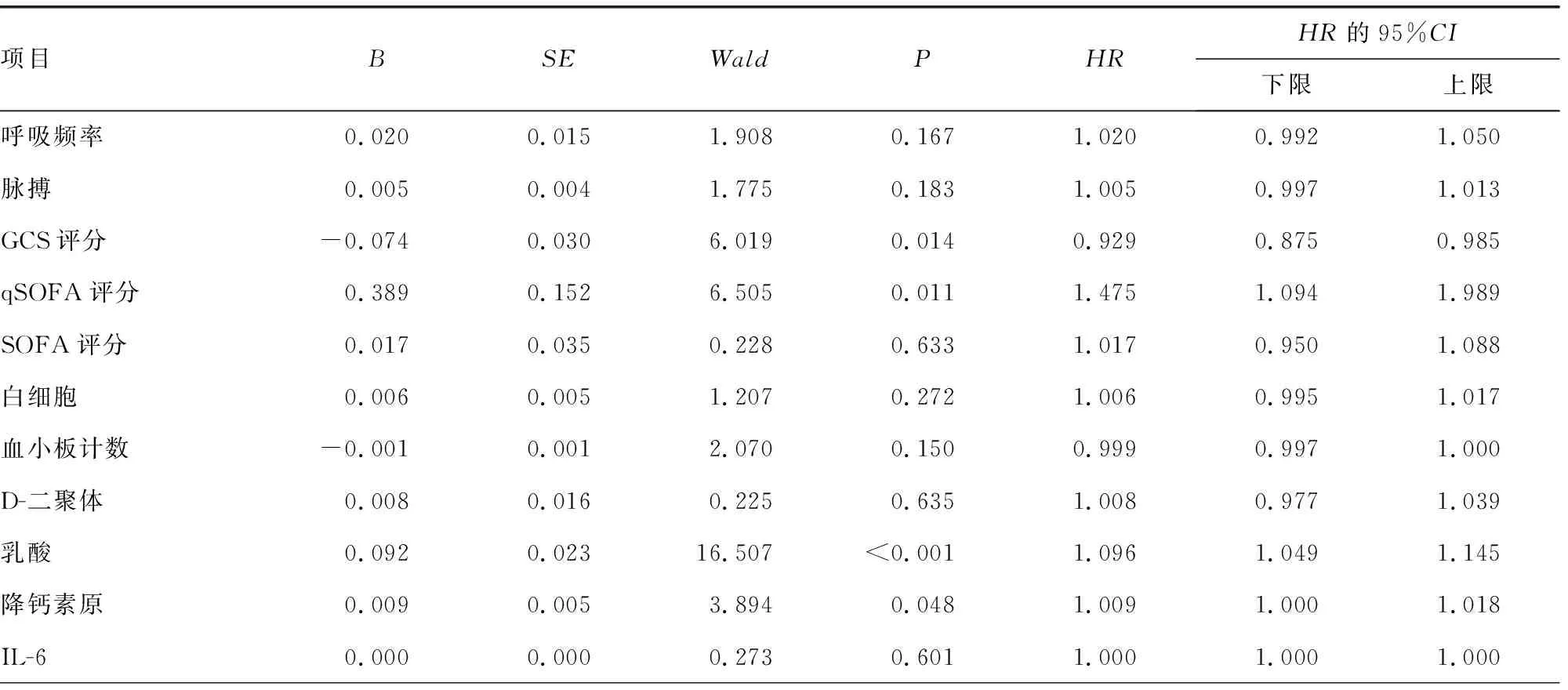
表4 影响脓毒症休克患者预后的多因素分析
2.4 脓毒症休克患者独立影响因素的ROC曲线分析
GCS评分、qSOFA评分、乳酸、降钙素原、清蛋白5个指标是脓毒症休克患者院内预后的独立影响因素,对其进行ROC曲线分析,结果发现:GCS评分、qSOFA评分、乳酸、降钙素原、清蛋白的曲线下面积(area under curve,AUC)分别为0.709、0.698、0.769、0.794和0.601;约登指数计算显示截断值分别为11.5分、1.5分、 2.6 mmol/L、2.3 μg/L 和28.7 g/L,见图1、表5。

表5 各独立影响因素预测脓毒症休克院内预后的ROC曲线分析结果
2.5 简易评分表的创建及其预测价值评估
根据截断值,将GCS评分、qSOFA评分、乳酸、降钙素原和清蛋白转换为二分类变量,各指标分别赋值为0分和1分,见表6。基于GCS评分、qSOFA评分、乳酸、降钙素原和清蛋白创建的简易评分表总分为0~5分。0~5分对应的院内死亡率分别为0(0/21)、9.3%(4/43)、36.8%(21/57)、66.7%(40/60)、88.9%(40/45),95.2%(20/21),差异有统计学意义(P<0.001),见表7;ROC曲线分析显示,简易评分表预测患者院内预后的AUC及其95%CI为0.866(0.822~0.910),最佳截断值为2.5分,灵敏度和特异度分别为80.0%和78.7%,见图2;不同简易评分表总分患者生存曲线比较,差异有统计学意义(Log Rankχ2=99.788,P<0.001),见图3。
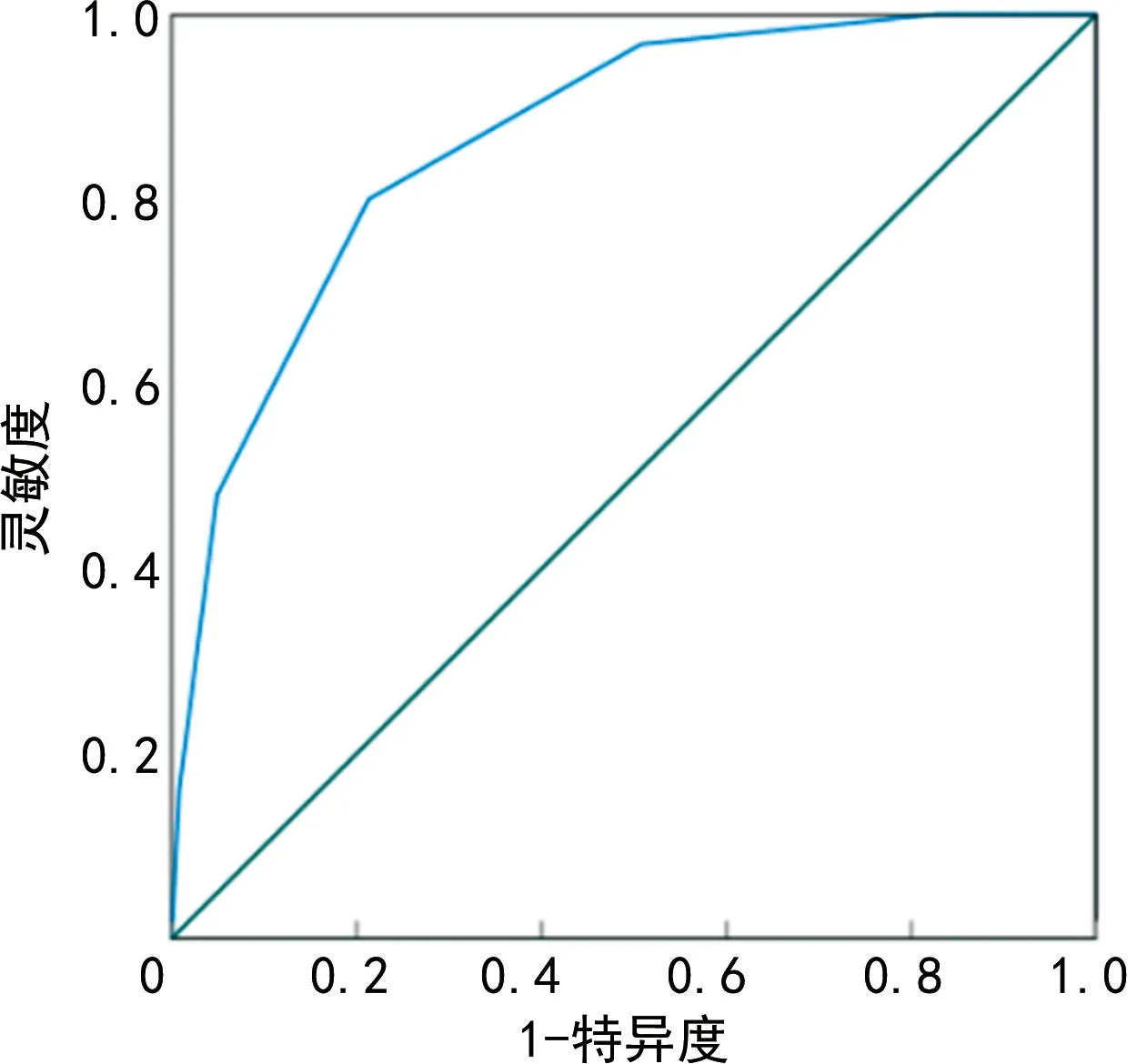
图2 简易评分表预测患者院内预后的ROC曲线

图3 不同简易评分表总分患者生存曲线

表6 简易评分各指标赋值

表7 不同简易评分表总分患者预后(n)
3 讨 论
脓毒症休克是脓毒症的一种严重形式,当发生脓毒症休克时,患者表现为全身性血管扩张和组织低灌注[6]。ICU内脓毒症患者的发病率和死亡率较高,其住院死亡率约为20%[7-8]。及时诊断和治疗脓毒症,以及开发早期预后评估工具是近年来重症医学领域研究的焦点之一。目前,SOFA、qSOFA和logistic器官功能障碍系统(logistic organ dysfunction system,LODS)评分是评估脓毒症患者预后的主要工具,通过量化患者的生理参数和器官功能来预测临床预后[9]。研究表明,与qSOFA评分(AUC=0.548)相比,LODS(AUC=0.668)和SOFA(AUC=0.611)评分在预测脓毒症预后准确性方面表现更佳,但qSOFA评分更简单,在急诊环境下更为实用[10]。然而,也研究指出在脓毒症院内死亡患者中,全身炎症反应综合征(systemic inflammatory response syndrome,SIRS)、qSOFA和qSOFA+乳酸标准(qSOFA+lactate criteria,qSOFA+L)评分间无明显差异,表明这些评分系统在预后评估中可能存在局限[11]。另一项关于脓毒症预测模型(sepsis prediction model,SPM)的研究显示,其在60 507次入院中展现出较高的平衡准确性(当评分>8分时为0.79),且与SIRS、SOFA和qSOFA评分相比,其对脓毒症患者的入院分类更准确。然而,SPM的时效性较差,从确定性时间到评分阳性的中位时间为68 min,而SIRS、qSOFA和SOFA评分的中位时间分别为7、74和28 min[12]。总之,目前临床常用评分在预测脓毒症患者预后方面具有一定价值,但它们各自存在局限性,如评分系统复杂、准确性和可靠性不足。
本研究发现GCS评分、qSOFA评分、乳酸、降钙素原和清蛋白是脓毒症休克患者院内死亡的独立影响因素。GCS评分作为一个用于评估患者意识状态的工具,与神经功能损害程度紧密相关,并被认为是早期诊断脓毒症及评估脓毒症患者严重程度的重要指标之一[13],也是老年脓毒症患者院内死亡率的独立影响因素[14]。此外,GCS评分降低是脓毒症发生的独立危险因素,即使在调整年龄、合并症等因素后,轻度的精神状态改变(GCS评分为13~14分)仍然与死亡率独立相关[15]。qSOFA评分作为一个简易工具在早期诊断脓毒症患者时具有价值,但它在预测脓毒症的严重性和患者预后方面相对较弱,这限制了其在临床的应用[16]。乳酸水平升高在脓毒症状态下常见,反映了组织缺氧和血流动力学的改变。乳酸是评估组织灌注不足和缺氧的关键指标,与脓毒症的严重程度和预后密切相关[17-18],通过降低乳酸水平,可能改善患者预后。降钙素原作为急性期反应蛋白,在诊断和监测脓毒症方面已得到广泛认可,特别是由于其检测迅速、周转时间短,在临床中的应用价值明显提高[19]。研究表明,降钙素原是影响脓毒症患者预后的独立影响因素,与非脓毒症患者相比,脓毒症患者降钙素原水平更高(P<0.01)[20],与本研究结果一致。然而,也有研究提出,尽管降钙素原能敏感地反映感染状态,但单独以降钙素原水平作为预后指标是不可靠的[21-22]。另外,低蛋白血症(定义为血清清蛋白水平<35 g/L)是脓毒症患者死亡率增加的独立危险因素,在危重症患者中低蛋白血症发病率为24%~87%[23-24]。此外,清蛋白每降低10 g/L,重症患者的住院死亡率增加137%,并发症发生率增加89%,住院时间延长72%[25]。有研究指出,清蛋白水平与脓毒症患者短期和长期预后相关,对于清蛋白水平<26 g/L的脓毒症患者补充清蛋白可能有益,并且清蛋白水平每增加10 g/L,28、60、180 d和1年的死亡风险降低59%[26]。另外,一项多变量分析也得出相似的结果,清蛋白每降低10 g/L,患者在未来1个月内死亡的风险是清蛋白水平未下降时的近3倍[27]。以上研究结果与本研究结果一致。因此,积极的营养支持对改善脓毒症患者的临床预后具有重要意义。
综上所述,通过早期的GCS评分、qSOFA评分、乳酸、降钙素原和清蛋白指标,可以从多方面评估脓毒症休克患者预后,其时效性和简便性适合急诊环境。然而,本研究为单中心研究,其结果适用性可能受限,未来需通过更大规模、多中心研究来进一步验证,并探索新的生物标志物,以优化预后评估。
