泼尼松联合环磷酰胺治疗肾病综合征的效果及安全性分析
2024-03-09孙莹
孙 莹
(蒙阴县人民医院肾内科,山东 临沂 276299)
肾病综合征(nephrotic syndrome,NS)是以高脂血症、大量蛋白尿、水肿、低蛋白血症等为主要特征的临床症候群,该病起病隐匿,易损害肾功能,诱发心血管系统疾病、感染等,甚至可进展为终末期肾病,因此如何治疗NS是一个不可忽视的问题[1-3]。目前,临床针对NS患者以免疫调节为主,其中泼尼松等糖皮质激素是治疗NS的主要药物,该类药物可抑制免疫及炎症反应,但长期用药易出现库欣综合症、消化道症状、感染等并发症[4]。相关报道指出,环磷酰胺(cyclophosphamide,CTX)具有较强的免疫抑制效果,与泼尼松联合使用可发挥协同增效的作用,有效保护NS患者的肾功能[5]。但此类报道较少,故本研究旨在探究泼尼松联合CTX治疗NS患者的效果及安全性,现报道如下。
1 资料与方法
1.1 一般资料选取2020年10月至2022年10月蒙阴县人民医院收治的86例NS患者为研究对象,以随机数字表法分对照组(43例)和观察组(43例)。对照组患者中男性25例,女性18例;年龄22~68岁,平均年龄(45.3±5.6)岁;病程1~9个月,平均病程(5.0±1.1)月;体质量45~83 kg,平均体质量(63.9±2.9)kg。观察组患者中男性23例,女性20例;年龄24~70岁,平均年龄(45.8±6.1)岁;病程1~8个月,平均病程(4.6±1.0)月;体质量44~81 kg,平均体质量(63.6±2.5)kg。两组患者一般资料比较,差异无统计学意义(P>0.05),组间具有可比性。本研究经蒙阴县人民医院医学伦理委员会审批通过,患者及家属对本研究知情同意并签署知情同意书。纳入标准:①符合《内科学(第8版)》[6]中NS的诊断标准;②经肾功能、尿常规、肾脏超声等确诊为原发性NS;③临床资料完整。排除标准:①有免疫缺陷、免疫抑制药物治疗史者;②受试药物过敏史或过敏体质者;③哺乳、妊娠期妇女;④正在参与其他临床试验者;⑤重要脏器功能障碍者;⑥意识、沟通、精神、视听障碍者;⑦严重感染者;⑧合并恶性肿瘤者。
1.2 治疗方法两组患者入院后均接受利尿消肿、降压调脂、抗凝、限制水和钠摄入量、纠正水电解质平衡等干预。对照组患者接受泼尼松治疗,口服醋酸泼尼松片(天津信谊津津药业有限公司,国药准字H31020675,规格:5 mg×100片),早餐后服用,1.0 mg/(kg·d)、1次/d。每天最大使用量为60 mg,服药12周后调节剂量为15 mg/d。观察组患者接受泼尼松联合CTX治疗,泼尼松用法用量同对照组,静脉注射环磷酰胺注射液(德国Baxter Oncology GmbH,国药准字HJ20160467,规格:0.2 g×1瓶),1次/月、0.8 g/次。两组患者均治疗6个月后评估治疗效果。
1.3 观察指标①临床疗效。参照《临床诊疗指南:肾脏病学分册》[7]评估,包括完全缓解[临床症状消失,肾功能恢复正常,24 h尿蛋白定量(24 h UP)<0.1 g]、显著缓解(临床症状显著改善或消失,肾功能显著好转或恢复正常,0.1 g≤24 h UP <0.2 g)、部分缓解(临床症状有所改善,肾功能有所好转,0.2 g≤24 h UP <3.0 g)、无效(临床症状加重或无改善,肾功能恶化或无好转,24 h UP≥3.0 g)。治疗总有效率=[(部分缓解+显著缓解+完全缓解)例数/总例数]×100%。②肾功能指标水平。采集40 mL患者空腹晨尿,置于2~8℃保存24 h,使用免疫比浊法(试剂盒:上海信帆生物科技有限公司)检测24 h UP。取患者空腹3 mL静脉血以转速3 000 r/min,离心10 min,置于-20 ℃待检。以全自动生化分析仪(美国贝克曼库尔特公司,型号:AU680)检测患者血尿素氮(BUN)、血肌酐(Scr)。③炎症因子水平。取患者3 mL空腹静脉血以转速3 000 r/min,离心10 min,使用酶联免疫吸附法(试剂盒:北京博迈斯科技有限公司)检测患者超敏C反应蛋白(hs-CRP)、白细胞介素-6(IL-6)、肿瘤坏死因子-α(TNF-α)。④不良反应发生情况。详细记录用药期间患者不良反应类型、出现及持续时间、严重程度、处理方法等,不良反应包括白细胞减少、血糖升高、胃肠道不适等。不良反应总发生率=各不良反应发生例数之和/总例数×100%。
1.4 统计学分析采用SPSS 23.0统计学软件进行数据分析,计数资料以[例(%)]表示,采用χ2检验;计量资料以(±s)表示,采用t检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者临床疗效对比观察组患者治疗总有效率(93.02%)高于对照组(74.42%),差异有统计学意义(P<0.05),见表1。

表1 两组患者临床疗效对比[例(%)]
2.2 两组患者肾功能指标水平对比治疗前,两组患者24 h UP、BUN、Scr水平比较,差异均无统计学意义(均P>0.05)。治疗6个月后,两组患者24 h UP、BUN、Scr水平均降低,且观察组均低于对照组,差异均有统计学意义(均P<0.05),见表2。
表2 两组患者肾功能指标水平对比(±s)
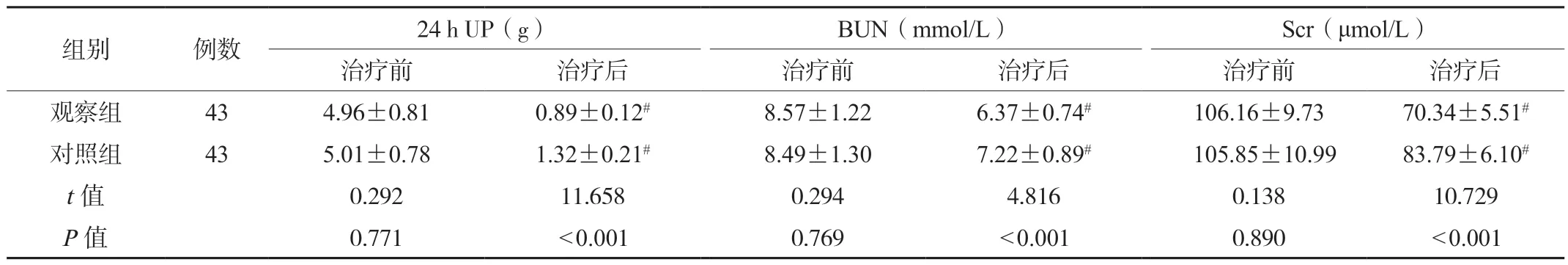
表2 两组患者肾功能指标水平对比(±s)
注:与治疗前比较,#P<0.05。24 h UP:24 h尿蛋白定量;BUN:血尿素氮;Scr:血肌酐。
组别例数24 h UP(g)BUN(mmol/L)Scr(μmol/L)治疗前治疗后治疗前治疗后治疗前治疗后观察组434.96±0.810.89±0.12#8.57±1.226.37±0.74#106.16±9.7370.34±5.51#对照组435.01±0.781.32±0.21#8.49±1.307.22±0.89# 105.85±10.9983.79±6.10#t值0.29211.6580.2944.8160.13810.729 P值0.771<0.0010.769<0.0010.890<0.001
2.3 两组患者炎症因子水平对比治疗前,两组患者hs-CRP、IL-6、TNF-α水平比较,差异均无统计学意义(均P>0.05)。治疗6个月后,两组患者hs-CRP、IL-6、TNF-α水平均降低,且观察组均低于对照组,差异均有统计学意义(均P<0.05),见表3。
表3 两组患者炎症因子水平对比(±s)
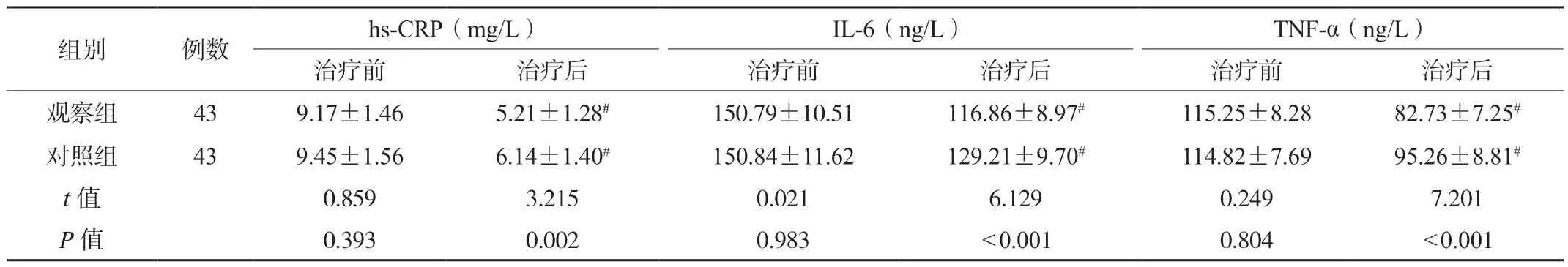
表3 两组患者炎症因子水平对比(±s)
注:与治疗前比较:#P<0.05。hs-CRP:超敏C反应蛋白;IL-6:白细胞介素-6;TNF-α:肿瘤坏死因子-α。
组别例数hs-CRP(mg/L)IL-6(ng/L)TNF-α(ng/L)治疗前治疗后治疗前治疗后治疗前治疗后观察组439.17±1.465.21±1.28#150.79±10.51116.86±8.97#115.25±8.2882.73±7.25#对照组439.45±1.566.14±1.40#150.84±11.62129.21±9.70#114.82±7.6995.26±8.81#t值0.8593.2150.0216.1290.2497.201 P值0.3930.0020.983<0.0010.804<0.001
2.4 两组患者不良反应发生情况对比观察组患者不良反应总发生率为13.95%高于对照组的9.30%,组间比较,差异无统计学意义(P>0.05),见表4。
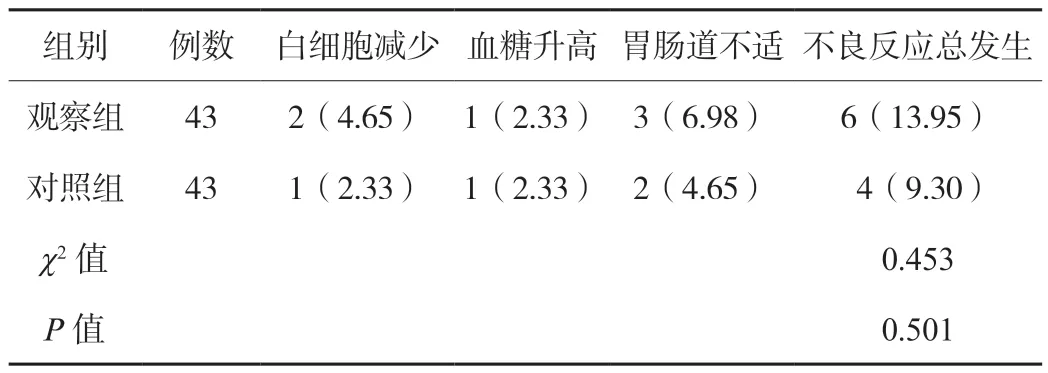
表4 两组患者不良反应发生情况对比[例(%)]
3 讨论
NS是常见的肾脏疾病,目前尚未完全阐明其发病机制,但多认为其与B细胞功能紊乱、遗传等多方面因素有关。其起病隐匿,易延误治疗时机,并可能进展为终末期肾脏病,威胁患者生命安全[8]。现阶段临床针对NS患者重在进行对症支持治疗,如卧床休息增加肾血流量、保持低盐及低碱饮食、结合肾功能调节蛋白质摄入量、水肿明显者配合利尿剂治疗、严格控制血压、以阿司匹林及肝素等抗凝药物预防血栓形成等。在此基础上常用糖皮质激素抑制急性炎症渗出,阻止纤维蛋白沉着,减弱成纤维细胞活性,但大量、长期用药易引起下丘脑-垂体-肾上腺轴功能紊乱,诱发感染等不良反应,出现神疲乏力、腰酸腰痛、浮肿等不适症状,尚需完善治疗方案。CTX是烷化剂类免疫抑制剂,具有抗炎、调节免疫功能等作用。
本研究结果显示,泼尼松联合CTX治疗对NS患者有较好效果,观察组患者治疗总有效率高于对照组,24 h UP、BUN、Scr水平低于对照组,这与刘敏等[9]学者的结果一致。分析其原因为,泼尼松是治疗NS常用的糖皮质激素药物,通过抑制巨噬细胞、白细胞在炎症部位聚集发挥抗炎作用,能抑制细胞介导的免疫反应,减少T淋巴细胞、单核细胞水平等,从而阻断细胞表面受体结合免疫球蛋白,缓解NS症状,但单用此药治疗周期长,易引起一系列不良反应,故需进行联合用药治疗[10]。 CTX为细胞周期非特异性药物,经肾脏内磷酸铵酶水解产生丙烯醛、磷胺氮介,从而强效杀灭肿瘤细胞,且环磷酰胺吸收快速,能迅速达到较高的血药浓度[11-12],同时亦能选择性抑制B淋巴细胞功能、NK细胞功能。因此,采用泼尼松联合CTX方案时,前者可诱导肝药酶系统产生抑制作用,延长烷化作用;后者具有较强免疫抑制作用,二者联用可发挥协同增效作用,抑制特异性免疫应答对肾脏的损伤,有效保护肾功能。hs-CRP、IL-6、TNF-α可评估炎症严重程度,IL-6易造成系膜细胞增殖,加重肾脏炎症反应。TNF-α可以分泌自肾固有细胞(如系膜细胞、近曲小管上皮细胞)、肾脏局部炎症细胞,参与肾脏病理损伤[13]。本研究结果显示,泼尼松联合CTX可降低hs-CRP、IL-6、TNF-α水平。分析其原因为NS患者由于免疫功能异常,易激活多种炎症细胞因子并释放入血液,损伤肾小球。泼尼松可抑制白细胞等炎症细胞在炎症部位聚集,并可抑制其吞噬作用,减少溶酶体酶释放,减轻炎症反应,而CTX通过干扰细胞增殖,发挥抗炎作用[14]。因此,泼尼松联合CTX有助于阻止炎症反应发展。两组患者不良反应情况比较,差异无统计学意义,所以泼尼松联合CTX方案具有一定安全性。药物安全性是影响药物推广的重要指标[15],但本次研究样本量偏小,今后将通过扩大样本量,深入探析泼尼松联合CTX治疗的安全性。
综上所述,泼尼松联合CTX能够有效治疗NS患者,并可降低hs-CRP、IL-6、TNF-α水平,减轻肾损伤,加之安全性高,具有应用价值。
