口服制剂防治鸭浆膜炎的临床效果
2024-03-06高航柴贝贝张春杰张丽媛
高航,柴贝贝,张春杰,张丽媛
郑州赛科药业科技有限公司,郑州 450000
鸭疫里默氏杆菌病是由鸭疫里默氏杆菌(Riemerellaanatipestifer)引起的1 种接触性传染性疾病,又称为鸭传染性浆膜炎、鸭疫综合症等[1]。多发于1~6 周龄的小鸭,发病率可达90%,若不及时控制,死亡率可达80%。该病的主要症状有急性或慢性败血症、鼻分泌物增多、咳喘、下痢、头颈震颤,少数慢性病例出现头颈歪斜等症状,会形成较明显的“泪痕”,且大多生长缓慢形成“僵鸭”[2]。剖检主要有纤维素性心包炎、肝周炎、气囊炎、关节炎等症状,常引起小鸭的大批发病和死亡,目前已成为危害肉鸭养殖业的一种最常见细菌病[3],并且不仅感染鸭类,鹅、火鸡等禽类也可感染发病[4]。
该病的控制难点在于鸭疫里默氏杆菌的血清型较多,目前较认同的有25 种,不同时期、不同地区、不同场址的主要流行血清型都有所不同,并且在同一鸭场,甚至是同一批鸭群也可能同时存在多个血清型,且不同血清型之间的交叉保护性较低,而且难以净化,较为有效的方法是分离流行菌株进行疫苗研制,疫苗的抗原血清型与养殖中流行菌株的血清型最大程度吻合,才能保证免疫效果最佳[5]。防治该病最根本的是做好预防工作,加强鸭场的饲养管理,改善卫生条件,减少鸭群应激,建立完善的防疫和消毒制度[6];在上述情况满足的条件下合理进行疫苗免疫,合理用药,综合防治,有效减少鸭群的发病和死亡[7]。
河南周口的鸭场在2023 年3–4 月阶段性暴发该病,发病率33.43%,死亡率11.12%,瘫痪率23.57%,损失严重,通过临床症状和剖检症状初步判定为鸭疫里默氏杆菌病,然后进行实验室诊断,确诊为鸭疫里默氏杆菌引起的鸭疫里默氏杆菌病。通过对发病鸭群进行中西药结合治疗,延缓了病情发展,同时采集病料进行鸭浆膜炎口服制剂的制备,通过灌服或饮水饲喂后,疾病得到明显地控制,死亡率和瘫痪率显著下降。
1 材料与方法
1.1 材 料
1)样品来源:河南周口某鸭场发病死亡鸭3 只(3~4周龄)。
2)试验鸭来源:河南周口某鸭场樱桃谷鸭,4 周龄、6周龄SPF雏鸭各9只,2周龄SPF雏鸭39只。
3)试剂与培养基:无菌蒸馏水、无菌生理盐水、甲醛、胎牛血清、胰蛋白胨大豆肉汤(TSB)、胰蛋白胨大豆琼脂(TSA)、市售蜂胶、95%乙醇。
4)仪器与工具:MD30-B 显微镜(江南)、WJ-160A 二氧化碳恒温培养箱(上海诵诚)、XFS-280 高压灭菌锅(浙江新丰)、低温离心机(Sigma)、SHA-C恒温摇床(常州普天司)、锥形瓶、250 mL 和500 mL灭菌疫苗瓶、移液器、剪刀、镊子。
2.2 方 法
1)剖检:将病鸭置于无菌托盘,腹部向上,使用灭菌后的剪刀剖开腹腔,检查腹腔与内脏情况。
2)菌株纯化:将3株保藏菌株进行活化,分别抽取200 μL 保藏菌液加入含5%胎牛血清的TSB 中,37 ℃的恒温摇床培养24 h 后,接种于含有5%胎牛血清的TSA,并于37 ℃二氧化碳恒温培养箱中培养24 h,观察是否有污染,并挑取单个菌落镜检。将挑取的单个菌落在37 ℃的恒温摇床中培养48 h,进行扩大培养后备用。
3)蜂胶提纯:将市售蜂胶放置4 ℃储存,用时取出,及时粉碎后过筛,按照重量比1:2 加入95%乙醇,室温浸泡24~48 h,浸泡期间可以超声,增加溶解,浸泡后4 ℃ 8 000 r/min 离心取上清,用无菌纱布过滤,得到清澈透明的纯净蜂胶浸液。
4)口服制剂的制备:将扩大培养后的3 种菌液培养至浓度为109cfu/mL 时加入0.2%甲醛进行灭活,继续37 ℃恒温培养12 h 后取100 μL 涂板鉴定菌液是否完全灭活。将灭活后的菌液进行离心,留下菌体沉淀备用。将所有菌体用无菌生理盐水重悬后混匀,然后缓慢加入已处理好的蜂胶液,边加边混匀,使蜂胶液终浓度为10 mg/mL,最后根据需求量补足无菌生理盐水。
5)口服制剂的效果验证:①无菌检测:用移液器吸取250 μL 口服制剂,分别接种于TSA,37 ℃恒温培养12 h。
②紧急接种:将制备好的口服制剂按照每只灌服或饮水300 μL应用在鸭场,同时增加鸭群日粮中的蛋白质和维生素含量,可适量配合黄芪多糖[8],控制饮水量。
③安全性试验:分别取2、4、6周龄SPF雏鸭各9只,分3 组,每组3 只,一共9 组,按照低、中、高剂量进行灌服,即:第1、2、3 组处理分别在2 周龄饲喂200、500、1 000 μL,第4、5、6组处理分别在4周龄饲喂200、500、1 000 μL,第7、8、9 组处理分别在6 周龄饲喂200、500、1 000 μL。观察饲喂后0.5、6.0、24.0 h,是否有鸭只出现不良反应,如呕吐、拉稀、瘫痪、死亡等情况。
④免疫试验:选取60 只2 周龄SPF 雏鸭分为5组,每组12 只,分组名称为第1、2、3、4、5 组,第1 组处理为生理盐水,第2组为市售鸭浆膜炎产品组,按照说明书要求每只肌注200 μL,第3、4、5 组均为口服制剂,剂量分别为200、500、1 000 μL。免疫当天为第0 天,于免疫后7、14、24 d 鸭跖骨内侧静脉采血,分离血清检测抗体。
⑤攻毒试验:将已免疫过的5 组雏鸭每组随机选取6 只进行攻毒试验,每只肌肉注射200 μL,观察鸭只是否出现瘫痪、下痢、死亡等症状,并计算保护率。保护率=(对照组发病率-接种组发病率)/对照组发病率。
2 结果与分析
2.1 剖 检
解剖发现纤维素性心包炎、肝周炎、关节炎症状,见图1。
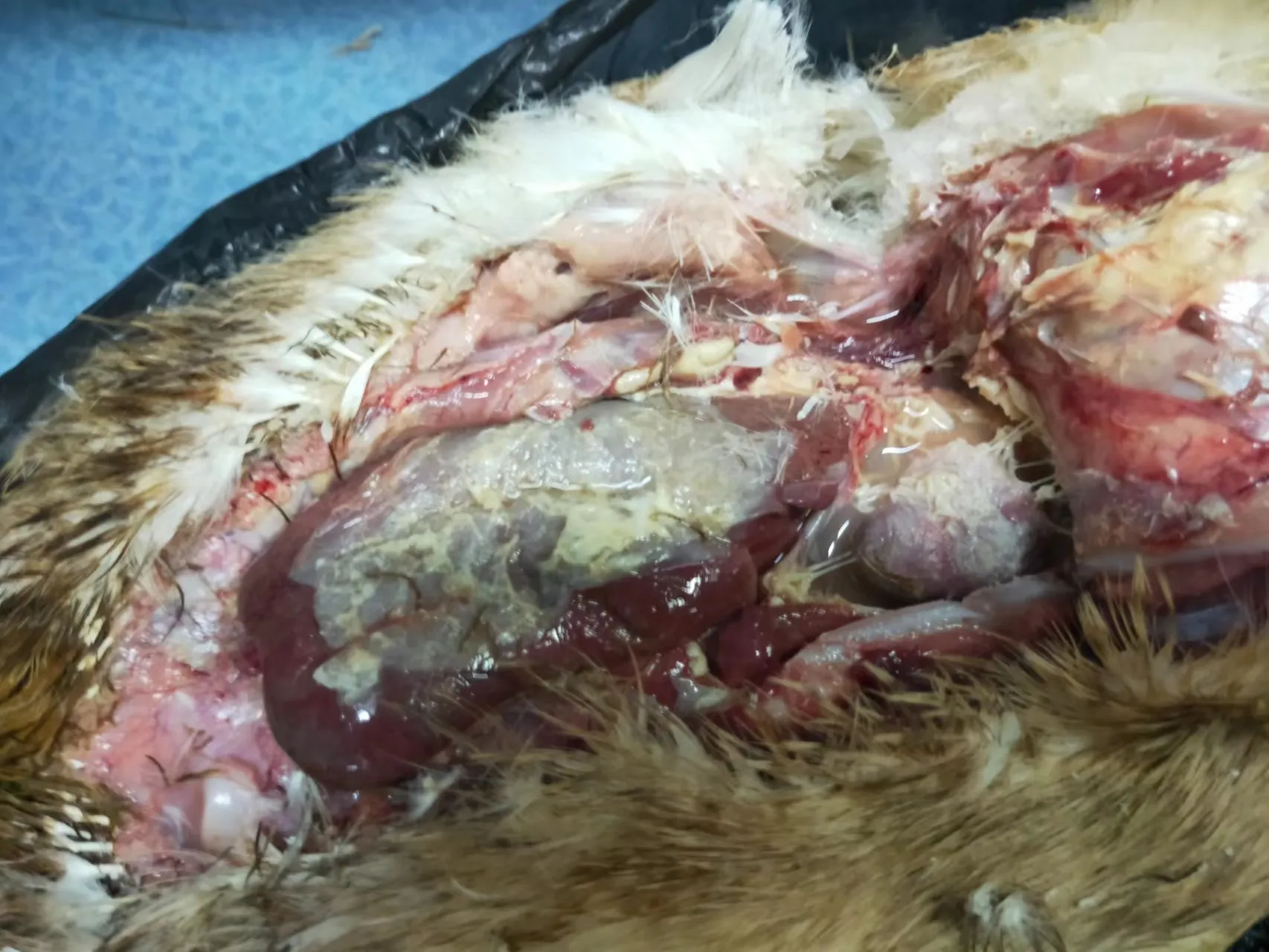
图1 肝周炎病变
2.2 菌株纯化
镜检没有发现杂菌污染,见图2。
图2 革兰氏阴性菌(10×100)
2.3 蜂胶提纯
称取500 g 市售蜂胶,加入1 L 95%乙醇,25 ℃浸泡48 h后,4 ℃ 8 000 r/min离心取上清,用无菌纱布过滤,最终得到0.5 g/mL 的清澈透明蜂胶液800 mL 放置4 ℃备用。
2.4 口服制剂制备
本次制备了100 g 湿菌体,采用500 mL 生理盐水重悬后,缓慢加入已处理好的蜂胶液,使蜂胶液终质量浓度为10 mg/mL,边加边混匀,最后加入无菌生理盐水,补足至40 L。
2.5 口服制剂效果验证
1)灭活检测:将涂布的TSA 平板放入培养箱37 ℃培养12 h后无菌生长,灭活检测合格。
2)安全性试验:饲喂后鸭只没有出现不良反应,偶有应激系抓取导致,待平静后恢复正常状态。
3)紧急接种:应用该口服液后3 d,鸭群临床无新增死亡鸭,发病率降低至7.3%,说明该口服制剂产生了较好的应急免疫作用。
4)免疫试验:在免疫后7、14、21 d 跖骨内侧静脉采血,分离血清检测抗体,结果采用SPASS 22.0分析。由表1 可知:该口服制剂中剂量组在第14 天就可以达到较高的抗体水平,高剂量组在第21天仍有较高的抗体水平,但考虑到成本问题,临床使用时,可以在第1天使用中剂量,即每只鸭灌服或饮水500 μL,在第21天加强免疫1次。
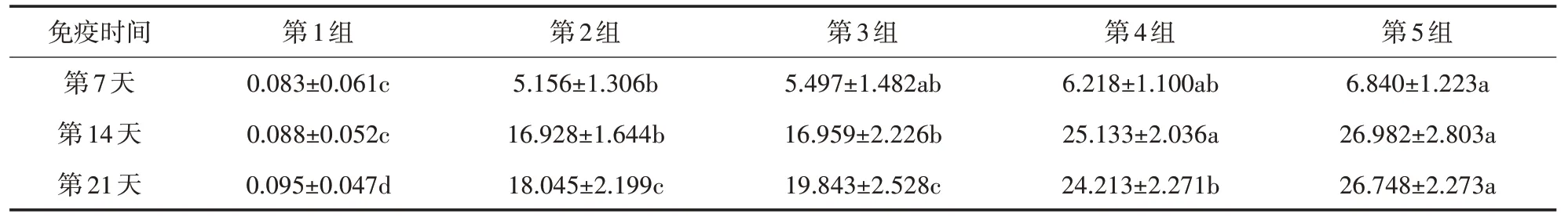
表1 免疫后7、14、21 d抗体含量 ng/L
5)攻毒试验:在96 h 内,第2 组和第3 组处理的保护率为60.1%,第4 组和第5 组处理的保护率为100%。
3 讨 论
鸭疫里默氏杆菌病对肉鸭行业的危害很大,在预防和治疗上虽然使用抗菌药物有一定的效果,但抗菌药物的长期使用,会导致鸭疫里默氏杆菌的耐药性增加,治疗效果不明显[9]。因此,通过增强机体对病菌的抵抗力,降低药物使用量,是预防鸭疫里默氏杆菌病及降低发病率的重要措施之一[10]。本次制备的口服制剂选择的菌株均是从该养殖场分离的,针对性强,可以改善普通疫苗血清型不同导致的保护率低的问题,更好地发挥应急免疫作用,且蜂胶免疫佐剂是1种天然产物,有研究表明,蜂胶本身无明显抗原性和过敏性,毒副作用较小[11]。作为1 种具有广谱生物活性的物质,不仅能够提高机体的特异性免疫,增强巨噬细胞的吞噬能力,而且还能增强机体的非特异性免疫,促进抗体的产生,应用蜂胶配合抗原进入机体可以增加抗体产量和保护率[12-13],将蜂胶与抗原按比例混合接种于机体后,可以增强补体的功能,产生较多的抗体,提升血清抗体水平,是天然的免疫增效佐剂,并且具有抑菌性和更高的安全性[14]。但是市售的鸭浆膜炎产品多为注射剂,易造成鸭只的应激反应,并且鸭疫里默氏杆菌血清型较多,市售的注射剂不一定符合本场流行菌株,可能出现疫苗保护率低的问题[15]。本试验结果表明,该口服制剂中剂量组在第14天可以达到较高的抗体水平,高剂量组在第21天仍有较高的抗体水平,能够起到快速治疗和应急免疫的辅助作用。该口服制剂是针对个别养殖场的病原血清型制备,在一定程度上可以起到很好的应急免疫作用,但也存在一定的应用范围制约,因此应规范应用,不随意扩大应用范围。
