肝门再阻断法在肝切除术后胆漏中的预防效果
2024-02-21宋林泉梁志宏
宋林泉,梁志宏
(中山小榄人民医院肝胆外科,广东 中山 528415)
原发性肝癌(HCC)是临床常见疾病之一,发病机制与病毒性肝炎、环境因素、肝硬等因素有关,其具有发病率高、死亡率高等特征,严重危害患者的生存质量[1]。目前,临床治疗HCC主要采用手术切除病灶,肝切除术是目前治疗肝癌最有效的方法。但肝脏结构较为复杂,人体血供较为丰富,在该区域进行手术整体难度较大,加之手术具有创伤性,术后极易引发并发症发生[2]。研究调查显示,肝切术后胆漏、出血及肝功能损伤等并发症发生率高达40.2%~ 55.5%[3]。胆漏是肝切除术后患者常见并发症,如若处理不当,则会继发细菌性腹膜炎、膈下感染及肝衰竭,严重时甚至会危及患者的生命[4]。研究调查显示,术后并发症中胆漏发生率仍维持在高位,在1.9%~12.0%,甚至高达33.0%[5]。肝切除术后胆漏不仅延长患者的住院时间,还给患者增加了心理与经济压力,严重影响患者的生活质量。目前临床大多数学者认为发生胆漏的主要原因为肝断面的处理不当[6],因此如何预防肝切术后胆漏发生是临床肝胆医师亟待解决的重要问题。临床上针对肝脏切除后进行肝门再次阻断法处理切面血管、胆管等的研究报道相对较少,本研究探究肝门再次阻断法在肝切除术中预防胆漏的应用效果,为临床在肝切术后预防胆漏提供思路和参考。
1 资料与方法
1.1一般资料:选取2021年1月~2021年6月在我院接受单纯性肝切除术的80例患者纳入研究,以数字随机法将所选患者分为对照组40例和观察组40例。对照组男30例,女10例,年龄34~87岁,平均年龄(55.42±3.35)岁,其中原发性肝癌35例,肝脏良性肿瘤5例,肿瘤直径(5.53±1.04)cm,采用传统肝门阻断法。观察组男25例,女15例,年龄35~88岁,平均年龄(56.31±3.26)岁,其中原发性肝癌32例,肝脏良性肿瘤8例,肿瘤直径(5.17±1.12)cm,采用肝门再次阻断法。纳入标准:①所有患者经临床症状、影像检查或病理检查确证为肝脏良、恶性肿瘤;②所有患者均符合手术指征;③年龄≥18岁;④肝功能 Child-Pugh 分级 A 级;⑤临床资料完整者;⑥所有患者对本次研究知晓并签订知情同意书。排除标准:①合并严重心肺疾病者;②预测生存期低于3个月者;③存在精神、认知功能障碍者;④凝血功能障碍者;⑤临床资料不齐全者;⑥不能接受随访者。两组患者年龄、性别等一般资料对比差异无统计学意义(P>0.05),具有可比性。本研究已通过本院医学伦理机构审核批准。
1.2方法
1.2.1手术方法:所有患者均采用气管插管方式进行全身麻醉,采用右侧肋缘下切口,均由同年资、手术水平相当的外科医生操作。入腹后探查腹腔内大致情况,并探明肝脏病灶位置、大小,同时确定病灶与周围血管及器官之间的关联,随后将肝周韧带游离,打开小网膜后采用钝头钳将阻断带置于第一肝门,将阻断带加紧,从而对第一肝门的血流起到阻断作用。肝门阻断15 min内将肝实质切除全过程完成,若无法完成则将阻断放开,采用纱布压迫,暂时止血,在5 min以后再继续完成切除肝实质的操作,反复操作,直至肝实质完全切除。
1.2.2对照组采用传统肝门阻断法:对照组患者则在进行肝实质病灶完全切除,并完全止血后将肝脏创面合拢并缝合,若少数患者创面合拢困难则不应强求,强行对拢创面可能会造成患者胆管扭曲,对胆汁回流产生影响,可采用“8”字缝扎对创面进行止血处理,同时也能有效预防胆漏,后行生物胶喷涂或大网膜填塞来封闭创面。
1.2.3观察组采用肝门再次阻断法:完成肝实质切除后止血,用蒸馏水冲洗创面后对肝门再次阻断,阻断位置在于胆总管远端,可能会导致患者胆管压力提升,胆汁可能会由胆管残端或破口处外溢,选用纱布对创面进行加压覆盖5 min,对纱布情况进行观察,确认其是否发生黄染,并明确其黄染位置,若出现可疑黄染位置,则应采用3-0或5-0无损伤血管缝线进行逐一缝合结扎。再次确认其是否存在胆漏后,才能将阻断带松开,随后将肝创面进行缝合,手术完成后由主刀医生依据术中情况判断引流管放置位置及数量。两组均持续随访30 d,观察应用效果。
1.3观察指标:观察两组临床指标情况,比较两组肝功能指标水平,并统计两组胆漏及并发症发生率。①记录手术时间、术中出血量、术中输血量、术后腹腔引流量、术后住院时间等。②术后1 d、5 d及1个月采用常规肝功能检查丙氨酸氨基转移酶(ALT)、总胆红素(TBIL)、血浆凝血酶原时间(PT)、前白蛋白等指标水平。③根据不同分级标准统计胆漏发生率[7]。A级:胆漏引起的临床表现不需进一步的临床治疗;B1级:在没有任何治疗下胆漏的持续时间为1 w以上;B2级:胆漏需要行影像学或内镜下治疗;C级:胆漏所引起的临床表现较为严重,需要进行剖腹探查。④统计切口感染、胸腔积液、腹水并发症发生率。
1.4统计学处理:选择SPSS24.0统计软件分析数据,选择t及χ2检验。
2 结果
2.1两组临床指标情况比较:两组患者手术时间、术中出血量、术中输血量、术后腹腔引流量比较,差异无统计学意义(P>0.05),但观察组住院时间短于对照组,差异有统计学意义(P<0.05)。见表1。
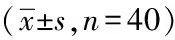
表1 两组临床指标情况比较
2.2两组术后1 d、5 d及1个月肝功能指标水平对比:两组患者术后1 d、5 d及1个月ALT、TBIL、PT、前白蛋白指标水平比较,差异无统计学意义(P>0.05)。见表2。
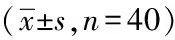
表2 两组术后1 d、5 d及1个月肝功能指标水平对比
2.3两组患者并发症发生率比较:观察组并发症发生率2.50%(1/40,胸腔积液1例)低于对照组的10.00%(4/40,切口感染1例,胸腔积液1例,腹水2例),但差异无统计学意义(χ2=1.920,P=0.0160)。
2.4两组患者胆漏发生率比较:观察组40例未发生胆漏情况,发生率为0.00%;对照组40例发生5例压力性损伤,发生率为12.5%,两组差异有统计学意义(χ2=5.333,P<0.05)。
3 讨论
HCC 是临床较为常见的恶性肿瘤,临床症状表现为肝区疼痛、食欲减退、消瘦等,极易侵犯胆总管、肝内门静脉,严重危害患者生命健康[8]。随着外科手术的技术水平不断进步,目前临床治疗HCC患者重心可能向“微创”和“巨创”(肝移植)方面倾斜,但肝切除术仍然是临床的首选方法[9]。由于肝脏特殊的内、外复杂解剖的特殊性和丰富的血液供应关系,术中术后容易发生出血、肝衰竭、胆漏等并发症。胆漏是指胆汁从正常胆管流出的临床表现,若胆漏得不到及时处理,会增加盆腔炎、腹膜炎发生概率,影响患者预后康复,甚至危及患者生命安全[10]。因此,如何合理有效的预防肝切除术后胆漏的发生对于临床具有重要意义。
肝切除术后胆漏主要原因有以下几种:①肝断面细小胆管未被发现;②操作不当导致胆管损伤或横断未及时发现;③肝断面的肝组织缺血坏死,从而致使末梢胆管漏胆;④胆道梗阻后胆管压力增高;⑤肝断面的感染;⑥术中未能对较大胆管进行有效的结扎。对于肝切除后肝断面胆漏发生重在预防,提高外科医生操作技能并正确处理肝断面尤为关键。目前国内外学者对预防肝切术后胆漏研究方法较多,如肝断面生物封闭;术中生理盐水、脂肪乳剂等胆漏试验;术中胆道造影及对胆管内注入气体发现渗漏处等。其中临床应用较为广泛的为术中胆漏试验,但临床效果不太理想,术后胆漏的发生率仍存在较高的风险。此外,使用造影剂可能造成肝脏断面发生污染,容易使机体发生过敏反应,致使小的胆漏点难以发现,增加胆管打开的概率,不仅延长患者手术时间,还增加对身体的手术创伤,其临床应用价值仍有待商榷。自Pringle首次拇指、食指和中指捏住肝蒂来暂时止血的方法,广泛应用于临床,一直沿用至今。但由于一次肝门血流阻断时间有限,一次阻断不能完成肝切除,尤其是较为复杂的肝切除术需多次阻断肝门。Pringle阻断法对于较复杂的肝切除术多采用间歇阻断法,而间歇期增加肝断面出血。Pringle法入肝血流后,使肝脏处于缺血状态,肝脏对缺血、缺氧更敏感,增加肝功能损伤,甚至有可能发生肝衰竭,影响术后恢复[11]。目前,尚未有HCC病灶切除后应用肝门再次阻断的方式进行肝断面血管和胆管的检查及降低胆管发生率的相关研究报道。本研究提示肝门再次阻断法与传统阻断法对肝功能指标、围术期指标及并发症差异无统计学意义,但观察组术后未发生胆漏。分析其原因,实施再次阻断肝门后使肝内胆管内部压力升高,使胆管内的胆汁可通过胆管破口或残端处向外流出,然后观察纱布是否有黄染现象或黄染位置,达到准确的判断术中胆漏的发生情况,可以及时对胆漏做出处理,从而降低术后胆漏的发生。然而,本研究也存在一定的不足之处,如样本量较少,肝门再次阻断法阻断次数增加,增加手术时间,可能会增加肝功能损伤的风险,故还需后续临床扩大样本量研究其应用价值。
综上所述,肝门再次阻断法能够有效降低肝切除术后胆漏的发生率,临床效果良好。
