水合作用与 pH 调控两性离子聚合物刷的相变行为
2024-01-18李康睿王书恒刘彼得赵新军李九智
李康睿,李 循,王书恒,刘彼得,赵新军,李九智
(1.伊犁师范大学 物理科学与技术学院 新疆凝聚态相变与微结构实验室,伊宁 835000;2.伊犁师范大学 微纳电传感器技术与仿生器械实验室,伊宁 835000; 3.新疆维吾尔自治区人民医院 泌尿外科,乌鲁木齐 830000)
1 引 言
防污材料在生物传感器、生物医学植入物和海洋工业中有着广泛的应用[1,2].近年的研究发现[3-5],由于两性离子聚合物(ZP)单体含有相等数量的阳离子和阴离子基团,可以保持整体电荷中性状态,并且聚合物中阳离子和阴离子官能团的结合,通过提供水合保护层来防止与活性生物体中的细胞和细胞成分发生不必要的相互作用.因此,ZP刷作为防污表面材料呈现了极强的抗污性,在各种生物医学、组织工程领域应用中具有潜在的应用前景[6-10].
ZP的防污能力与表面的静电诱导水合层密切相关,因为紧密结合的水分子形成物理和能量屏障,以防止生物分子和生物体的非特异性吸附[11].ZP在不同应用中的性能归因于其单体特异的水合特性,这产生蛋白质-聚合物缔合的物理和能量障碍[12].实验研究表明,两性离子材料的表面水合性能受材料的化学结构、离子强度、pH 等影响[13].通过离子、pH,可调节ZP单体的带电特性[14],由于静电链间/链内结合,水合程度降低,许多两性离子刷会在低离子强度下采用塌缩构象.因为静电链间/链内偶极-偶极相互作用会因离子强度的增加而减弱,两性离子刷在高离子强度下会表现出溶胀的构象,水化程度相对较高.由于水合作用在和大程度上调节两性离子刷的构象行为,因此,两性离子刷的蛋白质抵抗性能与刷的构象密切相关[14,15].这样,大多数两性离子刷的水合性,以及刷内的离子强度、pH 值等环境因素会显著改变两性离子刷的防污性能[16-18].确定ZP刷特异的构象行为对其改变材料界面特性至关重要[19,20].深刻理解水合作用与 pH 调控ZP刷的相变行为,对于设计ZP抗污材料是非常重要的.Kumar 和 Fredrickson[21]通过变分方法研究了水溶液中多两性离子分子的构象特征,研究发现了在小离子存在的情况下,回转半径显示为静电相互作用的筛选和两性离子位点上的反离子吸附的相互作用,给出了筛选的电荷-偶极子和偶极子-偶极子相互作用势的函数形式,预言了两性离子单体上的抗衡离子吸附是不对称的.Mahalik 等人[22]通过建立理论模型,研究了浸入极性溶剂中的平面偶极聚合物刷的结构特性,结果表明,对偶极相互作用的显式处理会产生宏观浓度依赖性有效“χ”(Flory-Huggins-like 相互作用)参数.此外,依赖于浓度的χ参数促进了ZP刷的相分离,由偶极相互作用引起的均相失稳表现为平面聚合物刷中的垂直相分离.Peng 等人还[23]使用两性离子聚(4-乙烯基吡啶)丙烷-1-磺酸盐 (PVPS)合成了嵌段共聚物(BCP),研究发现,由于多两性离子中静电相互作用引起的自聚集趋势,PVPS 和大多数中性聚合物之间的 Flory-Huggins 参数(χ)相对较高.我们也应用分子场理论[24]研究了暴露于水蒸气中的亲水性ZP刷的构象与结构.尽管对ZP体系的性质进行了许多详细的研究,但尚不清楚水合作用与pH 对ZP刷构象转变的调控特性,水合性耦合 pH 调控的静电效应,将会使得ZP刷呈现出更为丰富的相行为.
在本文中,我们将 Flory-Huggins 理论模型推广应用到 ZP 刷体系,考虑聚考虑体系中的水合作用、静电作用,以及 ZP 刷体系中的水合作用的耦合特性,研究水合作用与 pH 调控 ZP 刷的构象转变行为,深刻揭示水合作用与 pH 调控ZP刷的构象转变的机理,预言新的相变特性.
2 理论模型
ZP 刷浸没在不同 pH 的水溶液中,pH 调控 ZP 单体的解离、质子化.ZP链与水的水合作用,以及体系中的静电效应,ZP 刷体系单位面积的巨势可表示为:
βF=Fel+Fα+Fmix+FE+Urep+Fμ
(1)
上式中β表示1/kBT,巨势方程 (1)中第一项表示 ZP 刷的弹性能[25],以及 ZP 链与水分子的相互作用能:
βFel=N(T)σφ-7/4+χφφw
(2)
式中N(T) 表示与温度相关的弹性强度[25],σ为单位面积的聚合物链数,即接枝密度,可取值N(T)σ=0.08.φ=φ0(L0/L)为 ZP 刷内聚合物链单体的体积分数,L0和φ0分别为平衡态时ZP刷的高度与体积分数.φw是水分子的体积分数,χ为 Flory 相互作用参数,χ表示 ZP 刷与水分子间的有效相互作用势,还参数代表水分子-ZP间的水合作用,χ<0表示了 ZP 刷与水分子间的吸引作用,χ>0 则表示排斥作用.
巨势方程 (1)第二项表示 ZP 单体质子与解离对体系巨势的贡献,可表示为[21]
(3)

巨势方程 (1)第三项表示体系混合熵[24],可表示为
Fmix=φw[ln(φw)-1]+φ+[ln(φ+)-1]+
φ-[ln(φ-)-1]
(4)
式中φ+与φ-分别表示氢离子浓度([H+])和氢氧根离子浓度([OH-]).
巨势方程 (1)第四项表示体系静电相互作用[26],可表为
FE=(φ+-φ-+α+φ-α-φ)ψ
(5)
体系电中性的约束条件为:
φ+-φ-+α+φ-α-φ=0
(6)
巨势方程 (1)第五项表示排斥体积相互作用
Urep=λ(φ++φ-+φ+φw-1)
(7)
式中λ为排斥作用力场,可以通过约束条件
φ++φ-+φ+φw=1
(8)
确定.
巨势方程 (1)中的最后一项表示 H+和OH-的化学势对巨势的贡献[24],可表为
(9)

对巨势方程 (1)中的φ、φw、φ+与φ-取变分并最小化巨势,可得以下非线性方程组:
(10)
φw-exp(-χwφ-λ)=0
(11)
φ+-exp(-λ-ψ-μ+)=0
(12)
φ--exp(-λ+ψ-μ-)=0
(13)
ZP 单体的带正电荷与带负电荷的分数,即:质子化度与解离度可表为[26]
(14)
(15)
上式中K+与K-为酸碱反应平衡常数,在本文中可取值为K+=K-=0.5.
上述方程中的未知量,可通过将方程式 (10)-(15)代入约束条件 (6)和 (8)确定.
3 结果与讨论
本节中,分析讨论χ与 pH 调控ZP刷的相变行为,深刻揭示水合作用与 pH 调控 ZP 刷构象转变.
图1 呈现了在不同 pH 条件下,ZP 刷的体积分数随水合作用改变的函数关系.从图中可以看出,随着χ的增加(之前的研究已经揭示出通过温度、氢键形成均可以使得水合作用改变),ZP 刷的体积分数先是缓慢增大,而后经过急剧升高到达稳定值不变.由此表明了随着水合作用的减弱,ZP 刷经历了从溶胀到塌缩的转变,出现了明显的相变行为.这是由于,水合作用增强时,水对于 ZP 是良溶剂,ZP 单体很容易溶于水溶液中,ZP 分子链将会处于伸展状态,以降低构象熵,与此同时,由于 ZP 分子链的伸展导致的 ZP 刷的溶胀,会使得刷内出现较多的水分子,增加了水分子的平动熵,ZP 刷体系总的熵增加.随着水合作用的减弱,水分子对 ZP 链单体有吸引作用变为排斥作用,展现了从良溶剂-θ溶剂-不良溶剂的转变,ZP 链在水分子排斥作用下逐渐蜷缩,ZP 刷出现从溶胀到塌缩的转变.当 ZP 刷处于塌缩态,ZP 链的构象熵增加,刷内水分子被排出刷外,增加了平动熵.从图1 a 还可以看出,当 pH= 7 时,ZP 刷呈现了与中性高分子刷相同的构象转变行为(插图显示了中性高分子刷的体积分数随水合作用改变的函数关系).随着 pH 的变化,ZP 刷构象转变行为明显改变,当 pH<7 时,随着 pH 的减小,ZP 刷体积分数减小,由此表明了随着 pH 的降低,ZP 刷的溶胀程度增加;当 pH>7 时,随着 pH 的增加,ZP 刷体积分数减小,表明了增加的 pH 也会使得 ZP 刷的溶胀程度增加,并且,较小的 pH 与较大的 pH 期呈现了完全相同的调控作用[27].这是由于当 pH= 7 时,ZP单体带有等量的正负电荷,每个单体呈现了电中性状态,静电作用对于ZP 刷的构象转变几乎不起作用,其构象转变行为完全取决于水合作用,溶剂效应对刷的构象转变起的主要作用.随着 pH 的改变,当 pH<7 时,ZP 单体所带正电荷多于负电荷量,在 ZP 链内产生静电排斥作用,使得 ZP 链进一步伸展,ZP 刷溶胀度增加.当 pH>7 时,ZP 单体所带负电荷则多于正电荷量,增多的负电荷同样可以在 ZP 链内产生静电排斥作用,使得 ZP 链进一步伸展,因此,较小 pH 与较大的 pH 对于 ZP 刷的调控展现了完全相同的调控效应.另外,从图中还可以看出,pH 改变 ZP 刷构象转变的临界χ值,由此也表明了,除了水合作用,通过 pH 调控的 ZP 刷的带电特性的改变,也可以在很大程度上调控 ZP 刷的构象转变行为.
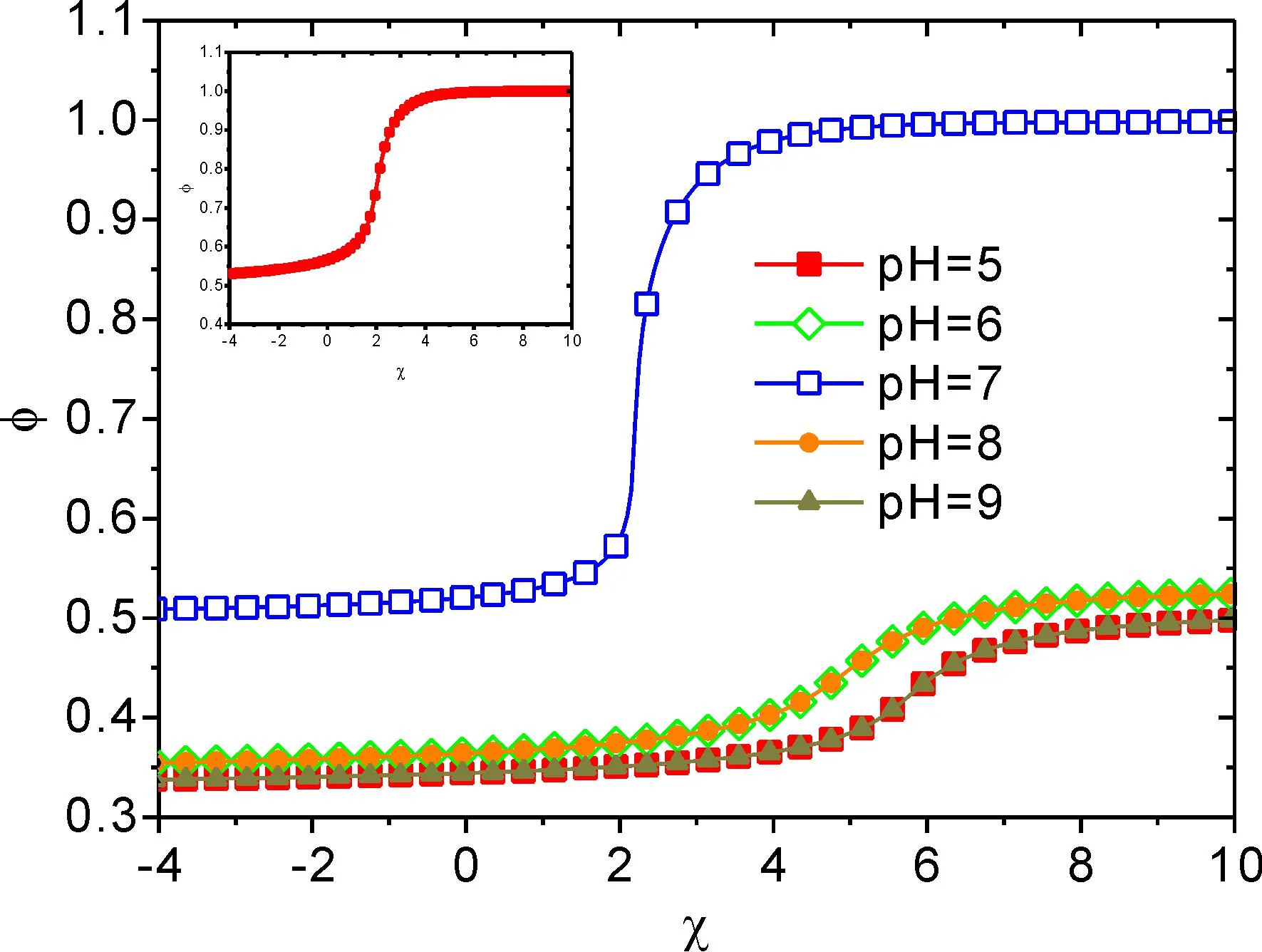
图1 在不同 pH 条件下,ZP 刷的体积分数随水合作用变化的函数关系.插图为:中性高分子刷的体积分数随水合作用χ 改变的函数关系.
图2 显示了不同 pH 条件下 ZP 单体质子化度和解离度随水合作用变化的函数.从图中可以看出,ZP 单体质子化度和解离度随着 ZP 刷水合性减弱而减小.这是由于,ZP 刷水合性减弱使得刷塌缩,蜷缩状态的 ZP 链单体减少了与 H+、OH-的酸碱反应几率,因此,ZP 单体质子化度与解离度随着水分子与 ZP 链水合性减弱而减小.由此也表明了,ZP 链水合性与链内的静电作用相互耦合,共同调控这 ZP 刷的相变行为.另外,从图4 还可以看出,ZP 链单体的质子化度和解离度随着 pH 改变表现出相似的变化行为:当 pH<7 时,ZP链的质子化度随着 pH 的降低而升高;当 pH>7 时,ZP链的解离度随着 pH 的增大而增大.这是由于,当 pH<7 时,溶液中 H+浓度增加,ZP 聚合物单体的酸碱平衡向带电状态移动,聚合物变得更带正电,ZP 链将会带有较多的正电荷.当 pH>7 时,继续增加 pH 值,OH-浓度增加,ZP 会有较多而单体解离,使得带负电的单体数目增多.随着 ZP 链单体出现过多净电荷的增加,静电排斥导致 ZP 链拉伸,进而使得 ZP 刷溶胀.
图3a、3b、3c 显示:在不同 pH 条件下,阳离子(H+)体积分数与阴离子体积分数随χ的变化关系.从图中 3 可以看出,当 pH=7 时,ZP 链带正电荷与带负电荷单体数目相同,ZP 刷呈现了和中性聚电解质刷相同的构象转变行为,离子的分布特性将几乎完全决定于 ZP 刷体系的渗透压,刷内阳离子(H+)体积分数与阴离子体积分数呈现了和溶液中几乎相同的分布.图3 c 呈现了pH=7 时的 ZP 刷体系渗透压随着χ先较快减小后增加之稳定不变,由此表明了 ZP 刷体系维持水分子、阳离子、阴离子一定的化学过程中的势渗透压效应.
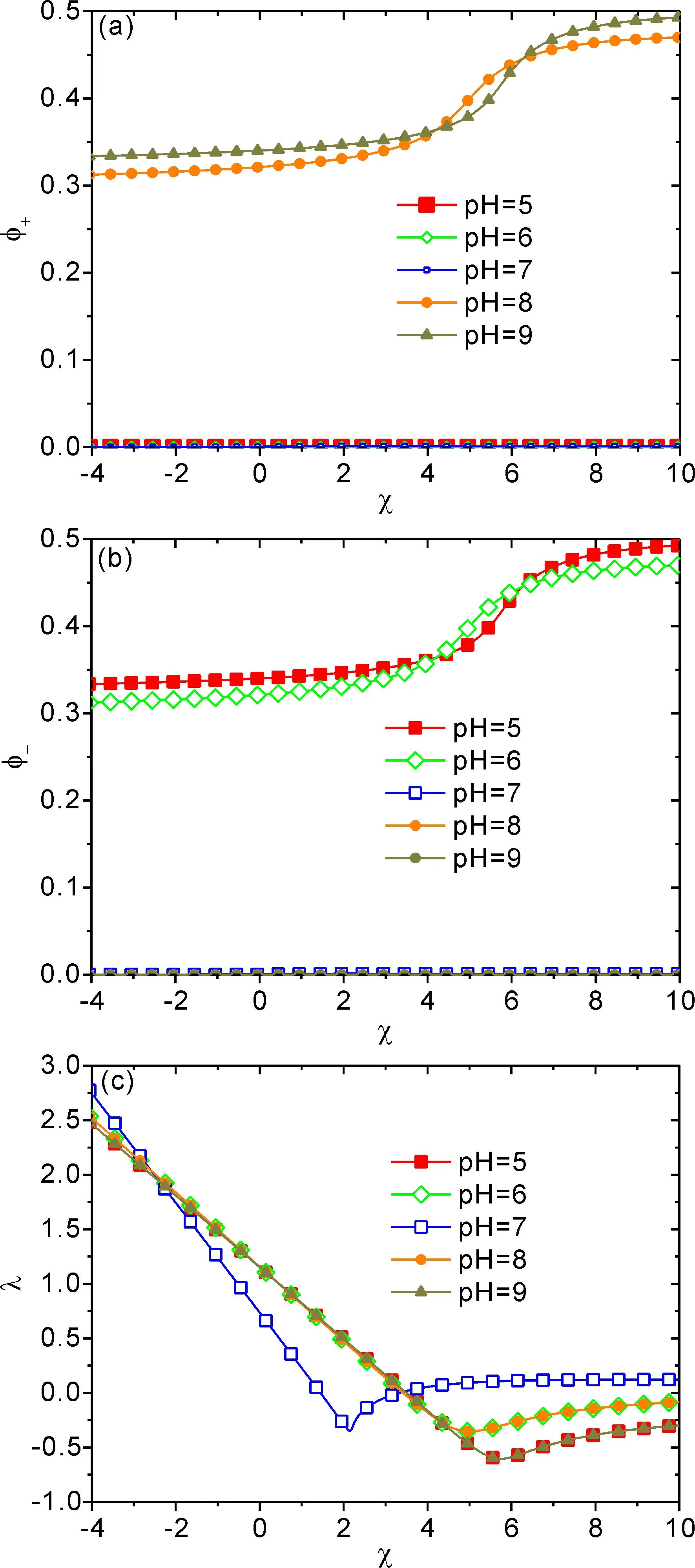
图3 在不同 pH 条件下阳离子、阴离子体积分数、渗透压随水合作用变化的函数关系.
随着 pH 的改变,从图中 3a、3b 显示了阳离子体积分数在当 pH>7 时呈现了较高的分布,并且随着 pH 增大而增加;阴离子体积分数在 pH<7 时呈现了较高的分布,并且随着 pH 减小而增加;这是由于当 pH>7 时,ZP 单体有与解离度增加,其带负电荷单体多于带正电荷单体,出现了带负电荷的单体与 H+的静电吸引作用,使得过多的 H+凝聚在 ZP 链附近,导致在 ZP 刷内 H+分布较多,同时,ZP 链其带负电荷单体会与 OH-产生静电排斥,使得 OH-很难分布于 ZP 链附近,导致在刷内的 OH-分布过少.与此相反,当 pH>7 时,ZP 链所带正电荷单体多与带负电荷的单体,由于带正电荷的单体与OH-的静电吸引,使得较多OH-凝聚在 ZP 链附近,在 ZP 刷内OH-分布较多,而对 OH-,由于受到 ZP 链带正电荷的单体的静电排斥,使其较少分布于 ZP 刷内.因此,当 ZP 链单体呈现绝对多的净电荷会使得 ZP 刷体系静电势改变,进而改变阳离子(H+)体积分数与阴离子分布特性.因此,当 ZP 链单体呈现绝对多的净电荷阳离子与阴离子的分布不仅决定于渗透压效应(图3a和图3b中pH>7 与 pH<7 阳离子与阴离子随着χ增大而增加,以及 图3 c 呈现的 ZP 刷体系渗透压变化随着χ先减小后增加,且 PH<7 与 pH>7 时的 ZP 刷体系渗透压变化缓于 pH=7 时的 ZP 刷体系渗透压),而且在很大程度上取决于刷体系的静电势.
图4 显示了不同 pH 值条件下,ZP 刷内部的静电势分布,应该强调的是,溶液中的所有带电物质都会产生相应的静电势.从图4 和可以看出,pH=7 时,ψ随着χ的变化关系呈现了ψ=0不变.这是由于,ZP 链ZP 刷呈现了和中性聚合物刷相同的构象转变行为,离子的分布完全决定于ZP 刷体系的渗透压,刷内阳离子(H+)体积分数与阴离子体积分布相同的,使得体系电中性.
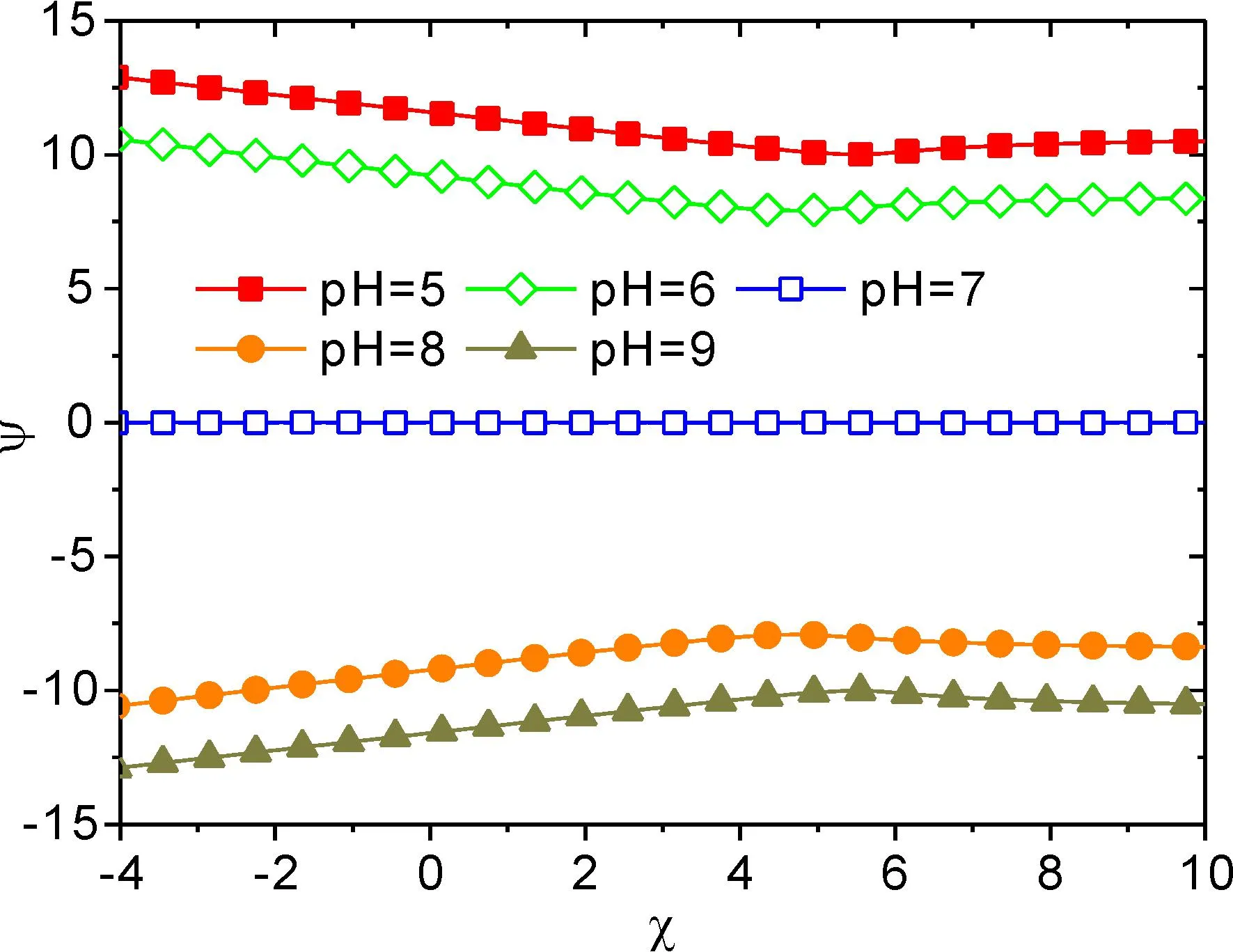
图4 在不同 pH 条件下,体系静电势随水合作用变化的函数关系.
当 pH>7 时,ZP 单体解离度增加,ZP 链呈现了负电荷特性,导致在 ZP 刷内静电势呈现负值;当 pH<7 时,ZP 链带电性反转,其多数单体带正电荷,使的 ZP 刷电势呈现正值.因此,当 ZP 链单体呈现过多的正负电荷,会在很大程度上决定 ZP 刷体系静电势,进而影响其相变行为.当 pH>7 时与当 pH<7 时,随着水合性的减弱,ZP 刷会在一定程度上溶胀,使其单体质子化度与解离度,随着刷的溶胀塌缩行为改变,进而影响体系静电势,由此进一步表明了,这种由于水合性与静电特性的耦合效应,共同决定着 ZP 刷的构象转变行为.水合性与静电特性的耦合作用,使得 ZP 刷体系向这些自由能降低的方向演化,调控 ZP 刷的相变行为.
图5 中显示了不同 pH 值条件下,ZP 刷体系自由能随χ改变的函数关系.从图中可以看出,随χ改变自由能呈现了极大值,随着 pH 值的变化,自由能呈现的极大值随之改变.在自由能极大值处表明了体系的不稳定性,由此导致 ZP 刷出现相变行为.从图6 可以看出,随着 pH 的较小或增大,自由能变大,并且极大值进一步增加,由此表明了 pH 改变体系的自由能状态,使得体系失稳.通过 pH 调节,ZP 链单体带有过多的净电荷,使得 ZP 刷排斥性增加,体系自由能升高.相比较中性聚合物刷,pH 通过调节 ZP 链单体的带电荷状态,改变着 ZP 刷构象转变的相变行为,在一定程度上决定着 ZP 链构象的溶胀、塌缩状态.
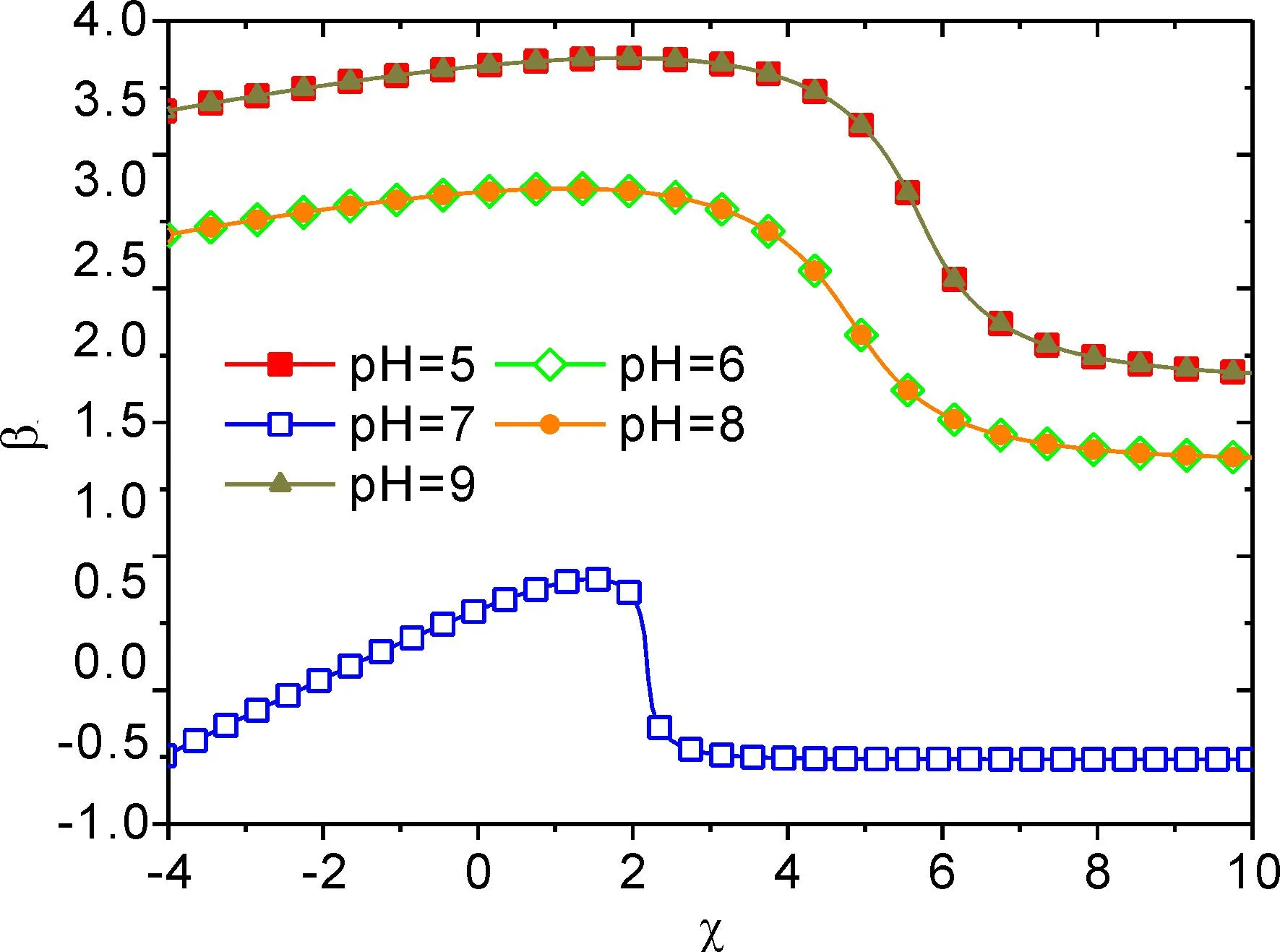
图5 在不同 pH 条件下,自由能随水合作用变化的函数关系.
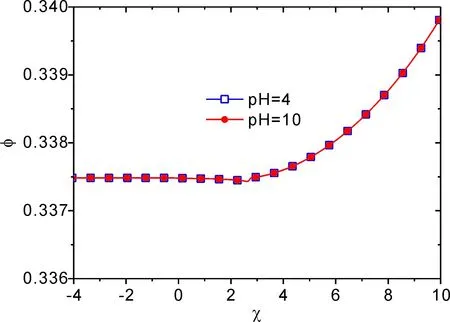
图6 pH=4与pH=10时,ZP 刷的体积分数随水合作用变化的函数关系.
图6 呈现了pH=4 与 pH=10 时,ZP 刷的体积分布,从图中可以看出 ZP 刷体积分数始终处于较小状态,由此表明了 ZP 刷构象始终处于溶胀态,Alswieleh 等人[28]的实验的确发现,在 Ph<4 和 Ph>10 时,ZP 刷会呈现出极为相似的溶胀特性.这是由于当 Ph<4 和 Ph>10 时,ZP 链单体将会分别完全处于质子化和解离度状态,使得 ZP 刷静电排斥作用极强,水合性在改变其构象转变行为过程中几乎不起作用.因此,ZP 刷始终处于溶胀的构象状态,这是 ZP 刷的相变行为完全由静电作用调控,其构象行为完全取决于静电效应,随着水合性变化,ZP 刷不会出现相变行为.
4 结 语
我们基于 Flory-Huggins 理论,建立理论模型,研究水合作用与 pH 调控ZP刷的相变行为.理论模型考虑 ZP 刷体系中的静电作用与水合作用的耦合特性.研究发现,在不同 pH 条件下,ZP 刷的体积分数随着水合作的减弱而的增加随着 pH 的变化,ZP 刷构象转变行为明显改变,当 pH<7 时,随着 pH 的减小,ZP 刷体积分数减小,由此表明了随着 pH 的降低,ZP 刷的溶胀程度增加;当 pH>7 时,随着 pH 的增加,ZP 刷体积分数减小,表明了增加的 pH 也会使得 ZP 刷的溶胀程度增加,并且,较小的 pH 与较大的 pH 期呈现了完全相同的调控作用.这是由于,当 pH<7 时,溶液中 H+浓度增加,ZP 聚合物单体的酸碱平衡向带电状态移动,聚合物变得更带正电,ZP 链将会带有较多的正电荷.当 pH>7 时,继续增加 pH 值,OH-浓度增加,ZP 会有较多而单体解离,使得带负电的单体数目增多.随着 ZP 链单体出现过多净电荷的增加,静电排斥导致 ZP 链拉伸,进而使得 ZP 刷溶胀.当 pH>7 时,ZP 单体解离度增加,ZP 链呈现了负电荷特性,导致在 ZP 刷内静电势呈现负值;当 pH<7 时,ZP 链带电性反转,其多数单体带正电荷,使的 ZP 刷电势呈现正值.因此,当 ZP 链单体呈现过多的正负电荷,会在很大程度上决定 ZP 刷体系静电势,进而影响其相变行为.当 pH>7 时与当 pH<7 时,随着水合性的减弱,ZP 刷会在一定程度上溶胀,使其单体质子化度与解离度,随着刷的溶胀塌缩行为改变,进而影响体系静电势,由此表明了,这种由于水合性与静电特性的耦合效应,共同决定着ZP 刷的构象转变行为.水合性与静电特性的耦合作用,使得 ZP 刷体系向这些自由能降低的方向演化,调控 ZP 刷的相变行为.通过考察体系自由能我们还发现,ZP 刷体系自由能呈现了极大值,随着 pH 值的变化,自由能呈现的极大值随之改变,由此表明了体系的不稳定性,进而导致 ZP 刷出现相变行为.
之前的研究[21-24,27,28,30]已经揭示出通过温度、氢键、盐离子等形成均也可以使得水合作用改变.另外,H+和OH-作为 ZP 链带负电荷与带正电荷时的抗衡离子,由于静电相互作用,会在沿 ZP 链方向产生H+和 OH-介导的 ZP 刷链之间的静电吸引力,以及抗衡离子熵压,进而促使 ZP 刷进一步塌缩[29].本文理论模型没有考虑盐离子效应,对于抗衡离子的静电屏蔽效应还没有进一步讨论,只考虑了 pH 与水合性对 ZP 刷的构象转变作用,理论结果符合实验观测[27,28,30],由此表明了,水合性与静电特性的耦合作用会在很大程度上调控 ZP 刷的相变行为.
