25例儿童患者应用免疫检查点抑制剂的不良反应调查和分析Δ
2024-01-18郑英明李新刚
杜 丰,李 哲,郑英明,李新刚
(首都医科大学附属北京友谊医院西药剂科,北京 100050)
近年来,儿童血液肿瘤学者逐步开始关注以程序性死亡受体1(programmed death-1,PD-1)或程序性死亡受体配体1(programmed death-ligand 1,PD-L1)为靶点的免疫检查点抑制剂在儿童肿瘤及恶性血液系统疾病方面的研究进展[1-6]。但是,目前上市的PD-1/PD-L1抑制剂的药品说明书中均提到,“尚无本品在18岁以下儿童及青少年中的安全性和有效性数据”,或“在儿童人群(<18岁)中的安全性和有效性尚不明确”。本研究对PD-1/PD-L1抑制剂治疗儿童恶性实体肿瘤和血液系统肿瘤期间出现的不良反应进行调查和临床分析。
1 资料与方法
1.1 资料来源
2019年1月1日至2022年9月15日于我院接受PD-1/PD-L1抑制剂治疗各类恶性实体肿瘤和血液系统肿瘤的儿童患者共25例,共接受137次治疗。其中男性16例,女性9例,年龄1~17岁,其他一般资料见表1。本研究涉及患儿的隐私信息,已做好相应保密措施,经我院生命伦理委员会审查批准(批件号:2021-P2-162-01)。

表1 25例患儿的一般资料Tab 1 General data of 25 children
1.2 常用的PD-1/PD-L1抑制剂及其用法与用量
常用的PD-1/PD-L1抑制剂:信迪利单抗注射液,1次200 mg,每3周给药1次;帕博利珠单抗注射液,1次200 mg,每3周给药1次,或1次400 mg,每6周给药1次;利妥昔单抗注射液,375~500 mg/m2,1周1次;派安普利单抗注射液,1次200 mg,每2周给药1次。25例患儿中,5例按照常规剂量给药,20例减少剂量给药。
1.3 方法
通过医院病案查询系统,记录使用PD-1/PD-L1抑制剂的患儿在治疗期间有关药品不良反应发生情况,如患儿的入院记录、病程记录、护理单、实验室检查、影像学检查、用药医嘱等,并根据患儿情况,对每例药品不良反应进行相关性评价,包括不良反应的类型和分级,评价标准参考不良事件评价标准(CTCAE)5.0版[7]。
1.4 统计学方法
对本研究收集的实验数据采用统计学软件SPSS 19.0进行统计分析,相关计数信息采用χ2检验进行比较,P<0.05为差异有统计学意义。
2 结果
2.1 不良反应发生情况
16例患儿出现了药品不良反应,程度各不相同,其中12例患儿发生1种不良反应,4例患儿发生2种不良反应,最终共纳入20次不良反应,平均0.8次/例,相关内容见表2。PD-1/PD-L1抑制剂的具体药品及其不良反应发生情况见表3。
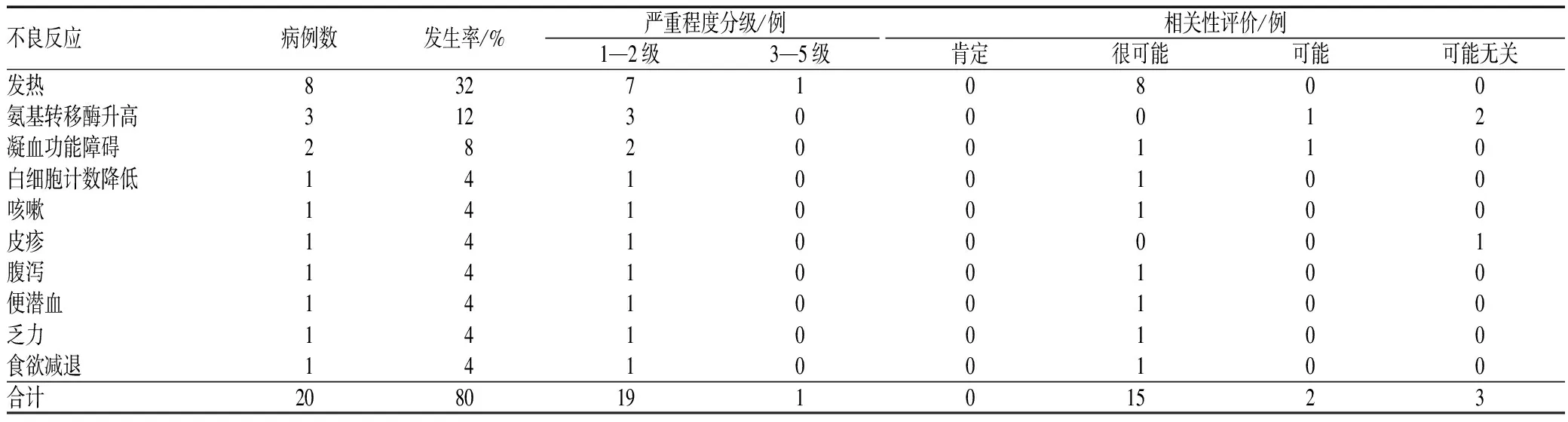
表2 使用PD-1/PD-L1抑制剂患儿的不良反应发生情况Tab 2 Adverse drug reactions in children treated with PD-1/PD-L1 inhibitors

表3 PD-1/PD-L1抑制剂的具体药品及其不良反应发生情况Tab 3 Specific drugs and adverse drug reactions of PD-1/PD-L1 inhibitors
2.2 影响因素
患儿的性别、年龄、是否为一线使用及是否与其他抗肿瘤药物联合应用等因素对患儿使用PD-1/PD-L1抑制剂的不良反应发生率的影响进行分析,结果见表4。
2.3 不良反应再激发情况
有4例发生不良反应的患儿,在不良反应缓解或不影响后续治疗的情况下,再次接受了PD-1/PD-L1抑制剂治疗。其中2例患儿出现了新的不良反应:1例患儿先前的不良反应为白细胞计数降低,其严重程度分级为3—5级,相关性评价为“很可能”,出现的新的不良反应为发热;1例患儿先前的不良反应为腹泻,其严重程度分级为1—2级,相关性评价为“很可能”,出现的新的不良反应为白细胞计数降低。
3 讨论
研究结果证实,PD-1/PD-L1抑制剂是恶性实体肿瘤及血液系统肿瘤的安全、有效、广谱的治疗药物[5-6,8]。在霍奇金淋巴瘤、噬血细胞综合征、EB病毒感染等儿童患者中,以PD-1/PD-L1为代表的免疫检查点抑制剂表现出良好的抗肿瘤作用[9-10]。但为了儿童肿瘤患者能够从PD-1/PD-L1治疗中有更多获益,需要更深入地研究其作用机制,以使更多儿童肿瘤患者达到完全缓解或更长久的无进展生存期。
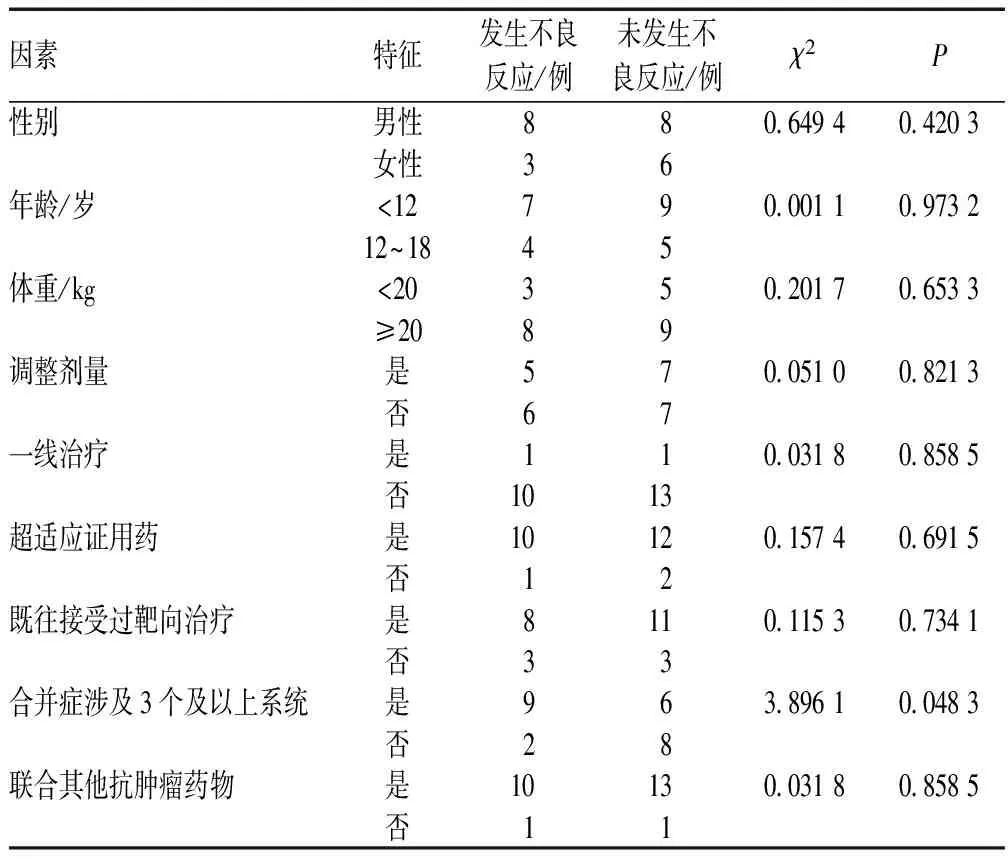
表4 不同因素对患儿使用PD-1/PD-L1抑制剂的不良反应发生率的影响Tab 4 Different influencing factors on incidence of adverse drug reactions of PD-1/PD-L1 inhibitors in children
虽然目前免疫检查点抑制剂的新药和相关研究不断,但其仍是一类应用时间较短的治疗药物,尤其是对于缺少临床数据的儿童患者,要重视安全性研究,需进一步观察应用过程中发生的严重感染及其相关不良反应[11]。并且,临床存在超说明书用药的现象,因此,需重点关注用药安全性。本研究中,使用PD-1/PD-L1的患儿较为常见的不良反应有发热(发生率为32%)、氨基转移酶升高(发生率为12%)、凝血功能障碍(发生率为8%)、白细胞计数降低(发生率为4%)、咳嗽(发生率为4%)、皮疹(发生率为4%)、腹泻(发生率为4%)、便潜血(发生率为4%)、乏力(发生率为4%)以及食欲减退(发生率为4%)等,基本与多种PD-1/PD-L1的药品说明书及其他研究中的不良反应种类相似[12]。从发生率的角度分析,发热的发生率显著高于其他研究。尽管本研究入组的患儿多为血液系统疾病患儿,发热的概率相较于其他疾病高,但与其他同样以血液系统疾病为主的研究比较,仍处于较高水平。例如,Younes等[13]和Chen等[14]针对霍奇金淋巴瘤的研究中,PD-1/PD-L1抑制剂引起发热的发生率分别为14%和24.3%。分析原因,可能与年龄差异有关。儿童患者使用PD-1/PD-L1抑制剂的过程中,应多关注体温的变化,及时采取不良反应的应对措施。
本研究结果显示,患儿的年龄、性别、体重、是否一线治疗、是否接受过靶向治疗、是否与其他抗肿瘤药物联合应用、是否超适应证用药等因素对不良反应发生率没有显著影响;而合并症涉及3个及以上系统对不良反应发生率有显著影响。当然,合并疾病对不良反应发生率有显著影响的结果也存在过度归因的可能性,因为该部分患儿的不良反应无法完全排除是PD-1/PD-L1以外的原因引起,但无论是哪种可能性,都提示临床在该类患儿使用PD-1/PD-L1期间应加强监护[15-18]。其他因素没有显著影响的原因可能为样本量过小,但由于儿童使用PD-1/PD-L1的比例较低,故现阶段难以进行大样本分析,下一步计划采取与其他医疗机构合作的方式扩大样本量,进行更加客观的数据分析。
综上所述,通过本研究的分析,儿童患者使用PD-1/PD-L1抑制剂进行免疫治疗时,其不良反应发生情况与成人有所差异,临床需注意用药监护,提高儿童用药的安全性。
