艾迪注射液联合紫杉醇+顺铂化疗方案治疗非小细胞肺癌临床疗效及安全性的Meta分析Δ
2024-01-18董昱男巫志姗张景媛庄昌龙吴嘉瑞
董昱男,时 锐,巫志姗,张景媛,庄昌龙,吴嘉瑞#
(1.北京中医药大学中药学院,北京 100102; 2.贵州益佰制药股份有限公司战略市场中心,贵阳 550014)
肺癌是在临床治疗过程中最常见的恶性肿瘤之一,肺癌的发病率、死亡率均极高[1]。2020年,全球因肺癌而死亡的人数多达179.6万例,远超其他恶性肿瘤[2]。肺癌分型中,非小细胞肺癌(non-small cell lung cancer,NSCLC)最为常见。针对不敏感的中晚期NSCLC患者,化疗仍然是一线治疗方案[3]。研究结果显示,紫杉醇/紫杉醇脂质体联合含铂双药治疗可作为NSCLC一线治疗方案[4],紫杉醇联合顺铂(TP)可发挥协同作用[5]。但化疗常出现程度不一的不良反应,以致影响治疗效果。研究结果显示,在原化疗方案基础上加入中医药辅助治疗可以延长老年患者的生存期,改善不良反应,提高生活质量[6-7]。艾迪注射液是目前临床上广泛使用的抗肿瘤中成药,也是NSCLC相关临床研究、循证研究较为丰富的中成药注射剂。为了客观评价艾迪注射液联合TP化疗方案治疗中晚期NSCLC的疗效,本研究采用Meta分析方法,对艾迪注射液联合TP化疗方案治疗晚期NSCLC的有效性和安全性展开评价,以期为临床合理用药提供可参考的依据。
1 资料与方法
1.1 纳入与排除标准
(1)研究类型:艾迪注射液联合TP化疗方案治疗中晚期NSCLC的随机对照试验(RCT),对研究是否采用盲法不做限制,要求论文一般资料齐全。(2)研究对象:所有患者诊断符合《NCCN非小细胞肺癌临床实践指南》[8],并确诊为NSCLC,自愿签署研究知情同意书,年龄、性别、种族不限。(3)干预措施:对照组患者首先进行预处理,予以醋酸地塞米松、盐酸苯海拉明注射液等药物,随后予以紫杉醇注射液和注射用顺铂静脉滴注;研究组患者在对照组用药基础上联合应用艾迪注射液静脉滴注。除此无手术或针灸等其他治疗手段辅助,不对用药剂量、疗程设限。(4)结局指标:主要结局指标为临床疗效、生活质量改善;次要结局指标为不良反应,以上指标包含其一即可纳入。①临床疗效。主要依据世界卫生组织《实体瘤近期疗效评价标准》[9],将疗效分为4个等级。完全缓解,可见肿瘤完全消失,且维持时间≥1个月;部分缓解,肿瘤病灶减少>50%,且维持时间>1个月,无新病变出现;无变化,肿瘤病灶减少≤50%或增大<25%,无新病变,且维持时间≥1个月;进展:肿瘤病灶增大≥25%,发现新的肿瘤病灶。有效率=(完全缓解病例数+部分缓解病例数)/总病例数×100%。②生活质量改善。应用卡诺夫斯凯计分(KPS)对生活质量改善效果进行评价。③不良反应。包括白细胞减少、血小板减少、红细胞减少、胃肠道反应、肝损害、肾损害、周围神经炎。(5)排除标准:重复、不相关的综述及个例相关报道的文献;无法获取全文或数据的文献;治疗过程中存在其他中药、针灸等中医药治疗手段的研究。涉及以上任意一条即可排除。
1.2 文献检索策略
计算机检索中国知网(CNKI)、维普数据库(VIP)、中国生物医学文献数据库(CBM)、万方数据库(Wanfang Data)、PubMed、the Cochrane Library等中外数据库。中文数据库以“艾迪注射剂”或“艾迪注射液”(药物名称)、“非小细胞肺癌”或“肺癌”(疾病名称)及“RCT”或“随机对照试验”为检索词进行检索;英文检索结合主题词与自由词,包括“Eddy’s injection”“Aidi injection”“Non-small cell lung cancer”“Lung neoplasms”“Carcinoma, non small cell lung”等。发表语言不限。同时对纳入文献的参考文献进行手工检索。检索时间为各数据库建库至2023年1月15日。
1.3 文献筛选与数据提取
2名研究员分别进行首次文献筛选。阅读文献题目和摘要,利用NoteExpress软件去重,筛选明显不相关文献(如综述、药理实验等),筛出临床对照研究进行全文阅读,判断其是否达到纳入标准。随即交叉核对数据,遇到分歧时讨论处理,或交由第三方解决。提取数据内容应涵盖:纳入研究的基本信息,包括第一作者、发表年份等;研究病例的基本特征,包括研究组和对照组的病例数、性别组成、平均年龄、干预措施药物用量、疗程等具体细节;观察结局指标和结果测量数据;偏倚风险评价的关键因素。
1.4 纳入研究的质量评价
2名研究者采用Cochrane系统评价手册中的“偏倚风险评估工具”[10]分别评估纳入研究的偏倚风险,如果产生分歧,则讨论处理或由第三方决定。对每项研究的质量评价包括以下主要内容:随机序列生成;分配隐藏;研究者和受试者盲法的实施;结果评价者盲法的实施;结果数据的完整性;选择性报告;其他来源的偏倚。每项内容的评价均分为3个等级,即“高风险”“未知风险”和“低风险”。“高风险”指该实施方法错误并对结果测量造成影响;“未知风险”指研究中未提及,或信息不足无法进行判断;“低风险”指该实施方法正确或不会对结果造成影响。
1.5 统计学方法
数据整理后采用RevMan 5.4软件处理,本研究中仅涵盖二分类变量指标,选用相对危险度(RR)表示,计算P值及95%CI。P<0.05为差异有统计学意义。采用CochraneQ检验分析研究间异质性,并用I2来评价异质性大小;P>0.1,且I2<50%时,采用固定效应模型,否则采用随机效应模型。若结果无显著性,利用风险差异(RD)代替RR再次进行Meta分析,如定性结果无变化,证明Meta分析结果具有可靠性。若发现结果存在临床或方法学异质性,则采用亚组分析或运用STATA 12.0软件运行敏感性分析。应用逐个排除法进行敏感性分析,即每次排除1项研究,对剩余研究重新进行Meta分析,以判断结果的稳定性。若纳入研究数量满足条件,则绘制倒漏斗图,评估其潜在发表偏倚。
2 结果
2.1 文献检索及筛选流程
按照资料收集方法及制定的检索策略,共搜集到相关文献557篇;去重以及通过阅读标题、摘要初筛后纳入文献372篇;进一步阅读文献排除重复或不达标文献105篇,可能符合标准的文献有26篇;再按照排除标准及数据完整性进行筛选,共纳入16篇RCT文献,见图1。
2.2 纳入文献的基本特征
共纳入16篇文献[11-26],合计1 131例患者,其中研究组570例,对照组561例;以中老年人为主,患者年龄最小28岁;单篇文献样本量为39~100例;肺癌分型:鳞癌520例(占45.98%),腺癌522例(占46.15%),鳞腺癌48例(占4.24%),其他类型41例(占3.63%)。同一文献中共同化疗方案相同,研究组相较对照组仅联合应用艾迪注射液。纳入文献的基本特征见表1。
2.3 文献质量评价
纳入研究中,有5项研究[12-16]使用了随机对照表法,对应随机序列产生的选择性偏倚评估为“低风险”;所有研究均未提及选择性偏倚,所有研究数据完整且均未出现选择性报告的现象,以上各项评价为“低风险”;其余风险评价条目由于信息不足均评价为“未知风险”。纳入文献的风险偏倚评价见表2。
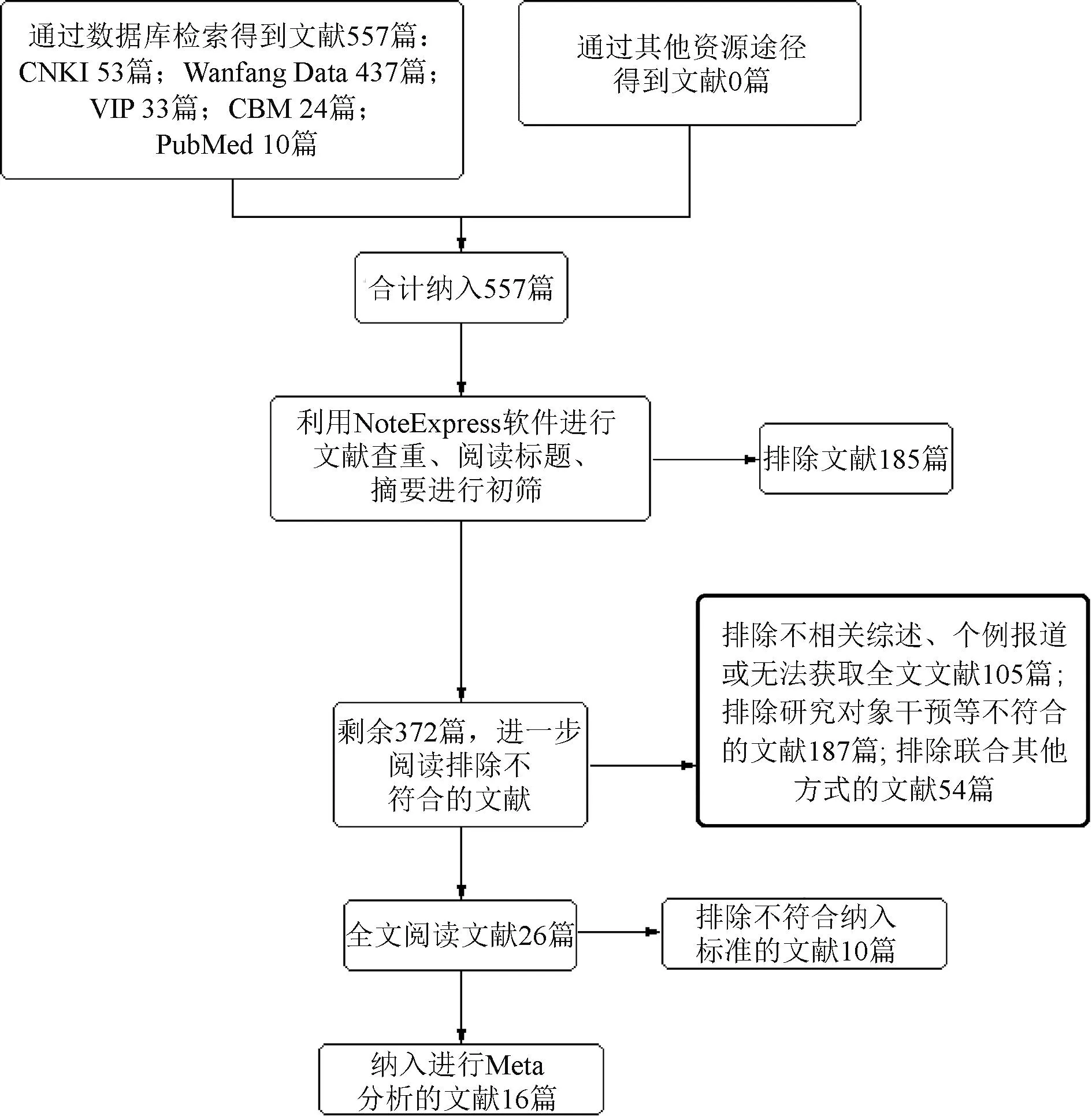
图1 文献检索及筛选流程Fig 1 Retrieval and screening process of literature
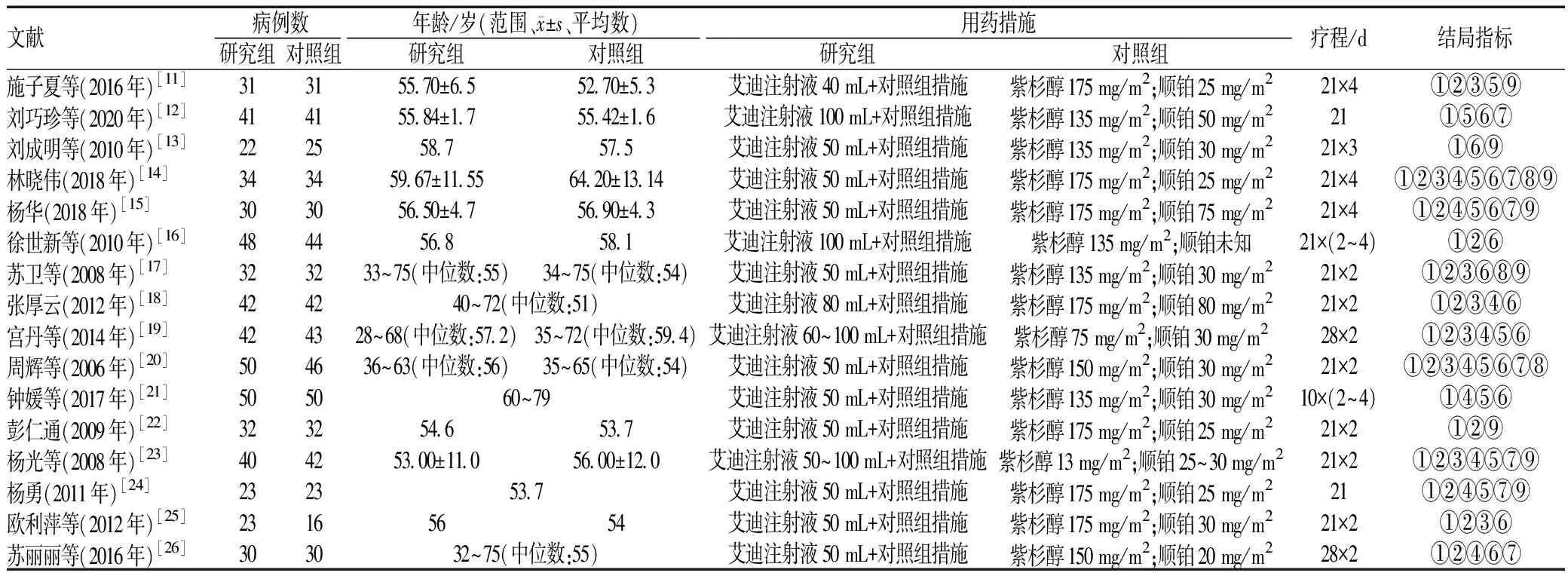
表1 纳入文献的基本特征Tab 1 General characteristics of included literature
2.4 Meta分析结果
2.4.1 有效率:16项研究[11-26]比较了有效率,共540例患者,其中研究组319例,对照组221例。异质性结果显示,P=0.97,I2=0%,采用固定效应模型。Meta分析结果显示,研究组患者的有效率明显高于对照组,差异有统计学意义(RR=1.42,95%CI=1.26~1.61,P<0.000 01),见图2。
2.4.2 KPS评分:11项研究[11,13-15,17-19,22-25]比较了KPS评分,共371例患者,其中研究组237例,对照组134例。异质性结果显示,P=0.75,I2=0%,采用固定效应模型。Meta分析结果显示,研究组患者的KPS评分明显高于对照组,差异有统计学意义(RR=1.76,95%CI=1.52~2.04,P<0.000 01),见图3。
2.4.3 不良反应:(1)白细胞减少。13项研究[11,14-20,22-26]比较了白细胞减少发生率,共319例患者,其中研究组104例,对照组215例。异质性分析结果显示,P=0.21,I2=23%,采用固定效应模型。Meta分析结果显示,与对照组比较,研究组患者的白细胞减少发生率较低,差异有统计学意义(RR=0.47,95%CI=0.39~0.57,P<0.000 01),见图4。(2)血小板减少。8项研究[11,14,17-20,23,25]比较了血小板减少发生率,共107例患者,其中研究组33例,对照组74例。异质性分析结果显示,P=0.86,I2=0%,采用固定效应模型。Meta分析结果显示,与对照组比较,研究组患者的血小板减少发生率较低,差异有统计学意义(RR=0.44,95%CI=0.31~0.62,P<0.000 01),见图5。(3)红细胞减少。3项研究[14,17,20]比较了红细胞减少发生率,共42例患者,其中研究组14例,对照组28例。异质性分析结果显示,P=0.57,I2=0%,采用固定效应模型。Meta分析结果显示,与对照组比较,研究组患者的血小板减少发生率较低,差异有统计学意义(RR=0.48,95%CI=0.27~0.86,P=0.01),见图6。(4)胃肠道反应。14项研究[12-21,23-26]比较了肠胃道反应发生率,共297例患者,其中研究组105例,对照组192例。异质性分析结果显示,P=0.07,I2=38%,采用随机效应模型。Meta分析结果显示,与对照组比较,研究组患者的胃肠道反应发生率较低,差异有统计学意义(RR=0.56,95%CI=0.43~0.72,P<0.000 1),见图7。(5)肝损害。9项研究[11-12,14-15,19-21,23-24]比较了肝损害发生率,共61例患者,其中研究组20例,对照组41例。异质性分析结果显示,P=0.81,I2=0%,采用固定效应模型。Meta分析结果显示,与对照组比较,研究组患者的肝损害发生率较低,差异有统计学意义(RR=0.51,95%CI=0.31~0.81,P=0.005),见图8。(6)肾损害。9项研究[14-15,18-21,23-24,26]比较了肾损害发生率,共22例患者,其中研究组7例,对照组15例。异质性分析结果显示,P=0.94,I2=0%,采用固定效应模型。结果显示,偏向研究组,但无显著性,利用RD代替RR再次进行Meta分析,定性结果无变化,证明Meta分析结果具有可靠性。因此,与对照组比较,研究组患者的肾损害发生率较低,但差异无统计学意义(RR=0.53,95%CI=0.25~1.17,P=0.12),见图9。(7)周围神经炎。7项研究[12,14-15,20,23-24,26]比较了周围神经炎发生率,共68例患者,其中研究组29例,对照组39例。异质性分析结果显示,P=0.92,I2=0%,采用固定效应模型。结果显示,偏向研究组,但无显著性,利用RD代替RR再次进行Meta分析,定性结果无变化,证明Meta分析结果具有可靠性。因此,与对照组比较,研究组患者的周围神经炎发生率较低,但差异无统计学意义(RR=0.76,95%CI=0.50~1.15,P=0.19),见图10。

图2 两组患者有效率比较的Meta分析森林图Fig 2 Meta-analysis of comparison of clinical efficacy between two groups

表2 纳入文献的风险偏倚评价Tab 2 Risk bias assessment of included literature

图3 两组患者KPS评分比较的Meta分析森林图Fig 3 Meta-analysis of comparison of KPS score between two groups
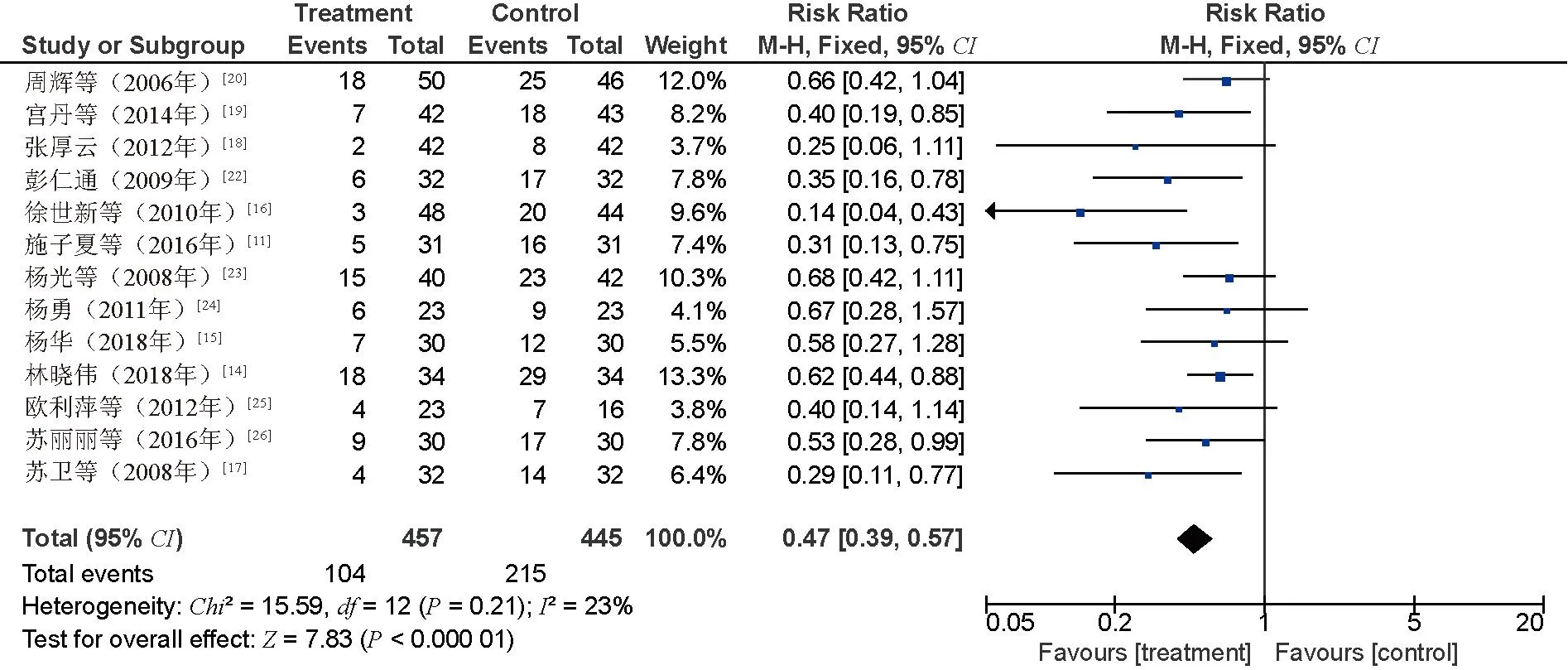
图4 两组患者白细胞减少发生率比较的Meta分析森林图Fig 4 Meta-analysis of comparison of incidence of leukopenia between two groups
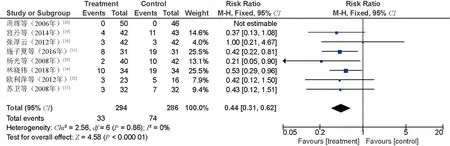
图5 两组患者血小板减少发生率比较的Meta分析森林图Fig 5 Meta-analysis of comparison of incidence of thrombocytopenia between two groups

图6 两组患者红细胞减少发生率比较的Meta分析森林图Fig 6 Meta-analysis of comparison of incidence of erythrocytopenia between two groups
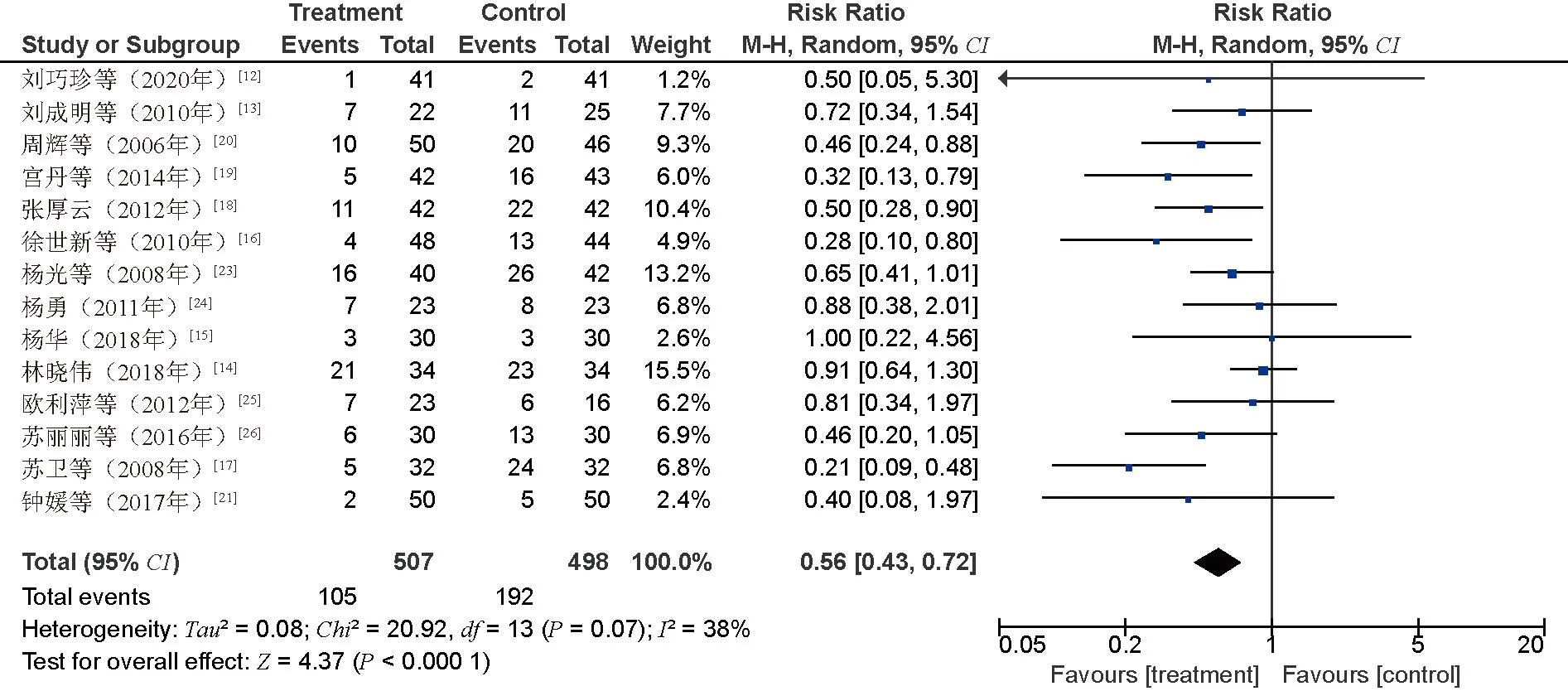
图7 两组患者胃肠道反应发生率比较的Meta分析森林图Fig 7 Meta-analysis of comparison of incidence of gastrointestinal reactions between two groups
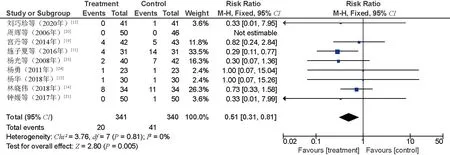
图8 两组患者肝损害发生率比较的Meta分析森林图Fig 8 Meta-analysis of comparison of incidence of liver injury between two groups

图9 两组患者肾损害发生率比较的Meta分析森林图Fig 9 Meta-analysis of comparison of incidence of kidney injury between two groups
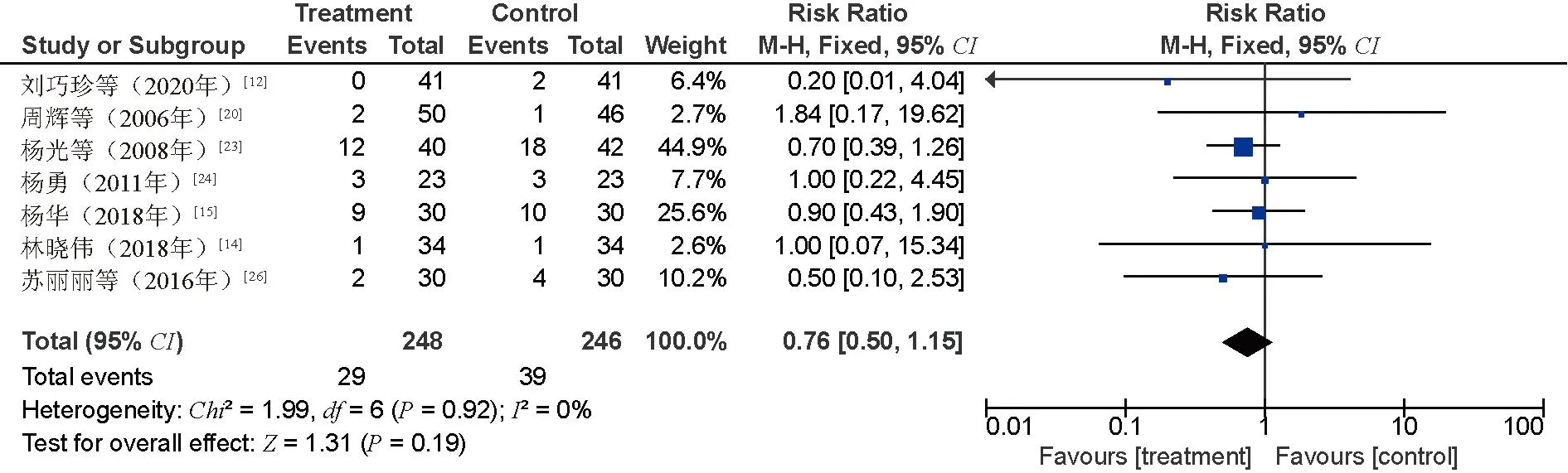
图10 两组患者周围神经炎发生率比较的Meta分析森林图Fig 10 Meta-analysis of comparison of incidence of peripheral neuritis between two groups
2.5 文献发表偏倚评价
有效率指标纳入了16项研究,故针对有效率绘制倒漏斗图,漏斗图图形不对称,提示可能存在发表偏倚,见图11。经Egger’s检验,P=0.063。

图11 文献发表偏倚漏斗图Fig 11 Funnel plot of literature publication
2.6 敏感性分析
将临床疗效结果指标(有效率)与效应量总体合并,结果表明,效应量并没有发生质的变化,表明临床疗效结果指标具有较好的稳定性,见图12。

图12 有效率的敏感性分析Fig 12 Sensitivity analysis of clinical efficacy
3 讨论
中医中关于肺癌的记载并不少见,如“石瘕”“癖结”和“昔瘤”等[27]。致癌原因众多,肺癌的常见病因包括吸烟、职业、环境污染等,肺脾气虚是肺癌发病的内在根本原因[28]。肺癌中最常发生的是NSCLC,而且多数确诊患者病情已发展至中晚期,不再满足手术条件,治疗难度进一步加大。目前,临床上大部分中晚期NSCLC患者都需要进行化疗[29]。有学者认为,导致恶性肿瘤的原因是气血不足,邪气不散。恶性肿瘤本身和长期治疗对身体的消耗反过来也会促进疾病进一步发展。
在临床上,中医药维持治疗NSCLC是一种切实可行的方法,特别是对靶向治疗不敏感或放化疗效果不明显的中晚期患者,可延长其生存时间,获得治疗机会。近年来,临床使用艾迪注射液治疗NSCLC的报道多见,但普遍为单中心、小样本的临床研究。
本研究基于Meta分析方法,系统评价艾迪注射液联合TP化疗方案治疗中晚期NSCLC的临床效果,结果表明,艾迪注射液与TP化疗方案联合应用可以提高治疗有效率,提高患者生活质量,减少化疗的不良反应;其中,肾损害与周围神经炎2项结局指标结果显示偏向研究组,但无显著性,利用RD代替RR再次进行Meta分析,定性结果无变化,则证明Meta分析结果具有可靠性。本研究纳入文献数量较多,在纳入与排除时严格按照标准筛选文献,在一定程度上可减少发表偏倚。本研究综合分析了包括临床疗效在内的9项结局指标,使结果更加严谨。此外,本研究严格控制了对照组干预措施,除施用某些药物进行预处理以防过敏外,仅为TP化疗方案,以此避免复杂的中药成分或其他干预措施介入而导致的影响,使研究结果更加准确。
本研究的局限性:(1)纳入的16篇文献均为中文文献,可能造成文献选择性偏倚。(2)仅5项研究使用了随机对照表法,且所有研究均未提及临床是否使用盲法、如何施盲,可能存在实施偏倚和测量偏倚。(3)纳入的研究在用药剂量、疗程方面并未设限,可能导致一定程度的临床异质性。本研究建议:临床进行RCT时,应增加是否使用盲法及分配隐藏的资料描述,并且规范研究中用药的剂量、疗程;同时,应进行更多大样本的RCT,为艾迪注射液联合TP化疗方案治疗NSCLC的临床研究提供更为可靠的科学依据。
综上所述,本次Meta分析结果显示,艾迪注射液联合TP化疗方案治疗NSCLC患者,可显著提高临床疗效,改善患者生活质量,降低白细胞减少、血小板减少的发生率等。但仍需严谨的多中心、大样本的临床随机双盲对照研究,进一步评价其有效性和安全性。
(本研究并无潜在利益相关)
