亚甲蓝分光光度法测定阴离子表面活性剂的影响因素
2024-01-16陈明星
*陈明星
(泉州市南安环境监测站 福建 362000)
阴离子表面活性剂是合成洗涤剂的主要成分之一,它进入水体后聚集在其它微粒表面,产生泡沫或发生乳化现象,阻断水中氧气的交换,同时消耗水中的溶解氧,导致水体恶化[1]。阴离子表面活性剂作为《地表水环境质量标准》(GB 3838—2002)控制指标之一,属于水质监测检验中的必检项目,也是环境监测实验室必认证的项目。阴离子表面活性剂的分析方法主要有分光光度法、流动注射法、两相滴定法、高效液相色谱法、光谱法等[2]。分光光度法虽然分析步骤繁琐,氯仿用量大,对操作条件的要求比较严格,但因分光光度计价廉易操作,水样前处理更为灵活可控,因此仍是主流分析方法。因此本试验参照《水质阴离子表面活性剂的测定亚甲蓝分光光度法》(GB/T 7494—1987)标准,对亚甲蓝分光光度法测定阴离子表面活性剂进行探索,对相关实验环节进行优化。
1.实验部分
(1)主要仪器与试剂
T6新悦可见分光光度计、250mL分液漏斗(配聚四氟乙烯活塞)、50mL具塞比色管。
十二烷基苯磺酸钠(LAS)溶液标准样品:500mg/L(生态环境部环境发展中心环境标准样品研究所)。
LAS标准使用液(10μg/mL):移取10mL LAS标准溶液纯水稀释定容到500mL。
亚甲蓝溶液(1):将50g磷酸二氢钠一水合物(NaH2PO4·H2O、AR、阿拉丁公司)、6.8mL浓硫酸和30mg亚甲蓝(指示剂级)配制成1000mL,贮存于棕色瓶中,可保存6个月。
亚甲蓝溶液(2):将56.5g磷酸二氢钠二水合物(NaH2PO4·2H2O、AR、国药集团)、6.8mL浓硫酸和30mg亚甲蓝(指示剂级)配制成1000mL,贮存于棕色瓶中。
洗涤液(1):1000mL纯水中含有50g磷酸二氢钠一水合物(NaH2PO4·H2O、AR、阿拉丁公司)、6.8mL浓硫酸,贮存于普通玻璃瓶中,可保存6个月。
洗涤液(2):1000mL纯水中含有56.5g磷酸二氢钠二水合物(NaH2PO4·2H2O、AR、国药集团)、6.8mL浓硫酸,贮存于普通玻璃瓶中。
氯仿(国药、AR)。
(2)标准工作液配制
取一组分液漏斗,分别移入100mL、99mL、97mL、95mL、93mL、90mL、85mL纯水,然后分别准确移取0.00mL、1.00mL、3.00mL、5.00mL、7.00mL、10.0mL、15.0mL直链烷基苯磺酸钠标准使用液,摇匀[3]。加入25mL亚甲蓝溶液,摇匀,加入10mL氯仿剧烈振摇30s静置,将下层氯仿层放入预先盛有50mL洗涤液的第二个分液漏斗中。用数滴氯仿淋洗第一个分液漏斗的放液管,重复萃取3次,每次氯仿用量10mL。合并所有氯仿层至第二个分液漏斗中,再次激烈摇动30s,静置分层。将氯仿层通过玻璃棉,放入50mL比色管中,再用氯仿萃取洗涤液两次(每次用量5mL),此氯仿层也并入比色管中,加氯仿至标线,待测。
(3)样品测定
将样品经中速定性滤纸过滤,量取100mL试样或适量试样用纯水稀释定容到100mL,按上述步骤萃取后分光测定。
2.试验主要影响因素分析
(1)装置气密性
试验中,分液漏斗气密性对分析结果影响很大,可购买带聚四氟乙烯活塞的分液漏斗,使用时不可涂抹凡士林,若发现漏液应重新取样分析。
(2)药品影响
本试验分别探究了磷酸二氢钠一水合物(NaH2PO4·H2O)和磷酸二氢钠二水合物(NaH2PO4·2H2O)对实验结果的影响。经折算后,称取56.5gNaH2PO4·2H2O配置亚甲蓝溶液(2)和洗涤液(2)。使用同一批氯仿,不同亚甲蓝溶液和洗涤液,标准系列浓度点吸光度测定结果如表1。
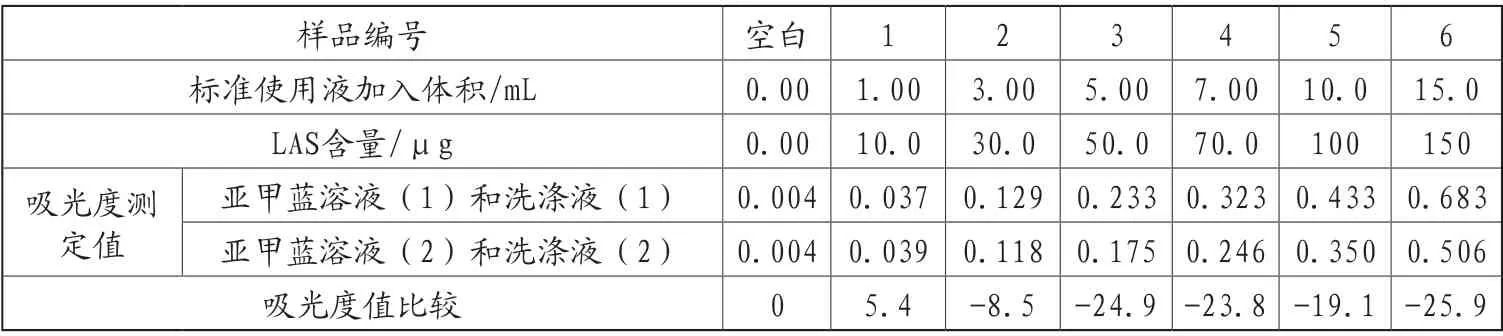
表1 不同亚甲蓝溶液和洗涤液各校准点吸光度分析结果
由表1可知,以NaH2PO4·2H2O替代NaH2PO4·H2O,除空白和第一个校准点(LAS含量10.0μg)外,其余校准点吸光度均降低,各校准点吸光度平均下降13.8%。即该显色条件下,萃取液摩尔吸光系数变小。因此虽然NaH2PO4·2H2O与NaH2PO4·H2O只相差一个结晶水,但不可混用。
(3)静置时间影响
手工萃取时,合并所有氯仿至第二个分液漏斗,振摇30s,静置分层。静置分层时间对分析结果的影响见表2。萃取后,形成明显分层现象立即过滤(静置分层时间30s)、静置分层时间2min后过滤分析结果,前者测定值大于后者,分析误差分别是-5.7%和-3.3%。当延长静置分层时间至5min,导致分析结果偏低,且结果不合格。
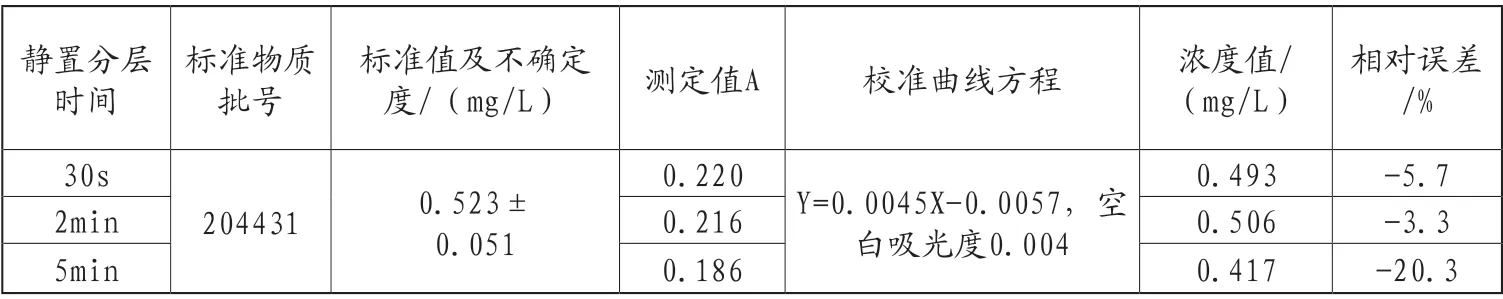
表2 不同静置分层时间标准物质分析结果
(4)萃取振摇方式对分析结果的影响
萃取时,分别采用前后振摇和旋转振摇两种方式分析同一标准物质,结果见表3。萃取时,旋转振摇测定值高于前后振摇测定值,且更接近真值。

表3 不同萃取振摇方式对分析结果的影响
(5)显色时间影响
测定标准系列浓度点0.500mg/L萃取液,不同显色时间下的吸光度,结果见表4。萃取液吸光度值在36h内无明显变化,显色物质稳定性好。
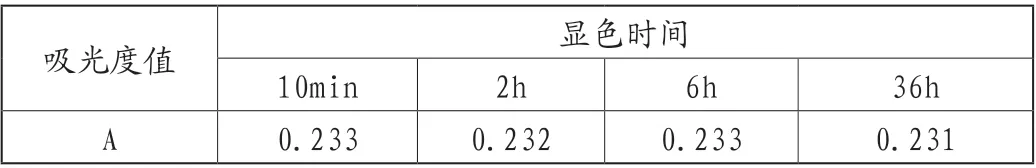
表4 显色时间对样品吸光度值的影响
(6)反应体系酸度影响
王楚强[4]分析了pH对萃取结果的影响,指出当pH值在8~10之间时的吸光度保持稳定,并且此时的萃取浓度最大。实验分析不同类别水样经酸度调整和未经酸度调整,分析结果见表5。当水样pH在6~9时,水样是否经过酸度调整,对分析结果的影响较小,水样吸光度值测定结果相对偏差在15%以内。当水样pH为4.8或11.5时,水样未经酸度调整直接过滤后分析可导致样品LAS测定值变小,相对偏差超过50%。因此对于地表水、地下水等清洁水样可以不调整酸度,直接取样过滤后分析。对于污染源样品,应根据现场pH测定结果,进行酸度调整后分析。
(7)萃取液过滤介质的影响
测定标准系列浓度点1.00mg/L,萃取后分别经索氏提取处理过的脱脂棉过滤和经未处理的市售玻璃棉过滤,测定结果见表6。萃取液经两种不同介质过滤,测定结果基本无异。

表6 不同过滤介质对分析结果的影响
(8)自动萃取代替手工萃取分析结果对比
以自动萃取代替手工萃取,绘制的校准曲线如图1。自动萃取消除了手工萃取人员误差,改善了线性。
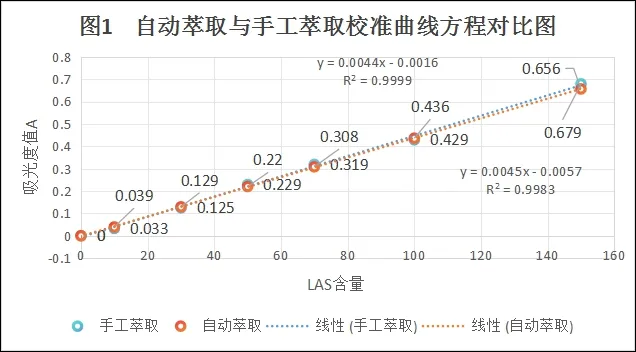
图1 自动萃取与手工萃取校准曲线方程对比图
(9)质控及安全防护
校准及样品分析应使用同一批次的氯仿,每批样品分析一个实验室空白及一个中间校核点,曲线中间点测定值相对误差不超过正负10%,否则需重新绘制校准曲线。当关键试剂氯仿生产批号改变,需重新绘制校准曲线。
氯仿挥发性极强,样品萃取及分光测定均应在通风橱内进行。完善安全防护设施,包括但不限于实验服、3M防毒面具带有机蒸汽/酸性气体滤毒盒、丁腈手套等。可使用分液器移取氯仿,尽量避免氯仿与手部的接触。
3.结论
经对比试验,影响标准(GB/T 7494—1987)的因素有分液漏斗的气密性,药品纯度、萃取后静置分层时间、萃取振摇方式等。以二水合磷酸二氢钠(NaH2PO4·2H2O)替代一水合磷酸二氢钠(NaH2PO4·H2O)配置亚甲蓝溶液和洗涤液,可导致样品吸光度测定值变小,各校准点吸光度平均下降13.8%;萃取时延长静置分层时间,可导致结果偏低;旋转振摇方式优于前后振摇方式,不同振摇方式相对偏差3.3%。萃取液吸光度在36h内基本无变化,萃取络合物稳定性好。采用自动萃取代替手工萃取,降低工作量,消除人员萃取误差,同时改善了线性。
