7 种微小RNA 检测试剂的多中心评估
2024-01-12黄中强侯铁英林发全卢志明刘小琦沈敏娜张平安军0肖艳群王华梁
黄中强 代 娣 侯铁英 林发全 卢志明 刘小琦 沈敏娜 吴 洁 张平安 周 军0 肖艳群 王华梁
(1.上海市临床检验中心 上海市实验医学研究院,上海 200126;2.中国医科大学附属第一医院检验科,辽宁 沈阳 110001;3.广东省人民医院检验科,广东 广州 510030;4.广西医科大学附属第一医院检验科,广西 南宁 530021;5.山东第一医科大学附属省立医院临床医学检验部,山东 济南 250021;6.四川省人民医院医学遗传中心,四川 成都 610031;7.复旦大学附属中山医院检验科,上海 200032;8.北京协和医院检验科,北京 100140;9.武汉大学人民医院检验科,湖北 武汉 430060;10.海军军医大学第三附属医院检验科,上海 201805)
微小RNA(microRNA,miRNA)是稳定存在于血浆中的内源性非编码单链小RNA,可调控细胞增殖、分化和凋亡等生物学功能,其表达异常与恶性肿瘤等多种疾病的发生、发展密切相关[1-2]。有研究结果显示,循环游离miRNA在肝细胞肝癌(hepatocellular carcinoma,HCC)癌前和肿瘤负荷极低状态等早期阶段即可表达异常,但单一的miRNA检测不足以为肿瘤的早期诊断提供证据,因此针对多个miRNA的高灵敏和高特异性的检测,对了解miRNA的生物学功能、肿瘤的早期诊断和发现新的药物靶点具有重要意义[3-4]。2011年,7种miRNA特定数学模型被建立[5],使多个miRNA的组合检测在辅助判断肝癌疾病进程和治疗效果方面起到了至关重要的作用,在《原发性肝癌诊疗规范(2019年版)》[6]中,miRNA首次被提出作为肝癌的新型分子标志物,特别是对于血清甲胎蛋白(alpha fetoprotein,AFP)阴性人群。当前,多个miRNA的检测通常基于实时荧光定量聚合酶链反应(polymerase chain reaction,PCR)技术[7-8],该方法操作相对简单,分析便捷,且检测成本较低,同时具有较高的灵敏度和特异性。2017年,国产某品牌基于PCR技术的“7种微小核糖核酸(miRNA)检测试剂盒”获得国家药品监督管理局三类医疗器械注册证,可用于检测7种miRNA(miR-21、miR-26a、miR-27a、miR-122、miR-192、miR-223和miR-801),被广泛应用于临床。为了全面、客观地评价该试剂盒的检测性能,本研究采用多中心性能评估模式评价该试剂盒性能。
1 材料和方法
1.1 研究对象
选取我国不同地区的10家检测中心,分别为上海市临床检验中心、中国医科大学附属第一医院检验科、广东省人民医院检验科、广西医科大学附属第一医院检验科、山东第一医科大学附属省立医院临床医学检验部、四川省人民医院医学遗传中心、复旦大学附属中山医院检验科、北京协和医院检验科、武汉大学人民医院检验科、海军军医大学第三附属医院检验科,在2021年9月13日—9月17日使用同一批样本,对同一批号试剂进行性能评估,评估参数包括精密度、符合率、检出限和抗干扰能力。10家检测中心分别以A、B、C、D、E、F、G、H、I、J编号,各检测中心环境温度为19 ℃~25 ℃,湿度为38%~70%。
1.2 试剂与仪器
骏实生物科技(上海)有限公司“7种微小核糖核酸(miRNA)检测试剂盒”(PCR荧光探针法,批号21071555),试剂盒内包含核酸提取试剂和核酸扩增试剂。10家检测中心所用的检测仪器包括:ABI 7500荧光定量PCR仪(美国赛默飞世尔科技公司)、ABI QuantStudio 5荧光定量PCR仪(美国赛默飞世尔科技公司)、Roche Z480Ⅱ荧光定量PCR仪(瑞士罗氏公司)。
用于精密度评估的阴性和阳性样本均为美国Integrated DNA Technologies公司合成的寡核苷酸对照参考品,共10套样本,每套含阴性样本和阳性样本各3支,每支5.00 mL。收集2021年1—3月复旦大学附属中山医院HCC患者临床血浆样本10份,作为用于符合率评估的阳性样本;收集健康人群血浆样本10份,作为阴性样本。每份样本分装为10支,共200支样本,分装为10套,每套含阴性样本和阳性样本各10支,每支500 μL。用于检出限评估的样本为Integrated DNA Technologies公司合成的1份寡核苷酸标准参考品,浓度为5×105拷贝/μL,使用超纯水梯度稀释至50拷贝/μL并分装为10套,每套1支,每支5.00 mL。用于抗干扰能力评估的干扰物分别为血红蛋白、胆红素和甘油三酯。血红蛋白购自德国Sigma-Aldrich公司(批号SLCJ0443),胆红素购自美国Frontier Scientific公司(批号JH21-14583),三酰甘油购自四川科伦药业股份有限公司(批号F17060801)。抗干扰能力评估的样本为1份弱阳性临床混合血浆样本,由骏实生物科技(上海)有限公司提供,样本分装为10套,每套1支,每支3.00 mL。以上评估所需的样本和干扰物均-20 ℃冷链保存,24 h内运送至10家检测中心。
1.3 方法
采用手工磁珠法提取核酸,所有评估实验所需的核酸均重新提取。采用“7种微小核糖核酸(miRNA)检测试剂盒”检测miR-21、miR-26a、miR-27a、miR-122、miR-192、miR-223和miR-801的相对表达量,以miR-1228为内参。循环扩增反应条件:42 ℃逆转录60 min→85 ℃预变性5 min→95 ℃变性15 s→60 ℃退火/延伸60 s,共40个循环。采用2-ΔΔCt法计算各miRNA的相对表达量。
1.3.1 精密度
参考美国临床实验室标准化协会(the Clinical and Laboratory Standards Institute,CLSI)EP15-A2[9]文件计算精密度。批内精密度:对1个阴性和1个弱阳性样本各重复检测10次;批间精密度:对1个阴性和1个弱阳性样本每天各重复检测3次,连续检测5 d。根据检测结果计算不同miRNA循环阈值(cycle threshold,Ct)的变异系数(coefficient of variation,CV),用于评估精密度。
1.3.2 符合率
参考CNAS GL039-2019文件[10]中符合率的验证方法,对10例HCC患者和10名健康者的临床血浆样本进行检测,比较检测结果与靶值,并计算总符合率。
1.3.3 检出限
参考CLSI EP 17-A文件[11]中检出限的评估方法,对标准参考品(50拷贝/μL)在不同检测批次中进行20次重复检测,根据检测结果计算检出率。
1.3.4 抗干扰能力
参考CNAS GL039-2019文件[10]中的抗干扰能力验证方法和《WS/T 416—2013 干扰实验指南》[12],结合试剂盒说明书中的性能指标,以在弱阳性样本中加入干扰物质溶液(血红蛋白、胆红素、三酰甘油)为实验组,使干扰物的最终浓度分别为血红蛋白200 g/L、胆红素1 000 μmol/L和三酰甘油100 mmol/L;以加入等量的0.9%NaCl溶液为对照组。各组重复检测3次,比较实验组和对照组检测结果的差异。
1.4 统计学方法
采用Excel 2016软件进行统计分析。计算计量资料的均值和CV,计数资料以率表示。采用Logistic回归分析评价各miRNA联合检测的诊断效能。试剂说明书中的计算公式为:Logit=-1.944 9+0.106 33×dCt miR21+0.102 19×dCt miR26a-0.0124 41×dCt miR27a-0.289 02×dC tmiR122-0.327 79×dCt miR192+0.258 55×dCt miR223-0.029 515×dCt miR801。根据试剂说明书要求,当样本Logit≥-0.5时,判定为该样本检测结果为阳性。
2 结果
2.1 精密度
2.1.1 批内精密度
10家检测中心对1个阴性和1个弱阳性样本各重复检测10次,均能全部检出;10家检测中心检测8个miRNA的Ct值的CV均<5.00%,其中最大值为4.79%,最小值为0.20%。见表1。
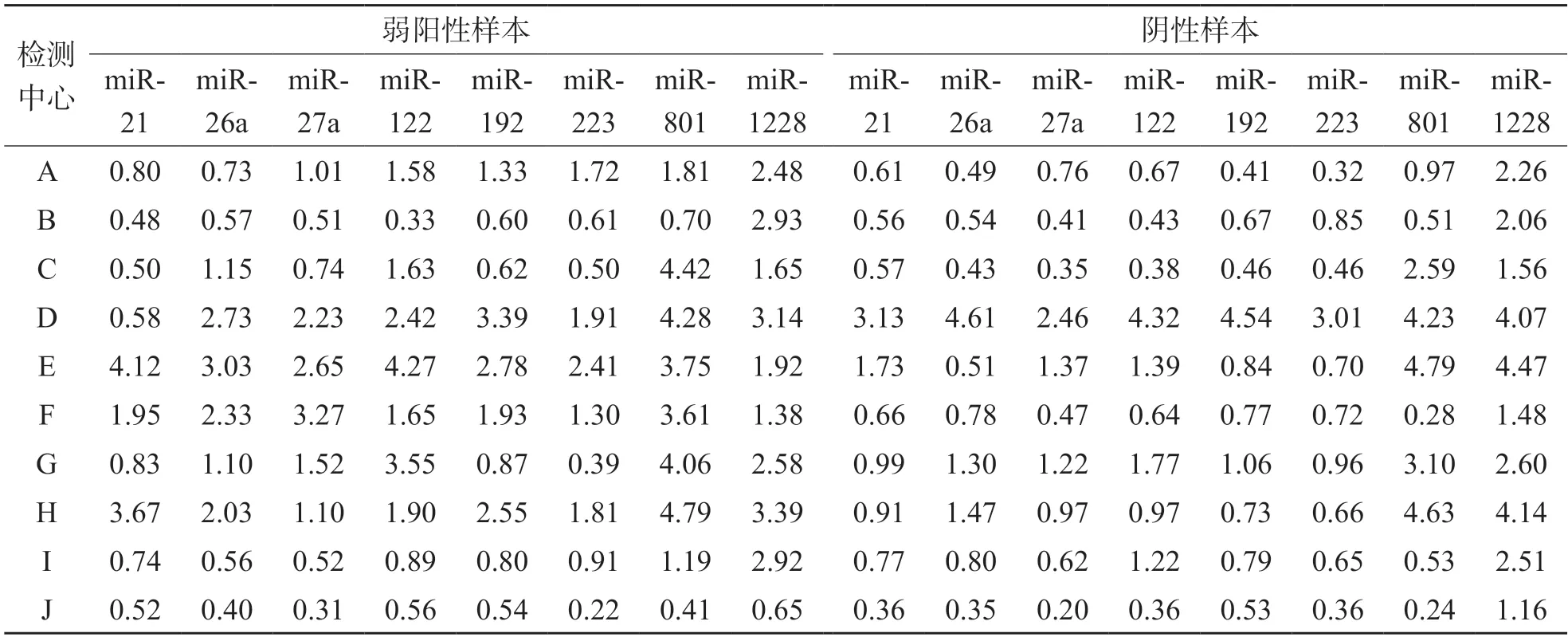
表1 批内精密度(CV)评估结果 %
2.1.2 批间精密度
10家检测中心对1个阴性和1个弱阳性样本每天各重复检测3次,连续检测5 d,均能全部检出;10家检测中心检测8个miRNA的Ct值的CV均<6.50%,其中最大值为6.38%,最小值为0.45%。见表2。

表2 批间精密度(CV)评估结果 %
2.2 符合率
10家检测中心检测10例HCC患者和10名健康者临床血浆样本的总符合率均为100.00%(20/20)。见表3。

表3 10家检测中心Logit值结果
2.3 检出限
10家检测中心对50拷贝/μL标准参考品进行20次重复检测,检出率均为100.00%(20/20)。见表4。
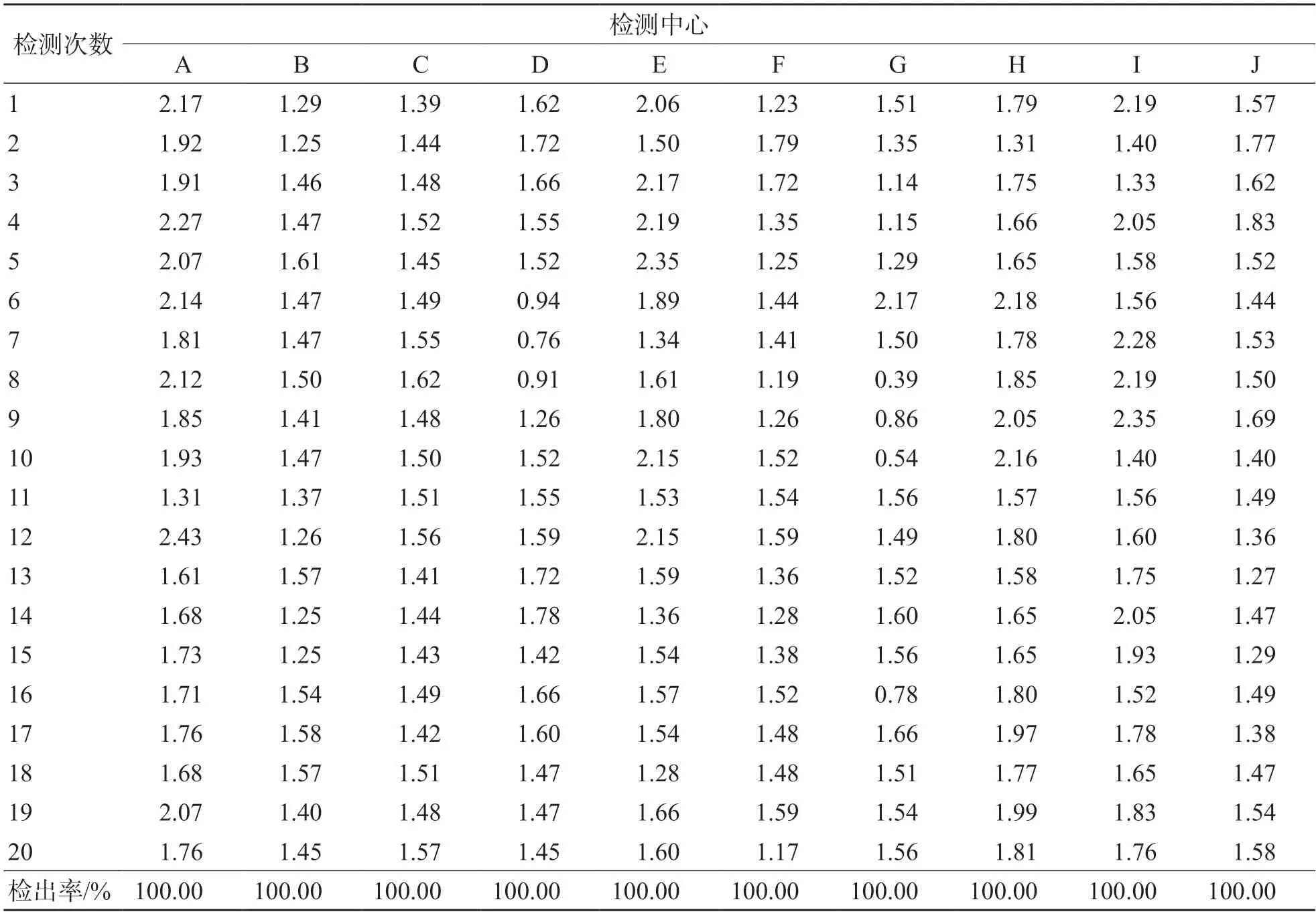
表4 10家检测中心检出限样本的Logit值结果
2.4 抗干扰能力
10家检测中心对3个实验组样本的检测结果均为阳性,与对照组检测结果一致。进一步对Logit值进行分析,并计算实验组与对照组的相对偏差,结果显示,10家检测中心的相对偏差均<20.00%,其中检测中心E检测100 mmol/L三酰甘油干扰样本的偏差最大,为19.93%。见表5。

表5 10家检测中心抗干扰能力评估结果
3 讨论
原发性肝癌是我国常见的恶性肿瘤,发病率和死亡率高,患者5年整体生存率仅为14.1%,约70%的肝癌患者就诊时已处于中晚期,因此肝癌的早期诊断和治疗是提升肝癌患者存活率的关键[13-14]。
近年来,循环游离miRNA作为新型的肝癌基因检测分子标志物,其组合检测对于辅助肝癌早期诊断具有较高价值,如采用7种血浆miRNA联合检测可准确地诊断早期肝癌,敏感性较传统肝癌标志物AFP提高约30%,对于血清AFP阴性人群也可准确诊断(敏感性为77.7%,特异性为84.5%)[5]。由于检测结果会受到检测系统、人员能力、实验室环境等因素的影响,单一实验室对试剂检测性能的评价具有一定局限性,本研究采用多中心性能评估模式,选取10家检测中心,实验室环境、检测系统和检测人员均不相同,可代表我国临床PCR实验室的检测能力。但10家检测中心所用的扩增仪均为国外进口,缺乏国产主流品牌,因此在后续的评价中将加以完善。
精密度作为评估检测系统的主要性能指标之一,可反映实验室检测系统的重复性,尤其是检测人员的规范化操作水平。本研究精密度评估结果显示,评估的试剂盒8个miRNA对应Ct值的批内CV<5.00%,批间CV<6.50%,均能达到试剂盒说明书中厂家声明的指标,说明该试剂盒的检测重复性较好;但10家检测中心的CV范围较宽(批内CV为0.22%~4.42%,批间CV为0.45%~6.38%),说明不同实验室之间精密度差异较大。
本研究参考CNAS GL039-2019文件[10]的性能验证方法,选取临床确诊肺癌患者和健康对照者的血浆样本用于符合率评估,10家检测中心的总符合率均为100.00%。检出限是指能可靠检出分析物的最低实际浓度,是体现检测系统灵敏度的主要指标之一,CLSI EP17-A文件[11]指出,检出限测定需在不同日期和不同批次内对样本进行检测,检测数据不少于20个,由于目前缺乏miRNA相关的定值标准物质,本研究选用人工合成的寡核苷酸标准参考品作为检出限评估样本;结果显示,10家检测中心的检出率均为100.00%(20/20),与厂家声明的指标相符。在临床检验过程中,检测结果经常会受到异常样本的影响,本研究评估了肝癌患者常见的溶血、脂血和黄疸样本对miRNA检测结果是否存在影响,结果显示,含干扰物的样本均能正常检出,且与对照样本的相对偏差<20.00%,表明血红蛋白200 g/L、胆红素1 000 μmol/L和三酰甘油100 mmol/L对检测无明显影响。
综上所述,7种miRNA检测试剂的精密度、符合率、检出限和抗干扰能力表现良好,可满足不同地区、不同实验室和不同检测系统的使用需求和预期用途。但在临床应用中,因检测过程以手工法为主,应特别注意规范检测人员操作,以降低随机误差对检测结果的影响,在规范的质量管理体系下保证检测结果的准确性和可靠性。
致谢:感谢武汉大学人民医院、北京协和医院、四川省人民医院、复旦大学附属中山医院、中国医科大学附属第一医院、海军军医大学第三附属医院、广东省人民医院、广西医科大学附属第一医院、山东第一医科大学附属省立医院的配合和协助,感谢所有作者在实验和数据处理等方面作出的支持和帮助。
