基于标准汤剂的海金沙草配方颗粒质量标准研究
2023-12-24魏家保唐双燕赵伟志黄凯伟蔡素琴张辉谭沛
魏家保,唐双燕,赵伟志,黄凯伟,蔡素琴,张辉,谭沛
(华润三九现代中药制药有限公司,广东 惠州 516000/华润三九医药股份有限公司,广东 深圳 518000)
海金沙草为海金沙科植物海金沙Lygodium japonicum(Thunb.)Sw. 及小叶海金沙Lygodium microphyllum(Cav.)R.Br.的干燥地上部分。收载于《广东省中药材标准》(2011 年版)中,具有清热解毒、利水通淋的功效[1],主产于广东、浙江、湖南、四川、重庆、广西、福建等地[2-3]。海金沙草中的化学成分主要有酚酸类和苯丙素类、黄酮类、三萜类、挥发油类以及脂肪酸类成分[4-6]。研究表明海金沙草具有利胆、降血糖、防治尿结石、抗氧化、抗菌、抗病毒和抗雄性激素等作用[7-9]。
中药配方颗粒是以标准汤剂为基准,采用现代方法经标准化工艺制备而成,既符合传统中医辨证论治的要求,又具备质量稳定、携带方便、卫生可靠等优势[10-12],在临床被越来越广泛使用。为保障中药配方颗粒临床用药与传统汤剂的一致性,在《中药配方颗粒质量控制与标准制定技术要求》中,将标准汤剂作为桥接,评价及控制中药配方颗粒的质量。近年来,对海金沙草的研究多限于成分研究[13-14]、含量测定[15-17]等,关于特征图谱及薄层的研究甚少[18],更无海金沙草标准汤剂质量标准的相关报道。故本研究以市售5 个主产地18 批海金沙草饮片为材料,遵循标准汤剂制备方法,计算出膏率,并以咖啡酸为指标成分,考察其在标准汤剂中的转移率,同时建立了标准汤剂的特征图谱分析方法及薄层色谱法(TLC)鉴别方法,为建立海金沙草配方颗粒的质量标准提供数据支撑。
1 仪器与试药
1.1 仪器
高效液相色谱仪:Thermo Ultimate 3000 色谱系统,包括LPG-3400SDN 型四元梯度输液泵、WPS-3000SL 型自动进样器、TCC-3000SD 型色谱柱温箱、DAD-3000 型二极管阵列紫外检测器、Chromeleon 7 色谱管理系统(赛默飞世尔科技有限公司);ME36S 百万分之一天平[梅特勒托利多科技(中国)有限公司];XS204十万分之一天平[梅特勒托利多科技(中国)有限公司];SK5200H 超声波仪(上海科导超声仪器有限公司);薄层自动成像仪(TLC visualizer2)、展开缸、硅胶GF254薄层板(青岛海洋化工厂)。
1.2 试药
海金沙草对照药材(批号:280067-202103)购于上海鸿永生物科技有限公司;对照品咖啡酸(批号:110885-201703,质量分数:99.7%)、原儿茶酸(批号:110809-202207,质量分数:97.5%)、4-香豆酸(批号:112037-202102,质量分数:99.7%)、异槲皮苷(批号:111809-202205,质量分数:96.3%)、山柰酚-3-O-芸香糖苷(批号:112007-202103,质量分数:94.0%)、蒙花苷(批号:111528-202213,质量分数:94.6%)均购于中国食品药品检定研究院。甲醇、乙腈为色谱纯,水为超纯水;三氯甲烷、甲酸、甲醇、正丁醇等其他试剂均为分析纯。
1.3 样品及制备方法
18 批海金沙草药材分别来源于四川宜宾县、重庆合川区、江西泰和县、广东湛江遂溪县以及广西来宾合山市。经安徽中医药大学刘守金教授鉴定为海金沙科植物海金沙Lygodium japonicum(Thunb.)Sw.的干燥地上部分。详细信息见表1。

表1 18批海金沙草药材信息及编号Table 1 Sample information and number of 18 batches of Lygodium japonicum(Thunb.)Sw
本研究根据《中药配方颗粒质量控制与标准制定技术要求》[19]制备海金沙草标准汤剂,并根据标准汤剂的标准制备海金沙草配方颗粒。
海金沙草标准汤剂制备方法:取海金沙草饮片100 g,加12 倍水,浸泡30 min,采用砂锅先武火煮沸,再文火煎煮30 min,200 目滤布趁热滤过,药渣再加10 倍水,先武火煮沸,再文火煎煮25 min,200目滤布趁热滤过,合并滤液;减压浓缩(60°C)成浸膏,冷冻干燥,即得标准汤剂冻干粉。
海金沙草配方颗粒制备方法:取海金沙草饮片7 500 g,加12 倍量水,浸泡30 min,武火煮沸,再文火煎煮30 min,200目滤布过滤;药渣再加10倍量水煎煮25 min,合并2 次滤液,经70 ℃减压浓缩为相对密度1.02~1.10 g/mL 的流浸膏,喷雾干燥(进风温度:150~210 ℃,出风温度:70~115 ℃),加麦芽糊精至1 000 g,混匀,制粒,即得海金沙草配方颗粒(每1 g配方颗粒相当于7.5 g饮片)。
2 方法与结果
2.1 含量测定
2.1.1 色谱条件 色谱柱为Agilent Eclipse XDBC18(4.6 mm×250 mm,5µm),流动相为甲醇∶乙腈∶0.2%磷酸溶液(6∶6∶88),检测波长为320 nm,柱温为30 ℃,流速为1.0 mL/min,进样量为10 µL,理论板数按咖啡酸峰计算应不低于3 000。
2.1.2 对照品溶液的制备 取咖啡酸对照品适量,精密称定,加50%(体积分数,下同)甲醇制成每1 mL含10 μg的溶液,即得。
2.1.3 供试品溶液的制备 取海金沙草饮片粉末(过3 号筛)1.0 g,精密称定,置具塞锥形瓶中,精密加入50%甲醇20 mL,称定质量,超声处理(功率250 W,频率40 kHz)30 min,取出,放冷,用50%甲醇补足减失的质量,摇匀,滤过,取续滤液,即得。
取海金沙草标准汤剂、配方颗粒适量,研细,取约0.1 g,精密称定,置具塞锥形瓶中,精密加入50%甲醇20 mL,密塞,称定质量,超声处理(功率350 W,频率40 kHz)30 min,放冷,再称定质量,用50%甲醇补足减失的质量,摇匀,滤过,取续滤液,即得。
2.1.4 含量测定方法学验证
2.1.4.1 专属性试验 分别精密吸取“2.1.2”项下的对照品溶液、“2.1.3”项下供试品溶液及阴性样品(空白溶剂)溶液10 μL,按“2.1.1”项下色谱条件依法进样测定,结果见图1。结果显示,待测成分咖啡酸与相邻成分达到基线分离,阴性样品无干扰。

图1 海金沙草饮片、标准汤剂及配方颗粒中咖啡酸测定的HPLC色谱图Figure 1 HPLC chromatograms of caffeic acid determination in decoction pieces,standard decoction and formula granules of Lygodium japonicum(Thunb.)Sw.
2.1.4.2 精密度试验 取同一份海金沙草标准汤剂供试品溶液(批号:BT01),重复进样6 次,结果显示咖啡酸峰面积RSD为0.9%,表明仪器精密度良好。
2.1.4.3 重复性试验 取同一批海金沙草标准汤剂(批号:BT01),制备6 份供试品溶液,按“2.1.1”项下色谱条件测定。结果显示,咖啡酸平均质量分数为0.74 mg/g,RSD为1.5%,表明方法重复性良好。
2.1.4.4 稳定性试验 取同一份海金沙草标准汤剂供试品溶液(批号:BT01),配制后在第0、2、6、10、12、18、24 h 按“2.1.1”项下色谱条件进行测定,结果显示,咖啡酸峰面积的RSD 值为1.4%,表明供试品溶液在24 h内稳定性良好。
2.1.4.5 线性关系考察 精密称取咖啡酸对照品10.360 mg,置25 mL 容量瓶中,加50%甲醇制成每1 mL 含咖啡酸413.157 μg 的对照品储备液。精密量取对照品储备液0.5、1、2、2.5、5、10 mL,分别置于100 mL容量瓶中,加50%甲醇至刻度,摇匀,制得咖啡酸质量浓度分别为2.066、4.132、8.263、10.329、20.658、41.316 μg/mL 的系列对照品溶液,进样测定,记录各浓度的色谱峰面积。以色谱峰峰面积为纵坐标(Y),对照品质量浓度为横坐标(X)绘制标准曲线,得到回归方程Y=5.288 261×104X-8.935 719×104,R2=0.999。结果表明咖啡酸对照品在2.066~41.316 μg/mL范围内线性关系良好。
2.1.4.6 加样回收率考察 分别精密称取咖啡酸对照品1.911、3.612、5.621 mg,置3 个25 mL 量瓶中,加50% 甲醇制成每1 mL 含咖啡酸0.076、0.144、0.224 mg的对照品储备液。精密量取上述对照品储备液1 mL,分别置于100 mL 容量瓶中,加50%甲醇至刻度,摇匀,制得咖啡酸质量浓度分别为0.000 76、0.001 44、0.002 24 mg/mL的系列对照品溶液。取海金沙草标准汤剂(批号:BT01)约0.05 g,精密称定,置具塞锥形瓶中,平行操作9份,每份分别精密加入25 mL 上述对照品溶液,按“2.1.3”项下方法制备9份供试品溶液,进样测定,结果显示,咖啡酸的平均加样回收率分别为100.1%、98.9%、99.4%,结果见表2,表明回收率良好。
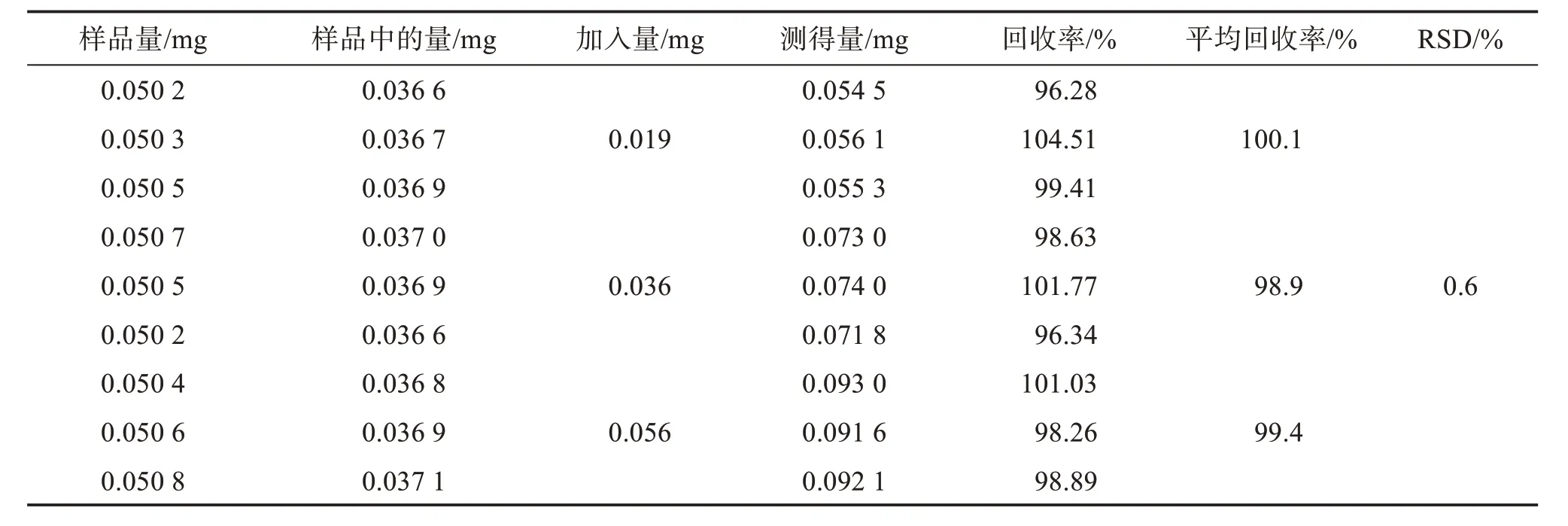
表2 海金沙草标准汤剂中咖啡酸加样回收率试验结果Table 2 The caffeic acid of recovery rate of Lygodium japonicum(Thunb.)Sw.standard decoction
2.1.5 样品的测定 按照“2.1.1”项下色谱条件,测定18 批海金沙草饮片、标准汤剂以及3 批配方颗粒中的咖啡酸质量分数,标准汤剂中咖啡酸转移率按照以下公式进行计算:
式中:Wa 为标准汤剂中咖啡酸的质量分数,X为饮片出膏率(标准汤剂出膏率根据标准汤剂冻干粉质量占饮片投入量比例计算),Wb 为饮片中咖啡酸的质量分数。配方颗粒理论含量值按照以下公式进行计算:
式中:Wa为标准汤剂中咖啡酸的质量分数,Wc为配方颗粒中咖啡酸的理论质量分数,X为饮片出膏率(标准汤剂出膏率根据标准汤剂冻干粉质量占饮片投入量比例计算),Y为配方颗粒对应饮片量,结果见表3。
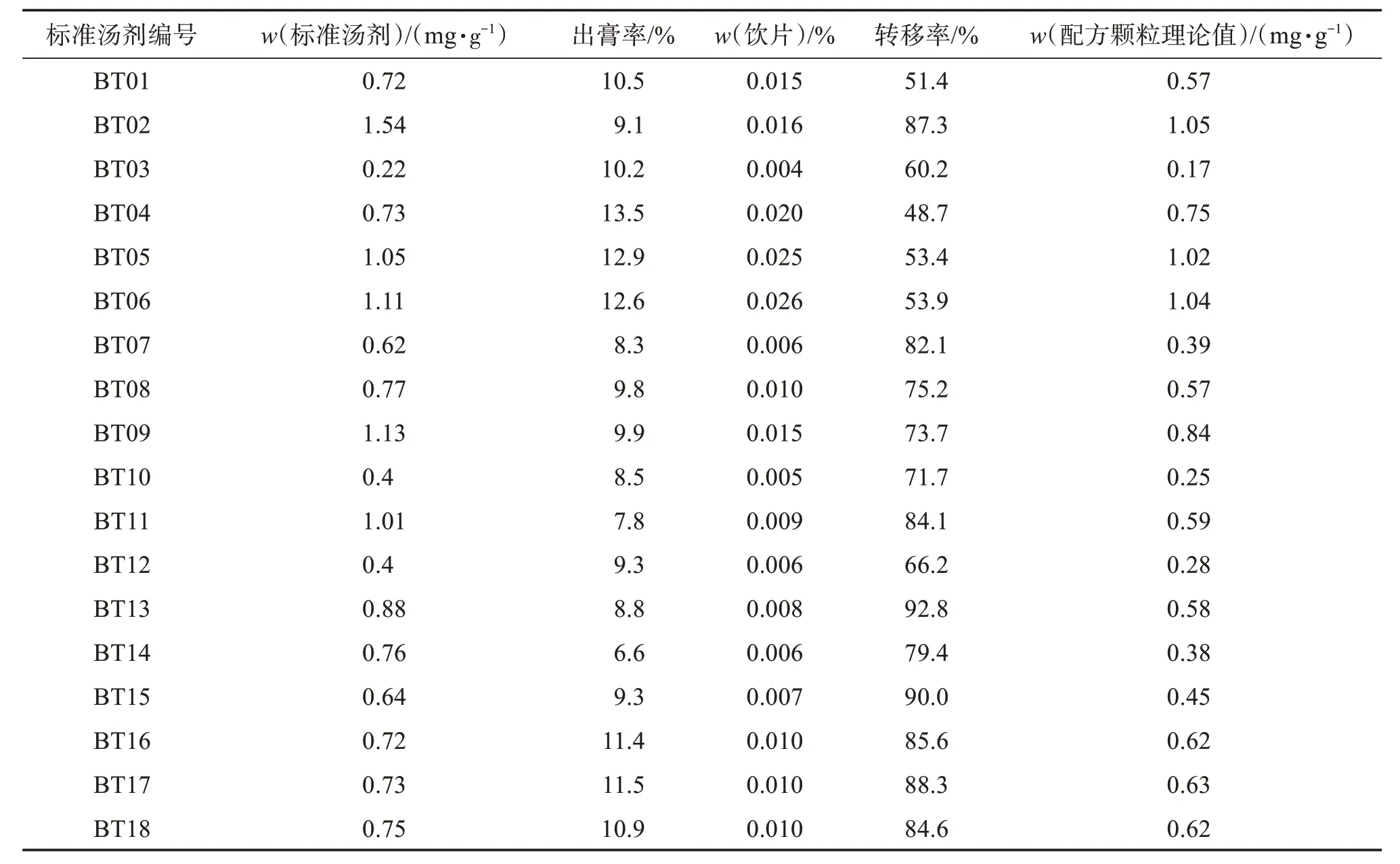
表3 海金沙草标准汤剂中咖啡酸质量分数及转移率结果Table 3 The caffeic acid content and transfer rate of Lygodium japonicum(Thunb.)Sw.standard decoction
2.1.6 质量分数测定结果分析 由测定结果可知,海金沙草配方颗粒中咖啡酸质量分数理论值范围为0.17~1.05 mg/g,均值为0.60 mg/g,均值±30%为0.42~0.78 mg/g,最终以实测范围确定配方颗粒的咖啡酸质量分数为0.17~1.10 mg/g,在均值±2SD 范围内(0.05~1.11 mg/g);18 批标准汤剂中咖啡酸转移率范围为48.7%~92.8%,均值73.8%,均值±30%范围为51.7%~96.0%。确定配方颗粒中咖啡酸转移率范围为48.0%~93.0%。
另外,3 批配方颗粒中咖啡酸实测质量分数(转移率)分别为0.65 mg/g(86.5%)、0.64 mg/g(85.1%)、0.61mg/g(81.1%),均在相关范围内,且与对应批次的标准汤剂冻干粉各质量属性(出膏率、含量及转移率)基本一致,表明该制备工艺及质量范围较为合理。
2.2 特征图谱的建立
2.2.1 色谱条件 色谱柱为CAPCELL CORE C18柱(4.6 mm × 150 mm,2.7 µm),流动相为乙腈(A)和0.2%甲酸水溶液(B),梯度洗脱(0~20 min,6%A→15%A;20~40 min,15%A→20%A;40~50 min,20%A→32%A;50~55 min,32%A),检测波长0~14 min 为254 nm,14 min~55 min 为320 nm,柱温为20 ℃,流速为0.70 mL/min,进样量为10µL,理论板数以咖啡酸峰计算应不低于3 000。
2.2.2 参照物溶液的制备 取海金沙草对照药材0.6 g,置具塞锥形瓶中,加水25 mL,加热回流30 min,滤过,滤液用水饱和的正丁醇振摇提取2次,每次25 mL,合并正丁醇液,蒸干,放冷,残渣加70%甲醇20 mL,超声处理(功率250 W,频率40 kHz)30 min,滤过,取续滤液,作为对照药材参照物溶液。另取“2.1.2”项下的咖啡酸对照品溶液,作为对照品参照物溶液。
2.2.3 供试品溶液的制备 分别取海金沙草标准汤剂、配方颗粒0.1 g,加水10 mL使溶解,用水饱和正丁醇萃取2 次,每次20 mL,合并正丁醇液,蒸干,放冷,残渣加70%甲醇20 mL,超声处理(功率250 W,频率40 kHz)30 min,滤过,取续滤液,作为供试品溶液。
2.2.4 特征图谱方法学验证
2.2.4.1 精密度试验 取同一份供试品溶液(批号:BT01),连续进样6 次,记录色谱图,计算各特征峰的相对保留时间和相对峰面积的RSD 值,结果表明,11 个特征峰的相对保留时间和相对峰面积RSD值均小于2%。表明方法的精密度良好。
2.2.4.2 重复性试验 取同一批样品(批号:BT01),制备6 份供试品溶液,进样分析,记录色谱图,计算各特征峰的相对保留时间和相对峰面积的RSD 值。结果表明,11 个特征峰的相对保留时间和相对峰面积RSD均小于2%。表明本方法的重复性良好。
2.2.4.3 稳定性试验 取同一份供试品溶液(批号:BT01),分别在配制后第0、4、8、12、16、24 h 进样。记录色谱图,计算各特征峰的相对保留时间和相对峰面积的RSD 值。结果表明,11个特征峰的相对保留时间和相对峰面积RSD 均小于2%,供试品溶液在24 h内稳定性良好。
2.2.5 特征图谱的建立与分析
2.2.5.1 特征峰的指认 参照“2.2.1”项下色谱条件,经对照品比对,确认色谱峰1 为原儿茶酸,色谱峰4 为咖啡酸,色谱峰6 为4-香豆酸,色谱峰7 为异槲皮苷,色谱峰8 为山柰酚-3-O-芸香糖苷,色谱峰11为蒙花苷,结果见图2。
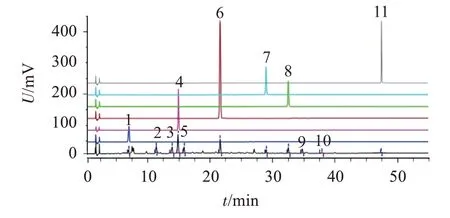
图2 海金沙草标准汤剂对照品定位液相色谱图Figure 2 Reference location chromatograms of Lygodium japonicum(Thunb.)Sw.standard decoction
2.2.5.2 特征图谱的建立 取“1.3”项下18 批海金沙草药材制备成海金沙草标准汤剂,同时制备3 批海金沙配方颗粒,按“2.2.3”项下方法制备供试品溶液,再按“2.2.1”项下色谱条件进行测定,将实验数据导入“中药色谱指纹图谱相似度评价系统(2012版)”,将各色谱峰匹配,建立对照特征图谱,结果见图3-图4,18批海金沙草标准汤剂对照特征图谱具有11个特征峰,共有特征峰峰面积之总和占总峰面积91.8%,表明选定的11 个特征峰可以作为海金沙草鉴定的标志峰。根据各峰响应值,选择以峰4(咖啡酸)参照峰相应的峰为S 峰,计算其余特征峰与S峰相对保留时间,相对保留时间应在规定值的±10%之内,规定值为:0.48(峰1)、0.77(峰2)、0.94(峰3)、1.06(峰5)、1.45(峰6)、1.93(峰7)、2.17(峰8)、2.32(峰9)、2.52(峰10)、3.16(峰11)。
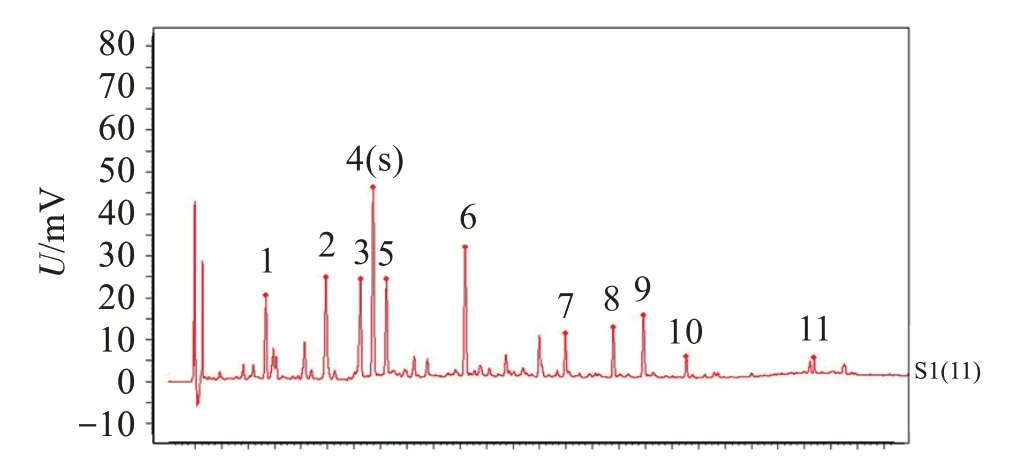
图3 海金沙草标准汤剂对照特征图谱Figure 3 Reference fingerprints of Lygodium japonicum(Thunb.)Sw.standard decoction
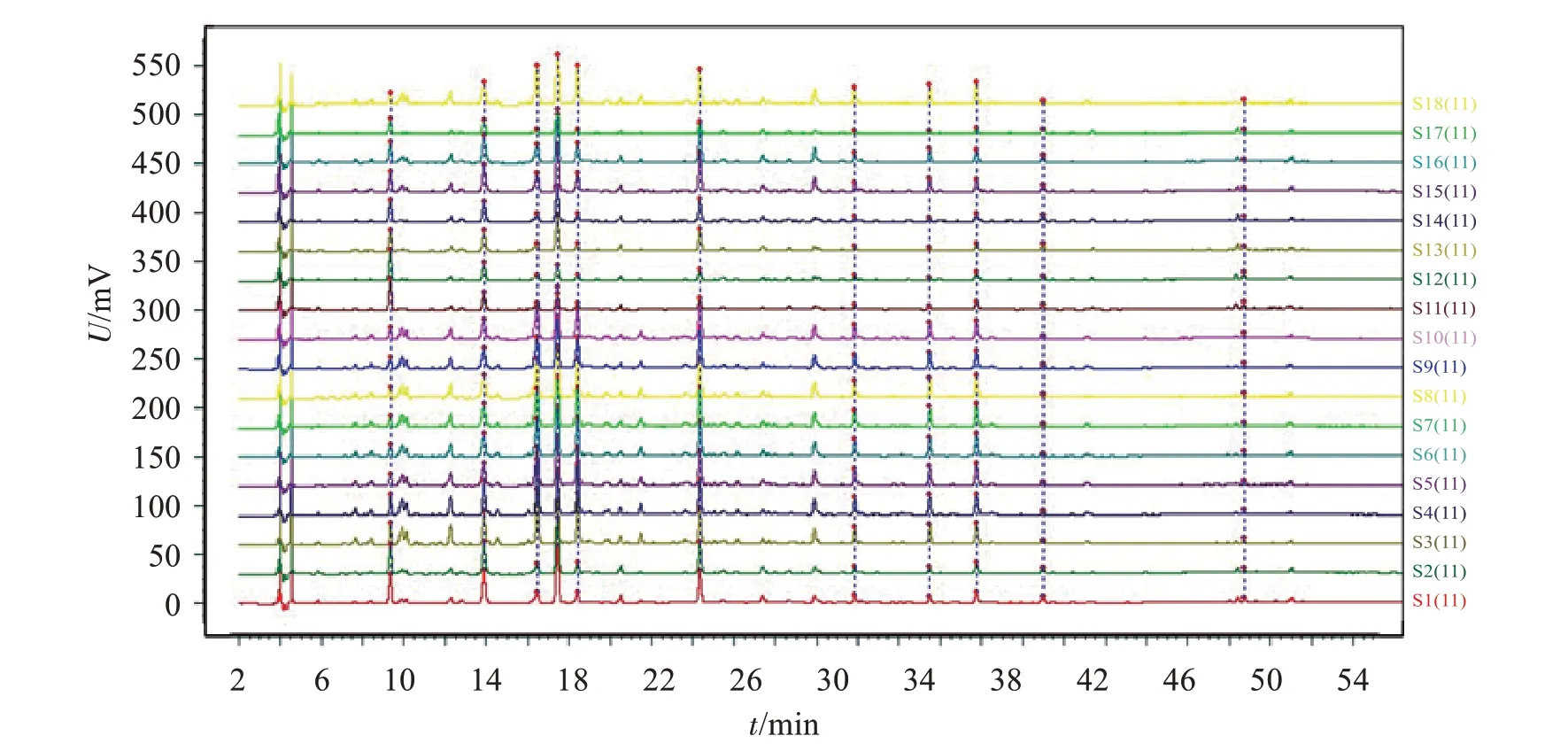
图4 18批海金沙草标准汤剂特征图谱共有模式图Figure 4 Common pattern chromatograms of 18 batches of Lygodium japonicum(Thunb.)Sw.standard decoction
2.2.5.3 相似度评价 测得18 批海金沙草标准汤剂结果见表4-表5,将图谱中各色谱峰匹配后,建立对照特征图谱,计算得到各批次与对照图谱的相似度在0.954~0.996之间,见表6。相似度较高,结果表明18 批样品的化学成分较为类似,测得3 批配方颗粒的相似度分别为0.974、0.988、0.989,表明配方颗粒与标准汤剂具有较好的一致性。
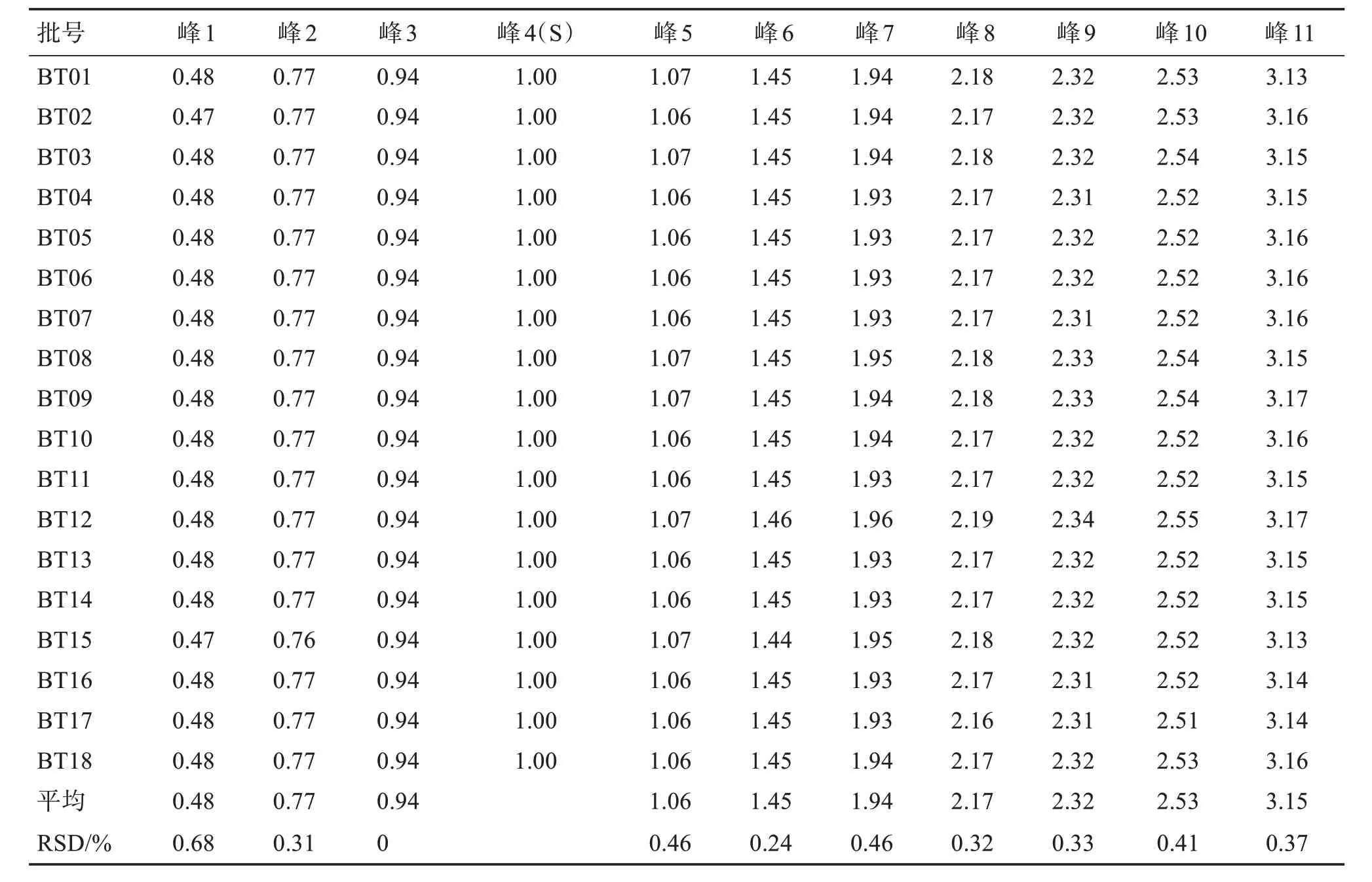
表4 18批海金沙草标准汤剂相对保留时间结果Table 4 Results of relative retention time of 18 batches Lygodium japonicum(Thunb.)Sw.standard decoction
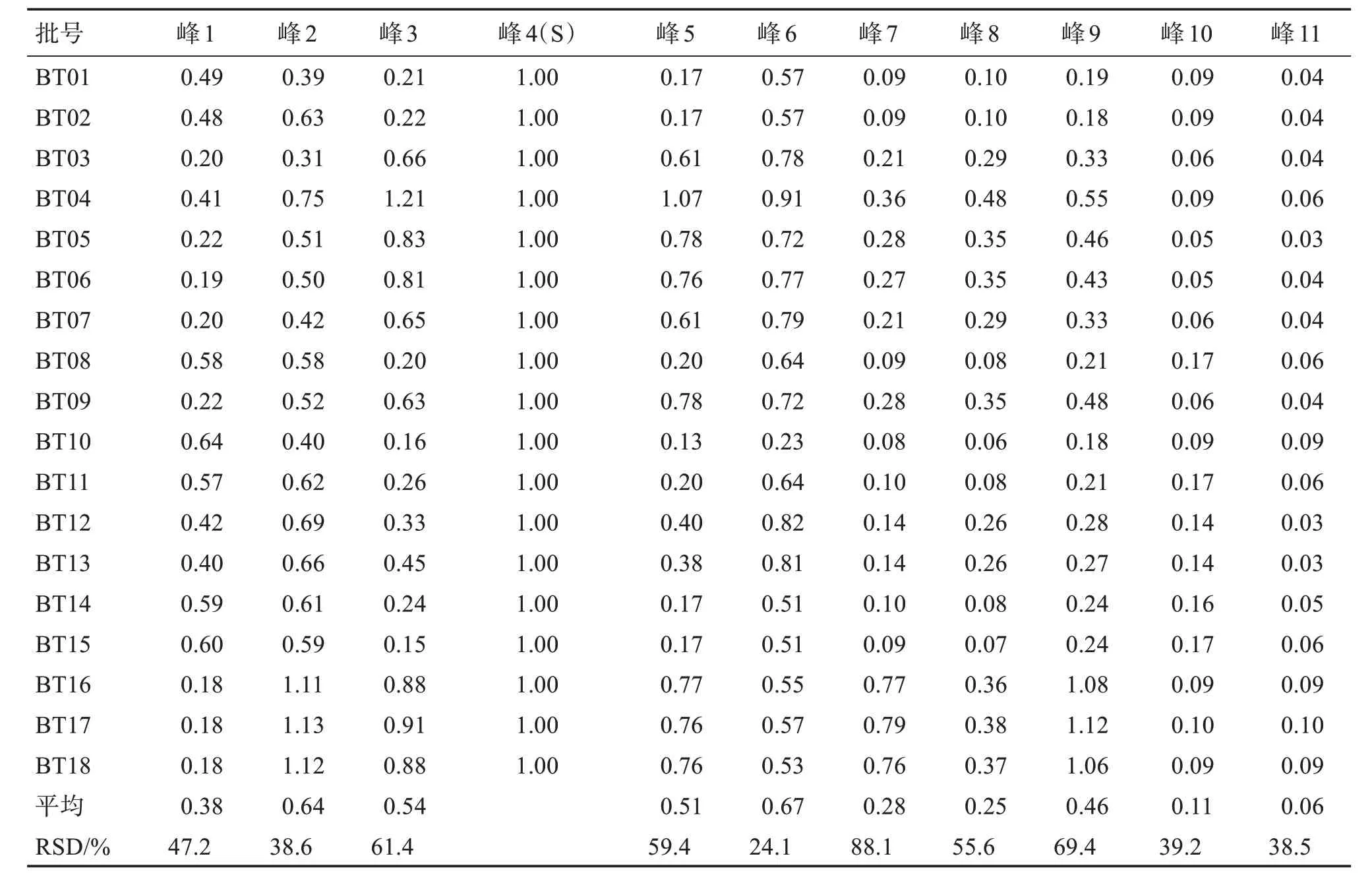
表5 18批海金沙草标准汤剂的相对峰面积结果Table 5 Results of relative peak area of 18 batches Lygodium japonicum(Thunb.)Sw.standard decoction
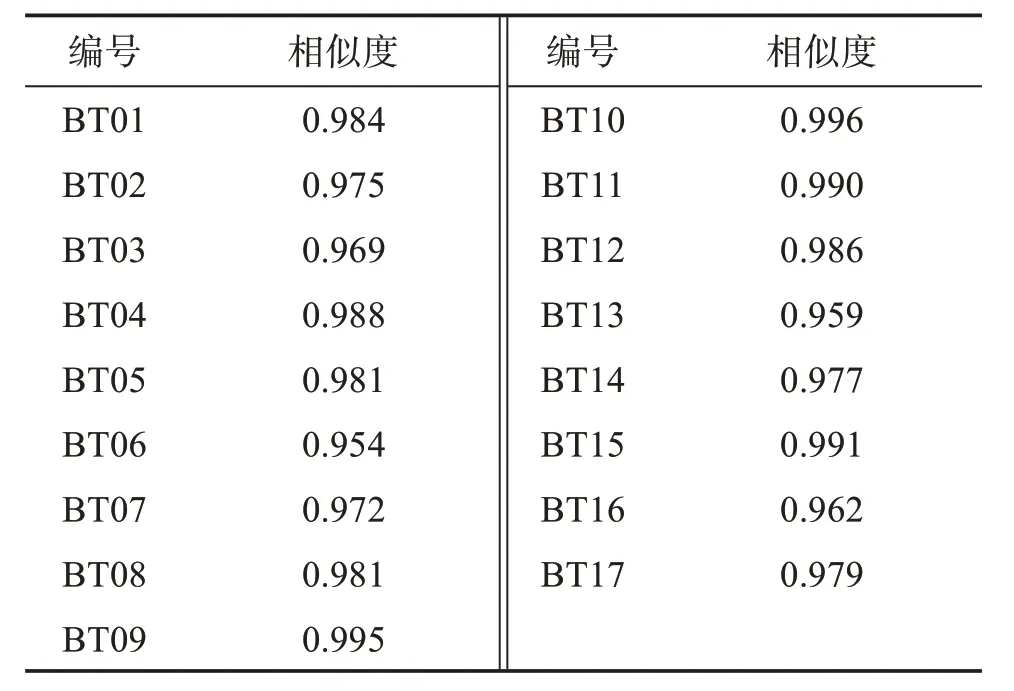
表6 18批海金沙草标准汤剂的相似度结果Table 6 Similarity results of 18 batches Lygodium japonicum(Thunb.)Sw.standard decoction
2.2.5.4 聚类分析评价 采用SPSS 22.0 软件,以共有峰的峰面积为变量,采用组间联接法、欧平方式距离对18批海金沙草标准汤剂进行聚类分析,结果如图5 所示。根据聚类分析结果,欧式间距小于5时,18 批海金沙草标准汤剂样品可以分为3 类:第1类为BT16、BT17、BT18;第2 类为BT01、BT02、BT08、BT10、BT11、BT12、BT13、BT14、BT15;第3类为BT03、BT04、BT05、BT06、BT07、BT09,由聚类分析的结果可知,共有峰的峰面积与产地分布无明显关联。而特征峰峰面积在一定程度上反映了标准汤剂冻干粉中所含有的特征成分的质量分数高低,因此间接表明所含化学成分的种类与质量分数高地与产地关联性不强。

图5 系统聚类分析结果Figure 5 Results of systematic cluster analysis
2.2.5.5 主成分分析评价 采用SPSS 22.0 软件,以11 个共有峰的峰面积为变量,进行主成分分析,结果见表7。以特征值大于1 和贡献率达到85%以上作为提取原则,提取的主成分1 的特征值为7.146,贡献率达到64.97%;提取的主成分2 的特征值为2.113,贡献率达到19.21%;提取的主成分3 的特征值为1.065,贡献率达到9.68%,这3个主成分的贡献率达到了93.86%。对成分矩阵进行了具有Kaiser标准化的正交旋转,得到11 个指标(峰)在3 个主成分旋转成分矩阵,见表8。成分载荷矩阵的数值及符号代表变量在主成分当中的载荷,载荷越大,表明该化合物在主成分分析中作用越大。由表8结果可知,峰2、7、9、11 对主成分1 的影响力较大,其中峰7为异槲皮苷。峰6对主成分2的影响力较大,峰6 为4-香豆酸。峰1、10 对主成分3 的影响力较大,峰1为原儿茶酸,峰11为蒙花苷。
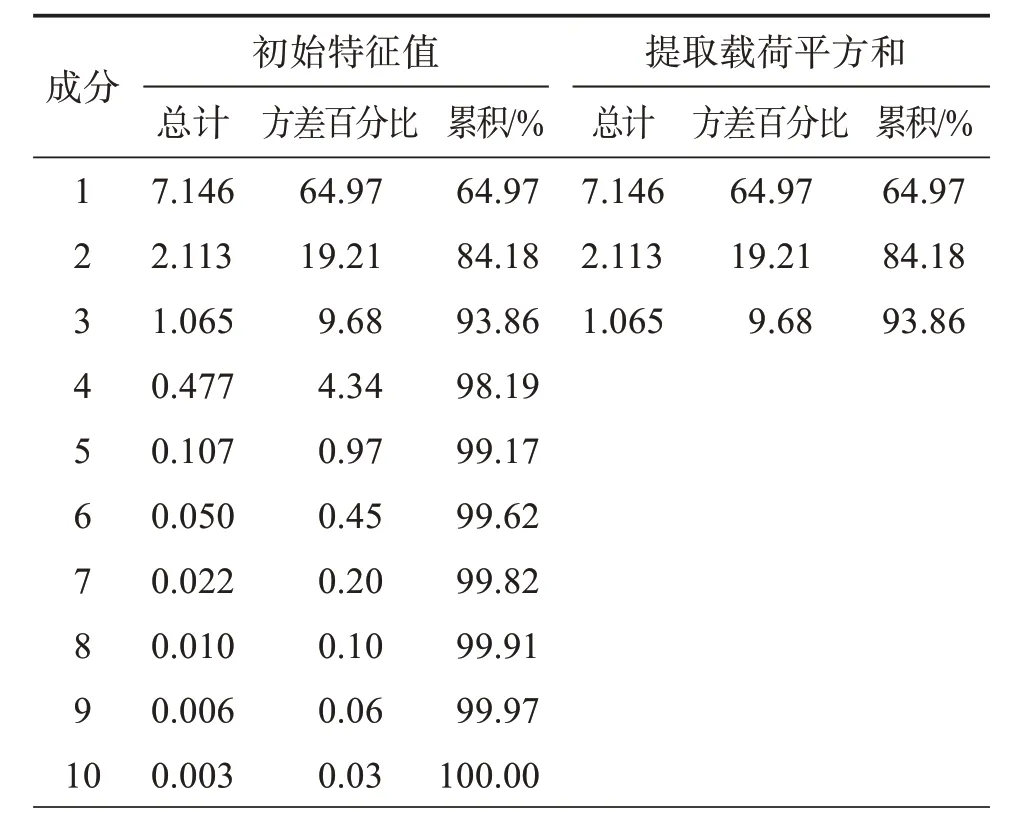
表7 主成分的特征值和方差贡献率Table 7 Eigenvalues and variance contribution rates of principal components

表8 旋转成分矩阵Table 8 Rotational component matrix
2.3 TLC法鉴别
2.3.1 TLC 法条件 取海金沙草标准汤剂冻干粉或配方颗粒1 g,研细,加无水乙醇30 mL,加热回流30 min,滤过,滤液蒸干,残渣加无水乙醇1 mL 使溶解,作为供试品溶液。另取海金沙草对照药材1 g,加水50 mL,加热回流30 min,滤过,滤液蒸干,残渣加无水乙醇30 mL,同法制成对照药材溶液。按照薄层色谱法(《中华人民共和国药典》2020 年版“通则0502”)进行试验。分别吸取供试品溶液4 µL、对照药材溶液8 µL,分别点于同一硅胶GF254薄层板上,以三氯甲烷-甲醇-甲酸(10∶1∶0.5)为展开剂,展开,取出,晾干,分别置紫外光灯254、365 nm 下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点和荧光斑点,结果见图6-图7。

图6 18批海金沙草标准汤剂TLC色谱图Figure 6 Results of TLC of 18 batches Lygodium japonicum(Thunb.)Sw.standard decoction
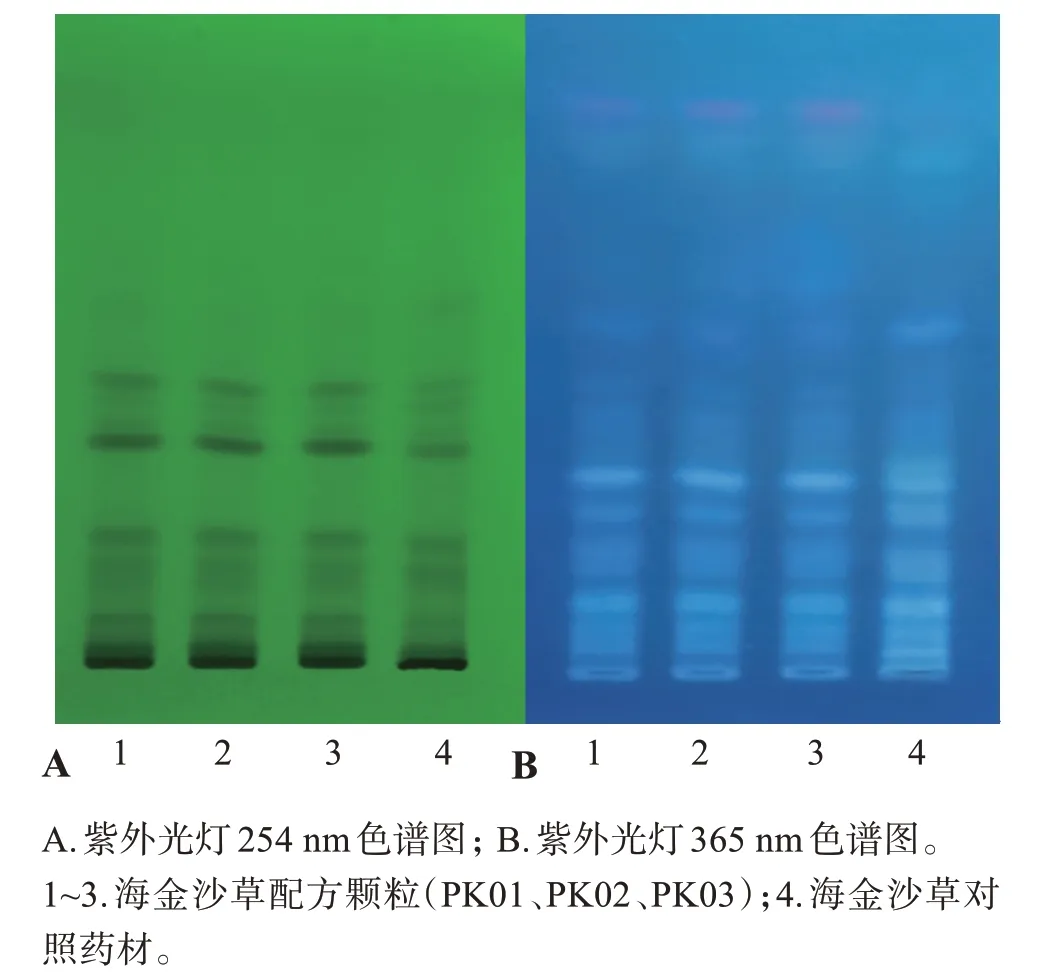
图7 3批海金沙草配方颗粒的TLC色谱图Figure 7 Results of TLC of 18 batches Lygodium japonicum(Thunb.)Sw.formula granules
2.3.2 TLC法鉴别结果 由图6-图7可见,海金沙草标准汤剂冻干粉供试品色谱中,在254、365 nm下,与海金沙草对照药材色谱相应的位置上,均显示相同颜色的斑点和荧光斑点,且斑点清晰、分离度好。3 批海金沙草配方颗粒的TLC 结果表明,斑点与标准汤剂基本一致、信息丰富,因此该方法可作为海金沙草标准汤剂及配方颗粒的有效鉴别方法。
3 讨论
2020 年版《中华人民共和国药典》[20]仅收载了海金沙药材,来源为海金沙科植物海金沙Lygodium japonicum(Thunb.)Sw.的干燥成熟孢子,而海金沙草被广泛收载于各地方药材标准,其中《广东省中药材标准》(2011 年版)[1]规定海金沙草为海金沙科植物海金沙Lygodium japonicum(Thunb.)Sw.及小叶海金沙Lygodium microphyllum(Cav.)R.Br.的干燥地上部分。因此本研究过程中收集了海金沙基原,建立了相关标准。
本研究在特征图谱方法开发过程中发现,海金沙草中化学成分色谱峰信息量极为丰富,采用的常规梯度洗脱方法也很难保证各特征峰的有效分离,因此在供试品制备方法考察中对比了不同提取溶剂(水、50%甲醇、甲醇、乙醇)、不同萃取溶剂(乙酸乙酯、三氯甲烷、水饱和正丁醇)的效果。三氯甲烷、乙酸乙酯因极性较小,导致萃取时部分特征峰缺失,水、50%甲醇、甲醇、乙醇所得特征峰数量虽多,但基线噪音过大,分离效果不佳。水饱和正丁醇萃取所得特征峰数量多且能呈现标准汤剂水溶性成分,共有峰峰面积占总峰面积90%以上,能较好地代表海金沙草配方颗粒整体质量,且特征峰更容易辨别和指认,因此最终确定了使用水饱和正丁醇进行萃取,可用于海金沙草配方颗粒的质量监测。
本文通过对海金沙草标准汤剂出膏率、主要成分质量分数及转移率、HPLC 特征图谱以及TLC 鉴别方法的研究,建立了海金沙草标准汤剂的质量标准,并验证了配方颗粒与标准汤剂的一致性,可全面反映其质量,为相关质量控制和临床应用提供依据。
