黄芩苷对注意缺陷多动障碍动物模型SHR 大鼠核心症状影响研究
2023-12-13张永婷周荣易马丙祥吴晨蕾谢新月丁雪颖
张永婷周荣易马丙祥吴晨蕾谢新月丁雪颖
(1.河南中医药大学儿科医学院,郑州 450000;2.河南中医药大学第一附属医院,郑州 450000)
注意缺陷多动障碍( attention deficit/hyperactivity disorder, ADHD)是儿童时期常见的神经发育障碍性疾病,全球范围研究显示,ADHD 患病率约为7.2%,并呈上升趋势[1]。 ADHD 临床以注意力不集中、多动、冲动为核心症状[2],常共患品行障碍、抽动障碍、行为障碍及对立违抗性障碍[3-5],约有50%在儿童或青少年时期被诊断为ADHD 的个体成年后仍会持续多动症症状[6],这导致患者社会适应能力下降,对其生活、学习和社交造成极大困扰,给家庭带来极大压力。 目前ADHD 临床上以药物治疗为主,精神兴奋剂MPH 为一线治疗药物,临床疗效显著,但存在长期应用成瘾性、影响发育、体重等不良反应,导致患者依从性差[7]。 黄芩苷是课题组早期在临床治疗ADHD 疗效显著的中药复方研究过程中发现的单体成分[8]。 前期研究显示,黄芩苷控制ADHD 核心症状疗效显著,且未发现明显副作用[9]。 截止目前,ADHD 的发病机制尚不明确,围绕多巴胺(dopamine,DA)系统的研究成为当前全球范围内ADHD 发病机制的研究热点,受国际社会广泛关注[10]。 课题组前期基础研究表明,黄芩苷对DA 系统具有特殊亲和力[11-12],不同剂量的黄芩苷均能控制ADHD 核心症状,且在150 mg/kg 剂量下疗效最为稳定[9]。 深入机制研究表明,这一疗效或许与黄芩苷调控前额叶皮质、纹状体内DA 囊泡转运环节中囊泡单胺转运体Ⅱ型(VMAT2)的表达有关[8]。 囊泡转运是DA 囊泡循环过程中极为关键的环节,对脑内DA 正常释放、维持脑内DA 正常水平意义重大;VMAT2 作为主要表达于中枢神经系统多巴胺能神经末梢的关键蛋白[13],在DA 转运和释放中发挥关键作用。 研究显示,ADHD 患者及其动物模型SHR 大鼠均存在脑内VMAT2 表达下调现象,导致DA 转运速度降低和释放减少,形成脑内DA 缺陷[8,14-15]。 研究显示,VMAT2 功能异常导致大鼠脑内DA 含量显著降低而表现出ADHD 核心症状[16]。 基于课题组前期研究和以上理论基础,作者推测VMAT2 可能作为黄芩苷发挥药效的潜在作用靶点。 为验证黄芩苷是否通过作用于DA 囊泡循环中VMAT2 这一靶点达到控制ADHD 核心症状的疗效,进而探究其潜在疗效机制。 本研究在前期研究基础上,应用VMAT2 抑制剂丁苯那嗪继续开展研究工作,以期为进一步阐明黄芩苷的疗效机制以及后期新药开发奠定基础。
1 材料和方法
1.1 实验动物
4 周龄SPF 级SHR 雄性大鼠36 只,体重(103±10)g;4 周龄SPF 级WKY 雄性大鼠6 只,体重(93.5±7)g,均采购于北京维通利华实验动物技术有限公司[SCXK(京)2021-0001]。 SHR 大鼠起源于东京高血压Wistar 大鼠,经交叉培育获得,幼龄SHR 大鼠是国际公认的ADHD 动物模型,该模型在10 周龄前不表现高血压特征,而表现出ADHD 核心临床症状,被广泛应用于ADHD 的研究,WKY 大鼠为其天然对照组[17-18]。 所有动物均饲养于河南中医药大学SPF 级动物实验中心[SYXK(豫)2021-0015],自由饮水进食,温度21 ~24℃,湿度50%~60%。 动物伦理申请经由河南中医药大学实验动物伦理委员会审核批准(DWLL202202007),符合《实验动物福利伦理审查指南》(GB/T 35892-2018)、《关于善待实验动物的指导性意见》和《河南中医药大学实验动物伦理委员会章程》的相关规定。 在实验中,我们严格遵循实验动物使用的3R 原则,减少对动物的伤害并给予人道主义关怀。
1.2 主要试剂与仪器
黄芩苷(货号:A0016)购自成都曼斯特生物科技有限公司,保存于4℃冰箱;丁苯那嗪(货号:GC13672)购自上海宏叶生物科技有限公司,保存于-20℃冰 箱; MPH (批 号: 1IE648, 分 装 批 号:1IE648C)购自河南中医药大学第一附属医院,生产于Janssen-Cilag Manufacturing,LLC,西安杨森制药有限公司分装,规格为每片18 mg,保存于4℃冰箱。旷场实验设备:包含旷场实验箱、SMART V3.0 软件,购自深圳市瑞沃德生命科技有限公司(型号:63041);水迷宫实验设备:包含Morris 摄像系统、恒温水箱、SMART V3.0 软件,购自深圳市瑞沃德生命科技有限公司(型号:63034)。
1.3 实验方法
1.3.1 动物给药及分组
大鼠适应性饲养5 d 后,进行给药。 配药:根据给药量150 mg/kg[9],灌胃量1 mL/100 g,配制黄芩苷溶液,冰箱4℃保存;根据给药量1.5 mg/kg[19],灌胃量1 mL/100 g,配制MPH 溶液,每颗药(含18 mg MPH)配120 mL 纯水,冰箱4℃保存;根据给药量3 mg/kg[20],注射量0.5 mL/100 g,配制丁苯那嗪溶液,即配即用;灌胃前将药物溶液定量取出,水浴复温至30℃后予大鼠灌胃。 给药前称重,根据体重调整给药量,每天给药1 次,时间固定于上午8:00~12:00。 灌胃前将药物溶液定量取出,水浴复温至30℃后予大鼠灌胃,MPH 组(1.5 mg/kg)、黄芩苷组(150 mg/kg)按体重(1 mL/100 g)灌胃给药,空白组、模型组给等量生理盐水,MPH+丁苯那嗪组、黄芩苷+丁苯那嗪组在灌胃给药同时,按体重(0.5 mL/100 g)腹腔注射丁苯那嗪(3 mg/kg)。
1.3.2 旷场实验
在给药第0、7、14、21、28 天进行旷场实验,使大鼠从中央区域进入旷场中,电脑持续稳定追踪大鼠轨迹,SMART V3.0 软件记录大鼠运动总距离及平均速度,每只大鼠每次旷场实验时间为5 min,实验结束后将大鼠放回笼中,清理旷场后进行下一只。
1.3.3 Morris 水迷宫实验
在给药第3 周进行为期6 d 的Morris 水迷宫实验,前5 d 为隐匿站台实验,将水箱内注水,水面高出逃生平台约1 cm;水面分为4 个象限,按方位分别命名为西北象限、东北象限、东南象限、西南象限。 逃生平台置于西南象限中央区域。 将大鼠从四个象限依次放入水中,连续5 d 入水象限的顺序采取半随机循环方式,避免固定入水顺序影响实验结果[21];将大鼠依次从不同象限放入水中,当大鼠找到逃生平台并停留10 s 后,停止信号追踪,若大鼠120 s 内未找到逃生平台,将其引导至逃生平台并停留15 s 后,进行下一次实验,结束后烘干放回笼中。 实验第6 天为空间探索实验,撤除逃生平台,将大鼠从东北象限放入水中,记录120 s 内大鼠穿越平台次数和运动轨迹,实验进行两次求均值。
1.4 统计学方法
采用SPSS 25.0 统计学软件对实验数据进行统计学分析,计量资料以平均数±标准差(±s)表示,两组间比较采用t检验,多组定量数据的组间比较采用单因素方差分析,若等方差(P>0.05)则用LSD进行组间比较,若不等方差(P<0.05)则用DunnettT3 进行组间比较。 组间比较结果中,P<0.05 表示差异具有统计学意义。
2 结果
2.1 旷场实验结果
2.1.1 旷场实验中大鼠运动总距离实验结果
实验第0 天,空白组运动总距离显著小于各实验组(P<0.05)。 实验第7、14、21、28 天,MPH 组、黄芩苷组运动总距离较模型组显著减少(P<0.05),且这两组间无明显差异;MPH+丁苯那嗪组运动总距离较MPH 组显著增加(P<0.05)。 实验第14、21天,黄芩苷+丁苯那嗪组运动总距离较黄芩苷组显著增加(P<0.05)。 实验第28 天,黄芩苷+丁苯那嗪组运动总距离较模型组显著减少(P<0.05),较黄芩苷组显著增加(P<0.05)。 见表1,图1。

图1 旷场实验每组大鼠运动总距离比较Figure 1 Comparison of total distance traveled by each group of rats in the open field experiment
表1 旷场实验中每组大鼠运动总距离的比较结果(±s,m,n=6)Table 1 Comparison of total distance traveled by each group of ratsin the open field experiment

表1 旷场实验中每组大鼠运动总距离的比较结果(±s,m,n=6)Table 1 Comparison of total distance traveled by each group of ratsin the open field experiment
注:与空白组比较, aP<0.05;与模型组比较, bP<0.05;与MPH 组比较, cP<0.05;与黄芩苷组比较,dP<0.05;与MPH+丁苯那嗪组比较,eP<0.05。Note.Compared with normal control group, aP<0.05.Compared with model group, bP<0.05.Compared with methylphenidate hydrochloride group,cP<0.05.Compared with baicalin group, dP<0.05.Compared with MPH+tetrabenazine group, eP<0.05.
组别Groups第0 天Day 0第7 天Day 7第14 天Day 14第21 天Day 21第28 天Day 28 Normal空co白nt组rol group 7.9±3.9 4.3±1.3 4.0±0.5 3.3±0.4 3.6±1.2 Mo模de型l g组roup 45.8±3.7a 31.0±5.4a 29.9±5.0a 30.7±4.5a 28.4±5.6a MethylphenidaM te P h Hy d组rochloride group 44.2±2.5a 19.7±5.5ab 17.2±5.9ab 16.2±3.0ab 14.5±5.8ab Ba黄ica芩lin苷g组roup 42.4±8.7a 21.6±2.2ab 17.8±5.8ab 14.9±6.1ab 12.3±5.4ab MP MH P+H tet+ra丁be苯na那zin嗪e组group 46.1±4.5a 33.6±5.9ac 29.2±5.2ac 30.4±4.1ac 28.4±6.1ac Baic黄al芩in+苷te+tr丁ab苯ena那zin嗪e组group 45.1±5.6a 28.2±6.7a 26.5±6.7ad 24.3±6.6ad 20.2±6.1abde F 33.514 18.646 14.148 21.040 13.348 P<0.001 <0.001 <0.001 <0.001 <0.001
2.1.2 旷场实验中大鼠运动平均速度实验结果
实验第0 天,空白组运动平均速度较各实验组显著降低(P<0.05)。 实验第7、14、21、28 天,黄芩苷组、MPH 组运动平均速度较模型组显著降低(P<0.05),且这两组间无明显差异。 实验第14、21、28天,MPH+丁苯那嗪组运动平均速度较MPH 组显著升高(P<0.05)。 实验第7、14、21、28 天,黄芩苷+丁苯那嗪组运动平均速度较模型组明显降低,较黄芩苷组明显升高。 见表2,图2。
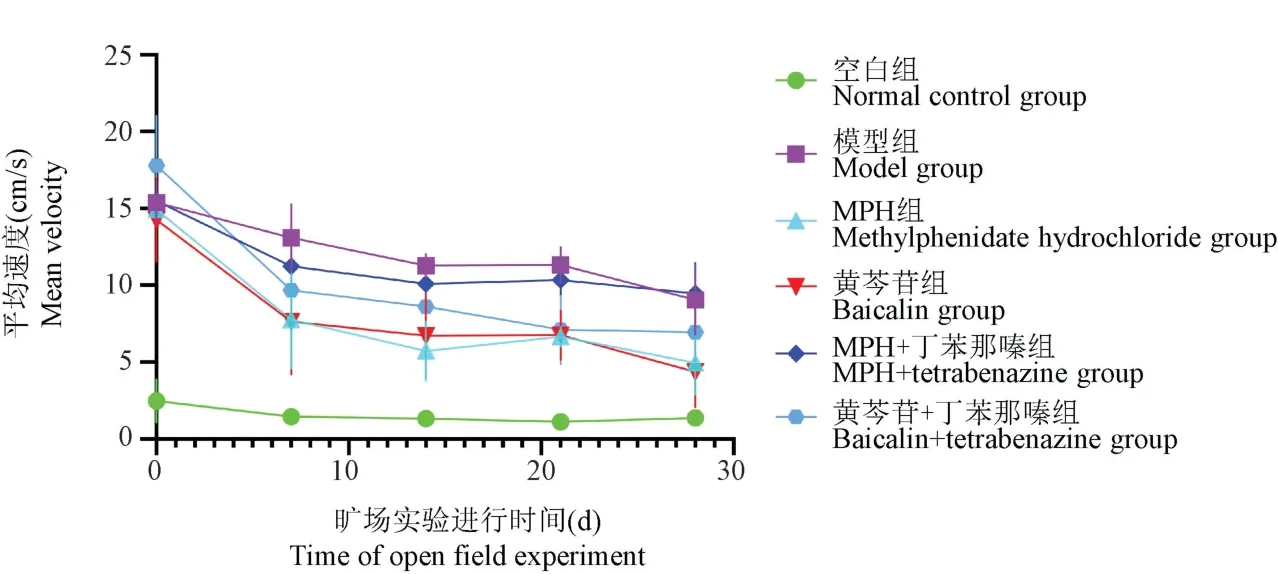
图2 旷场实验每组大鼠运动平均速度比较Figure 2 Comparison of average exercise speed of rats in each group in open field experiment
表2 旷场实验中每组大鼠运动平均运动速度比较(±s,cm/s,n=6)Table 2 Comparison of average movement speed of each group of rats in the open field experiment
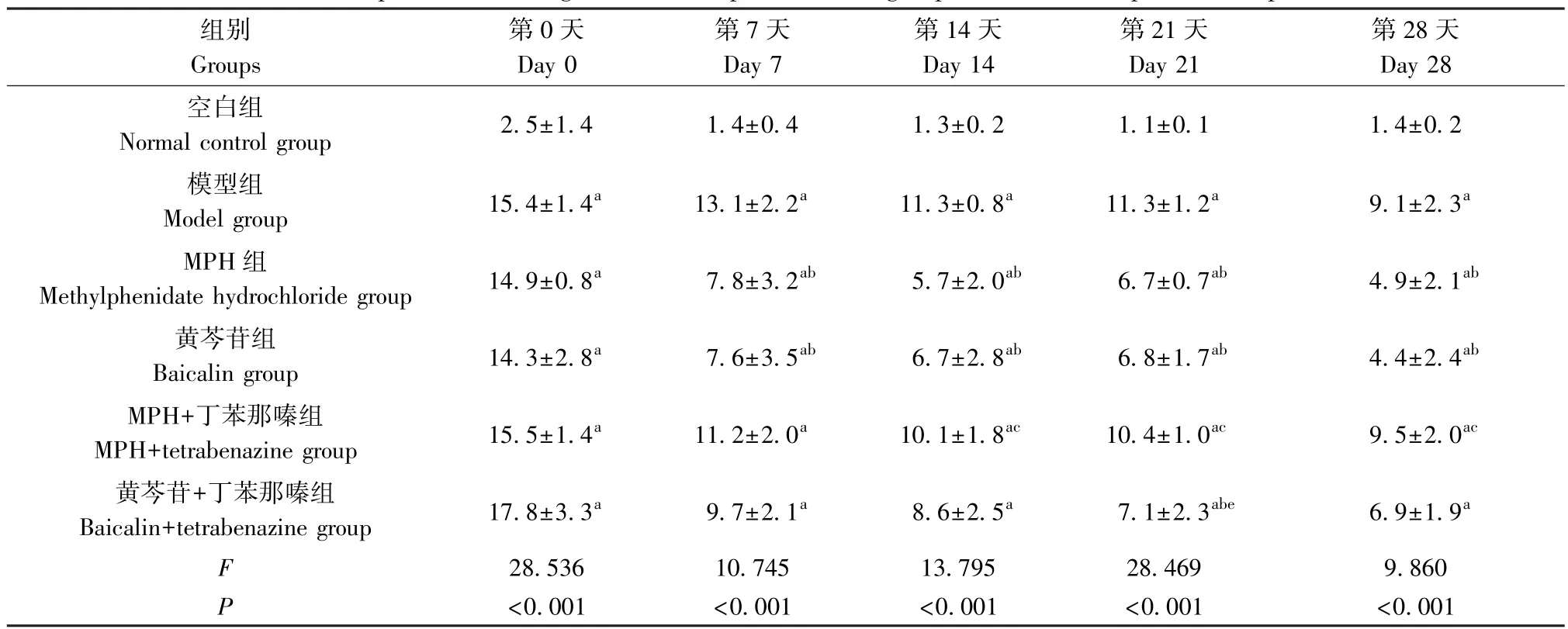
表2 旷场实验中每组大鼠运动平均运动速度比较(±s,cm/s,n=6)Table 2 Comparison of average movement speed of each group of rats in the open field experiment
注:与空白组比较, aP<0.05;与模型组比较, bP<0.05;与MPH 组比较, cP<0.05;与MPH+丁苯那嗪组比较, eP<0.05。Note.Compared with normal control group, aP<0.05.Compared with model group, bP<0.05.Compared with methylphenidate hydrochloride group, cP<0.05.Compared with MPH+tetrabenazine group, eP<0.05.
组别Groups第0 天Day 0第7 天Day 7第14 天Day 14第21 天Day 21第28 天Day 28 Normal空co白nt组rol group 2.5±1.4 1.4±0.4 1.3±0.2 1.1±0.1 1.4±0.2 Mo模de型l g组roup 15.4±1.4a 13.1±2.2a 11.3±0.8a 11.3±1.2a 9.1±2.3a MethylphenidaM te P h Hy d组rochloride group 14.9±0.8a 7.8±3.2ab 5.7±2.0ab 6.7±0.7ab 4.9±2.1ab Ba黄ica芩lin苷g组roup 14.3±2.8a 7.6±3.5ab 6.7±2.8ab 6.8±1.7ab 4.4±2.4ab MP MHP+H tet+ra丁be苯na那zin嗪e组group 15.5±1.4a 11.2±2.0a 10.1±1.8ac 10.4±1.0ac 9.5±2.0ac Baic黄al芩in+苷te+tr丁abe苯na那zin嗪e组group 17.8±3.3a 9.7±2.1a 8.6±2.5a 7.1±2.3abe 6.9±1.9a F 28.536 10.745 13.795 28.469 9.860 P<0.001 <0.001 <0.001 <0.001 <0.001
2.1.3 旷场实验轨迹
旷场实验轨迹中,空白组在中央区域进入旷场后立即进入周围区域运动,未进入中央区域,运动轨迹短。 模型组进入旷场后运动轨迹遍布整个旷场,中央区域运动轨迹明显增加,运动轨迹长。MPH 组在周围区域运动轨迹多,中央区域运动少,运动轨迹较模型组明显减少。 黄芩苷组进入旷场后立即进入周围区域运动,未进入中央区域,运动轨迹较模型组明显减少;MPH+丁苯那嗪组在中央区域运动轨迹占比较MPH 组增大,运动轨迹长;黄芩苷+丁苯那嗪组在中央区域运动轨迹较模型组减少,较黄芩苷组增加,如图3。
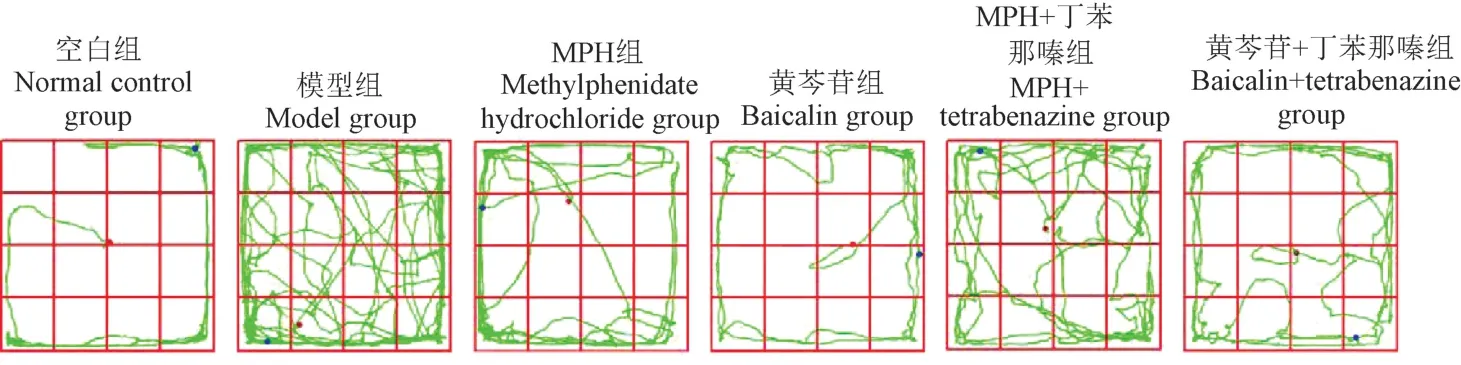
图3 旷场实验中各组大鼠典型运动轨迹图Figure 3 Typical movement trajectory plots of different groups of rats in the open field experiment
旷场实验结果显示,在给药第7、14、21、28 天,MPH 组和黄芩苷组运动总距离和平均速度较模型组显著降低(P<0.05),且这两组间无明显差异;在给药第14、21、28 天,黄芩苷+丁苯那嗪组运动总距离较黄芩苷组显著增大(P<0.05),平均速度较黄芩苷组明显增大,运动总距离和平均速度较模型组明显减小。
2.2 Morris 水迷宫实验结果
2.2.1 Morris 水迷宫空间隐匿站台实验中各组大鼠潜伏期实验结果
实验第2 ~5 天,各实验组潜伏期较空白组显著缩短(P<0.05)。 实验第1 天,黄芩苷组潜伏期较模型组显著缩短(P<0.05);第2 ~5 天,黄芩苷组、MPH 组潜伏期较模型组显著缩短(P<0.05),这两组在2~4 d 组间无明显差异,在第5 天黄芩苷组潜伏期较MPH 组显著缩短(P<0.05)。 实验第1 ~5天,MPH+丁苯那嗪组潜伏期较MPH 组显著延长(P<0.05)。 实验第1、3、4、5 天,黄芩苷+丁苯那嗪组潜伏期较黄芩苷组显著延长(P<0.05);第4、5 天,黄芩苷+丁苯那嗪组潜伏期较模型组显著缩短(P<0.05)。 见表3,图4。

图4 Morris 水迷宫隐匿站台实验各组大鼠潜伏期随时间的变化情况Figure 4 Changes in the latency period of rats in different groups during the Morris water maze experiment over time
表3 Morris 水迷宫隐匿站台实验每天各组大鼠潜伏期时间比较 (±s,s,n=6)Table 3 Comparison of latency periods of different groups of rats in the hidden platform experiment of the Morris water maze each day

表3 Morris 水迷宫隐匿站台实验每天各组大鼠潜伏期时间比较 (±s,s,n=6)Table 3 Comparison of latency periods of different groups of rats in the hidden platform experiment of the Morris water maze each day
注:与空白组比较, aP<0.05;与模型组比较, bP<0.05;与MPH 组比较, cP<0.05;与黄芩苷组比较, dP<0.05。Note.Compared with normal control group, aP<0.05.Compared with model group, bP<0.05.Compared with methylphenidate hydrochloride group, cP<0.05.Compared with baicalin group, dP<0.05.
组别Groups第1 天Day 1第2 天Day 2第3 天Day 3第4 天Day 4第5 天Day 5空白组Normal control group 38.3±9.8 41.3±3.9 38.9±4.7 47.9±8.0 28.8±4.1模型组Model group 27.6±3.0a 20.6±6.4a 26.5±5.1a 25.4±4.1a 22.6±6.2a MPH 组Methylphenidate hydrochloride group 20.6±4.8a 10.2±1.8ab 12.6±6.4ab 9.8±4.7ab 13.7±1.6ab黄芩苷组Baicalin group 14.8±3.2ab 11.6±2.8ab 14.9±3.6ab 8.9±2.4ab 9.3±3.6abc MPH+丁苯那嗪组MPH+tetrabenazine group 33.2±9.0c 16.5±3.7ac 21.8±4.7ac 19.0±4.0ac 20.7±5.1ac黄芩苷+丁苯那嗪组Baicalin+tetrabenazine group 27.4±7.8ad 15.4±3.4a 22.8±5.8ad 16.8±2.7abd 16.5±1.3abd F 6.122 33.834 13.277 37.522 11.725 P 0.002 <0.001 <0.001 <0.001 <0.001
2.2.2 Morris 水迷宫空间探索实验中各组大鼠穿越平台次数、在目标象限运动距离和停留时间占比实验结果
实验第6 天,除MPH+丁苯那嗪组外,各实验组穿越平台次数、在目标象限运动距离和停留时间占比较空白组显著增加(P<0.05);MPH 组、黄芩苷组穿越平台次数、在目标象限运动距离和停留时间占比较模型组显著增加(P<0.05),且这两组间无明显差异;MPH+丁苯那嗪组穿越平台次数、在目标象限运动距离和停留时间占比较MPH 组显著减少(P<0.05);黄芩苷+丁苯那嗪组在目标象限运动距离和停留时间占比较黄芩苷组显著降低(P<0.05),较模型组明显升高。 见表4。
表4 Morris 水迷宫空间探索实验各组大鼠穿越平台次数、目标象限运动距离和停留时间占比(±s,n=6)Table 4 Number of platform crossings, distance moved within the target quadrant and proportion of time spent in the target quadrant in the Morris water maze spatial exploration experiment for each group of rats
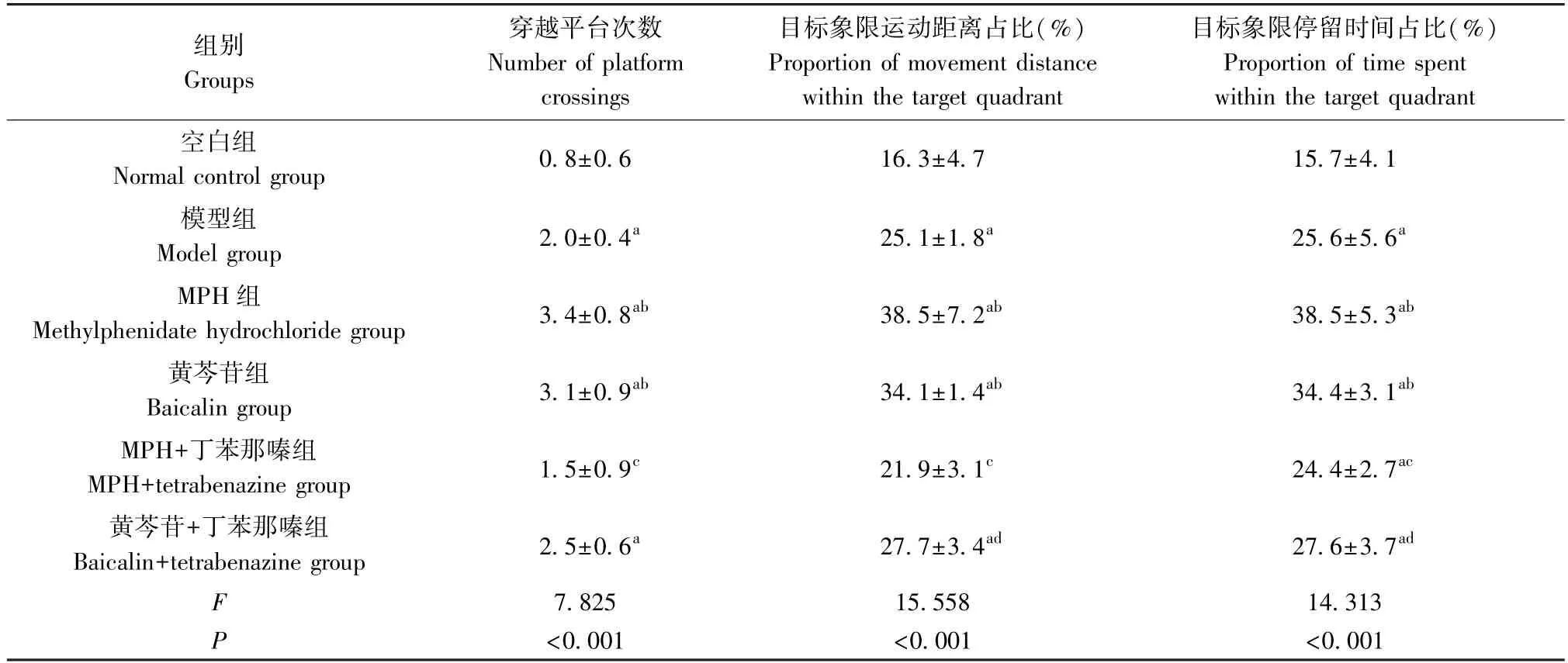
表4 Morris 水迷宫空间探索实验各组大鼠穿越平台次数、目标象限运动距离和停留时间占比(±s,n=6)Table 4 Number of platform crossings, distance moved within the target quadrant and proportion of time spent in the target quadrant in the Morris water maze spatial exploration experiment for each group of rats
注:与空白组比较, aP<0.05;与模型组比较, bP<0.05;与MPH 组比较, cP<0.05;与黄芩苷组比较, dP<0.05。Note.Compared with normal control group, aP<0.05.Compared with model group, bP<0.05.Compared with methylphenidate hydrochloride group, cP<0.05.Compared with baicalin group, dP<0.05.
组别Groups穿越平台次数Number of platform crossings目标象限运动距离占比(%)Proportion of movement distance within the target quadrant目标象限停留时间占比(%)Proportion of time spent within the target quadrant空白组Normal control group 0.8±0.6 16.3±4.7 15.7±4.1模型组Model group 2.0±0.4a 25.1±1.8a 25.6±5.6a MPH 组Methylphenidate hydrochloride group 3.4±0.8ab 38.5±7.2ab 38.5±5.3ab黄芩苷组Baicalin group 3.1±0.9ab 34.1±1.4ab 34.4±3.1ab MPH+丁苯那嗪组MPH+tetrabenazine group 1.5±0.9c 21.9±3.1c 24.4±2.7ac黄芩苷+丁苯那嗪组Baicalin+tetrabenazine group 2.5±0.6a 27.7±3.4ad 27.6±3.7ad F 7.825 15.558 14.313 P<0.001 <0.001 <0.001
2.2.3 Morris 水迷宫空间探索实验典型轨迹图
Morris 水迷宫空间探索轨迹图中,空白组运动轨迹较短,各象限运动轨迹分布均匀;模型组运动轨迹混乱,各象限平均分布;MPH 组、黄芩苷组在目标象限运动轨迹占比较模型组明显增大;MPH+丁苯那嗪组运动轨迹与模型组相当;黄芩苷+丁苯那嗪组在目标象限运动轨迹占比较模型组增加,较黄芩苷组减少。 如图5。
Morris 水迷宫实验结果显示,MPH 组、黄芩苷组潜伏期较模型组显著缩短(P<0.05),穿越平台次数、在目标象限运动距离和停留时间占比较模型组显著升高(P<0.05),且这两组在实验1~4 d 组间无明显差异,第5 天黄芩苷组潜伏期较MPH 组显著缩短(P<0.05)。 黄芩苷+丁苯那嗪组潜伏期在实验第1、3、4、5 天,较黄芩苷组显著延长(P<0.05),在实验第4、5 天较模型组显著缩短(P<0.05);黄芩苷+丁苯那嗪组在目标象限运动距离和停留时间占比相较于黄芩苷组显著降低(P<0.05),相较于模型组明显升高。
3 讨论
脑内DA 是由胺能神经吸收血液中酪氨酸,在酪氨酸羟化酶催化下形成左旋多巴,再由多巴脱羧化酶最终合成[22]。 合成后的DA 主要在突触前膜经囊泡单胺转运体Ⅱ型(VMAT2)转运进入突触小泡储存,从而避免DA 被细胞质中单胺氧化酶(monoamine oxidase,MAO)氧化降解失活,当动作电位到达神经末梢时,突触小泡与突触前膜融合,胞吐释放DA[23]。 VMAT2 的正常表达对脑内DA 的转运、释放以及维持脑内DA 正常水平意义重大。 课题组前期研究发现,黄芩苷能够显著提高VMAT2蛋白及RNA 表达水平,尤其对纹状体内VMAT2 表达的影响最为直接[12],但其具体的作用靶点尚不明确。 这为本次探讨黄芩苷潜在作用靶点的研究奠定了基础。
旷场实验中大鼠的运动距离和平均速度反映大鼠的多动和冲动行为[24]。 Morris 水迷宫实验通过检测大鼠的学习记忆能力来评估大鼠注意力情况[25-26]。 本次实验研究显示,在给药前的旷场实验中,所有实验组运动总距离和平均速度较空白组显著升高,实验组各组间无明显差异,表明实验组大鼠与空白组对比,存在明显多动、冲动症状。 在给药过程中的旷场实验中,MPH 组和黄芩苷组运动总距离和平均速度较模型组显著降低,且这两组间无明显差异,表明黄芩苷与MPH 均能控制SHR 大鼠多动、冲动症状,并且两种药物的疗效无明显差异。研究表明,MPH 通过与DA 转运体(DAT)结合,抑制DAT 的生理功能,减少DA 重摄取,增加脑内DA含量治疗ADHD 核心症状[27]。 丁苯那嗪在本实验中作为VMAT2 特异性阻断剂,能够可逆性抑制VMAT2 表达[28]。 在旷场实验过程中,MPH+丁苯那嗪组大鼠运动总距离和平均速度较MPH 组显著升高,与模型组对比无明显差异。 这一实验结果我们推测,可能是丁苯那嗪阻断VMAT2 对DA 的转运和释放,DA 释放减少,导致DAT 再摄取抑制过程中突触间隙DA 含量降低,即使MPH 发挥抑制作用也不能达到脑内DA 水平的正常峰度,导致MPH 疗效不佳,但其确切机制还需进一步研究。 Morris 水迷宫隐匿站台实验中,MPH 组、黄芩苷组大鼠潜伏期较模型组显著缩短,穿越平台次数、在目标象限运动距离和停留时间占比较模型组显著升高,且这两组间无明显差异。 这一结果表明,MPH 与黄芩苷均能提高大鼠空间记忆和学习能力,改善大鼠注意力不集中,且两种药物疗效相当。
黄芩苷+丁苯那嗪组大鼠在旷场实验中运动总距离和平均速度较模型组显著降低,较黄芩苷组显著升高,在隐匿站台实验中的潜伏期较黄芩苷组显著延长,较模型组稍有缩短且两组之间的差异随实验时间的延长逐渐显著,在空间探索实验中穿越平台次数、在目标象限运动距离和停留时间占比较模型组升高,较黄芩苷组显著降低。 实验结果表明,黄芩苷作用于VMAT2 控制ADHD 核心症状,但其作用靶点并不单一,存在黄芩苷治疗ADHD 的其他靶点,而这些靶点尚不明确,这也是课题组后期的研究方向。
本研究在前期研究基础上,应用VMAT2 特异性抑制剂丁苯那嗪初步探索黄芩苷治疗ADHD 的潜在疗效机制及作用靶点,但深入的机制分析尚未进行。 实验尚存在不足之处,缺乏VMAT2 的激动剂组,以便更加明确VMAT2 的表达对大鼠ADHD症状的影响,我们将在后期实验中进行补充和探索。
