人类嗜T 淋巴细胞病毒抗体血清学筛查与确证试验的相关性分析*
2023-11-30邓燕清王淏单振刚谢君谋杜荣松肖巽南李仲平戎霞黄伯泉
邓燕清 王淏 单振刚 谢君谋 杜荣松 肖巽南 李仲平 戎霞 黄伯泉
(广州血液中心 广州市血液安全重点实验室,广东 广州 510095)
人类嗜T 淋巴细胞病毒(human T - lymphotropic virus,HTLV),是20 世纪70 年代末发现的第1 个人类逆转录病毒,有4 个亚型(HTLV-Ⅰ、HTLV-Ⅱ、HTLV-Ⅲ和HTLV-Ⅳ)[1]。 目前较有临床意义的是Ⅰ型和Ⅱ型(即HTLV-Ⅰ、HTLV-Ⅱ),属逆转录病毒科的RNA 肿瘤病毒亚科[2]。HTLV-Ⅰ、Ⅱ的传播方式主要有输血(15%~60%)、注射或性接触,也可通过垂直传播(经胎盘、产道或哺乳),国内有报道献血者家庭成员阳性感染的情况[3]。 HTLV 病毒通过感染CD4+T 淋巴细胞引起T 细胞白血病、毛细胞白血病、HTLV 相关的脊髓病/热带痉挛性截瘫(HTLV-associated myelopathy /tropical spasticparaparesis)以及炎性疾病[4],严重可引起死亡。 目前尚未发现治愈HTLV 感染的特效药物,也无相关疫苗,有报道称少部分药物可以缓解HTLV 感染相关疾病。HTLV 目前主要流行于日本的西南部、撒哈拉沙漠以南的非洲地区、加勒比海地区、南美洲等。 近年,国内的HTLV 流行区域主要集中在福建省、广东省、浙江省等东南沿海地区[5]。由于HTLV 可经输血传播,国家卫生健康相关部门于2015年颁发《关于做好人类嗜T 淋巴细胞病毒监测工作的通知》,要求部分采供血机构对无偿献血者开展HTLV 的筛查工作[6]。 目前,我国采供血机构对献血者的抗-HTLV-Ⅰ、Ⅱ的筛查均采用酶联免疫吸附试验(enzyme linked immunosorbent assay,ELISA),本研究通过对广州地区无偿献血者抗-HTLVⅠ/ⅡELISA 检测反应性的标本进行免疫印迹法(Western blotting,WB)确证,采用受试者工作特征曲线(receiver operating characteristic curve,ROC)分析抗-HTLV-Ⅰ/ⅡELISA 检测S/CO 值与WB 确证试验结果的相关性与阳性预测值,旨在更好地选择HTLV 监测方法提供一定的参考依据。
1 材料与方法
1.1 标本来源 2016 年7 月—2022 年8 月广州血液中心无偿献血者标本共2 223 225 份,EDTA-K2抗凝全血标本5 mL,2 000×g 离心5 min,血浆作血清学筛查,长期血浆保存于低温冰箱(-30℃以下)。 参与本次研究的献血者均签订了知情同意书,本次研究也获得广州血液中心伦理委员会的批准【广州血液中心医伦[2023]第033 号】。
1.2 试剂与仪器 抗-HTLV-Ⅰ/ⅡELISA 试剂(北京万泰公司,批号:T20160101—T20220202B),HTLV BLOT 2.4(MPBiomedicals 公 司, 批 号: AK9013—AK1008 )。 Microlab STAR8CH 全 自 动 加 样 仪(HAMILTON 公 司), Microlab FAME24/30 全自动酶免分析仪(HAMILTON 公司),Multiskan MK3 酶标分析仪(Thermo Fisher 公司)、URANUS AE 288S 一体机(深圳爱康公司)。 所有试剂均在有效期内使用,仪器设备均按照要求操作,进行定期维护和校准。
1.3 方法 使用HTLV-Ⅰ/ⅡELISA 试剂对献血者标本进行筛查,初筛检测呈反应性的标本进行单试剂双孔检测,双孔均为阴性者则为初筛试验阴性,双孔为阳性则为初筛反应性,记录各筛查试验的S /CO 值。 抗体初筛呈反应性的标本均采用WB 进行确证,结果阳性的判定为HTLV 阳性,结果阴性的判定为HTLV 阴性,结果不确定则为不确定性,同时对献血者进行随访。 检测抗-HTLV 试验过程严格按照其试剂说明书及广州血液中心实验的相关SOP 进行操作。
1.4 统计学分析 采用SPSS26.0 软件建立数据库,同时以WB 确证结果作为HTLV 感染阳性的确证标准,绘制ROC 曲线,利用ROC 曲线寻找S/CO 最佳诊断临界值;当Youden 指数(Youden 指数=灵敏度+特异度-1)最大时,其对应的S/CO 值为最佳阈值,用CI 表示95%的置信区间。 分析在最佳S/CO 阈值下试剂的灵敏度和特异度,计算其对确证试验结果的预测率,P<0.05 为差异有统计学意义。
2 结果
2.1 献血者标本抗-HTLV ELISA 检测与WB 确证结果2016 年7 月—2022 年8 月区间广州血站共筛查了献血者2 223 225人次。 共395 份献血者标本抗-HTLV-Ⅰ/ⅡELISA检测反应性,初筛阳性率为18/10 万(395/2 223 225)。 395份初筛反应性标本经WB 确证有25 份为HTLV 阳性,不确定性为16 份,确诊阳性率为6.33%(25/395)。 广州地区献血者中HTLV 的感染率约为1.1/10 万(25/2 223 225)。
2.2 抗-HTLV-Ⅰ/ⅡELISA 检测的S/CO 值与确证试验结果相关性 绘制ROC 曲线分析:抗-HTLV ELISA 检测的S/CO值ROC 曲线下面积为0.938(P<0.05),Youden 指数为0.801,此时S/CO 值为3.789,灵敏度为92.00%,特异度为80.10%;95%CI:0.885~0.990,见如图1。 因此抗-HTLV ELISA 检测的S/CO 值≥3.789 时,对WB 确证试验的阳性预测率为35%,当S/CO 值<3.789 时,其阴性预测率为99.4%,见表1。
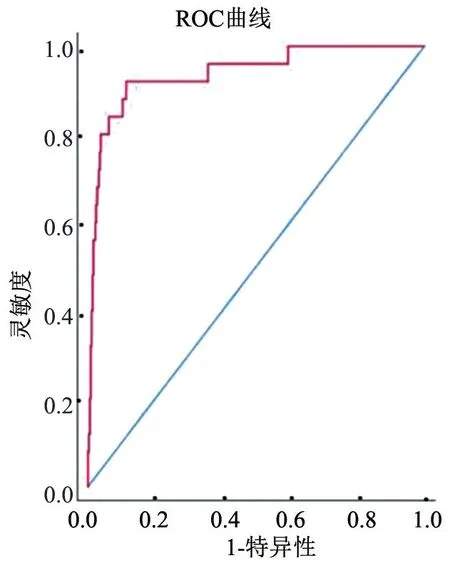
图1 抗-HTLV ELISA 检测S/CO 值的ROC 曲线
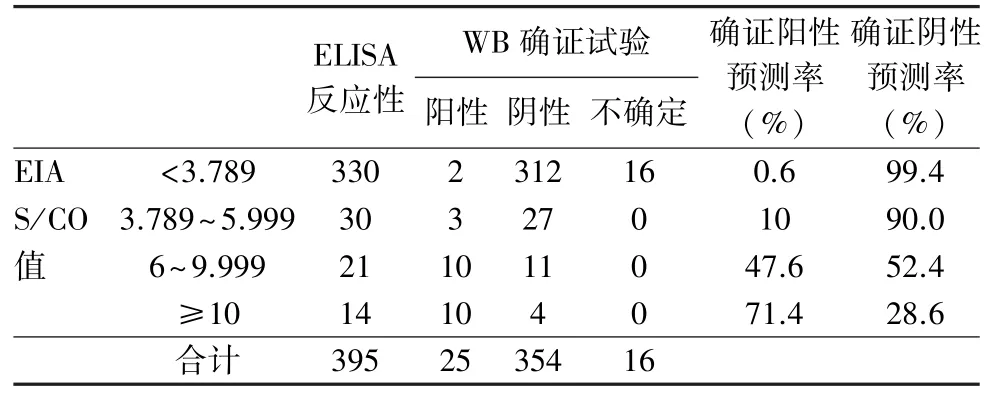
表1 抗-HTLV ELASA 检测的S/CO 值与WB 确证结果的相关性n(%)
2.3 WB 确证结果阳性、阴性、不确定性与ELISA 检测S/CO值的对比 确证阳性标本S/CO 均值、中位数与确证阴性标本、不确定标本比较存在差异(P<0.05),见表2,提示标本ELISA 检测S/CO 值越高,WB 确证试验阳性率相对应越高。
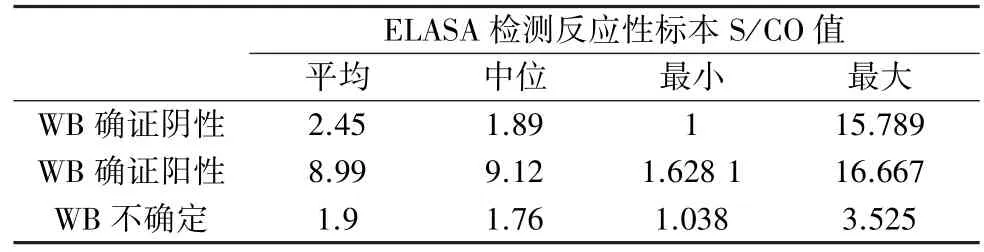
表2 ELASA 检测反应性标本S/CO 值分布
3 讨论
HTLV 在全球范围均有发现,各地区流行情况差异较大[7]。 日本于1984 年开始对献血者进行筛查,其人群流行率高达0.66%~1.02%[8]。 其他发达国家如美国、法国,其感染率较低,分别为0.025 0%[9]、0.005 6%[10]。 我国HTLV 的流行区域主要集中在东南沿海城市,王惠榕等[11]、张秋文等[12]对我国福建宁德地区HTLV 感染情况作了早期报道。HTLV 流行情况调查主要是通过对献血人群进行筛查,加拿大、美国、韩国、法国,以及中国香港特别行政区、中国澳门特别行政区、中国台湾地区等已将HTLV-Ⅰ筛查列入献血者常规筛查项目[7]。 目前我国大陆地区并未将HTLV 纳入献血者的法定常规筛查项目,仅于2015 年底提出对福建、广东、浙江3 省献血者进行全面筛查,其他各省、市按照10%比例进行献血者抽样筛查。
目前我国常见的HTLV 检测方法主要为血清学与核酸检测,血清学检测方法以双抗原夹心ELISA 为主,按方法学分有一步法和两步法,确证方法则主要为WB 确证试验。 对于无偿献血者这类低危感染人群,由于被检者体内存在与被检测病原体无关的非特异性抗原抗体,往往会造成WB 确证结果不确定。 国外研究表明,出现“不确定”确证结果的受检者在半年内随访中一般转为阴性,或继续保持不确定性,即为假阳性,故在阴性预测值计算中,把不确定结果等同于阴性[13]。 在本研究中确证阳性率为6.32%(25/395),与同属于低流行区域的广东省深圳市(6.06%,2/33)[14]、广东省中山市(3.2%,4/125)[15]、北京市(7.7%,2/26)[16]、天津市(5.3%,1/19)[17]差异不大,低于高流行区域福建省(26.8%,254/947)[18]。 本研究采用ELISA 法(一步法)对献血者标本进行筛查,非特异性抗体可引起假阳性反应率较高[19],这与文献报道ELISA 试剂的S/CO 值与阳性率呈正相关[20-21]相符。 有文献报道2 种梅毒筛查ELISA 检测对应的S/CO 值分别≥9 以及≥5 时,梅毒确认阳性率超过95%[20];抗-HCV ELISA 检测S/CO 值>3.8 时,阳性预测率达95%以上[21]。 我们通过对献血者抗-HTLV-Ⅰ/ⅡELISA 检测反应性结果S/CO 值进行比对,同时绘制ROC 曲线分析抗-HTLV-Ⅰ/ⅡELISA 检测S/CO 值与WB 确证试验结果的相关性,综合考虑阳性预测率和阴性预测率,选用Youden 指数最大所对应的S/CO 值作为报告确证阳性的参考阈值,得出ELISA 检测最佳S/CO 值为3.789。 S/CO 值<3.789 时其阴性预测率为99.4%,当S/CO 值为≥10 其确证阳性预测率可达71.4%。验证结果阳性的S/CO 值与阴性的S/CO 值比较有差异(P<0.05),此结果与欧山海[22]结论一致。 在确证阳性的标本中,有2 份ELISA 反应性标本S/CO 值<3.789,献血者很可能为初期感染,HTLV 病毒载量较低,抗体滴度较低。 ELISA 法存在检测结果假阳性的问题很难避免,用WB 进行确证就很有必要。 欧山海等[18]研究指出,HTLV 初筛同一试剂假阳性率跟当地流行率有关系,同一试剂在流行率较高的地区如宁德市,抗-HTLV-Ⅰ/ⅡELISA 检测S/CO 值>4 或5 时,其初筛试验的验证阳性率高达90%,而在HTLV 流行率较低的漳州市,其S/CO 值>4 时验证阳性率为33.3%,S/CO 值>5 时验证阳性率则为57.1%。 本地区2016—2022 年确诊阳性率为1.1/10 万,低于福建省宁德市的184.4/10 万,福建省漳州市的3.7/10 万,属于低流行区域,初筛假阳性率高[18]。 周晓真等[19]的研究指出,使用2 种抗-HTLV ELISA 试剂(北京万泰、意大利索尼)检测出的双试剂反应性标本,HTLV 确证试验均为阳性。 由于WB 确认试剂昂贵,供应有限,操作复杂,很难普及使用。 因此,我们认为对于初筛反应性标本,可用另一厂家的ELISA 试剂进行复核,对于单试剂检测S/CO 值<3.789 可认为其为假阳性,对双试剂检测反应性标本或S/CO 值>3.789 进行确证试验。 确证试验结果为“不确定”的16 名献血者中仅有1 名进行归队复查,结果为阴性;本课题组将继续对余下15 名“不确定”的献血者追踪随访。
综上所述,S/CO 值的诊断阈值能为我们提供一个预估参考指标,对可疑ELISA 结果可以作一个初步判断。 广州地区献血人群HTLV 流行率较低;抗-HTLV-Ⅰ/ⅡELISA 试剂检测假阳性率较高,确证试验很有必要。
利益冲突:所有作者均声明不存在利益冲突。
