阿莫西林克拉维酸钾片溶出曲线检测方法的建立与验证
2023-11-15刘玉佳王淑君
刘玉佳,王淑君
(1.沈阳药科大学 药学院,辽宁 沈阳 110016;2.华北制药股份有限公司,河北 石家庄 050000)
阿莫西林克拉维酸钾片是世界上第一个含β-内酰胺酶抑制剂的抗生素复合制剂,其可有效抑制由多种耐药细菌产生的β-内酰胺酶,加强阿莫西林的抗菌活性,扩大其抗菌谱[1]。在对该药品进行仿制研究过程中,采用溶出曲线测定产品体外溶出行为是常用的筛选处方和提高体内生物等效试验通过率的方法,能最大程度地促使仿制药与原研制剂体内生物利用度一致[2]。因此,建立一种准确灵敏的溶出曲线分析方法对仿制药研究过程意义重大。本文开发了一种用于测定阿莫西林克拉维酸钾片溶出曲线的方法,采用桨法 75 rpm·min-1[3],以水为溶出介质,在 5、10、15、30、45 分钟时经自动取样仪取样后,使用一次性滤膜过滤,注入液相色谱仪进行检测。对该方法进行滤膜吸附、专属性、线性范围、回收率、定量限、精密度、稳定性等项目验证[4]。结果表明,本方法滤膜吸附低、专属性好、灵敏度高、溶出范围内线性关系良好,精密度与准确度均符合要求,能够用于仿制药处方工艺开发期间的溶出曲线检测。
1 主要仪器与试药
安捷伦 1200 serious 高效液相色谱仪,岛津 LC-2010AHT 高效液相色谱仪,Sartorius BP211D 电子天平(德国塞多利斯集团),FE28 型 pH 计(梅特勒 METTLER-TOLEDO),HANSON VISION G2 Elite 8 型溶出仪(美国 Hanson)。
克拉维酸化学对照品(中国药品生物制品检定所,批号:130429-201307,含量 95.0%);阿莫西林化学对照品(中检所,批号:130409-201011,含量 85.8%);阿莫西林克拉维酸钾系统适用性对照品(中检所,批号:130588-201202);磷酸二氢钠(天津永大,批号:20140728,优级纯)。
2 方法与结果
2.1 溶出及检验方法
溶出方法:桨法,溶出介质:水,体积:900 L,转速75 rpm·min-1[5],取样时间点:5、10、15、30、45 min,溶出介质温度:(37±0.5)℃,每个取样点时,自动取样仪吸取溶出杯内溶液约4 mL。经在线过滤器过滤后,加入到预先放置的试管内。然后,自动补充相同体积相同温度的溶出介质。取试管内液体经 0.45 μm 水系过滤器(津腾)过滤后,加入液相进样瓶内,待检。
检验方法:色谱柱为 Welch ultimate AQ-C18(4.6×250 mm,5 μm),流动相为甲醇—磷酸盐缓冲液(7.8 g·L-1磷酸二氢钠溶液,调节 pH 值至 (4.4±0.1))=5∶95,检测器波长为 220 nm,进样体积为 20 μL。
系统适用性要求:系统适用性溶液色谱图应与中检院该批系统适用性对照品所附标准图谱一致。
2.2 溶液配制
供试液:通过自动取样仪取溶出液 4 mL,使用 0.45 μm 滤膜滤过后作为供试液。
对照溶液:精密称取克拉维酸对照品和阿莫西林对照品约 14、28 mg,置 100 mL 量瓶中,加水超声溶解并定容,即得。
系统适用性溶液:精密称取阿莫西林克拉维酸钾系统适用性对照品约 8 mg,置 10 mL 量瓶中,加流动相溶解并定容,即得。
2.3 滤膜吸附试验
过滤溶出液时,使用的滤膜如果对主成分有吸附,会使过滤后的供试液浓度低于实际溶出液的浓度,从而造成检验误差。因此,设计滤膜吸附试验应确认使用的滤膜对主成分没有吸附。如果滤膜有吸附,则初滤液浓度会与弃去部分初滤液后的续滤液浓度有明显差异。取本品研细后,精密称取细粉适量,置 100 mL 量瓶中,加水溶解并定容,制成含阿莫西林约 0.06 mg·mL-1和0.28 mg·mL-1的溶液(即相当于全部溶出 20% 和 100%)。用一次性无菌注射器吸取溶液适量,经 0.45 μm 水系过滤器(津腾)过滤,分别取弃去初滤液 0、1、2、3 mL 后的续滤液作为供试液。分别精密量取各供试液 20 μL 注入液相色谱仪,记录色谱图,试验数据见表1。

Table 1 Results of adsorption test of filter membrane to solution表1 滤膜对溶液吸附性试验结果
结果表明,没有弃去初滤液时,主成分的峰面积与弃去部分初滤液后主成分的峰面积无明显差异。说明滤膜对本品溶出 20% 和 100% 的溶液中主成分均无吸附。
2.4 在线过滤器的吸附试验
精密称取本品细粉适量,用水溶解并稀释制成相当于溶出 20% 和 100% 的溶液。将溶出仪自动取样器管路润洗体积设为 7 mL,将溶液经自动取样器取出 4 mL,经滤膜过滤,弃去初滤液1 mL,取续滤液作为供试品溶液①;同时用一次性注射器吸取同一溶液4 mL,同法操作,取续滤液作为供试品溶液②。分别精密量取供试品溶液①和供试品溶液②各 20 μL,注入液相色谱仪,记录色谱图。试验结果见表2。
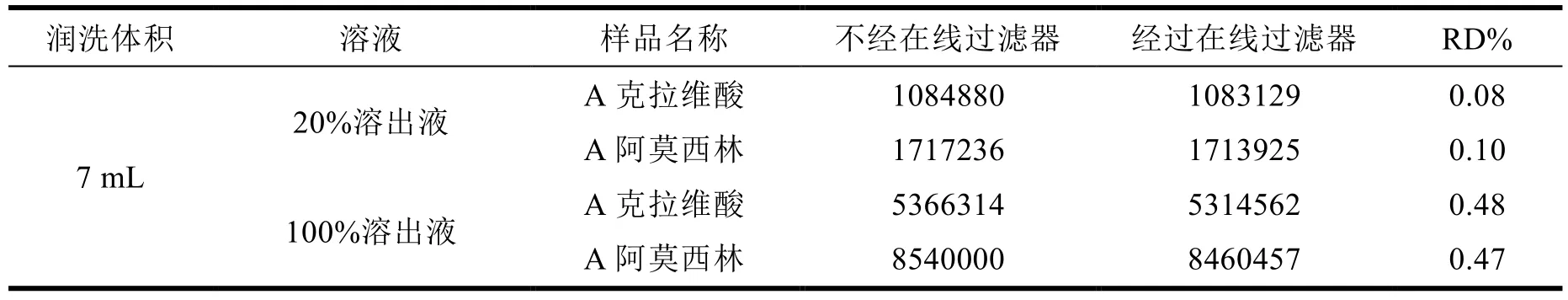
Table 2 Results of 20% solution adsorption test dissolved by on-line filter表2 在线过滤器对溶出20%的溶液吸附试验结果
结果表明,溶出仪自动取样器管路润洗体积设为7 mL,在线过滤器对本品溶出 20% 和 100%的溶液均无吸附,故溶出试验方法设置管路润洗体积为7 mL。
2.5 专属性试验
按照制剂处方比例以水为溶剂配制相当于阿莫西林和克拉维酸溶出均为 100% 的空白辅料,作为空白辅料溶液。取空白辅料溶液和空白溶剂按“2.1”项方法检测。结果表明,空白溶剂和空白辅料均未在主成分出峰位置有干扰峰,试验结果见图1~图2。说明该方法专属性良好。

Fig.1 Blank excipient solution chromatogram图1 空白辅料溶液色谱图

Fig.2 Blank solvent chromatogram图2 空白溶剂色谱图
2.6 线性范围考察
精密称取阿莫西林对照品和克拉维酸对照品约 45、22.5 mg,置于 25 mL 量瓶中,加水溶解并稀释至刻度,作为储备液。吸取储备液适量,逐步稀释制成线性溶液 1~线性溶液 6,浓度分别为0.018、0.072、0.144、0.216、0.288 和0.360 mg·mL-1。
取线性溶液 1~6 按“2.1”项方法进行检测,记录各主成分的峰面积 A 为纵坐标,以对应的质量浓度 C 为横坐标进行线性回归,得到线性回归方程为:阿莫西林:A=2.92×107C+5.55×104(R2=0.999 9),克拉维酸:A=3.35×107C+5.75×104(R2=0.999 8),两主成分的线性图见图3~4。实验结果表明,在验证浓度范围内主成分峰面积与浓度均呈良好的线性关系,各质量浓度下样品的峰面积结果见表3。
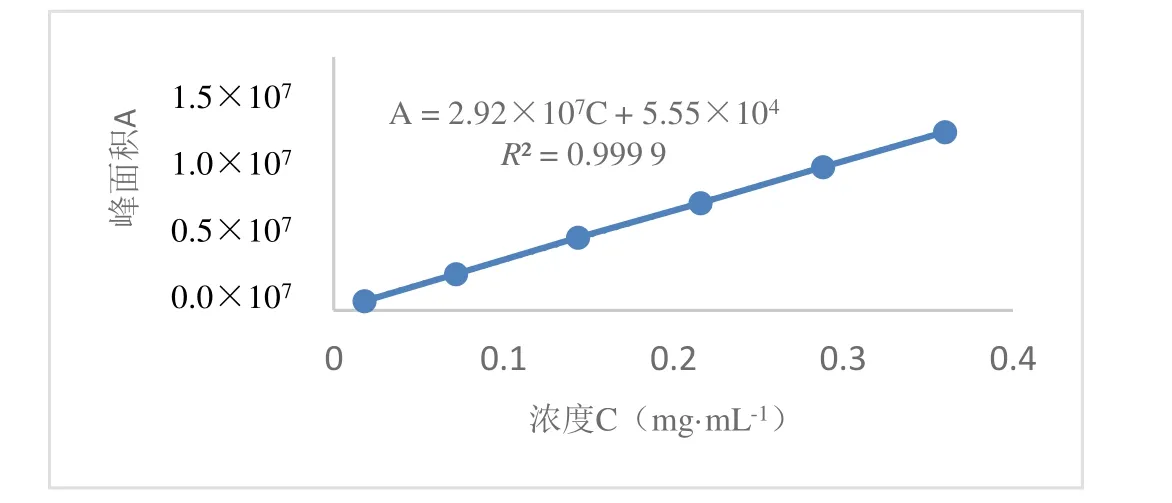
Fig.3 Linear plot of amoxicillin in water图3 阿莫西林在水中线性关系图
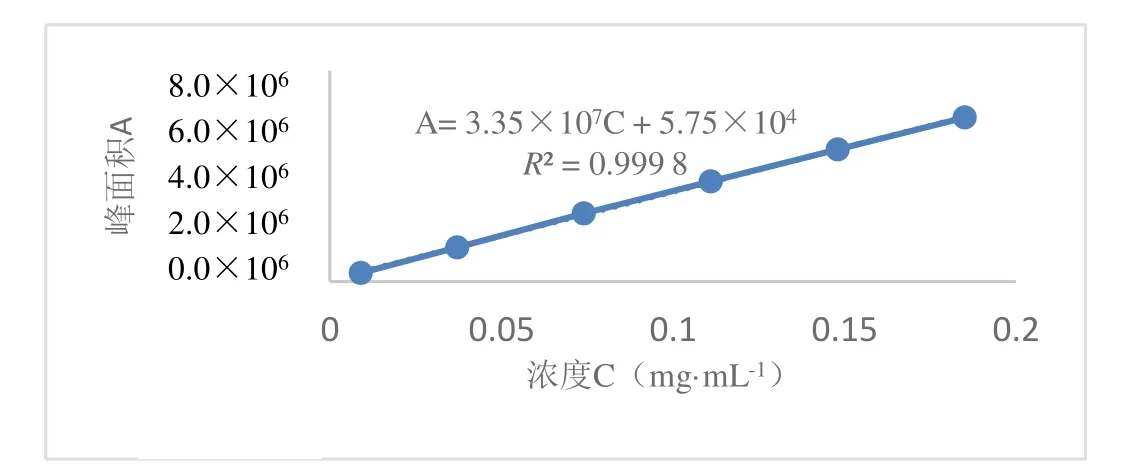
Fig.4 Linear plot of clavulanate acid in water图4 克拉维酸在水中线性关系图
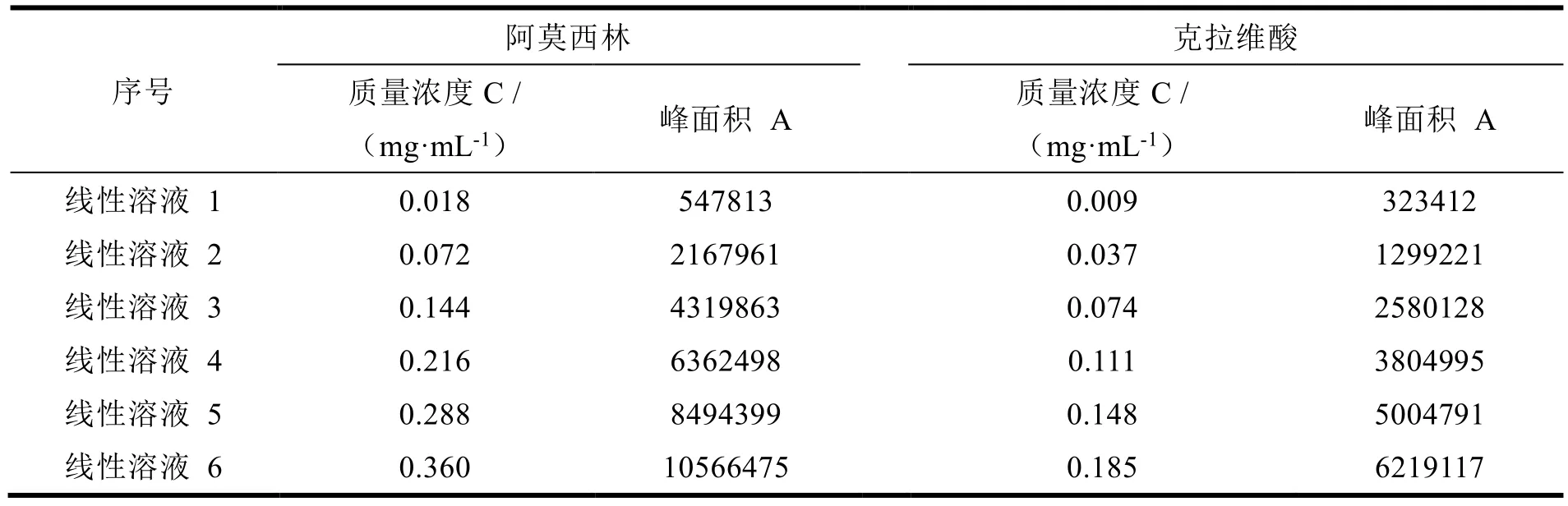
Table 3 Peak area results of samples at each mass concentrations表3 各质量浓度下样品的峰面积结果
2.7 回收率试验
评估溶出曲线各取样点实际溶出量后,选取阿莫西林和克拉维酸全部溶出的 20%、50%、80%、100% 和 120% 五个浓度进行回收率测定。精密称取阿莫西林约 35、42.5 mg 和克拉维酸对照品约 17.5、20 mg,置于 25 mL 量瓶中,分别加水溶解并定容,作为储备液①和储备液②。按照表4 配制回收率试验溶液。

Table 4 The preparation of recovery solution表4 回收率试验溶液的配制
精密量取供试液和对照溶液各 20 mL,注入液相色谱仪。测定供试液中主成分的含量,计算回收率,结果见表5。
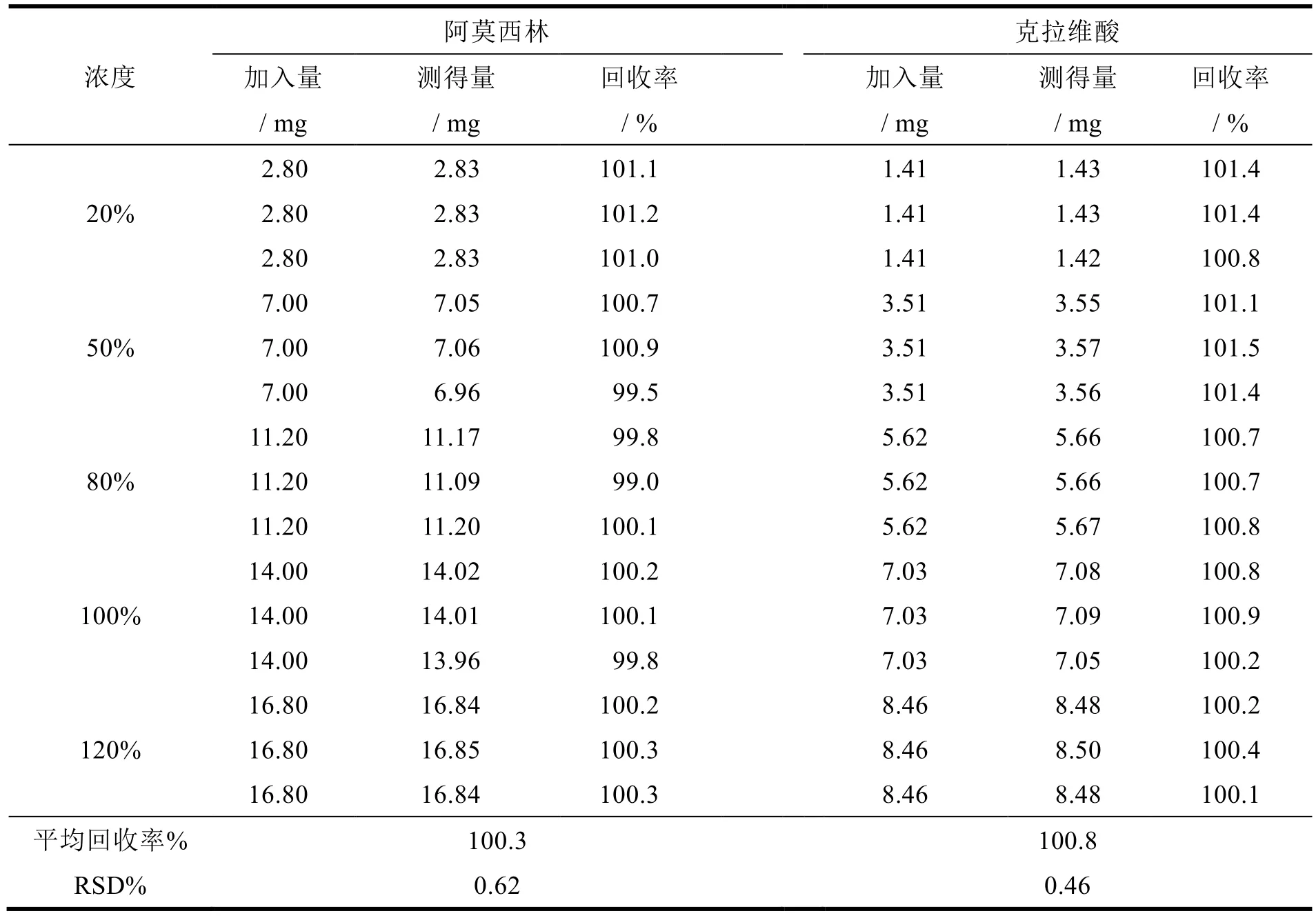
Table 5 Determination results of the recovery percent表5 回收率测定结果
结果表明,阿莫西林在溶出 20%~120% 范围内的平均回收率均在 98.5%~101.5%,RSD 均小于 1.0%;克拉维酸在溶出 20%~120% 范围内的平均回收率均在 98.5%~101.5%,RSD 均小于 1.0%。说明用本方法测定溶出曲线各溶出浓度的阿莫西林和克拉维酸准确度好。
2.8 定量限试验
精密称取阿莫西林和克拉维酸对照品约 15 mg,置于 50 mL 量瓶中,加水溶解并定容,摇匀;精密量取适量加水逐级稀释至主成分信噪比 S/N 约为 10∶1,阿莫西林定量限溶液浓度为 0.050 2 μg·mL-1,经计算定量限为 1.006 ng,克拉维酸定量限溶液的浓度为 0.033 1 μg·mL-1。计算定量限为0.662 ng。
2.9 精密度试验
(1)重复性
将本品研细,精密称取细粉适量,置于 50 mL 量瓶中,加水溶解并定容制成全部溶出 100%浓度的溶液(即每 1 mL 中含阿莫西林约为 0.28 mg 的溶液),重复配制 6 份,作为重复性试验溶液。精密称取阿莫西林对照品和克拉维酸对照品约 28、14 mg,置于 100 mL 量瓶中,加水并定容制成与供试液相同浓度的溶液,作为对照溶液。精密量取对照溶液和重复性试验溶液各 20 μL,注入液相色谱仪,记录色谱图。结果见表6。结果表明该方法的重复性良好。
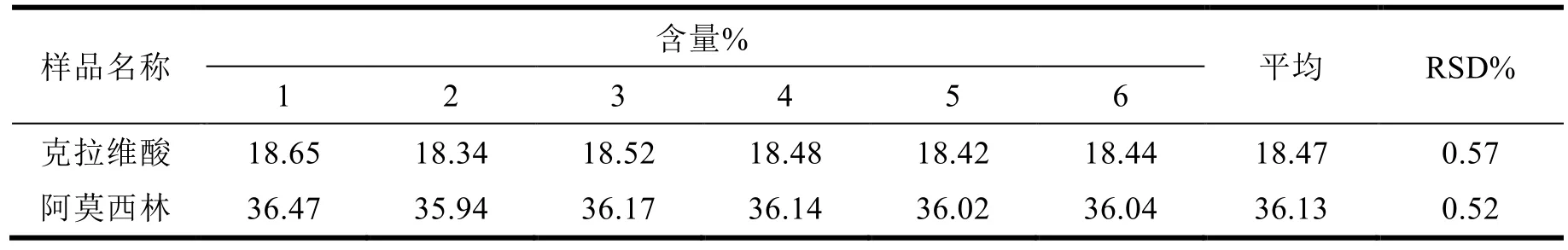
Table 6 Repetitive test results表6 重复性试验结果
(2)中间精密度
按照重复性试验项下的方法,由两个不同试验人员在不同时间分别使用 Agilent1200 和岛津LC-2010AHT 液相色谱仪,选取同一批样品进行溶出曲线测定。结果见表7。结果表明该方法的中间精密度良好。

Table 7 Intermediate precision test results表7 中间精密度试验结果
2.10 稳定性试验
将本品研细,取细粉适量,置 50 mL 量瓶中,加水溶解并定容制成每 1 mL 中含阿莫西林约为0.28 mg 的溶液,作为稳定性试验溶液。于室温放置,间隔 8 h 精密量取 20 μL,注入液相色谱仪,记录各供试液中主成分的峰面积,结果见表8。结果表明,供试液在 8 h 内的稳定性良好。

Table 8 Room temperature stability of the test products dissolved in water表8 溶出测定供试品在水中的室温稳定性结果
3 样品测定
分别取三批样品,按照以上确定的溶出曲线检验方法进行检测,结果见表9。
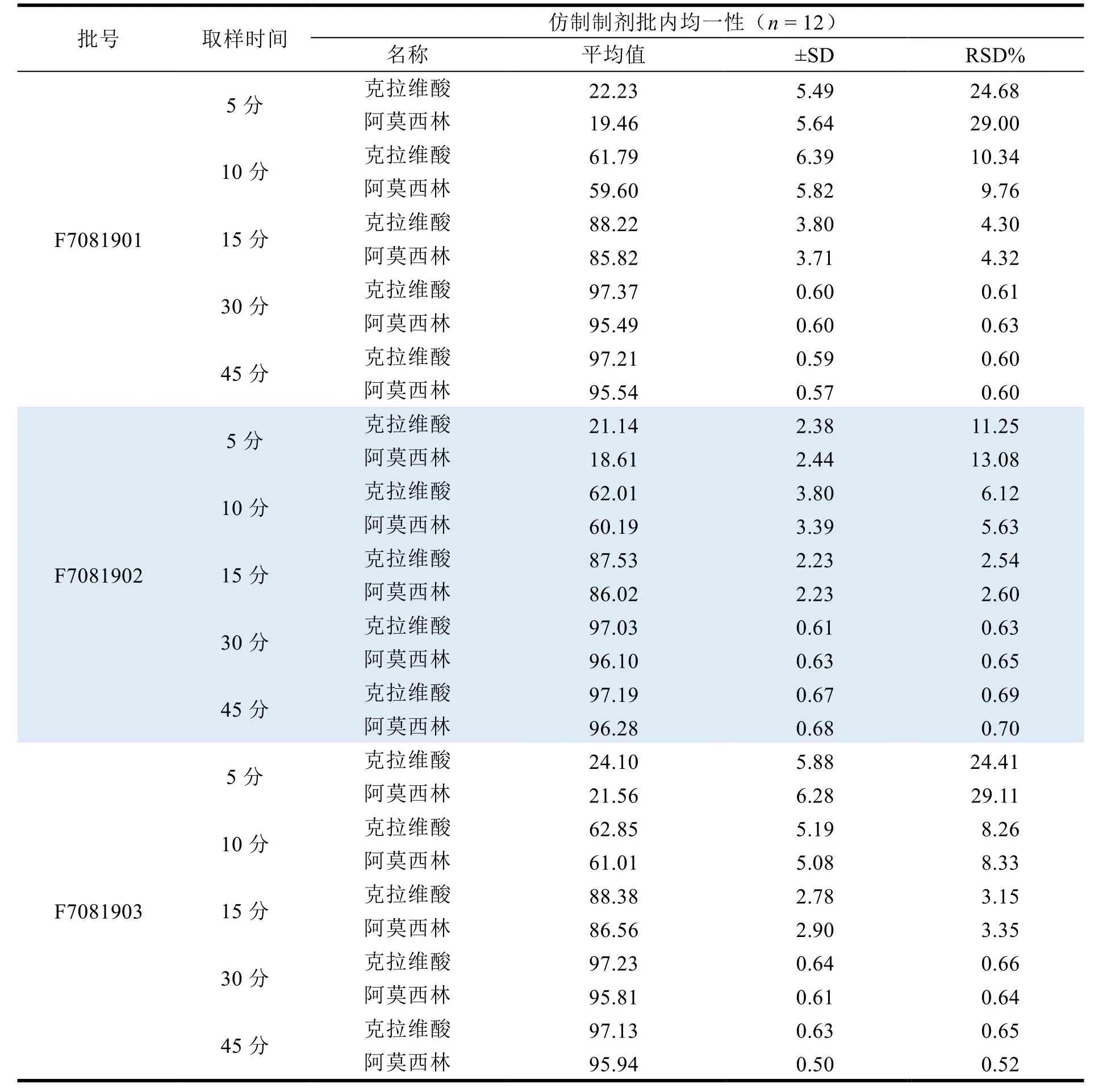
Table 9 Results of the dissolution curve investigation of self-made preparations表9 自制制剂溶出曲线考察结果
4 结语
本文建立了一种阿莫西林克拉维酸钾片水中溶出曲线的测定方法。该方法采用自动溶出仪桨法使片剂崩解溶出,在 5、10、15、30、45 min 时,使用自动取样仪取样,并经取样仪滤芯和一次性滤膜过滤后,使用高效液相色谱仪检测。我们对该方法进行了专属性、准确度、精密度等项目验证,结果符合要求,能够满足仿制药研发过程中处方筛选的需要。
