天津市抗骨质疏松治疗与药物相关性颌骨坏死问题的专家共识
2023-11-08
天津市医学会骨质疏松和骨矿盐疾病分会,天津市口腔医学会口腔颌面外科专业委员会
摘要:骨质疏松症(OP)和口腔疾患是老年人常见的健康问题,近年来OP治疗药物相关的颌骨坏死风险日益受到相关专业医生的关注。在OP治疗前和治疗中为避免或减少药物相关性颌骨坏死的发生,需要妥善处理口腔有创性操作与OP治疗间的关系。由天津市医学会骨质疏松和骨矿盐疾病分会、天津市口腔医学会口腔颌面外科专业委员会主持,经过从事OP治疗的医生和口腔专业医生的充分交流和沟通,在循证医学基础上达成临床共识,即明确了OP和OP治疗药物相关性颌骨坏死均是具有严重不良后果的疾病,规范OP治疗可减少骨折,有利于改善老年人生活质量;在治疗期间应采取恰当措施,尽可能避免OP治疗药物相关性颌骨坏死的发生。通过两个学科医生的共同努力,以期解决由于使用OP治疗药物而影响口腔操作的临床难题,促进和保障老年人的骨骼健康和牙齿健康。
关键词:骨质疏松;口腔手术操作;颌疾病;共识
中图分类号:R589.5,R782.1 文献标志码:A DOI:10.11958/20230147
Expert consensus on anti-osteoporosis therapy and medication-related jaw necrosis in Tianjin
Osteoporosis and Bone Mineral Disease Branch of Tianjin Medical Association;
Society of Oral and Maxillofacial Surgery of Tianjin Stomatological Association
Abstract: Osteoporosis (OP) and oral diseases are common health problems of the elderly. Recently, the risk of jaw necrosis with anti-OP medication has been increasingly concerned by relevant specialists. In order to avoid or reduce the incidence of medication-related jaw necrosis before and during OP treatment, it is necessary to properly deal with the relationship between oral invasive procedures and anti-OP treatment. It is conducted by the Osteoporosis and Bone Mineral Salt Disease Branch of Tianjin Medical Association and Society of Oral and Maxillofacial Surgery of Tianjin Stomatological Association. After full exchange and communication between doctors engaged in OP treatment and stomatological doctors, clinical consensus are reached on the basis of evidence-based medicine. It is clear that OP and OP medication-related necrosis of jaw are both diseases with serious adverse consequences, and standard OP treatment can reduce fractures and improve the quality of life of elderly. During the treatment period, appropriate measures should be taken to avoid the occurrence of OP medication-related jaw necrosis. Through the joint efforts of doctors from the two disciplines, we hope to solve clinical problems that affect oral operation due to the use of OP therapeutic drugs, and promote and protect the bone health and dental health of elderly.
Key words: osteoporosis; oral surgical procedures; jaw disease; consensus
中國已经进入老龄化社会,截至2021年底中国65岁以上老人已经占到全国总人口的14.20%[1]。天津市60岁以上人口比例达21.66%,65岁以上达14.75%,高于全国平均水平[2]。骨质疏松症(osteoporosis,OP)患病人数也随着老龄化而增加。据2018年进行的全国OP流行病学调查显示,中国65岁以上人口OP患病率为32.0%[3]。OP和牙齿疾患人群数量日益增加。更大剂量治疗OP的抗骨吸收药物也可用来治疗肿瘤骨转移,由于后者更容易造成颌骨坏死,临床上容易混淆两种情况的发生风险。当口腔医生接诊应用过此类药物,又需要进行口腔有创性操作的骨质疏松患者时往往有所顾虑,影响了这些患者口腔疾病的治疗。同时,因为口腔医生的顾虑,也影响了患者对于OP的治疗。
目前国内尚无相应的规范性指导文件。鉴于此,天津市医学会骨质疏松和骨矿盐疾病分会联合天津市口腔医学会口腔颌面外科专业委员会的部分专家,在检索、阅读相应专业文献的基础上,通过沟通和讨论达成了部分共识,旨在解决口腔医生为接受过OP治疗药物的患者进行诊疗时遇到的困扰,也为从事OP诊疗的医生尽可能降低此类患者颌骨坏死风险提供指引。鉴于两个专业领域各自的特殊性,本共识仅涉及双方共同关心且有交集的内容。也鉴于药物相关性颌骨坏死缺乏前瞻性的高级别临床证据支持,本共识不对推荐意见证据进行分级。
1 OP的诊疗亟待加强
OP是老年常见的、以骨强度下降为主要表现的骨骼疾病,主要表现在容易发生骨折,其发生率和经济负担远高于冠心病和肿瘤[4]。椎体骨折会出现明显的背部疼痛,严重影响患者生活质量;髋部骨折患者的生理功能明显减退,独立生活能力下降。这些情况不但影响患者的心理健康,更是导致老年人伤残和死亡的重要原因。
OP是一种随着年龄增长、骨骼不断衰老且有严重危害的疾病,长期化是OP治疗的必然要求。但目前OP的诊疗情况非常不乐观,如上海普陀区OP的治疗率仅为2.92%[5],北京91%的社區卫生服务医生很少或从未接诊过OP患者[6]。因此,包括口腔专业在内的所有临床医生都需要高度重视OP的诊疗。
2 药物是导致颌骨坏死的原因之一
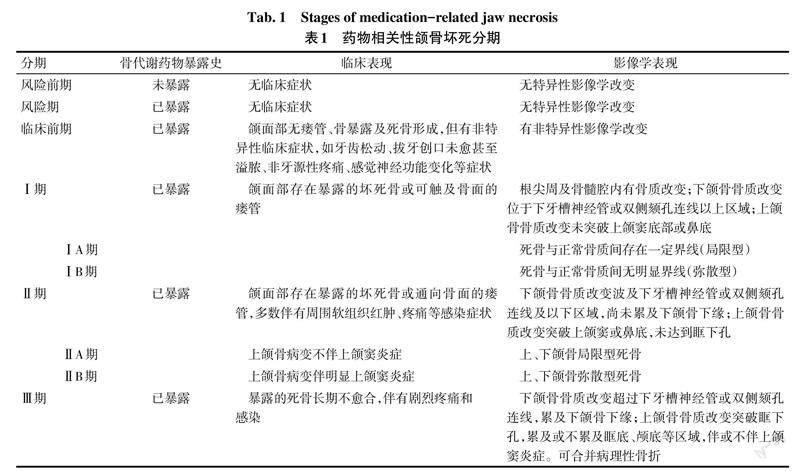
颌骨坏死是指由于颌骨及周边组织循环障碍引起的颌骨部位骨质缺血、缺氧,从而引起骨质硬化、坏死等一系列表现的颌骨疾病,颌骨坏死的分期见表1。
颌骨坏死往往与颌骨骨髓炎互为因果。病灶牙、创伤或有创性操作破坏了颌骨的完整性,使骨暴露,导致局部感染并向邻近骨组织侵袭,产生颌骨骨髓炎。骨坏死既可能是细菌感染引起的骨髓炎的进展,也可能是与放射治疗或药物相关的骨髓炎发病的前驱表现。颌骨坏死主要表现为患区肿胀,病变所累及的牙齿疼痛、松动和脱落,皮肤或口腔黏膜窦道形成,颌骨暴露等,严重影响患者的生活质量。骨髓炎累及的颌骨解剖部位不同,会产生相应的功能障碍,如张口困难、吞咽困难、口鼻腔瘘、病理性骨折等。
颌骨坏死是一个多因素疾病,其中药物导致的称为药物相关性颌骨坏死,抑制骨吸收的药物或肿瘤治疗药物均可导致颌骨坏死的发生。OP治疗药物相关性颌骨坏死多在合并其他因素时才会发生,如患者发病前往往伴有拔牙、牙周治疗等微小创伤或刺激,或存在感染性牙齿疾病,使用糖皮质激素,吸烟及高龄等其他因素。因此,重视药物相关性颌骨坏死有利于指导OP患者的治疗。
3 双膦酸盐类药物和地舒单抗是治疗OP的常用药物
目前OP治疗策略包括抑制骨吸收和促进骨形成2种治疗方法。抑制骨吸收治疗药物有双膦酸盐类药物、地舒单抗、雌激素/雌激素受体调节剂、降钙素类等;促进骨形成药物有特立帕肽(teriparatide)、阿巴洛肽(abaloparatide)和罗莫佐单抗(romosozumab)。这些药物均可有效减少OP所致骨折。相对而言,临床上更常用抑制骨吸收药物。
双膦酸盐类药物可以抑制破骨细胞活性,减少骨丢失,提高骨量以降低骨折风险。其包括静脉和口服2种给药方式,静脉应用的有唑来膦酸、伊班膦酸,口服的有阿仑膦酸钠、利塞膦酸钠、氯屈膦酸等。这类药物均能有效改善骨密度,减少骨质疏松骨折的发生[7-8],长期使用仍能获益[9]。
地舒单抗是核因子κB受体激活物配体(receptor activator for nuclear factor-κB ligand,RANKL)的人源化单克隆抗体,与RANKL有高亲和力,可抑制破骨细胞形成和活化。Freedom 3年临床研究[10]及10年的延伸研究[11]显示长期治疗可改善骨密度,降低各关键部位骨折的发生率,持续获益。
雌激素能够刺激产生骨保护素(OPG),阻断RANKL通路,减少破骨细胞前体向成熟破骨细胞的转化,抑制破骨细胞的骨吸收功能,减少骨质疏松骨折的发生。雌激素受体调节剂通过与雌激素受体结合,可发挥雌激素抗OP的作用。目前仅推荐绝经2年后女性使用此类药物。
降钙素通过与破骨细胞上的降钙素受体结合抑制刷状缘形成,减少骨吸收。目前仅用于骨折后急性骨丢失的预防,不推荐长期用降钙素来预防骨折。
特立帕肽是目前国内唯一使用的促骨形成药。使用该药24个月后能增加椎体骨密度[12-13],降低椎体骨折风险[14],特别适用于有多次骨折史的极高危骨折风险患者[15]。美国FDA已经取消了特立帕肽2年的使用限制。目前研究推荐在使用促骨形成药后,序贯抗骨吸收药物以维持获得的骨密度[16-17],常推荐的序贯用药为双膦酸盐类药物或地舒单抗。
综上,规范的OP治疗能够确切减少骨折事件而使患者获益,双膦酸盐类药物和地舒单抗作为目前常用的OP治疗药物,尚不能被其他药物完全取代。
4 客观评价抗骨吸收药物
双膦酸盐类药物相关性颌骨坏死的病例自2003年Marx[18]首次报道后逐渐增多。随着地舒单抗的广泛和长期应用,也有此类药物相关性颌骨坏死的报道。这2种药物在治疗肿瘤骨转移患者中出现颌骨坏死的发生率要远远高于接受抗OP治疗人群[19-20]。在使用双膦酸盐类药物的肿瘤人群中,颌骨坏死发生率为1%~12%[21];但在OP人群中,口服双膦酸盐相关颌骨坏死发生率为0.01%~0.04%[22-24],甚至低于0.001%[22,25-26]。中国国家药品不良反应监测系统2004年1月1日—2021年6月30日收到的唑来膦酸致颌骨坏死不良反应共73例,其中94.73%为肿瘤患者,5.27%为OP患者[27]。双膦酸盐类药物相关性颌骨坏死的发病机制可能与其抑制破骨细胞并诱导其凋亡的作用有关[28]。此外,双膦酸盐类药物还可抑制内皮细胞增殖[29],破坏血管生成能力,影响骨的血流与正常循环,最终因血循环不足而出现骨坏死[30]。
地舒单抗相关颌骨坏死的报道相对于双膦酸盐类药物数量较少。在Freedom的10年研究中累计有13例颌骨坏死病例,校正后每年每10 000例受试者中有5.2例发病。回顾性和前瞻性数据均显示超过90%的颌骨坏死病例发生在接受高剂量地舒单抗治疗的肿瘤患者中[31-32],并且发病率随用药时间延长而增加[33-34]。地舒单抗相关颌骨坏死的病理生理机制尚未明确。可能与抑制破骨细胞分化和功能,增加凋亡,从而减少骨吸收和骨重塑相关[35]。
双膦酸盐类药物和地舒单抗的使用确实与颌骨坏死事件相关,这两类药物相关性颌骨坏死的风险与过强的骨吸收抑制有关。由于肿瘤人群应用该两种药物剂量要远大于治疗OP所使用剂量,因此不能把抗OP治疗中颌骨坏死的风险与肿瘤治疗等同。OP治疗药物常规剂量造成的颌骨坏死仅略高于未应用药物者(0.001%~0.01%和<0.001%)[36]。
其他种类抗骨吸收药物导致的颌骨坏死事件报道相对较少。目前未发现促进骨形成药物导致颌骨坏死的报道,但有文献显示,特立帕肽可治疗药物相关性颌骨坏死[37]。
有研究表明,每治疗百例就能减少1例OP性骨折的发生[8-9],而治疗万例才可能出现1例药物相关性颌骨坏死[19-20,28]。OP骨折和颌骨坏死均为有严重后果的疾病,虽然发生率可能不同,但应当对两类疾病给予同样的重视。
本共识针对的是为治疗OP而使用相关药物造成的颌骨坏死。因此,首先客观认识肿瘤患者使用双膦酸盐类药物和地舒单抗所造成的颌骨坏死风险远高于OP人群;其次,抗OP治疗药物导致的颌骨坏死人数明显低于因用药而使骨折减少的人数,但不能因此忽视此类药物相关的颌骨坏死风险。
5 降低颌骨坏死风险的临床措施
5.1 医生在启动OP药物治疗前应通过问卷筛查出高危人群以利于口腔专业医生对患者的评估和治疗 目前尚无可靠预测OP治疗药物相关性颌骨坏死发生的方法。抑制骨吸收药通常会导致骨转换水平的降低,骨吸收的过度抑制可能与颌骨坏死的发生有关。肿瘤患者使用静脉双膦酸盐的剂量明显大于OP的治疗剂量,其颌骨坏死风险也高于OP治療人群[38]。但目前研究表明Ⅰ型胶原交联C端肽(CTX)等骨吸收指标无法预测颌骨坏死发生风险[35]。虽然过低的骨转换水平可能是相对的高危险因素,然而更多骨转换水平较低的人群并未发生颌骨坏死。
目前避免OP治疗时药物相关性颌骨坏死发生的方式就是有效预防。治疗OP的医生和患者都应当重视长期使用抗骨吸收药有发生颌骨坏死的风险。目前证据表明口腔感染和有创操作是该病的重要诱因,因此避免疾病发展到需要拔牙或其他口腔有创性操作的地步,对于减少颌骨坏死有益。在启动OP药物治疗前和治疗中定期评估口腔健康状况,保持良好的口腔卫生习惯,定期进行口腔检查和护理,及时有效治疗口腔疾患有助于降低颌骨坏死风险。推荐从事骨质疏松专业的医生采用问卷对患者口腔健康问题进行评估。本问卷参考了Diel等[38]的研究,为方便临床应用,本共识专家组进行了简化。
颌骨的影像学检查包括牙齿根尖X线片、曲面体层X线片、CT、MRI等,能够早于临床症状发现牙根周或病灶周硬化骨板的存在,虽然无法预测其必然发展为颌骨坏死,但存在颌骨坏死风险的患者通过定期检查并监测疾病进展具有一定的临床意义。
应用含氮双膦酸盐、地舒单抗等抗OP药物治疗的患者如需拔牙,建议采用最小创伤的技术,避免拔牙后比较大的陷窝,拔牙创面应严密关闭,避免拔牙窝空虚或骨嵴暴露。合理应用抗菌药物,包括预防性或治疗性全身和局部应用,以避免细菌感染[39]。
因此,在患者接受抗OP治疗过程中,医生应该对患者进行口腔健康状况调查,并提示患者注意口腔保健,定期口腔检查,及时处理口腔问题。
5.2 盲目停用抗骨质疏松药物可能增加患者骨折风险 尽管为了预防药物相关性颌骨坏死,在计划实施口腔有创性操作前停止相关药物似乎是合理的选择,但目前尚无证据显示这样做会更有益。日本一项研究表明,进行口腔有创性操作前停止使用双膦酸盐并未能预防颌骨坏死的发生[40]。即便已经发生颌骨坏死,也没有证据表明停用双膦酸盐类药物较持续用药更能改善颌骨坏死者的结局[41]。相反,较长时间的停药可能造成骨密度的下降及骨折风险的增加。
含氮双膦酸盐类药物摄入后会与骨骼持久牢固结合,短期内停用未必能达到清除体内药物或使其作用明显下降的目的。不恰当地停用双膦酸盐类药物可能对OP治疗不利[9,42]。
地舒单抗作用时间比双膦酸盐类药物短,但停止治疗是否能降低药物相关性颌骨坏死风险尚无证据。皮下注射地舒单抗60 mg后,骨吸收在5 d内下降80%,然后在4~6个月时恢复到注射前水平[43]。Freedom研究中1 001例停用地舒单抗的受试者停药后椎体骨折年发生率从1.2%增加到7.1%,接近安慰剂组的8.5%,停用地舒单抗的患者中多发性椎体骨折发生率高于安慰剂组[44]。其他研究也表明地舒单抗停药后椎体骨折发生风险增加[45-46]。
鉴于进行口腔有创性操作时停用抗OP药物对降低术后颌骨坏死风险的作用尚无理论依据和临床证据,因此不可盲目停药,避免可能增加的骨折风险。
5.3 合理把握抗OP治疗时口腔有创性操作的时机 由于OP治疗药物需要较长时间应用才能达到维持骨密度、减少骨折的目的,因此对于准备进行OP治疗的患者,首先完成必要的口腔有创性治疗再启动OP治疗。对于已经接受了OP治疗、准备进行口腔有创性操作的患者,如何选择合适的治疗时机目前鲜见相关研究,但根据药物特性和患者的骨折风险分层,是一个可以考虑的策略。
有研究表明,无论是口服还是静脉应用双膦酸盐或是地舒单抗,何时使用都不影响骨折的愈合[47-49]。口服双膦酸盐类药物相关性颌骨坏死很少在3年内发生[50],静脉应用双膦酸盐药物相关性颌骨坏死也在治疗10~38个月才会发生[51]。
因此,对于正在接受双膦酸盐类药物治疗的OP人群,如果治疗时间不足1年,发生颌骨坏死的风险非常低;如果不足3年,进行口腔有创性操作发生颌骨坏死的风险会很低,目前较少见颌骨坏死事件报道;超过3年尚无推荐的窗口期进行口腔有创性操作,如果停止治疗,建议不超过6个月。
对于接受地舒单抗治疗的患者,可将其注射3个月后视作一个窗口期,已经进行口腔有创性操作的患者可以接受推迟1个月注射。
总之,不能因为接受OP药物治疗而延迟进行口腔有创性操作,延迟操作可能延误患者的病情,由此带来的后果可能更严重。
6 药物相关性颌骨坏死的预后
大范围的颌骨坏死对患者的生理功能、容貌、心理影响很大,是一个后果严重的疾病。范围小且局限者经过恰当的处理,大部分能够获得较好的预后。OP患者采用地舒单抗治疗10年,其颌骨坏死发生率为0.052%,经过恰当的处理可全部治愈[52]。双膦酸盐类药物相关性颌骨坏死采用包括手术、换药、口服或静脉给予抗生素、臭氧治疗等,治愈率在80%以上[53]。笔者在Pubmed检索到523篇关于OP治疗药物相关性颌骨坏死者391例,其中83.63%(327/391)治愈,8.44%(33/391)好转,7.93%(31/391)在报道时仍然未愈。
因此,相对小范围的颌骨坏死病变通过恰当的处理,大部分能够得到有效的控制。
7 结语
骨骼健康和牙齿健康是老年生活的必然需求,OP和药物相关性颌骨坏死的危害均是客观存在的,忽视其中任何一个风险都不利于老年人的健康。因此,口腔专业医生应当重视OP的危害,在妥善处理口腔疾患的同时,尽力支持OP的规范化诊疗;OP专业医生也应当重视药物相关性颌骨坏死的危害,在治疗OP的过程中,做好药物相关性颌骨坏死的预防工作,使有高危风险的患者得到专业的诊疗,以促进老年人的口腔健康。总之,保障老年人骨骼健康和口腔健康需要两个专业医生的共同努力和团结合作,这是两个专业医生的共同责任。
口腔健康状况调查问卷①
1 您是否存在刷牙出血,牙龈肿胀、萎缩、破溃、化脓?
2 您的牙齿是否有松动或疼痛?
3 您是否有未经治疗的龋齿?
4 您是否有智齒或阻生齿?
5 您的牙齿是否经过口腔科治疗但仍感到不适?
6 您口腔内固定修复体(种植牙、烤瓷冠、全瓷冠等)周围牙龈是否有红肿或疼痛?
7 您的活动义齿(全口或局部)是否存在佩戴不适?
以上7个问题,只要有一个回答是“是”,则推荐到口腔科医生处就诊
① 本问卷参考了Diel等[38]的研究,为方便临床应用,本共识专家组进行了简化。
编写工作组组长
刘浩 天津市口腔医院
晁爱军 天津市天津医院
执笔人
晁爱军 天津市天津医院
杨立 天津市口腔医院
马贲 天津市天津医院
秘书
叶静 天津市天津医院
孙晓曦 天津市天津医院
参与本共识撰写的单位及人员(排名不分先后)
天津市第一中心医院(龚宝琪)
天津市口腔医院(吕东升,王家盛,向旭,杨立,严颖彬,张军)
天津市天津医院(程静,崔秀丽,房德敏,冯鑫,尼娜,孙晓曦,王淑丽,叶静)
参与本共识制定的审议专家(排名不分先后)
北京大学口腔医院(安金刚,贺洋)
中南大学湘雅二医院(盛志峰)
山西医科大学第二医院(朱亦堃)
上海交通大学附属第六人民医院(岳华,章振林)
上海复旦大学附属华东医院(程群)
上海交通大学附属第九人民医院(杨雯君)
首都医科大学附属北京友谊医院(常世民)
四川大学华西口腔医院(华成舸)
天津市宝坻医院(高丽荣)
天津市第五中心医院(王志兴)
天津市南开医院(闫卉)
天津市中心妇产科医院(徐玲)
天津医科大学口腔医院(陈刚)
天津医科大学朱宪彝纪念医院(单春艳)
天津医科大学第二医院(彭诚,杨丽敏)
天津医科大学总医院(戴晨琳,贾红蔚,张剑明,朱梅)
西安市红会医院(曾玉红)
致谢:感谢天津市口腔医院病理科陈瑞扬教授和天津市天津医院病理科王瑞林教授在本共识撰写过程中给予的帮助!
参考文献
[1] 国家统计局.国家数据.年度数据[EB/OL]. (2021)[2022-10-02]. https://data.stats.gov.cn/easyquery.htm?cn=C01&zb=A0301&sj=2021. National Bureau of Statistics. National data. Annual data. [EB/OL]. (2021)[2022-10-02]. https://data.stats.gov.cn/easyquery.htm?cn=C01&zb=A0301&sj=2021.
[2] 天津市统计局. 天津市2020第七次全国人口普查主要数据公报(第2号)[EB/OL].(2021)[2022-10-02]. https://stats.tj.gov.cn/tjsj_52032/tjgb/202105/t20210521_5457330.html. Tianjin Bureau of Statistics. Major Data Bulletin of the Seventh National Census of Tianjin 2020 (No. 2) [EB/OL]. (2021)[2022-10-02]. https://stats.tj.gov.cn/tjsj_52032/tjgb/202105/t20210521_5457330.html.
[3] 中國疾病预防控制中心. 国家卫生健康委发布中国骨质疏松症流行病学调查结果[EB/OL].(2020-09-20)[2022-10-02]. https://ncncd.chinacdc.cn/xwz/gzdt_11943/202009/t20200920_220365.htm. Chinese Center for Disease Control and Prevention. The National Health Commission has released the results of an epidemiological survey on osteoporosis in China[EB/OL]. (2020-09-20)[2022-10-02]. https://ncncd.chinacdc.cn/xwz/gzdt_11943/202009/t20200920_220365.htm.
[4] ZHANF C,FENG J,WANG S,et al. Incidence of and trends in hip fracture among adults in urban China:A nationwide retrospective cohort study[J]. PLoS Med,2020,17(8):e1003180. doi:10.1371/journal.pmed.1003180.
[5] 刘培培,温宇华,张丽亚,等. 上海市普陀区中老年人群骨质疏松患病率和治疗现状横断面研究[J]. 同济大学学报(医学版),2021,42(1):35-41. LIU P P,WEN Y H,ZHANG L Y,et al. Cross-sectional study on prevalence and treatment of osteoporosis among middle-aged and elderly people in Putuo District of Shanghai[J]. Journal of Tongji University (Medical Science),2021,42(1):35-41. doi:10.12289/j.issn.1008-0392.20439.
[6] 孙艳格,杜雪平,高明,等. 北京市社区骨质疏松症诊治状况调查[J]. 中国骨质疏松杂志,2013,19(5):522-524,518. SUN Y G,DU X P,GAO M,et al. Survey of the status of diagnosis and treatment of osteoporosis in the communities in Beijing[J]. Chin J Osteoporos,2013,19(5):522-524,518. doi:10.3969/j.issn.1006-7108.2013.05.022.
[7] POLS H A,FELSENBERG D,HANLEY D A,et al. Multinational,placebo-controlled,randomized trial of the effects of alendronate on bone density and fracture risk in postmenopausal women with low bone mass:results of the FOSIT study. Fosamax International Trial Study Group[J]. Osteoporos Int,1999,9(5):461-468. doi:10.1007/pl00004171.
[8] JACQUES R M,BOONEN S,COSMAN F,et al. Relationship of changes in total hip bone mineral density to vertebral and nonvertebral fracture risk in women with postmenopausal osteoporosis treated with once-yearly zoledronic acid 5 mg:the HORIZON-Pivotal Fracture Trial (PFT)[J]. J Bone Miner Res,2012,27(8):1627-1634. doi:10.1002/jbmr.1644.
[9] BLACK D M,REID I R,BOONEN S,et al. The effect of 3 versus 6 years of zoledronic acid treatment of osteoporosis:a randomized extension to the HORIZON-Pivotal Fracture Trial (PFT)[J]. J Bone Miner Res,2012,27(2):243-254. doi:10.1002/jbmr.1494.
[10] CUMMINGS S R,SAN MARTIN J,MCCLUNG M R,et al. Denosumab for prevention of fractures in postmenopausal women with osteoporosis[J]. N Engl J Med,2009,361(8):756-765. doi:10.1056/NEJMoa0809493.
[11] BONE H G,WAGMAN R B,BRANDI M L,et al. 10 years of denosumab treatment in postmenopausal women with osteoporosis: results from the phase 3 randomised FREEDOM trial and open-label extension[J]. Lancet Diabetes Endocrinol,2017,5(7):513-523. doi:10.1016/s2213-8587(17)30138-9.
[12] MIYAUCHI A,MATSUMOTO T,SUGIMOTO T,et al. Effects of teriparatide on bone mineral density and bone turnover markers in Japanese subjects with osteoporosis at high risk of fracture in a 24-month clinical study:12-month,randomized,placebo-controlled,double-blind and 12-month open-label phases[J]. Bone,2010,47(3):493-502. doi:10.1016/j.bone.2010.05.022.
[13] OBERMAYER-PIETSCH B M,MARIN F,MCCLOSKEY E V,et al. Effects of two years of daily teriparatide treatment on BMD in postmenopausal women with severe osteoporosis with and without prior antiresorptive treatment[J]. J Bone Miner Res,2008,23(10):1591-1600. doi:10.1359/jbmr.080506.
[14] NEER R M,ARNAUD C D,ZANCHETTA J R,et al. Effect of parathyroid hormone (1-34) on fractures and bone mineral density in postmenopausal women with osteoporosis[J]. N Engl J Med,2001,344(19):1434-1441. doi:10.1056/nejm200105103441904.
[15] PREVRHAL S,KREGE J H,CHEN P,et al. Teriparatide vertebral fracture risk reduction determined by quantitative and qualitative radiographic assessment[J]. Curr Med Res Opin,2009,25(4):921-928. doi:10.1185/03007990902790993.
[16] LEDER B Z,TSAI J N,UIHLEIN A V,et al. Denosumab and teriparatide transitions in postmenopausal osteoporosis (the DATA-Switch study):extension of a randomised controlled trial[J]. Lancet,2015,386(9999):1147-1155. doi:10.1016/s0140-6736(15)61120-5.
[17] OHTORI S,ORITA S,YAMAUCHI K,et al. Does discontinuing teriparatide treatment and replacing it with bisphosphonate maintain the volume of the bone fusion mass after lumbar posterolateral fusion in women with postmenopausal osteoporosis? [J]. Asian Spine J,2017,11(2):272-277. doi:10.4184/asj.2017.11.2.272.
[18] MARX R E. Pamidronate (Aredia) and zoledronate (Zometa) induced avascular necrosis of the jaws: a growing epidemic[J]. J Oral Maxillofac Surg,2003,61(9):1115-1117. doi:10.1016/s0278-2391(03)00720-1.
[19] SAAD F,BROWN J E,VAN POZNAK C,et al. Incidence,risk factors,and outcomes of osteonecrosis of the jaw:integrated analysis from three blinded active-controlled phase Ⅲ trials in cancer patients with bone metastases[J]. Ann Oncol,2012,23(5):1341-1347. doi:10.1093/annonc/mdr435.
[20] LIPTON A,FIZAZI K,STOPECK A T,et al. Superiority of denosumab to zoledronic acid for prevention of skeletal-related events:a combined analysis of 3 pivotal,randomised,phase 3 trials[J]. Eur J Cancer,2012,48(16):3082-3092. doi:10.1016/j.ejca.2012.08.002.
[21] JADU F,LEE L,PHAROAH M,et al. A retrospective study assessing the incidence,risk factors and comorbidities of pamidronate-related necrosis of the jaws in multiple myeloma patients[J]. Ann Oncol,2007,18(12):2015-2019. doi:10.1093/annonc/mdm370.
[22] MAVROKOKKI T,CHENG A,STEIN B,et al. Nature and frequency of bisphosphonate-associated osteonecrosis of the jaws in Australia[J]. J Oral Maxillofac Surg,2007,65(3):415-423. doi:10.1016/j.joms.2006.10.061.
[23] SEDGHIZADEH P P,STANLEY K,CALIGIURI M,et al. Oral bisphosphonate use and the prevalence of osteonecrosis of the jaw:an institutional inquiry[J]. J Am Dent Assoc,2009,140(1):61-66. doi:10.14219/jada.archive.2009.0019.
[24] LO J C,O'RYAN F S,GORDON N P,et al. Prevalence of osteonecrosis of the jaw in patients with oral bisphosphonate exposure[J]. J Oral Maxillofac Surg,2010,68(2):243-253. doi:10.1016/j.joms.2009.03.050.
[25] LIN T C,YANG C Y,KAO YANG Y H,et al. Incidence and risk of osteonecrosis of the jaw among the Taiwan osteoporosis population[J]. Osteoporos Int,2014,25(5):1503-1511. doi:10.1007/s00198-014-2624-6.
[26] GRBIC J T,BLACK D M,LYLES K W,et al. The incidence of osteonecrosis of the jaw in patients receiving 5 milligrams of zoledronic acid:data from the health outcomes and reduced incidence with zoledronic acid once yearly clinical trials program[J]. J Am Dent Assoc,2010,J Am Dent Assoc,2010,141(11):1365-1370. doi:10.14219/jada.archive.2010.0082.
[27] 熊瑋仪,任经天. 全国唑来膦酸致颌骨骨坏死不良反应监测数据分析[J]. 中国药物警戒,2022,19(6):641-644,653. XIONG W Y,REN J T. Survey of the status of diagnosis and treatment of osteoporosis in the communities in Beijing analysis of national monitoring data of adverse drug reactions related to zoledronic acidrelated osteonecrosis of the jaw[J]. Chinese Journal of Pharmacovigilance,2022,19(6):641-644,653. doi:10.19803/j.1672-8629.2022.06.12.
[28] ROGERS M J,GORDON S,BENFORD H L,et al. Cellular and molecular mechanisms of action of bisphosphonates[J]. Cancer,2000,88(12 Suppl):2961-2978. doi:10.1002/1097-0142(20000615)88:12+<2961::aid-cncr12>3.0.co;2-c.
[29] LANDESBERG R,COZIN M,CREMERS S,et al. Inhibition of oral mucosal cell wound healing by bisphosphonates[J]. J Oral Maxillofac Surg,2008,66(5):839-847. doi:10.1016/j.joms.2008.01.026.
[30] BADROS A,WEIKEL D,SALAMA A,et al. Osteonecrosis of the jaw in multiple myeloma patients:clinical features and risk factors[J]. J Clin Oncol,2006,24(6):945-952. doi:10.1200/jco.2005.04.2465.
[31] RHEE Y,CHANG D G,HA J,et al. Real-world safety and effectiveness of denosumab in patients with osteoporosis:A prospective,observational study in South Korea[J]. Endocrinol Metab (Seoul),2022,37(3):497-505. doi:10.3803/EnM.2022.1427.
[32] BOQUETE-CASTRO A,G?MEZ-MORENO G,CALVO-GUIRADO J L,et al. Denosumab and osteonecrosis of the jaw. A systematic analysis of events reported in clinical trials[J]. Clin Oral Implants Res,2016,27(3):367-375. doi:10.1111/clr.12556.
[33] EGLOFF-JURAS C,GALLOIS A,SALLERON J,et al. Denosumab-related osteonecrosis of the jaw:A retrospective study[J]. J Oral Pathol Med,2018,47(1):66-70. doi:10.1111/jop.12646.
[34] NICOLATOU-GALITIS O,SCHI?DT M,MENDES R A,et al. Medication-related osteonecrosis of the jaw:definition and best practice for prevention,diagnosis,and treatment[J]. Oral Surg Oral Med Oral Pathol Oral Radiol,2019,127(2):117-135. doi:10.1016/j.oooo.2018.09.008.
[35] RUGGIERO S L,DODSON T B,FANTASIA J,et al. American Association of Oral and Maxillofacial Surgeons position paper on medication-related osteonecrosis of the jaw--2014 update[J]. J Oral Maxillofac Surg,2014,72(10):1938-1956. doi:10.1016/j.joms.2014.04.031.
[36] KHAN A,MORRISON A,CHEUNG A,et al. Osteonecrosis of the jaw (ONJ):diagnosis and management in 2015[J]. Osteoporos Int,2016,27(3):853-859. doi:10.1007/s00198-015-3335-3.
[37] SIM I W,BORROMEO G L,TSAO C,et al. Teriparatide promotes bone healing in medication-related osteonecrosis of the jaw:A placebo-controlled,randomized trial[J]. J Clin Oncol,2020,38(26):2971-2980. doi:10.1200/jco.19.02192.
[38] DIEL I J,FOGELMAN I,AL-NAWAS B,et al. Pathophysiology,risk factors and management of bisphosphonate-associated osteonecrosis of the jaw:Is there a diverse relationship of amino-and non-aminobisphosphonates ?[J]. Crit Rev Oncol Hematol,2007,64(3):198-207. doi:10.1016/j.critrevonc.2007.07.005.
[39] FUSCO V,SANTINI D,CAMPISI G,et al. Comment on medication-related osteonecrosis of the jaw:MASCC/ISOO/ASCO clinical practice guideline summary[J]. JCO Oncol Pract,2020,16(3):142-145. doi:10.1200/jop.19.00645.
[40] HASEGAWA T,KAWAKITA A,UEDA N,et al. A multicenter retrospective study of the risk factors associated with medication-related osteonecrosis of the jaw after tooth extraction in patients receiving oral bisphosphonate therapy:can primary wound closure and a drug holiday really prevent MRONJ ?[J]. Osteoporos Int,2017,28(8):2465-2473. doi:10.1007/s00198-017-4063-7.
[41] SIGUA-RODRIGUEZ E A,DA COSTA RIBEIRO R,DE BRITO A C,et al. Bisphosphonate-related osteonecrosis of the jaw:a review of the literature[J]. Int J Dent,2014,2014:192320. doi:10.1155/2014/192320.
[42] BLACK D M,SCHWARTZ A V,ENSRUD K E,et al. Effects of continuing or stopping alendronate after 5 years of treatment:the Fracture Intervention Trial Long-term Extension (FLEX):a randomized trial[J]. JAMA,2006,296(24):2927-2938. doi:10.1001/jama.296.24.2927.
[43] CAMPISI G,MAUCERI R,BERTOLDO F,et al. A pragmatic window of opportunity to minimise the risk of MRONJ development in individuals with osteoporosis on Denosumab therapy:a hypothesis[J]. Head Face Med,2021,17(1):25. doi:10.1186/s13005-021-00280-4.
[44] CUMMINGS S R,FERRARI S,EASTELL R,et al. Vertebral fractures after discontinuation of denosumab:A post hoc analysis of the randomized placebo-controlled FREEDOM trial and its extension[J]. J Bone Miner Res,2018,33(2):190-198. doi:10.1002/jbmr.3337.
[45] BURCKHARDT P,FAOUZI M,BUCLIN T,et al. Fractures after denosumab discontinuation:A retrospective study of 797 cases[J]. J Bone Miner Res,2021,36(9):1717-1728. doi:10.1002/jbmr.4335.
[46] EVERTS-GRABER J,REICHENBACH S,GAHL B,et al. Risk factors for vertebral fractures and bone loss after denosumab discontinuation:A real-world observational study[J]. Bone,2021,144:115830. doi:10.1016/j.bone.2020.115830.
[47] DUCKWORTH A D,MCQUEEN M M,TUCK C E,et al. Effect of alendronic acid on fracture healing:A multicenter randomized placebo-controlled trial[J]. J Bone Miner Res,2019,34(6):1025-1032. doi:10.1002/jbmr.3679.
[48] COL?N-EMERIC C,NORDSLETTEN L,OLSON S,et al. Association between timing of zoledronic acid infusion and hip fracture healing[J]. Osteoporos Int,2011,22(8):2329-2336. doi:10.1007/s00198-010-1473-1.
[49] ADAMI S,LIBANATI C,BOONEN S,et al. Denosumab treatment in postmenopausal women with osteoporosis does not interfere with fracture-healing: results from the FREEDOM trial[J]. J Bone Joint Surg Am,2012,94(23):2113-2119. doi:10.2106/jbjs.k.00774.
[50] LEE L W,HSIAO S H,CHEN L K. Clinical treatment outcomes for 40 patients with bisphosphonates-related osteonecrosis of the jaws[J]. J Formos Med Assoc,2014,113(3):166-172. doi:10.1016/j.jfma.2012.04.010.
[51] MELO M D,OBEID G. Osteonecrosis of the jaws in patients with a history of receiving bisphosphonate therapy:strategies for prevention and early recognition[J]. J Am Dent Assoc,2005,136(12):1675-1681. doi:10.14219/jada.archive.2005.0110.
[52] WATTS N B,GRBIC J T,BINKLEY N,et al. Invasive oral procedures and events in postmenopausal women with osteoporosis treated with denosumab for up to 10 years[J]. J Clin Endocrinol Metab,2019,104(6):2443-2452. doi:10.1210/jc.2018-01965.
[53] RODRIGUEZ-LOZANO F J,O ATE-S NCHEZ R E. Treatment of osteonecrosis of the jaw related to bisphosphonates and other antiresorptive agents[J]. Med Oral Patol Oral Cir Bucal,2016,21(5):e595-600. doi:10.4317/medoral.20980.
(2023-02-10收稿 2023-04-09修回)
(本文編辑 李鹏)
