甲状腺残体的特征及其在甲状腺切除手术中的临床意义
2023-11-04王莹施杲旸徐文秀陆辉蒋军
王莹, 施杲旸, 徐文秀, 陆辉, 蒋军
近年来,甲状腺良恶性肿瘤发病率呈逐渐上升趋势,已成为最常见的内分泌系统肿瘤之一[1]。甲状腺肿瘤最基本、最有效的治疗是外科手术。手术方式多为甲状腺腺叶/全部切除,对于恶性肿瘤,需行同侧中央区淋巴结清扫术。对于伴侧颈区淋巴结转移的甲状腺恶性肿瘤患者,需行侧颈区淋巴结清扫术[2]。手术的彻底性是治疗的基本要素,对降低术后复发率、提高患者生存率起关键作用。在甲状腺手术中,外科医生常于甲状腺下极下方探及一甲状腺组织,这一结构为甲状腺胚胎发育异常所致。在胚胎期,若甲状腺原基在下降过程中出现滞留,可形成甲状腺水平以上的异位腺体,如舌根部甲状腺;若甲状腺原基在下降过程中偏离中线,可形成甲状腺水平的异位腺体,如胸锁乳突肌区甲状腺;若甲状腺原基下降过度,可形成甲状腺水平以下部位的异位腺体,如纵隔内甲状腺[3]。若仅部分甲状腺原基下降过度则于正常甲状腺下极下方形成一甲状腺残体组织[4]。甲状腺残体常表现为与甲状腺相连或远离甲状腺呈孤立状态,其大小、形态也存在较多变异。认识和了解这一结构对保证甲状腺切除的彻底性具有较重要的意义。对于因甲状腺乳头癌行甲状腺切除者,若甲状腺无法彻底切除,将影响术后甲状腺球蛋白的监测。目前与甲状腺残体相关的报道较少。本研究通过甲状腺手术中对残体的探查、解剖,从出现频率、大小、形态、与甲状腺的位置关系等方面进行具体的描述和分析,以提高对甲状腺残体的认识,促进甲状腺切除手术的彻底性。
1 资料与方法
1.1 临床资料
选择2021年11月至2022年10月于南京医科大学第一附属医院甲状腺外科行甲状腺切除手术患者。纳入标准:①超声检查或细针穿刺提示甲状腺恶性肿瘤者;②超声检查提示甲状腺良性肿瘤,但肿瘤直径>4 cm或伴有颈部压迫症状者;③胸骨后甲状腺肿患者。排除标准:①既往有甲状腺或甲状旁腺手术史;②既往有颈部放射性治疗史;③既往曾行甲状腺肿物消融治疗者。最终纳入患者879例,其中男289例(32.9%),女590例(67.1%),年龄21~77岁,平均(45.02±16.92)岁。本研究经南京医科大学第一附属医院伦理委员会批准(批准号:2022-NT-104),获患者知情同意并签署知情同意书。
1.2 术前检查
术前普通超声(My LabTMTwice,Esaote, 意大利)探查甲状腺,记录甲状腺肿物位置、直径、形态;探查甲状腺下极至胸腺区域,若探及与甲状腺等回声结构,无淋巴门结构,则判断其为甲状腺残体,并记录其大小、形态及与甲状腺的位置关系。
1.3 手术方法
若术前甲状腺超声或细针穿刺细胞学检查提示单侧甲状腺肿瘤,切除病灶侧腺叶;若术前甲状腺超声或细针穿刺细胞学检查提示双侧甲状腺肿瘤,行甲状腺全部切除,随即将切除甲状腺组织送至本院病理科行快速冰冻切片病理检查,切取甲状腺内肿瘤,进一步包埋、冷冻切片机(徕卡,德国)内制冷、切片,HE染色后显微镜下检查。若快速冰冻切片病理检查提示结节性甲状腺肿、甲状腺腺瘤或淋巴细胞性甲状腺炎等良性疾病,无需进一步清扫中央区淋巴结。若术中快速冰冻切片病理检查提示甲状腺癌,则根据癌灶所在位置行患侧中央区淋巴结清扫。若术前超声或颈部增强CT提示侧颈区淋巴结转移可能,追加患侧颈部淋巴结清扫。
1.4 观察指标
良性疾病未行中央区淋巴结清扫者,探查甲状腺下方至胸腺上缘区域;行中央区淋巴结清扫者,探查甲状腺下方至胸腺上缘区域及切除中央区脂肪淋巴结组织标本。若探及甲状腺残体,记录其直径、分型:Ⅰ型为甲状腺下极向下突出的残体组织与甲状腺相延续;Ⅱ型为甲状腺残体紧邻甲状腺下极,无任何组织相连;Ⅲ型为甲状腺残体通过细窄的纤维束带与甲状腺相连;Ⅳ型为甲状腺下方独立的甲状腺组织,与甲状腺无任何连接(图1)。若甲状腺残体外观与淋巴结相似,且孤立位于中央区区域内,则行病理学检查以明确。记录甲状腺残体与喉返神经的位置关系:以喉返神经所在平面为界,将甲状腺残体分为喉返神经前残体、喉返神经后残体。
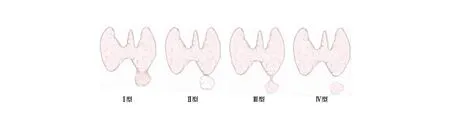
图1 各型甲状腺残体示意图
1.5 统计学方法
2 结果
2.1 患者一般资料、手术方式及术后病理结果
879例入组患者中,252例(28.7%)患者接受单侧腺叶切除,627例(71.3%)患者接受双侧腺叶切除,共涉及1 506例单侧腺叶。术后病理提示良性疾病者142例(16.2%),其中结节性甲状腺肿102例,甲状腺滤泡性腺瘤39例,Graves病1例;恶性疾病者737例(83.8%),其中甲状腺乳头状癌581例,甲状腺乳头状癌伴桥本氏甲状腺炎152例,髓样癌4例。详见表1。
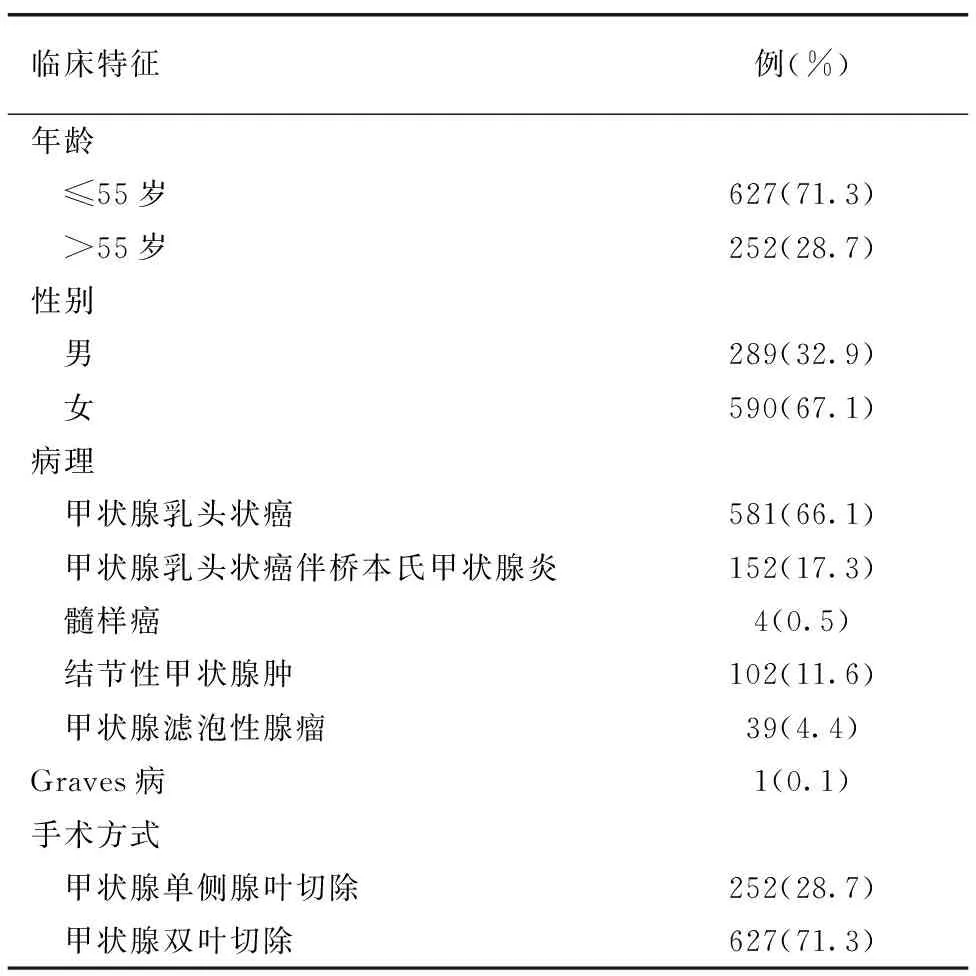
表1 879例患者的一般资料
2.2 甲状腺残体信息
2.2.1 术前超声探及甲状腺残体情况 103例(11.7%)患者术前普通超声探及甲状腺残体,其中探及双侧甲状腺残体38例,探及单侧甲状腺残体65例。超声探及141例甲状腺残体中,Ⅰ型72例(51.1%),直径(0.97±0.37)cm;Ⅳ型69例(48.9%),直径(1.44±0.68)cm;未探及Ⅱ、Ⅲ型甲状腺残体。18例Ⅰ型甲状腺残体术中探查证实为Ⅱ型甲状腺残体;47例Ⅳ型甲状腺残体术中探查证实为Ⅲ型甲状腺残体;另8例Ⅳ型甲状腺残体术中探查未见。结合手术探查情况,仅22.1%(133/602)甲状腺残体可通过术前超声探及。
2.2.2 手术探查甲状腺残体情况 430例(48.9%)患者术中探及甲状腺残体,其中106例患者行单侧甲状腺腺叶切除,324例患者行双侧甲状腺腺叶切除。1 506例腺叶中伴甲状腺残体602例(39.9%),其中Ⅰ型221例(36.7%)、Ⅱ型62例(10.3%)、Ⅲ型255例(42.4%)、Ⅳ型64例(10.6%)。不同病理类型中各型甲状腺残体分布见表2。仅5例甲状腺残体位于喉返神经后方,余甲状腺残体位于喉返神经前方。172例患者探及双侧甲状腺残体(图2),1例患者甲状腺残体内探及乳头状癌(图3)。
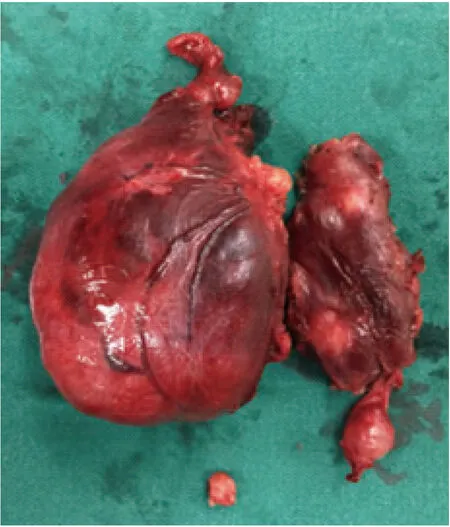
图2 典型病例(女,65岁)甲状腺左叶、右叶同时探及Ⅲ型、Ⅳ型甲状腺残体 手术方式为甲状腺全部切除,病理诊断为结节性甲状腺肿
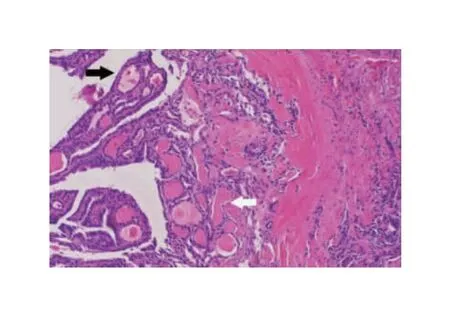
图3 甲状腺残体内探及乳头状癌病理学图像典型病例(女,33岁) 手术方式为甲状腺左侧腺叶切除+左侧中央区淋巴结清扫;病理学检查示:甲状腺残体可同时探及正常甲状腺滤泡结构(白色箭头)和乳头状癌结构(黑色箭头)
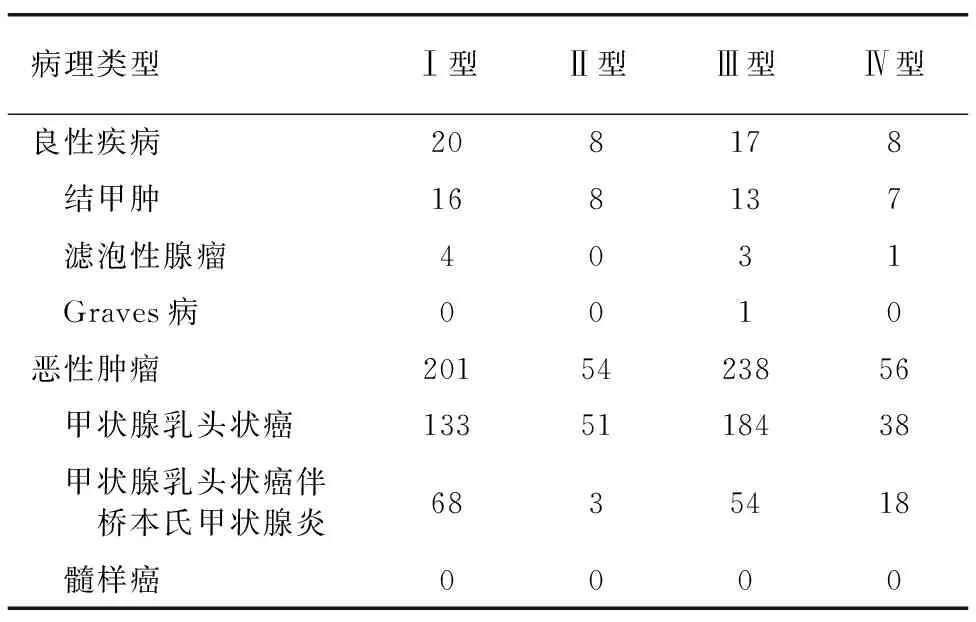
表2 不同病理类型中各型甲状腺残体数目(例)
良性疾病甲状腺残体直径大于恶性疾病(P<0.001)。良性疾病中,Ⅰ型、Ⅱ型、Ⅲ型甲状腺残体直径均大于恶性疾病中相应残体的直径(P<0.05);Ⅳ型甲状腺残体在良恶性甲状腺疾病中差异无统计学意义(P=0.187)。详见表3。
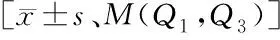
表3 各型甲状腺残体直径及良恶性疾病甲状腺残体直径比较
3 讨论
甲状腺发育起源于内胚层,在胚胎初期,甲状腺原基位于原始咽底正中,后沿中线下降,约在胚胎第7周到达颈部气管前,逐渐发育为成熟甲状腺。若甲状腺原基在下降过程中出现滞留、偏移、过度,均可形成异位甲状腺。根据是否存在正常位置的甲状腺组织,将异位甲状腺分为迷走甲状腺和副甲状腺。迷走甲状腺为正常解剖位置无甲状腺组织,约占异位甲状腺75%[5]。迷走甲状腺多位于颈部及以上区域,如口腔内壁、舌根部等区域,患者多无明显症状,少数因吞咽困难、呼吸困难、反复出血等症状就诊[6]。颈部以下区域的迷走型异位甲状腺较罕见,如纵隔内、腹腔内、盆腔内,一般无症状,少数因相关部位的压迫症状行切除手术意外发现[7]。副甲状腺为正常解剖位置及其他位置均存在甲状腺组织,占异位甲状腺25%[5],约83%的副甲状腺位于颈部以下区域[8]。本研究对象为甲状腺残体,因胚胎发育过程中,大部分甲状腺原基正常下降,仅少量甲状腺原基下降过度至正常甲状腺下极下方[9]。与其他异位甲状腺相比,甲状腺残体的主要表现为正常解剖位置的甲状腺组织下方临近胸腺甲状腺区域内延续性/孤立性甲状腺组织。若手术中未彻底切除甲状腺残体,可导致腺体残留,进而成为复发的潜在因素。在甲状腺乳头状癌患者的术后监测中,遗漏的甲状腺残体可影响甲状腺球蛋白的检测结果。
Sackett等[9]首次报道甲状腺残体,并根据其与甲状腺的关系将甲状腺残体分为4型。其中Ⅰ型为甲状腺残体与甲状腺下极相连;Ⅱ型为甲状腺残体通过细窄的甲状腺组织与甲状腺相连;Ⅲ型为甲状腺残体通过纤维束带与甲状腺相连;Ⅳ型为甲状腺残体与甲状腺分离。本研究根据甲状腺残体的临床意义将甲状腺残体分型进行了调整,传统分型中Ⅱ型甲状腺残体通过细窄甲状腺组织与甲状腺相连,术中此型甲状腺残体在沿甲状腺包膜分离时较容易被识别,该特征与Ⅰ型甲状腺残体相同,因此将传统的Ⅰ、Ⅱ型甲状腺残体均定义为Ⅰ型。此外,部分甲状腺残体与甲状腺紧邻但无任何组织相连,按照传统的分型应被定义为Ⅳ型,但其与远离甲状腺的Ⅳ型甲状腺残体临床意义差别较大,因此被定义为Ⅱ型甲状腺残体。
本研究结果显示,仅22.1%(133/602)甲状腺残体可通过超声探及,可能由于甲状腺残体大多体积较小,且受气管前及气管旁脂肪组织、淋巴结的干扰,超声对甲状腺残体的检查敏感度较低。此外,超声未探及Ⅱ型、Ⅲ型甲状腺残体,可能因Ⅱ型残体紧邻甲状腺组织,超声无法探及其边界,被误认为Ⅰ型甲状腺残体。Ⅲ型甲状腺残体通过一条纤维束带与甲状腺相连,该束带在超声上往往无法探及,被误认为Ⅳ型甲状腺残体。另有8例患者术前超声与甲状腺下方探及孤立状等回声结构,考虑为Ⅳ型甲状腺残体,但手术中未探及任何残体结构,推测超声探及甲状腺残体为甲状旁腺。因此,超声对甲状腺残体的探查敏感度较低,尤其对Ⅱ型、Ⅲ型甲状腺残体;对于Ⅳ型甲状腺残体,超声无法将其与甲状旁腺相鉴别。
根据术中探查及解剖的结果,各型甲状腺残体中,Ⅰ型(36.7%)、Ⅲ型(42.4%)甲状腺残体较为常见。Ⅰ、Ⅱ型甲状腺残体与腺体呈相连状态,术中较容易被探及。Ⅲ型、Ⅳ型甲状腺残体与甲状腺腺体距离较远呈孤立状态,其所占比例为53.0%。
Sackett等[9]研究发现86%的甲状腺残体直径<1 cm;Sheahan等[10]报道约5%的甲状腺残体表现为明显增大。本研究中约75.9%(457/602)甲状腺残体直径<1 cm,与上述研究结果一致。Sadacharan等[11]研究显示,甲状腺残体直径>5 cm者比例约为10.8%,直径<1 cm者占12%;该研究中入组患者约83.6%为结节性甲状腺肿、甲状腺炎、甲状腺腺瘤等良性疾病,此类甲状腺病变多伴有甲状腺及甲状腺残体的肿大。本研究中,良性疾病甲状腺残体直径大于恶性疾病甲状腺残体。伴甲状腺残体的良性疾病中,83%(44/53)病理类型为结节性甲状腺肿。结节性甲状腺肿表现为甲状腺内多发性结节样增生,多伴有甲状腺肿大。与甲状腺相同,甲状腺残体内也伴有多发性结节样增生,使其体积增大。在甲状腺乳头状癌、髓样癌等恶性疾病中,甲状腺残体的平均直径<1 cm。对于直径较小的甲状腺残体的识别需要术中仔细探查,需谨慎使用超声刀和电刀等能量器械且注意动作轻柔,以避免喉返神经及下位甲状旁腺的损伤。
既往研究发现,结节性甲状腺肿行部分腺叶切除术,复发率高于行腺叶全切者[12]。对于甲状腺腺叶切除者,复发多位于原甲状腺下方或胸骨后[13]。Gurleyik等[14]研究纳入3 044例结节性甲状腺肿行甲状腺切除的患者,10例患者在行甲状腺全切除术后出现复发性甲状腺肿需要再次手术,其中1例患者复发病灶位于甲状腺床,9例均位于胸骨后区域,推测为甲状腺残体未彻底切除所致。Cunha等[15]报道1例Graves’病患者甲状腺切除术后7年,再发胸骨后结节性甲状腺肿,考虑与甲状腺残体有关。本研究中结节性甲状腺肿患者中Ⅲ型、Ⅳ型甲状腺残体比例为45.5%(20/44)。若外科医生对甲状腺残体没有充分的认识而将甲状腺残体视为反应性淋巴结并予以保留;或未重视甲状腺下方脂肪组织的探查,则可能遗漏部分甲状腺残体并导致后期局部复发。
本研究中,仅5例甲状腺残体位于喉返神经后方,其中2例为Ⅲ型,3例为Ⅳ型,均与甲状腺分离呈孤立状态。此类甲状腺残体若体积较大,可从后方挤压喉返神经使其位置发生改变,因此,手术时需仔细探查以避免喉返神经损伤。对于甲状旁腺疾病患者,尤其是下位甲状旁腺肿瘤,其外观往往表现为暗红色结节,与甲状腺残体相似。若术中将甲状腺残体误认为甲状旁腺肿瘤而切除,则易导致病灶遗漏。因此除了仔细的探查,还需结合术中冰冻切片病理检查。本研究中1例患者甲状腺残体内伴乳头状癌病灶。Li等[16]报道1例隐匿性甲状腺癌患者表现为中央区转移性病灶而甲状腺内无原发性病灶,推测其起源于甲状腺下方的异位甲状腺组织。本研究中1例患者甲状腺残体内探及乳头状癌病灶,一定程度上佐证了上述推测。
综上所述,甲状腺残体是一种常见的甲状腺形态变异,在人群中具有较高的比例。甲状腺外科医生充分认识该结构对术中彻底切除甲状腺具有重要意义。
