他克莫司对原发性膜性肾病患者B淋巴细胞及T淋巴细胞亚群的影响研究*
2023-10-14罗成建胡俊恒
罗成建 胡俊恒
原发性膜性肾病在临床并不乏见,相关研究显示,本病患者的脂代谢呈现紊乱状态,同时大量蛋白尿及血清白蛋白较低也是其突出表现,因此本类患者治疗过程中,上述方面是评估较多的指标[1-2]。另外,本病还与机体免疫方面有一定关系,因此关于本病免疫方面的研究多见,而B 淋巴细胞及T 淋巴细胞亚群作为临床中研究较多的免疫指标,在本类患者中的调控需求较高,且其表达变化与疾病发展转归密切相关,因此上述免疫指标可作为疗效评估的重要参考方面[3-5]。临床中近年来采用他克莫司治疗原发性膜性肾病的研究不断增多,但是对于患者上述免疫指标的影响研究不足。因此,本研究现探究他克莫司对原发性膜性肾病患者B、T 淋巴细胞亚群的影响,现报道如下。
1 资料与方法
1.1 一般资料
选取2020 年7 月—2021 年12 月清远市人民医院的80 例原发性膜性肾病患者。纳入标准:18~75 岁;于本院诊治的原发性膜性肾病;疾病分期为Ⅰ~Ⅱ期;患者能够积极有效配合。排除标准:合并糖尿病;合并系统性红斑狼疮;合并肝脏疾病;3 个月内发生创伤及手术史;多系统器官功能不全;合并感染;临床资料不完整。将患者根据随机数字表法分为对照组40 例和观察组40 例,所有患者均知情同意本研究并签署知情同意书,研究经本院医学伦理委员会批准。
1.2 方法
对照组采用环磷酰胺联合泼尼松进行治疗。给予注射用环磷酰胺(生产厂家:山西普德药业有限公司,批准文号:国药准字H14023686,规格:0.2 g)静脉滴注,每次0.80 g 加入250 mL 0.9%氯化钠注射液中应用,每月1 次;另给予醋酸泼尼松(生产厂家:天津力生制药股份有限公司,批准文号:国药准字H12020123,规格:5 mg)按照1.00 mg/kg 服用,1 次/d,8 周后开始减量,每2 周减量10%,直至10.00~15.00 mg/d 时,维持应用。观察组则采用他克莫司胶囊(生产厂家:杭州中美华东制药有限公司,批准文号:国药准字H20084514,规格:1 mg)联合泼尼松进行治疗。他克莫司胶囊按照每天0.05~0.10 mg/kg 的剂量服用,2 次/d,于空腹状态下服用,1 周后进行血药浓度监测,维持在5.00~10.00 μg/L,如浓度较低则适当增加药量,但不宜超过每天0.15 mg/kg,本组泼尼松与对照组应用相同。两组均治疗3 个月。
1.3 观察指标及判定标准
评估、检测及比较两组治疗总有效率、治疗前后的血清白蛋白、24 h 尿蛋白定量、血脂、B 淋巴细胞亚群、T 淋巴细胞亚群指标。(1)治疗效果:以原发性膜性肾病相关症状体征消失、24 h 尿蛋白定量<0.15 g 及血清白蛋白为40~55 g/L,即两指标均正常为完全缓解;以相关症状体征、24 h 尿蛋白定量及血清白蛋白指标均显著改善为部分缓解;以上述方面均未见明显改善为无效[6]。治疗总缓解=完全缓解+部分缓解。(2)疾病相关检测指标:于两组治疗前及治疗1、3 个月后分别检测两组的血清白蛋白、24 h 尿蛋白定量、血脂指标,其中血脂指标包括三酰甘油及总胆固醇,均采用全自动生化仪进行检测。(3)免疫指标:于两组治疗前及治疗1、3 个月后检测,其中B 淋巴细胞亚群检测项目为CD19+及CD20+,T 淋巴细胞亚群检测项目为CD4+、CD8+及CD4+/CD8+,上述指标均采用流式细胞仪进行操作检测。
1.4 统计学处理
数据检验软件为SPSS 23.0,计数资料的表示方式为率(%),采用χ2检验处理,计量资料的表示方式为(±s),组间比较采用独立样本t 检验,组内比较采用配对t 检验,以P<0.05 表示差异有统计学意义。
2 结果
2.1 两组一般资料比较
对照组男23 例,女17 例,年龄18~74 岁,平均(49.33±13.69)岁,病程1.0~12.5 个月,平均(7.31±1.59)个月,疾病分期:Ⅰ期23 例,Ⅱ期17 例。观察组男25 例,女15 例,年龄19~75 岁,平均(49.36±13.75)岁,病程1.0~13.0 个月,平均(7.29±1.66)个月,疾病分期:Ⅰ期22 例,Ⅱ期18 例。两组上述一般资料比较,差异均无统计学意义(P>0.05),具有可比性。
2.2 两组治疗总缓解率比较
观察组总缓解率显著高于对照组,差异有统计学意义(χ2=9.038,P=0.002),见表1。

表1 两组总缓解率比较[例(%)]
2.3 两组血清白蛋白、24 h 尿蛋白定量及血脂指标比较
治疗前两组血清白蛋白、24 h 尿蛋白定量及血脂指标比较,差异均无统计学意义(P>0.05);治疗1、3 个月后两组血清白蛋白均较治疗前升高,且观察组均显著高于对照组,两组24 h 尿蛋白定量及血脂指标均较治疗前降低,且观察组均显著低于对照组,差异均有统计学意义(P<0.05)。见表2。
表2 两组治疗前后的血清白蛋白、24 h尿蛋白定量及血脂指标比较(±s)
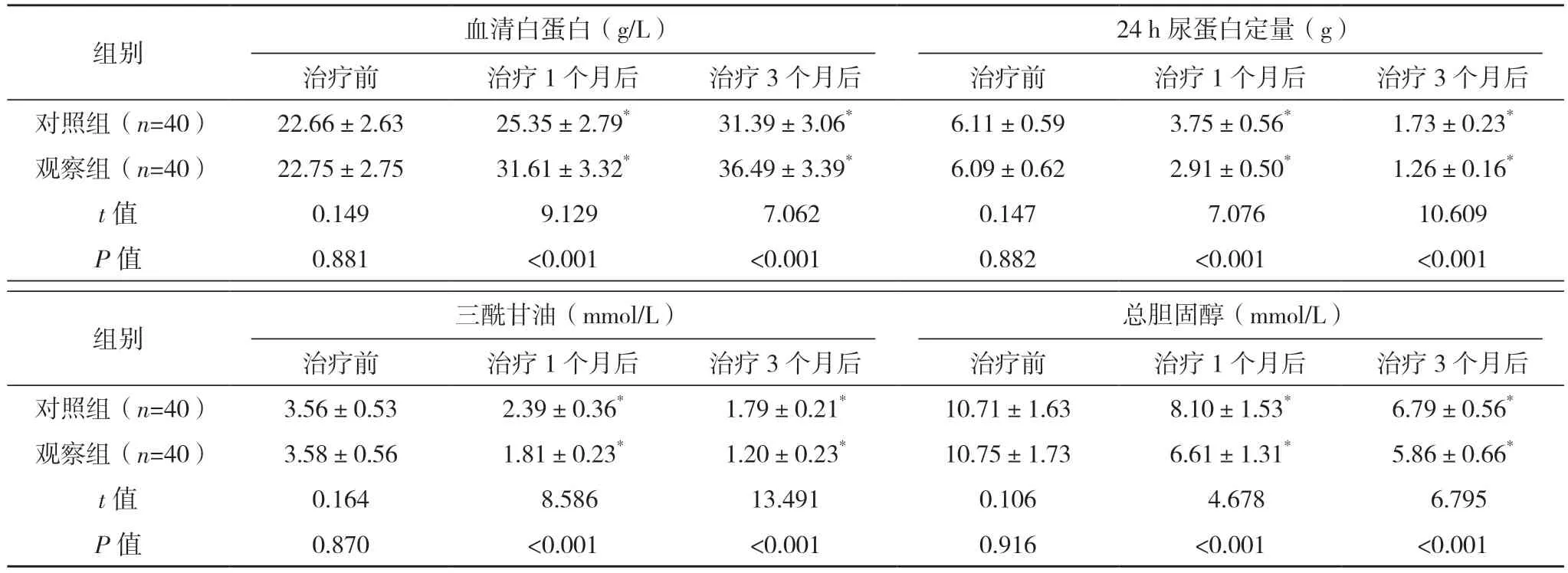
表2 两组治疗前后的血清白蛋白、24 h尿蛋白定量及血脂指标比较(±s)
*与本组治疗前比较,P<0.05。
组别 血清白蛋白(g/L)24 h 尿蛋白定量(g)治疗前 治疗1 个月后 治疗3 个月后 治疗前 治疗1 个月后 治疗3 个月后对照组(n=40) 22.66±2.63 25.35±2.79* 31.39±3.06* 6.11±0.59 3.75±0.56* 1.73±0.23*观察组(n=40) 22.75±2.75 31.61±3.32* 36.49±3.39* 6.09±0.62 2.91±0.50* 1.26±0.16*t 值 0.149 9.129 7.062 0.147 7.076 10.609 P 值 0.881 <0.001 <0.001 0.882 <0.001 <0.001组别 三酰甘油(mmol/L)总胆固醇(mmol/L)治疗前 治疗1 个月后 治疗3 个月后 治疗前 治疗1 个月后 治疗3 个月后对照组(n=40) 3.56±0.53 2.39±0.36* 1.79±0.21* 10.71±1.63 8.10±1.53* 6.79±0.56*观察组(n=40) 3.58±0.56 1.81±0.23* 1.20±0.23* 10.75±1.73 6.61±1.31* 5.86±0.66*t 值 0.164 8.586 13.491 0.106 4.678 6.795 P 值 0.870 <0.001 <0.001 0.916 <0.001 <0.001
2.4 两组CD19+及CD20+指标比较
治疗前两组CD19+及CD20+指标比较,差异均无统计学意义(P>0.05);治疗1、3 个月后两组上述指标均较治疗前降低,且观察组均显著低于对照组,差异均有统计学意义(P<0.05)。见表3。
表3 两组CD19+及CD20+指标比较[%,(±s)]

表3 两组CD19+及CD20+指标比较[%,(±s)]
*与本组治疗前比较,P<0.05。
组别 CD19+CD20+治疗前 治疗1 个月后 治疗3 个月后 治疗前 治疗1 个月后 治疗3 个月后对照组(n=40) 16.36±2.01 15.28±2.11* 14.76±1.95* 26.75±2.06 25.25±2.16* 23.79±1.95*观察组(n=40) 16.50±2.10 13.66±2.01* 13.03±1.62* 26.99±2.10 22.68±2.26* 21.63±1.90*t 值 0.305 3.515 4.316 0.515 5.199 5.017 P 值 0.761 <0.001 <0.001 0.607 <0.001 <0.001
2.5 两组CD4+、CD8+及CD4+/CD8+指标比较
治疗前两组CD4+、CD8+及CD4+/CD8+指标比较,差异均无统计学意义(P>0.05);治疗1、3 个月后两组CD8+指标均较治疗前升高,且观察组均显著高于对照组,两组CD4+及CD4+/CD8+指标均较治疗前降低,且观察组均显著低于对照组,差异均有统计学意义(P<0.05)。见表4。
表4 两组CD4+、CD8+及CD4+/CD8+指标比较(±s)

表4 两组CD4+、CD8+及CD4+/CD8+指标比较(±s)
*与本组治疗前比较,P<0.05。
组别 CD4+(%)CD8+(%)治疗前 治疗1 个月后 治疗3 个月后 治疗前 治疗1 个月后 治疗3 个月后对照组(n=40) 46.76±3.03 45.03±2.96* 43.11±2.90* 20.16±1.32 21.25±1.51* 22.01±1.59*观察组(n=40) 46.90±3.11 43.09±2.76* 40.01±2.93* 19.96±1.36 22.68±1.66* 23.96±1.75*t 值 0.203 3.031 4.755 0.667 4.030 5.215 P 值 0.838 0.003 <0.001 0.506 <0.001 <0.001组别 CD4+/CD8+治疗前 治疗1 个月后 治疗3 个月后对照组(n=40) 2.32±0.31 2.12±0.25* 1.96±0.19*观察组(n=40) 2.35±0.29 1.90±0.23* 1.63±0.15*t 值 0.446 4.095 8.621 P 值 0.656 <0.001 <0.001
3 讨论
原发性膜性肾病是临床高发病,对患者的危害较为突出,是临床较为重视的一类疾病。与原发性膜性肾病相关的各方面研究显示,本病患者除疾病相关的症状体征外,其24 h 尿蛋白定量较高及血清白蛋白较低的情况也相对突出[7-8],同时脂代谢的失衡也在本病患者中相对突出[9-10],因此对本类患者进行治疗的过程中,上述方面是本病治疗效果评估的重要参考方面。再者,本病患者机体免疫方面的变化也是研究重点之一,研究显示,本病患者的B 淋巴细胞亚群、T 淋巴细胞亚群均呈现失衡的状态,且其失衡的程度与疾病的严重程度及发展转归等密切相关[11-12],因此对本类患者进行治疗的过程中,B 淋巴细胞亚群、T 淋巴细胞亚群均是治疗效果评估的重要参考方面。临床与原发性膜性肾病相关的诊治研究中,关于他克莫司应用效果研究不断增多的同时,其差异仍普遍存在[13-15],且对上述B 淋巴细胞亚群、T 淋巴细胞亚群的影响研究仍相对不足,因此这方面的研究意义较高。
本研究结果显示,他克莫司对原发性膜性肾病患者的治疗效果相对更好,表现为观察组总缓解率相对更高,同时治疗1、3 个月后观察组血清白蛋白及CD8+指标均相比对照组更高,观察组24 h 尿蛋白定量、血脂、B 淋巴细胞亚群、CD4+及CD4+/CD8+指标均相比对照组更低(P<0.05),因此本研究认为他克莫司的应用效果相对较好,其对患者疾病相关的血脂、24 h 尿蛋白定量及血清白蛋白具有更好的改善效果,同时对于机体免疫失衡情况也有更好的改善作用,因此认为对于原发性膜性肾病的治疗效果较好。分析原因,他克莫司作为临床有效的免疫抑制剂,其在较多自身免疫性疾病中的应用效果较好[16-17],对于B 淋巴细胞亚群、T 淋巴细胞亚群均有积极的调控作用,因此表现为对上述指标失衡情况的有效控制,改善幅度较大[18-21],而这也是其疾病控制效果较好的重要原因之一。
综上所述,本研究认为他克莫司在原发性膜性肾病患者中的疗效较好,且可显著改善患者的B 淋巴细胞亚群、T 淋巴细胞亚群,因此在原发性膜性肾病患者中的应用价值较高。
