影响非小细胞肺癌非单发脑转移患者立体定向放疗效果的因素
2023-10-09王天昶张永彤李小龙吴磊王锋刚戴震冯杏
王天昶,张永彤,李小龙,吴磊,王锋刚,戴震,冯杏
陕西省肿瘤医院放疗一病区,西安710061
脑转移对晚期非小细胞肺癌患者生存影响大,且影响患者生活质量。放疗是脑转移的重要治疗手段,既往受制于放疗技术,对于脑转移多采用全脑放疗的方式,但其疗效不甚满意,且伴有明显的神经认知功能障碍。近年来,随着放疗技术的发展,立体定向放疗在临床使用中日益广泛,对于单发脑转移灶,立体定向外科放疗(SRS)已成为包括CSCO指南、NCCN指南在内多种诊疗指南推荐的标准放疗方式。最近研究证明,对于非单发脑转移患者立体定向放疗同样是可供选择的放疗方式。但影响非小细胞肺癌非单发脑转移患者立体定向放疗效果的因素目前尚不确定。2022年6月—8月,我们回顾性分析接受立体定向放疗非小细胞肺癌非单发脑转移瘤患者的临床资料,探讨影响其疗效的因素。
1 资料与方法
1.1 临床资料 选取陕西省肿瘤医院2015年6月—2020年6月收治的52例非小细胞肺癌非单发脑转移并接受脑转移灶立体定向放疗的患者。入选标准:有病理结果支持诊断的非小细胞肺癌;确诊脑转移时KPS评分≥60分;接受脑部立体定向放疗后生存时间≥1个月;头颅MR或CT证实脑部有不少于1个脑转移灶;脑转移灶与脑干距离≥5 mm;无急性出血或梗死;立体定向放疗前后未进行全脑放疗。52例患者中,男31例、女21例,中位年龄59岁。腺癌39例、鳞癌11例、腺鳞癌2例。脑转移灶数量为2~8个,中位数量为3个。患者脑转移灶总体积为5.6~68.4 cm3,中位体积为13.8 cm3。本研究通过医院伦理委员会批准([2021]第94号),患者或其家属知情并签署同意书。
1.2 放疗方法 患者均接受立体定向放疗,平静状态下使用西门子大孔径CT模拟定位机进行增强扫描定位(延迟时间90 s,层厚3 mm),图像传输至Eclips计划系统,参照诊断CT、MR及定位CT影像勾画GTV及周边重要器官,GTV外扩3 mm作为PTV,要求95%等剂量曲线包绕靶体积,靶区总剂量为18~50 Gy,单次剂量为10~24 Gy,分割次数为1~5次,使用瓦里安TRUEBEAM直线加速器,6MV-X线FFF模式下实施放疗。放疗后及放疗期间均接受不少于3 d的甘露醇和糖皮质激素脱水降颅压治疗。
1.3 观察指标及评价标准 短期疗效评价采用WHO实体瘤疗效评价标准(RECIST 1.1标准),以放疗结束后28~35 d内首次复查MR或CT影像作为评价资料,将脑转移灶治疗效果区分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)、疾病进展(PD)四大类,CR代表病灶完全消失,持续4周以上;PR代表病灶长径总和缩小≥30%;SD代表病灶长径缩小但未达PR或增加未达PD;PD代表病灶长径总和增加≥20%或发现新病灶;其中客观有效率(ORR)=(CR+PR)/总人数×100%,疾病控制率(DCR)=(CR+PR+SD)/总人数×100%。随访时间2年,放疗后长期疗效评价指标为颅内病灶无进展时间(iPFS)及总生存时间(OS)。
1.4 统计学方法 采用SPSS20.0统计软件。计量资料符合正态分布以表示,比较采用t检验;计数资料以频数和率(%)表示,比较采用χ2检验。ORR和DCR的影响因素分析中,单因素分析采用χ2检验,多因素分析采用Logistic回归模型;iPFS及OS的影响因素分析中,单因素采用Log-rank法,多因素分析采用Cox等比例风险模型。P<0.05为差异有统计学意义。
2 结果
2.1 不同临床特征患者短期疗效指标及长期疗效指标比较 见表1。

表1 不同临床特征患者短期疗效及长期疗效指标比较
2.2 放疗患者短期疗效的影响因素 多因素Logistic分析结果显示,ORR的独立影响因素主要有GPA评分、是否靶向治疗、转移灶最大直径、转移灶总体积、瘤周水肿带直径(P均<0.05),见表2;DCR的独立影响因素仅有转移灶总体积(P<0.05),见表3。
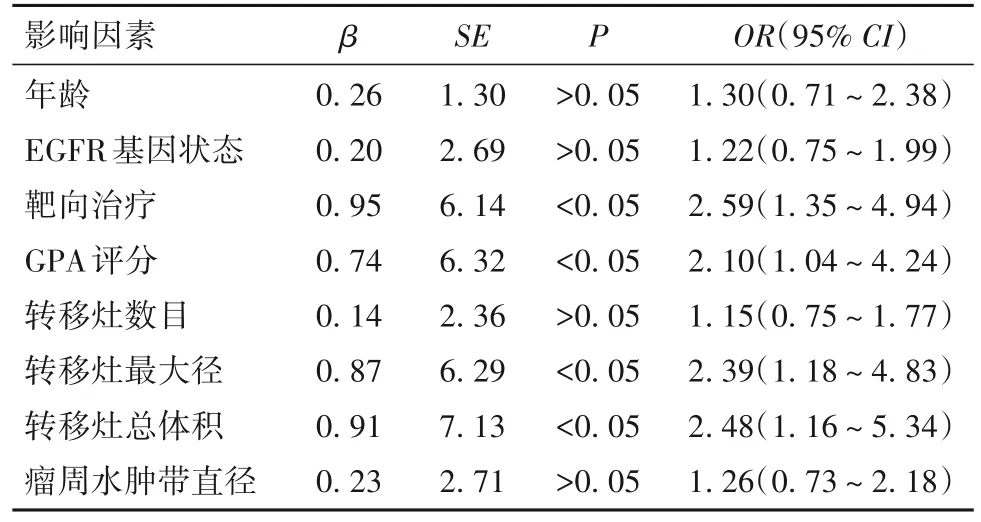
表2 ORR的Logistic多元回归分析结果
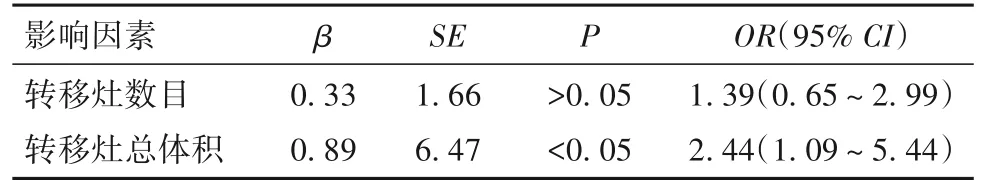
表3 DCR的Logistic多元回归分析结果
2.3 放疗患者长期疗效的影响因素 多因素Cox分析结果显示,iPFS的独立影响因素主要有颅外病灶控制情况、原发灶控制情况、是否靶向治疗、GPA评分、转移灶最大径、转移灶总体积(P均<0.05),见表4;OS的独立影响因素主要有颅外病灶控制情况、是否靶向治疗、GPA评分、转移灶最大径、转移灶总体积(P均<0.05),见表5。
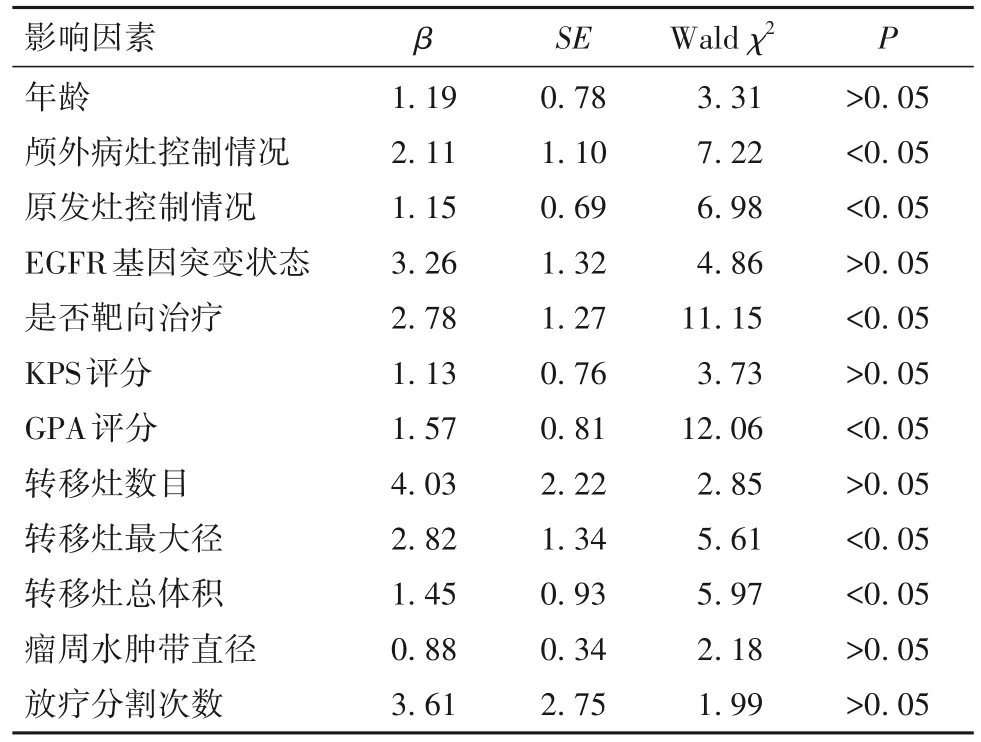
表4 iPFS的Cox多因素分析
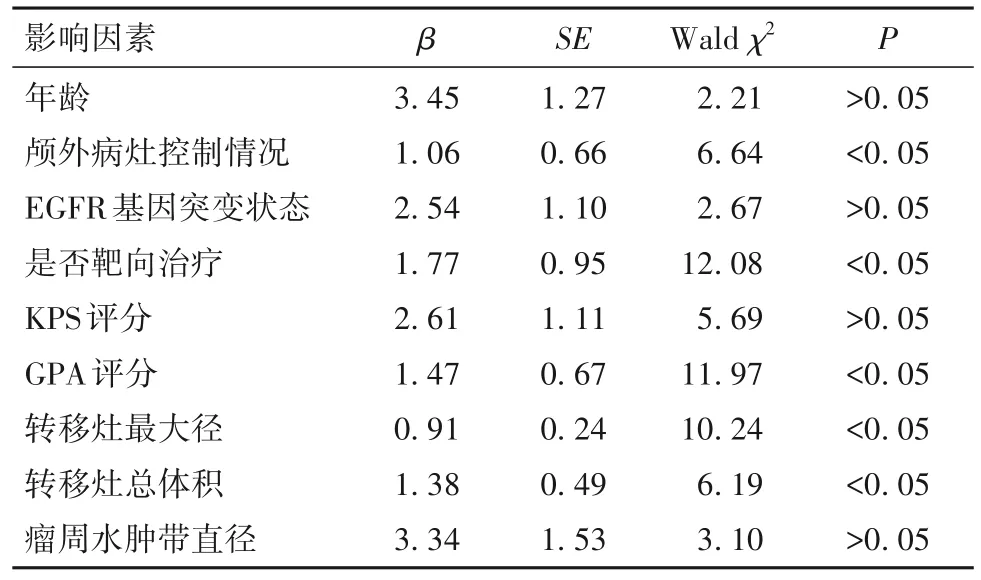
表5 OS的Cox多因素分析
3 讨论
目前,立体定向放疗已成为非小细胞肺癌单发脑转移的标准治疗方式[1]。但对于非单发脑转移,尤其是超过3个转移灶的非小细胞肺癌脑转移,目前并无标准推荐。既往全脑放疗(WBRT)及WBRT联合转移灶同步加量的调强放疗是非单发脑转移使用最多的放疗技术。近年研究证明,立体定向放疗在部分多发脑转移患者的治疗中同样具备良好的疗效和安全性[2-3]。但非小细胞肺癌非单发脑转移立体定向放疗后的疗效及预后影响因素,目前并不十分明确。
本研究将非单发脑转移立体定向放疗疗效分为短期疗效与长期疗效两个方面分别进行评价,分析相关影响因素。在对短期疗效指标ORR的分析中,我们发现对ORR有独立影响的因素主要有是否接受靶向治疗、GPA评分、转移灶最大径、转移灶总体积及瘤周水肿带直径。而DCR的独立影响因素仅有转移灶总体积。上述结果提示,对于脑转移灶短期控制,病灶总体积是最主要的影响因素,而患者一般状况、全身肿瘤控制情况等因素影响较为有限,但如果患者一般状况较好、肿瘤负荷较低或同时联合其他药物治疗时,可能对放疗后转移灶的缩小有更大帮助。这一点与BHATNAGAR等[4]研究结果一致,其在对4~18个脑转移瘤接受立体定向放疗的患者进行疗效观察发现,总转移灶体积的增加和较差的局部控制之间存在明显相关性,但遗憾的是并未确定影响局部控制的体积阈值。
在对iPFS这一长期疗效评价指标进行分析时发现,除了上述脑转移灶特征因素之外,颅外病灶控制情况和原发灶控制情况,对颅内病灶控制亦具有显著影响。而最终对生存时间的分析中我们发现,原发灶的控制并不是独立影响因素,而颅外病灶的控制可能对生存有直接影响,提示脑转移灶的放疗要使患者生存获益,单纯原发灶的控制不能满足要求,而是要求整个颅外病变均处在稳定状态。研究发现,患者的临床情况、有无颅外转移、脑转移瘤的大小、组织学或转移灶的数目是影响预后的最重要因素[5-7]。而本研究中,转移灶的数目、基因突变状态、KPS评分等,似乎对短期疗效指标或长期疗效指标均未产生影响。分析原因可能是随着放疗技术进步,多靶点放疗从TPS系统的计划制定到加速器的放疗实施,相关技术均已发展成熟,颅内转移灶数目多少对放疗实施影响较小,而对放疗实施影响更多的还是转移灶总体积,这提示我们在脑转移灶放疗原则制定中,既往以转移灶数目决定放疗方式的策略可能需要逐步改变为以转移灶体积为主要参考依据;EGFR突变状态不是独立影响因素,可能系入组病例中有部分患者在初诊时为EGFR敏感突变状态,但在后续靶向治疗中出现病情进展或不良反应无法耐受,但未进一步复查基因突变状态。本研究发现,在放疗同时接受靶向治疗的患者无论在局部控制还是在长期生存方面仍有获益。
本研究中,并未将放疗剂量作为可能的影响因素进行分析,而以分割次数作为替代,这样做的主要原因是,目前对不同剂量分割方案中放疗剂量的比较多通过LQ模型换算为等效生物剂量(BED)来进行,而立体定向放疗,尤其是立体定向外科中单次分割模式等效生物剂量的可靠性一直备受争议[8-10]。且在WIGGENRAAD等[11]的系统综述中报道,在几乎所有的研究系列中,6个月的局部控制率(LC)为80%,与处方剂量无关。同样在本研究中,即便以分割次数作为疗效的可能影响因素进行分析,除在iPFS这一指标的单因素分析中发现有统计学差异之外,在其他所有单因素和多因素分析中均未发现区别。笔者认为,这并不能证明放疗剂量对于脑转移灶立体定向放疗的疗效没有影响,而是提示目前我们临床常用的立体定向放疗剂量分割模式的生物等效剂量超过了某一阈值,在该阈值范围内放疗剂量对疗效影响有限,但这一观点尚需进一步临床研究去证实。
综上所述,影响ORR的因素主要有是否接受靶向治疗、GPA评分、转移灶最大径、转移灶总体积及瘤周水肿带直径,而对iPFS有影响的因素主要是颅外病灶控制情况、原发灶控制情况、是否靶向治疗、GPA评分、转移灶最大径、转移灶总体积,而最终影响OS的因素主要是颅外病灶控制情况、是否靶向治疗、GPA评分、转移灶最大径、转移灶总体积。本研究不足之处是由于回顾分析时资料缺失较多,立体定向放疗不良反应情况,尤其是晚期不良反应放射性脑坏死的发生情况未能进行客观评价。入组病例数有限,可能存在统计偏倚,尚需前瞻性大规模临床研究进一步证实。另外,随着内科治疗药物在非小细胞肺癌治疗中的快速进展,包括脑转移在内的晚期非小细胞肺癌患者生存期大幅延长,在合并药物治疗尤其是免疫治疗的情况下,脑转移立体定向放疗如何更好地与内科治疗联合,是进一步探索方向。
